文档内容
第2课时 关键能力——反应热的计算及比较
反应热的计算及比较是高考命题的热点和重点,在选择题中结合能量—反应过程图像
考查反应热与活化能的关系、反应热的比较等;在非选择题中侧重考查利用盖斯定律计算反
应热,或书写热化学方程式,另外还考查根据键能计算反应热等。此类试题大多以最新科研
成果、化工生产中反应机理等为命题情境,命题形式和命题角度灵活多变,体现《中国高考评
价体系》对知识获取能力、思维认知能力的要求,考生要能够客观全面地获取相关信息,能够
从情境中提取有效信息;能够准确概括和描述学科所涉及基本现象的特征及其相互关系,并
从中发现问题;能够灵活地、创造性地运用不同方法,发散地、逆向地解决问题能够通过敏锐
的洞察能力,发现复杂、新颖情境中的关键事实特征和有价值的新问题;能够将所学知识迁
移到新情境,解决新问题,得出新结论。
考向1 盖斯定律及其应用(理解与辨析能力)
借助“能量守恒定律”理解盖斯定律,并应用于分析多步反应的反应热与总反应的反
应热的定量关系,能解释化学变化中能量变化的本质,能运用反应焓变合理选择和利用化学
反应,要求考生能够从多个视角观察、思考同一个问题,发现复杂、新颖情境中的关键事实特
征和有价值的新问题,能够将所学知识迁移到新情境,解决新问题,体现《中国高考评价体
系》对“思维与辨析能力”“抽象思维能力”“数据处理能力”“信息转化能力”等关键
能力的要求。
1.盖斯定律的内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热是
相同的。即:化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。
2.盖斯定律的意义:间接计算某些反应的反应热。
3.盖斯定律的应用
(1)加合法:利用题给热化学方程式通过相加减得到目标热化学方程式,根据盖斯定律求
算反应热(ΔH),如
①C(s)+O(g)===CO (g) ΔH
2 2 1
②C(s)+O(g)===CO(g) ΔH
2 2
根据盖斯定律,由①-②可得:CO(g)+O(g)===CO (g) ΔH=ΔH-ΔH。
2 2 1 2
(2)虚拟路径法:根据物质之间的转化关系,合理设计反应途径,如
根据盖斯定律,路径“甲→乙”和路径“甲→丙→乙”的反应热相等,即ΔH=ΔH +
1
ΔH。
2
4.盖斯定律的理解
转化关系 反应热间的关系
aA――→B、A――→B ΔH=aΔH
1 2ΔH=-ΔH
1 2
ΔH=ΔH+ΔH
1 2
角度1 利用盖斯定律计算反应热
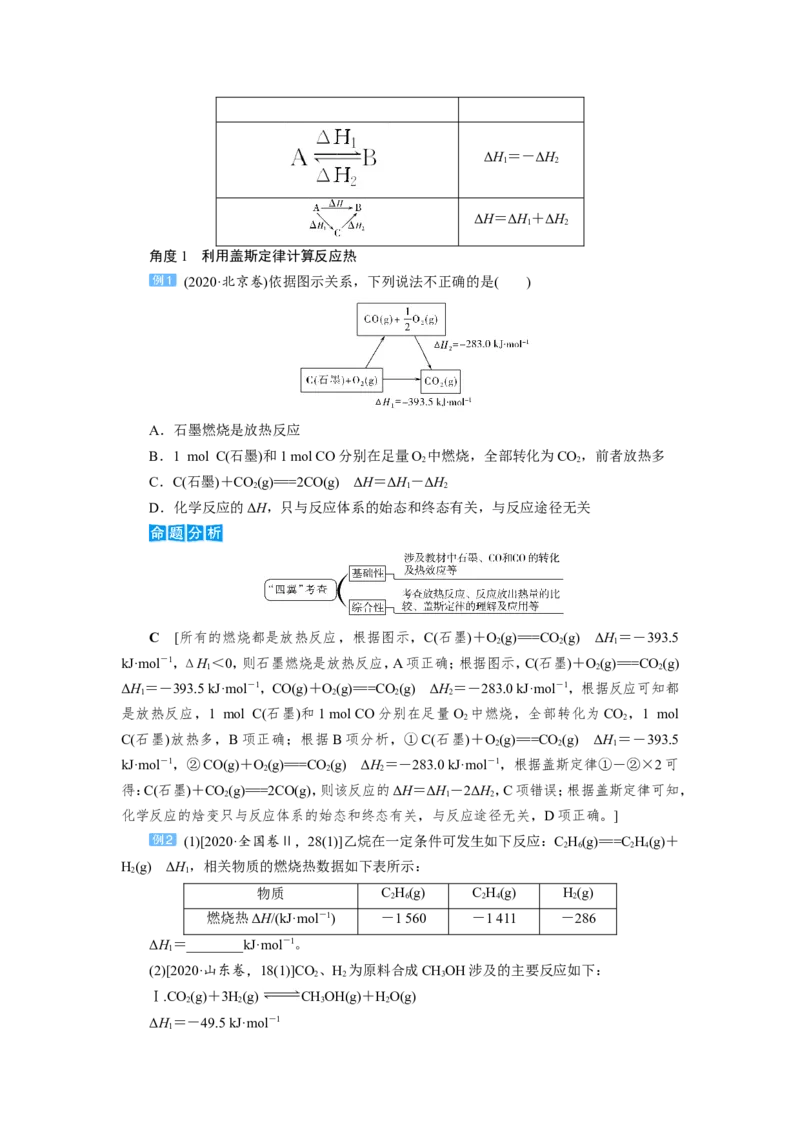
(2020·北京卷)依据图示关系,下列说法不正确的是( )
A.石墨燃烧是放热反应
B.1 mol C(石墨)和1 mol CO分别在足量O 中燃烧,全部转化为CO,前者放热多
2 2
C.C(石墨)+CO(g)===2CO(g) ΔH=ΔH-ΔH
2 1 2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
C [所有的燃烧都是放热反应,根据图示,C(石墨)+O(g)===CO (g) ΔH =-393.5
2 2 1
kJ·mol-1,ΔH<0,则石墨燃烧是放热反应,A项正确;根据图示,C(石墨)+O(g)===CO (g)
1 2 2
ΔH=-393.5 kJ·mol-1,CO(g)+O(g)===CO (g) ΔH=-283.0 kJ·mol-1,根据反应可知都
1 2 2 2
是放热反应,1 mol C(石墨)和1 mol CO分别在足量O 中燃烧,全部转化为CO ,1 mol
2 2
C(石墨)放热多,B项正确;根据B项分析,①C(石墨)+O(g)===CO (g) ΔH =-393.5
2 2 1
kJ·mol-1,②CO(g)+O(g)===CO (g) ΔH=-283.0 kJ·mol-1,根据盖斯定律①-②×2可
2 2 2
得:C(石墨)+CO(g)===2CO(g),则该反应的ΔH=ΔH-2ΔH,C项错误;根据盖斯定律可知,
2 1 2
化学反应的焓变只与反应体系的始态和终态有关,与反应途径无关,D项正确。]
(1)[2020·全国卷Ⅱ,28(1)]乙烷在一定条件可发生如下反应:C H(g)===C H(g)+
2 6 2 4
H(g) ΔH,相关物质的燃烧热数据如下表所示:
2 1
物质 C H(g) C H(g) H(g)
2 6 2 4 2
燃烧热ΔH/(kJ·mol-1) -1 560 -1 411 -286
ΔH=________kJ·mol-1。
1
(2)[2020·山东卷,18(1)]CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.CO (g)+3H(g) CHOH(g)+HO(g)
2 2 3 2
ΔH=-49.5 kJ·mol-1
1Ⅱ.CO(g)+2H(g) CHOH(g)
2 3
ΔH=-90.4 kJ·mol-1
2
Ⅲ.CO (g)+H(g) CO(g)+HO(g) ΔH
2 2 2 3
回答下列问题:
ΔH=________kJ·mol-1。
3
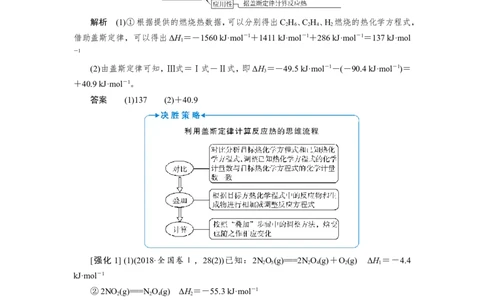
解析 (1)①根据提供的燃烧热数据,可以分别得出C H、C H、H 燃烧的热化学方程式,
2 6 2 4 2
借助盖斯定律,可以得出ΔH=-1560 kJ·mol-1+1411 kJ·mol-1+286 kJ·mol-1=137 kJ·mol
1
-1
(2)由盖斯定律可知,Ⅲ式=Ⅰ式-Ⅱ式,即ΔH=-49.5 kJ·mol-1-(-90.4 kJ·mol-1)=
3
+40.9 kJ·mol-1。
答案 (1)137 (2)+40.9
[强化1] (1)(2018·全国卷Ⅰ,28(2))已知:2NO(g)===2N O(g)+O(g) ΔH =-4.4
2 5 2 4 2 1
kJ·mol-1
②2NO (g)===N O(g) ΔH=-55.3 kJ·mol-1
2 2 4 2
则反应NO(g)===2NO(g)+O(g)的ΔH=_________kJ·mol-1。
2 5 2 2
(2)(2018·全国卷Ⅲ,28(2))三氯氢硅(SiHCl )是制备硅烷、多晶硅的重要原料。SiHCl 在催
3 3
化剂作用下发生反应:
①2SiHCl (g)===SiH Cl(g)+SiCl (g)ΔH=48 kJ·mol-1
3 2 2 4 1
②3SiHCl(g)===SiH (g)+2SiHCl (g)ΔH=-30 kJ·mol-1
2 2 4 3 2
则反应4SiHCl (g)===SiH (g)+3SiCl (g)的ΔH为_______ kJ·mol-1。
3 4 4
(3)(2019·全国卷Ⅱ,27(1))环戊二烯()是重要的有机化工原料,广泛用于农药、橡胶、塑料
等生产。回答下面问题:已知:(g)===(g)+H(g)
2
ΔH=100.3 kJ·mol-1①
1
H(g)+I(g)===2HI(g)
2 2
ΔH=-11.0 kJ·mol-1②
2
对于反应:(g)+I(g)===(g)+2HI(g)③
2
ΔH=________kJ·mol-1。
3
解析 (1)令2NO(g)===2N O(g)+O(g)
2 5 2 4 2
ΔH=-4.4 kJ·mol-1 a
1
2NO (g)===N O(g) ΔH=-55.3 kJ·mol-1 b
2 2 4 2
根据盖斯定律,a式×-b式可得:
NO(g)===2NO(g)+O(g) ΔH=+53.1 kJ·mol-1
2 5 2 2
(2)根据信息,可得反应4SiHCl (g)===SiH (g)+3SiCl (g)的ΔH=3①+②=[3×48+(-
3 4 4
30)] kJ·mol-1=+114 kJ·mol-1
(3)根据盖斯定律,反应①+②可得反应③,则ΔH =ΔH +ΔH =100.3 kJ·mol-1+(-
3 1 2
11.0 kJ·mol-1)=+89.3 kJ·mol-1。
答案 (1)+53.1 (2)+114 (3)+89.3
[强化2] (2019·全国卷Ⅲ,28(2))Deacon直接氧化法可按下列催化过程进行:
CuCl (s)===CuCl(s)+Cl(g) ΔH=83 kJ·mol-1
2 2 1
CuCl(s)+O(g)===CuO(s)+Cl(g)
2 2
ΔH=-20 kJ·mol-1
2
CuO(s)+2HCl(g)===CuCl (s)+HO(g)
2 2
ΔH=-121 kJ·mol-1
3
则4HCl(g)+O(g)===2Cl(g)+2HO(g)的ΔH=________kJ·mol-1。
2 2 2
解析 将已知热化学方程式依次编号为①②③,根据盖斯定律,由(①+②+③)×2得
4HCl(g)+O(g)===2Cl(g)+2HO(g) ΔH=-116 kJ·mol-1。
2 2 2
答案 -116
角度2 根据盖斯定律书写热化学方程式
(1)(2020·全国卷Ⅰ,28(1))钒催化剂参与反应的能量变化如图所示,VO(s)与
2 5
SO (g)反应生成VOSO(s)和VO(s)的热化学方程式为_______________________。
2 4 2 4
(2)(2018·北京卷,27(1))近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转
化与存储。过程如下:反应Ⅰ:2HSO (l)===2SO(g)+2HO(g)+O(g)
2 4 2 2 2
ΔH=+551 kJ·mol-1
1
反应Ⅲ:S(s)+O(g)===SO(g)
2 2
ΔH=-297 kJ·mol-1
3
反应Ⅱ的热化学方程式:____________________________________________。
解析 (1)根据图示写出热化学方程式:①VO(s)+2SO (g)===2VOSO (s) ΔH=-399
2 4 3 4 1
kJ·mol-1;②VO(s)+SO (g)===V O(s)+SO (g) ΔH=-24 kJ·mol-1,由 ①-②×2可得:
2 4 3 2 5 2 2
2VO(s)+2SO (g)===2VOSO (s)+VO(s),根据盖斯定律,该反应的ΔH=ΔH-2ΔH=(-
2 5 2 4 2 4 1 2
399 kJ·mol-1)-(-24 kJ·mol-1)×2=-351 kJ·mol-1。
(2)由题图可知,反应Ⅱ的化学方程式为3SO +2HO=====2HSO +S↓。根据盖斯定律,
2 2 2 4
反应Ⅱ=-(反应Ⅰ+反应Ⅲ)可得:3SO (g)+2HO(g)===2H SO (l)+S(s) ΔH =-254
2 2 2 4 2
kJ·mol-1。
答案 (1)2V O(s)+2SO (g)===2VOSO (s)+VO(s)
2 5 2 4 2 4
ΔH=-351 kJ·mol-1
(2)3SO (g)+2HO(g)===2H SO (l)+S(s)
2 2 2 4
ΔH=-254 kJ·mol-1
2[强化3][2019·天津卷·10(1)]硅粉与HCl在300 ℃时反应生成1 mol SiHC l 气体
3
和H,放出225 kJ热量,该反应的热化学方程式为____________。
2
解析 根据题干知,反应的热化学方程式为Si(s)+3HCl(g) =====SiHCl (g)+H(g) ΔH
3 2
=-225 kJ·mol-1。
答案 Si(s)+3HCl(g)=====SiHCl (g)+H(g)
3 2
ΔH=-225 kJ·mol-1
考向2 根据键能计算反应热(归纳与论证能力)
键能是指气态分子中 1 mol 化学键解离成气态原子所吸收的能量,键能通常是
298.15K、101kPa条件下的标准值,可通过实验测定。从化学反应的实质角度认识化学反应中
能量的变化,化学反应是反应物中化学键的断裂和生成物中化学键的形成过程,可以利用键
能估算化学反应的热效应。此类问题体现了《中国高考评价体系》对“归纳与论证能力”
“信息转化能力”“数据处理能力”“演绎推理能力”等关键能力的考查,要求考生能够
客观全面地获取相关信息,能够从情境中提取有效信息,能够透过现象看到本质,发现隐含
的规律或原理,并解决实际问题。
解题依据是反应热ΔH=Σ(反应物的键能)-Σ(生成物的键能),要注意分子结构及所含
共价键数目。
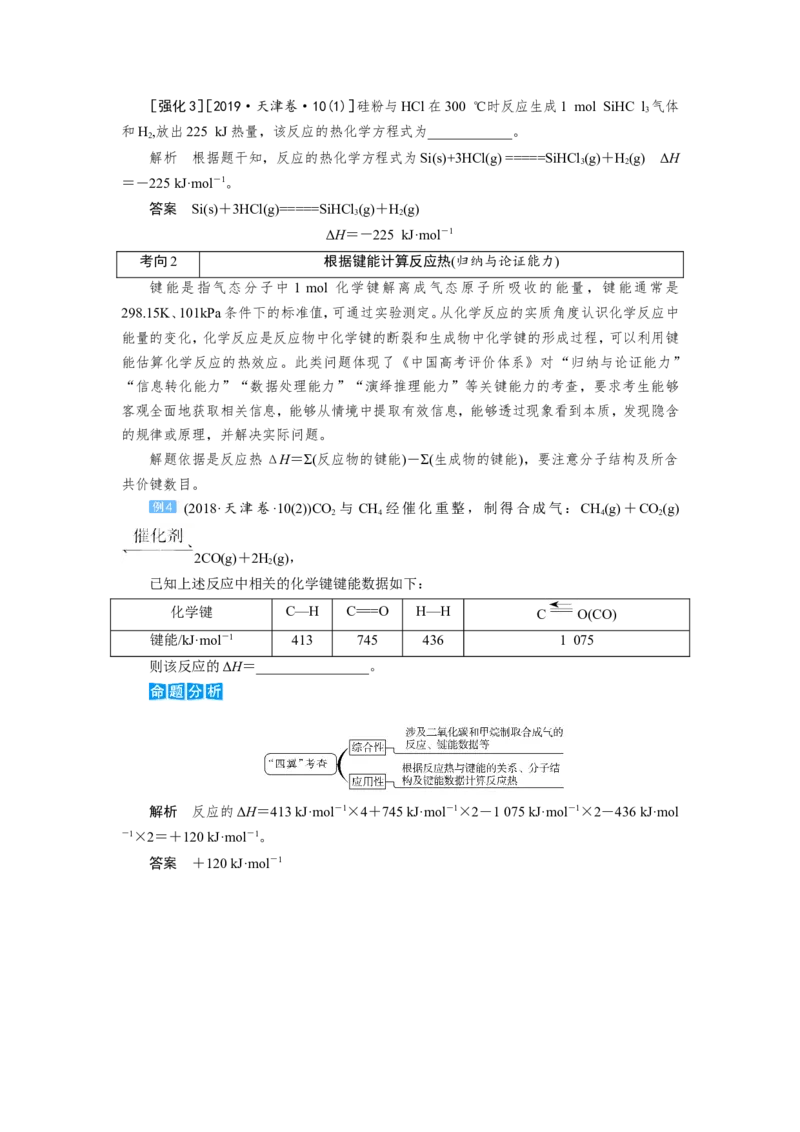
(2018·天津卷·10(2))CO 与 CH 经催化重整,制得合成气:CH(g)+CO(g)
2 4 4 2
2CO(g)+2H(g),
2
已知上述反应中相关的化学键键能数据如下:
化学键 C—H C===O H—H C O(CO)
键能/kJ·mol-1 413 745 436 1 075
则该反应的ΔH=________________。
解析 反应的ΔH=413 kJ·mol-1×4+745 kJ·mol-1×2-1 075 kJ·mol-1×2-436 kJ·mol
-1×2=+120 kJ·mol-1。
答案 +120 kJ·mol-1[强化4] (2021·河北辛集中学检测)已知:①C(s)+HO(g)===CO(g)+H(g) ΔH=+130
2 2 1
kJ·mol-1;②2C(s)+O(g)===2CO(g) ΔH=-220 kJ·mol-1,其中H—H键、O—H键的键能
2 2
分别为436 kJ·mol-1和462 kJ·mol-1,则O===O键的键能为( )
A.496 kJ·mol-1 B.248 kJ·mol-1
C.428 kJ·mol-1 D.284 kJ·mol-1
A [根据盖斯定律,由①×2-②可得:2HO(g)===O (g)+2H(g),则该反应的ΔH=2ΔH
2 2 2 1
-ΔH=2×(+130 kJ·mol-1)-(-220 kJ·mol-1)=+480 kJ·mol-1。根据ΔH与键能的关系,
2
2HO(g)===O (g)+2H(g)的ΔH=(4×462 kJ·mol-1)-E -2×436 kJ·mol-1,从而可得:+
2 2 2 O===O
480 kJ·mol-1=(4×462 kJ·mol-1)-E -2×436 kJ·mol-1,解得E =496 kJ·mol-1,故
O===O O===O
O===O键的键能为496 kJ·mol-1。]
考向3 反应热的大小比较(归纳与论证能力)
对不同反应的反应热(ΔH)的大小进行比较,是高考考查反应热的另一种形式。此类试题
往往提供多个热化学方程式,要求考生从物质的状态、反应进行的程度、盖斯定律等角度进
行分析,并作出合理的判断,体现了《中国高考评价体系》对“归纳与论证能力”的要求,识
别有效证据、科学推理论证、归纳总结规律。
对于可求得准确数值的反应热(ΔH),直接比较反应热(ΔH)即可得出大小关系,而对于无
法求得准确数值的反应热:
1.根据反应物的结构及性质比较
等物质的量的不同物质与同一物质反应时,其反应热不同。如等量的不同金属或非金属
与同一种物质反应,金属或非金属越活泼,反应越容易发生,放出的热量就越多,ΔH就越小。
2.利用物质的状态,迅速比较反应热的大小
(1)若反应为放热反应,当反应物状态相同,生成物状态不同时,生成固体放热最多,生成
气体放热最少。
(2)若反应为放热反应,当反应物状态不同,生成物状态相同时,固体反应放热最少,气体
反应放热最多。3.根据反应规律直接比较
(1)吸热反应的ΔH肯定比放热反应的大。(前者大于0,后者小于0);
(2)生成等量的水时,强酸和强碱的稀溶液反应比弱酸和强碱(或强酸和弱碱)的稀溶液反
应放出的热量多。
4.根据反应进行的程度进行比较
(1)对于多步进行的放热反应,当反应物和生成物的状态相同时,参加反应物质的量越多,
ΔH就越小。对于可逆反应,若正反应是放热反应,反应程度越大,反应放出的热量越多;若正
反应是吸热反应,反应程度越大,反应吸收的热量越多。
(2)对于可逆反应,由于反应物不可能完全转化为生成物,所以实际放出(或吸收)的热量
小于相应的热化学方程式中的ΔH的绝对值。
5.利用盖斯定律进行比较
依据盖斯定律,化学反应的反应热只与始态和终态有关,而与化学反应进行的途径无关。
热化学方程式像代数式一样,可进行移项、合并和加、减、乘、除等数学运算,依据进行数学运
算后所得新反应的ΔH可以比较运算前各反应的ΔH的大小。
(2020.7·浙江选考)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+H
2
O(l)⇌HCO(aq)+OH-(aq) ΔH
2
OH-(aq)+H+(aq)===H O(l) ΔH
2 3
OH-(aq)+CHCOOH(aq)===CH COO-(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH <ΔH
1 2 1 2
C.ΔH<0 ΔH>0 D.ΔH>ΔH
3 4 3 4
B [将题给四个热化学方程式依次编号为①②③④,反应①可看作NaCO 溶液和少量
2 3
稀盐酸反应,为放热反应,ΔH<0;反应②是CO的水解反应,为吸热反应,ΔH>0,故ΔH
1 2 1
<ΔH,A错误,B正确;反应③是中和反应,ΔH<0,反应④是CHCOOH和强碱的中和反
2 3 3
应,ΔH<0,由于CHCOOH电离要吸收热量,等量的OH-分别发生反应③和④时,反应③
4 3
放出的热量比④多,则有ΔH<ΔH,C、D均错误。]
3 4[强化5] (2021·河北唐山一中检测)室温下,将1 mol的CuSO ·5H O(s)溶于水会使溶液温
4 2
度降低,热效应为ΔH ,将1 mol的CuSO (s)溶于水会使溶液温度升高,热效应为ΔH ;
1 4 2
CuSO ·5H O(s)受热分解的化学方程式为CuSO ·5H O(s)=====CuSO (s)+5HO(l),热效应为
4 2 4 2 4 2
ΔH。则下列判断正确的是( )
3
A.ΔH>ΔH B.ΔH<ΔH
2 3 1 3
C.ΔH+ΔH=ΔH D.ΔH+ΔH>ΔH
1 3 2 1 2 3
B [根据题给信息写出热化学方程式:CuSO ·5HO(s)===Cu2+(aq)+SO(aq)+5HO(l)
4 2 2
ΔH>0 ①;CuSO (s)===Cu2+(aq)+SO(aq) ΔH<0 ②;
1 4 2
CuSO ·5HO(s)=====CuSO (s)+5HO(l) ΔH>0 ③;
4 2 4 2 3
根据盖斯定律,由②+③可得:CuSO ·5HO(s)===Cu2+(aq)+SO(aq)+5HO(l)
4 2 2
则有ΔH=ΔH+ΔH,由于ΔH>0,ΔH<0,ΔH>0,所以ΔH<ΔH。]
1 2 3 1 2 3 1 3
[强化6] (2020·湖北孝感联考)在同温同压下,下列各组热化学方程式中,ΔH>ΔH 的是(
2 1
)
A.2H(g)+O(g)===2H O(g) ΔH;
2 2 2 1
2H(g)+O(g)===2H O(l) ΔH
2 2 2 2
B.S(g)+O(g)===SO(g) ΔH;
2 2 1
S(s)+O(g)===SO(g) ΔH
2 2 2
C.C(s)+O(g)===CO(g) ΔH;
2 1
C(s)+O(g)===CO (g) ΔH
2 2 2
D.2HCl(g)===H (g)+Cl(g) ΔH;
2 2 1
H(g)+Cl(g)===HCl(g) ΔH
2 2 2
B [等量H(g)完全燃烧生成 HO(l)放出的热量比生成 HO(g)放出的热量多,则有
2 2 2
ΔH>ΔH,A项错误;等量S(g)具有的能量高于S(s)具有的能量,则等量S(g)反应放出的热量
1 2
比S(s)反应放出的热量多,则有ΔH>ΔH,B项正确;等量C(s)完全燃烧生成CO(g)放出的
2 1 2
热量比生成CO(g)放出的热量多,则有ΔH>ΔH,C项错误;HCl(g)分解生成H(g)和Cl(g)是
1 2 2 2
吸热反应,H(g)和Cl(g)生成HCl(g)是放热反应,则有ΔH>ΔH,D项错误。]
2 2 1 2
训练(二十八) 反应热的计算及比较
1.(2021·山东淄博期初调研)已知:25 ℃、101 kPa,H(g)+O(g)===H O(g)
2 2 2
ΔH=-241.8 kJ·mol-1
C(s)+O(g)===CO(g)
2
ΔH=-110.5 kJ·mol-1
将煤转化为清洁气体燃料时反应C(s)+HO(g)===H (g)+CO(g)的ΔH是( )
2 2
A.-131.3 kJ·mol-1 B.+131.3 kJ·mol-1
C.+352.3 kJ·mol-1 D.-352.3 kJ·mol-1
B [将题给热化学方程式依次编号为①②,由②-①可得:C(s)+HO(g)===H (g)+
2 2
CO(g),根据盖斯定律,该反应的ΔH=(-110.5 kJ·mol-1)-(-241.8 kJ·mol-1)=+131.3
kJ·mol-1。]
2.(2021·湖北武汉联考)根据以下热化学方程式,ΔH 和ΔH 的大小比较错误的是( )
1 2
A.2HS(g)+3O(g)===2SO(g)+2HO(l) ΔH
2 2 2 2 1
2HS(g)+O(g)===2S(s)+2HO(l) ΔH
2 2 2 2
则ΔH>ΔH
1 2
B.Br (g)+H(g)===2HBr(g) ΔH
2 2 1
Br (l)+H(g)===2HBr(g) ΔH
2 2 2
则ΔH<ΔH
1 2
C.4Al(s)+3O(g)===2AlO(s) ΔH
2 2 3 1
4Fe(s)+3O(g)===2Fe O(s) ΔH
2 2 3 2
则 ΔH<ΔH
1 2
D.Cl(g)+H(g)===2HCl(g) ΔH
2 2 1
Br (g)+H(g)===2HBr(g) ΔH
2 2 2
则 ΔH<ΔH
1 2
A [将A中的热化学方程式依次编号为①、②,由①-②可得2S(s)+2O(g)===2SO(g)
2 2
ΔH=ΔH-ΔH<0,即ΔH<ΔH,A项错误;Br (g)具有的能量高于等量的Br (l)具有的能量,
1 2 1 2 2 2
故1 mol Br (g)与H(g)反应生成HBr(g)放出的热量比1 mol Br (l)与H(g)反应生成HBr(g)放
2 2 2 2
出的热量多,则有ΔH<ΔH,B项正确;将C中的两个热化学方程式依次编号为①、②,根据
1 2
盖斯定律,由①-②得4Al(s)+2Fe O(s)===2AlO(s)+4Fe(s),则有ΔH=ΔH-ΔH<0,则
2 3 2 3 3 1 2
ΔH<ΔH,C项正确;Cl 比Br 活泼,与H 反应时越容易,放出的热量越多,ΔH越小,故
1 2 2 2 2
ΔH<ΔH,D项正确。]
1 2
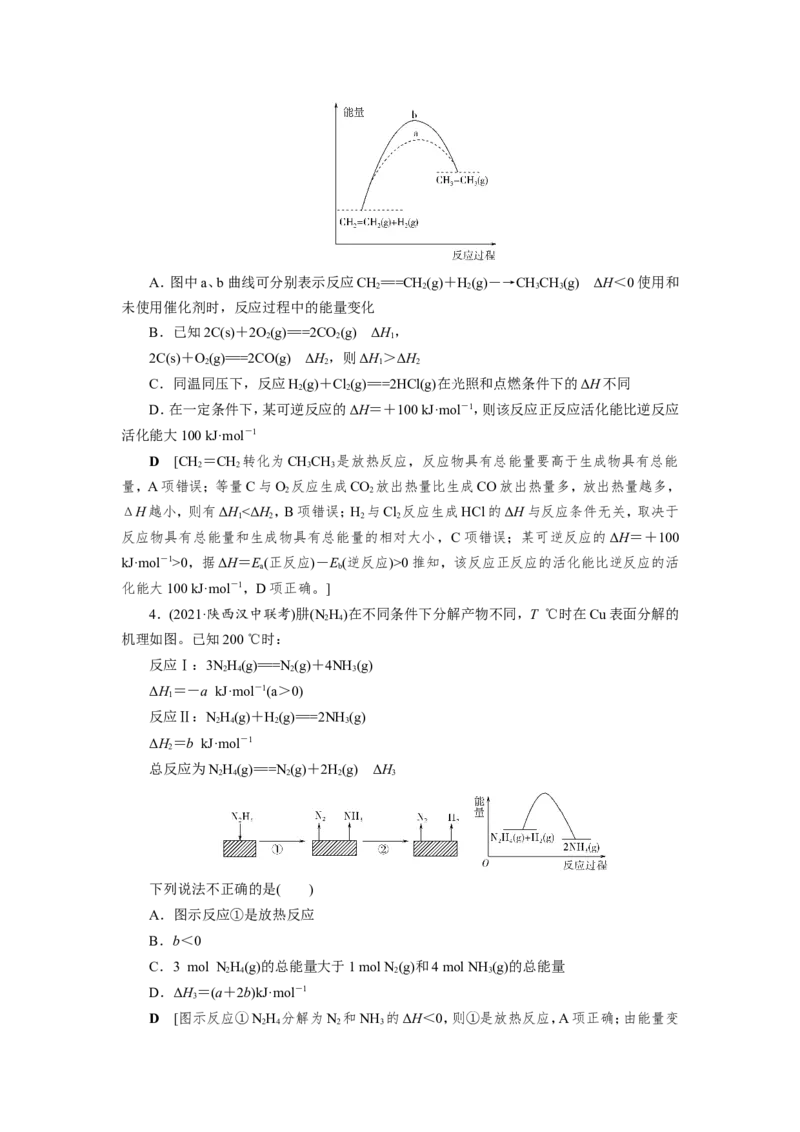
3.(2021·江苏常熟调研)下列关于反应过程中能量变化的说法正确的是( )A.图中a、b曲线可分别表示反应CH===CH (g)+H(g)―→CHCH(g) ΔH<0使用和
2 2 2 3 3
未使用催化剂时,反应过程中的能量变化
B.已知2C(s)+2O(g)===2CO (g) ΔH,
2 2 1
2C(s)+O(g)===2CO(g) ΔH,则ΔH>ΔH
2 2 1 2
C.同温同压下,反应H(g)+Cl(g)===2HCl(g)在光照和点燃条件下的ΔH不同
2 2
D.在一定条件下,某可逆反应的ΔH=+100 kJ·mol-1,则该反应正反应活化能比逆反应
活化能大100 kJ·mol-1
D [CH =CH 转化为CHCH 是放热反应,反应物具有总能量要高于生成物具有总能
2 2 3 3
量,A项错误;等量C与O 反应生成CO 放出热量比生成CO放出热量多,放出热量越多,
2 2
ΔH越小,则有ΔH<ΔH,B项错误;H 与Cl 反应生成HCl的ΔH与反应条件无关,取决于
1 2 2 2
反应物具有总能量和生成物具有总能量的相对大小,C项错误;某可逆反应的ΔH=+100
kJ·mol-1>0,据ΔH=E(正反应)-E(逆反应)>0推知,该反应正反应的活化能比逆反应的活
a b
化能大100 kJ·mol-1,D项正确。]
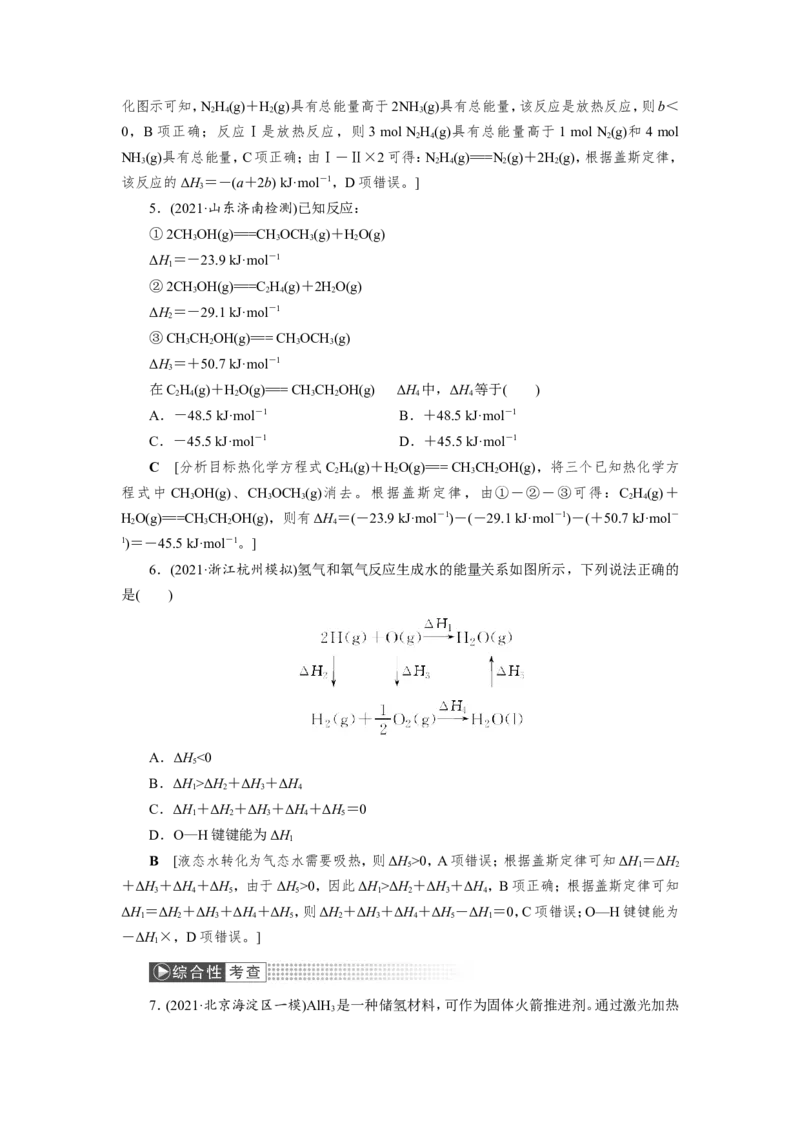
4.(2021·陕西汉中联考)肼(N H)在不同条件下分解产物不同,T ℃时在Cu表面分解的
2 4
机理如图。已知200 ℃时:
反应Ⅰ:3NH(g)===N (g)+4NH (g)
2 4 2 3
ΔH=-a kJ·mol-1(a>0)
1
反应Ⅱ:NH(g)+H(g)===2NH(g)
2 4 2 3
ΔH=b kJ·mol-1
2
总反应为NH(g)===N (g)+2H(g) ΔH
2 4 2 2 3
下列说法不正确的是( )
A.图示反应①是放热反应
B.b<0
C.3 mol NH(g)的总能量大于1 mol N (g)和4 mol NH (g)的总能量
2 4 2 3
D.ΔH=(a+2b)kJ·mol-1
3
D [图示反应①NH 分解为N 和NH 的ΔH<0,则①是放热反应,A项正确;由能量变
2 4 2 3化图示可知,NH(g)+H(g)具有总能量高于2NH (g)具有总能量,该反应是放热反应,则b<
2 4 2 3
0,B项正确;反应Ⅰ是放热反应,则3 mol N H(g)具有总能量高于1 mol N (g)和4 mol
2 4 2
NH (g)具有总能量,C项正确;由Ⅰ-Ⅱ×2可得:NH(g)===N (g)+2H(g),根据盖斯定律,
3 2 4 2 2
该反应的ΔH=-(a+2b) kJ·mol-1,D项错误。]
3
5.(2021·山东济南检测)已知反应:
①2CHOH(g)===CH OCH (g)+HO(g)
3 3 3 2
ΔH=-23.9 kJ·mol-1
1
②2CHOH(g)===C H(g)+2HO(g)
3 2 4 2
ΔH=-29.1 kJ·mol-1
2
③CHCHOH(g)=== CHOCH (g)
3 2 3 3
ΔH=+50.7 kJ·mol-1
3
在C H(g)+HO(g)=== CHCHOH(g) ΔH 中,ΔH 等于( )
2 4 2 3 2 4 4
A.-48.5 kJ·mol-1 B.+48.5 kJ·mol-1
C.-45.5 kJ·mol-1 D.+45.5 kJ·mol-1
C [分析目标热化学方程式C H(g)+HO(g)=== CH CHOH(g),将三个已知热化学方
2 4 2 3 2
程式中 CHOH(g)、CHOCH (g)消去。根据盖斯定律,由①-②-③可得:C H(g)+
3 3 3 2 4
HO(g)===CH CHOH(g),则有ΔH=(-23.9 kJ·mol-1)-(-29.1 kJ·mol-1)-(+50.7 kJ·mol-
2 3 2 4
1)=-45.5 kJ·mol-1。]
6.(2021·浙江杭州模拟)氢气和氧气反应生成水的能量关系如图所示,下列说法正确的
是( )
A.ΔH<0
5
B.ΔH>ΔH+ΔH+ΔH
1 2 3 4
C.ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5
D.O—H键键能为ΔH
1
B [液态水转化为气态水需要吸热,则ΔH>0,A项错误;根据盖斯定律可知ΔH=ΔH
5 1 2
+ΔH+ΔH+ΔH,由于ΔH>0,因此ΔH>ΔH+ΔH+ΔH,B项正确;根据盖斯定律可知
3 4 5 5 1 2 3 4
ΔH=ΔH+ΔH+ΔH+ΔH,则ΔH+ΔH+ΔH+ΔH-ΔH=0,C项错误;O—H键键能为
1 2 3 4 5 2 3 4 5 1
-ΔH×,D项错误。]
1
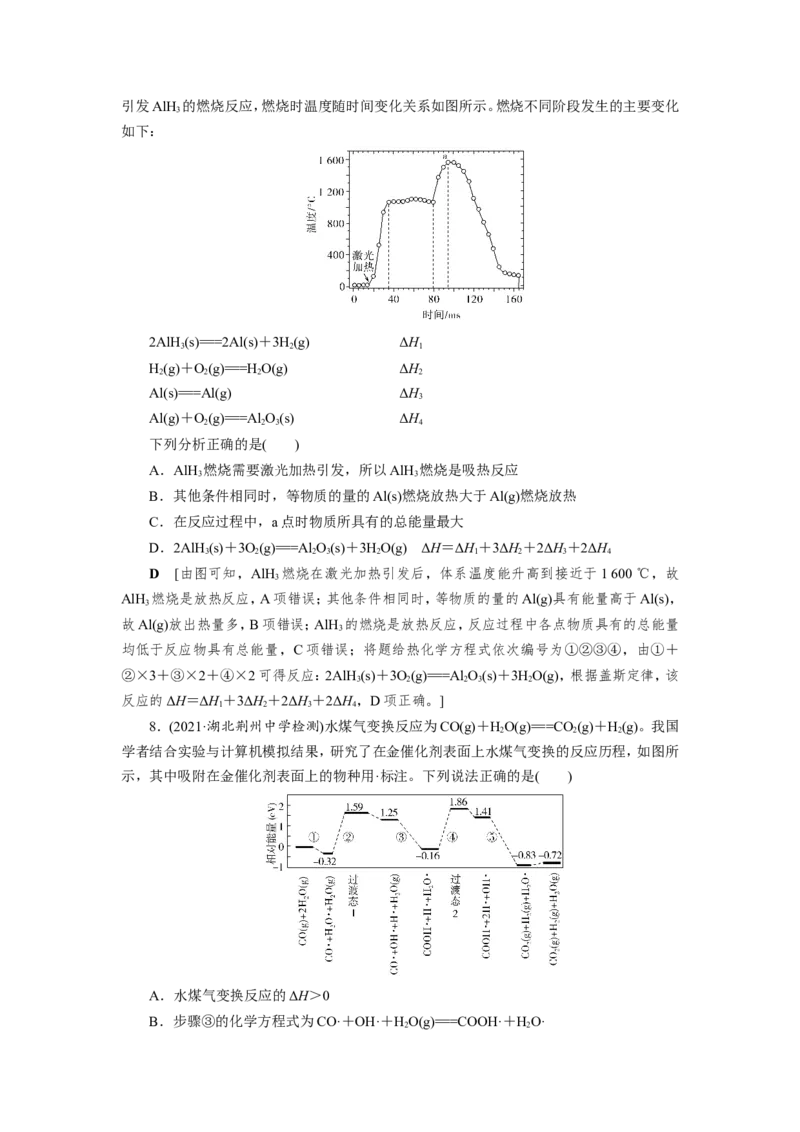
7.(2021·北京海淀区一模)AlH 是一种储氢材料,可作为固体火箭推进剂。通过激光加热
3引发AlH 的燃烧反应,燃烧时温度随时间变化关系如图所示。燃烧不同阶段发生的主要变化
3
如下:
2AlH(s)===2Al(s)+3H(g) ΔH
3 2 1
H(g)+O(g)===H O(g) ΔH
2 2 2 2
Al(s)===Al(g) ΔH
3
Al(g)+O(g)===Al O(s) ΔH
2 2 3 4
下列分析正确的是( )
A.AlH 燃烧需要激光加热引发,所以AlH 燃烧是吸热反应
3 3
B.其他条件相同时,等物质的量的Al(s)燃烧放热大于Al(g)燃烧放热
C.在反应过程中,a点时物质所具有的总能量最大
D.2AlH(s)+3O(g)===AlO(s)+3HO(g) ΔH=ΔH+3ΔH+2ΔH+2ΔH
3 2 2 3 2 1 2 3 4
D [由图可知,AlH 燃烧在激光加热引发后,体系温度能升高到接近于1 600 ℃,故
3
AlH 燃烧是放热反应,A项错误;其他条件相同时,等物质的量的Al(g)具有能量高于Al(s),
3
故Al(g)放出热量多,B项错误;AlH 的燃烧是放热反应,反应过程中各点物质具有的总能量
3
均低于反应物具有总能量,C项错误;将题给热化学方程式依次编号为①②③④,由①+
②×3+③×2+④×2可得反应:2AlH(s)+3O(g)===AlO(s)+3HO(g),根据盖斯定律,该
3 2 2 3 2
反应的ΔH=ΔH+3ΔH+2ΔH+2ΔH,D项正确。]
1 2 3 4
8.(2021·湖北荆州中学检测)水煤气变换反应为CO(g)+HO(g)===CO (g)+H(g)。我国
2 2 2
学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所
示,其中吸附在金催化剂表面上的物种用·标注。下列说法正确的是( )
A.水煤气变换反应的ΔH>0
B.步骤③的化学方程式为CO·+OH·+HO(g)===COOH·+HO·
2 2C.步骤⑤只有非极性键H—H键形成
D.该历程中最大能垒(活化能)E =1.91 eV
正
B [由图可知,CO(g)+2HO(g)具有总能量高于CO(g)+H(g)+HO(g)具有总能量,则
2 2 2 2
水煤气变换反应是放热反应,ΔH<0,A项错误;步骤③中CO·+OH·+HO(g)转化为COOH·
2
+HO·,B项正确;步骤⑤中COOH·+2H·+OH·转化为CO(g)+H(g)+HO·,故步骤⑤有
2 2 2 2
C===O键、H—H键和H—O键形成,C项错误;图中步骤④的能垒(活化能)最大,最大能垒E
=1.86 eV-(-0.16 eV)=2.02 eV,D项错误。]
正
9.(2021·山东烟台一中检测)通过以下反应均可获取H。
2
①C(s)+HO(g)===CO(g)+H(g)
2 2
ΔH=+131.3 kJ·mol-1
1
②CH(g)+HO(g)===CO(g)+3H(g)
4 2 2
ΔH=+206.1 kJ·mol-1
2
③CO(g)+HO(g)===CO (g)+H(g) ΔH
2 2 2 3
下列说法正确的是( )
A.①中反应物的总能量大于生成物的总能量
B.②中使用适当催化剂,可以使ΔH 减小
2
C.由①、②计算反应CH(g)===C(s)+2H(g)的ΔH=-74.8 kJ·mol-1
4 2
D.若知反应C(s)+CO(g)===2CO(g)的ΔH,结合ΔH 可计算出ΔH
2 1 3
D [①是吸热反应,反应物的总能量低于生成物的总能量,A项错误;使用催化剂,可以
改变活化能,但反应热ΔH 不变,B项错误;由②-①可得反应:CH(g)===C(s)+2H(g),根
2 4 2
据盖斯定律,则有ΔH=(+206.1 kJ·mol-1)-(+131.3 kJ·mol-1)=74.8 kJ·mol-1,C项错误;若
知反应C(s)+CO(g)===2CO(g)的ΔH,将该反应编号为④,由①-④可得反应③,根据盖斯
2
定律,则反应③的ΔH=ΔH-ΔH,D项正确。]
3 1
10.(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式
如下:
①CHOH(g)+HO(g)===CO (g)+3H(g)
3 2 2 2
ΔH=+49.0 kJ·mol-1
②CHOH(g)+O(g)===CO (g)+2H(g)
3 2 2 2
ΔH=-192.9 kJ·mol-1
又知③HO(g)===H O(l) ΔH=-44 kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程
2 2
式为________________________________________________________________________
________________________________________________________________________。
(2)如表所示是部分化学键的键能参数。
化学键 P—P P—O O===O P===O
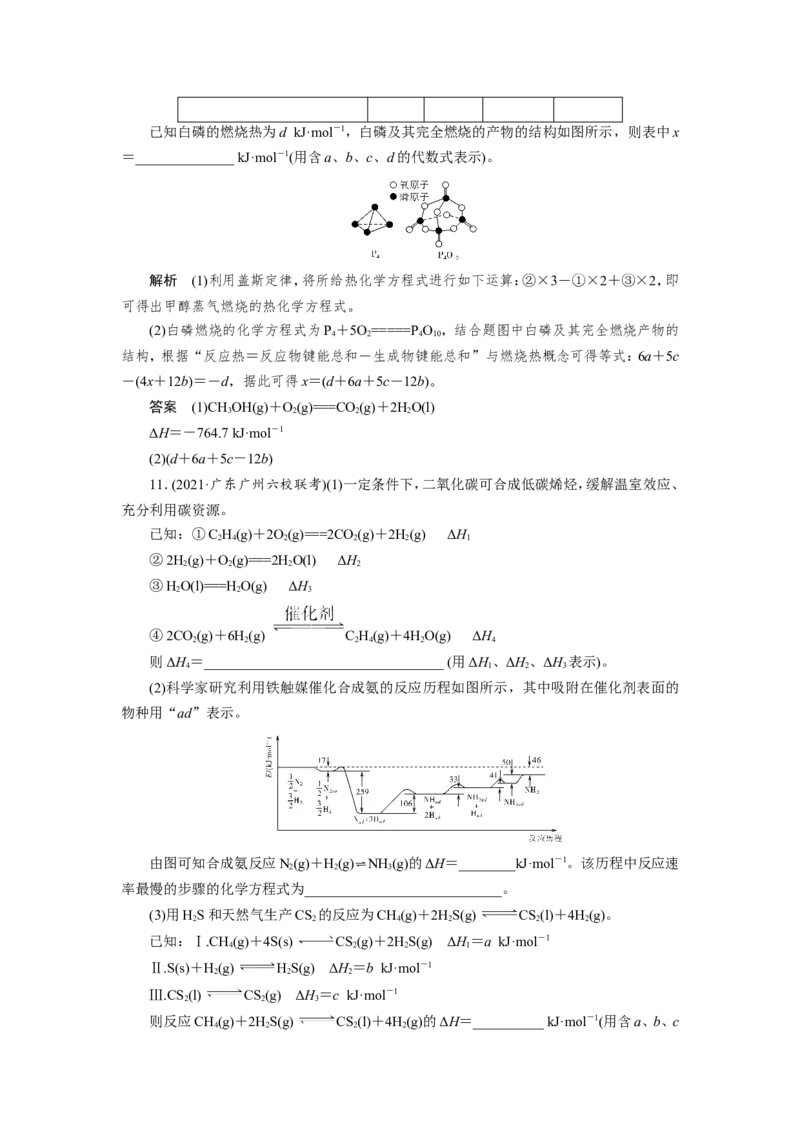
键能/(kJ·mol-1) a b c x已知白磷的燃烧热为d kJ·mol-1,白磷及其完全燃烧的产物的结构如图所示,则表中x
=______________ kJ·mol-1(用含a、b、c、d的代数式表示)。
解析 (1)利用盖斯定律,将所给热化学方程式进行如下运算:②×3-①×2+③×2,即
可得出甲醇蒸气燃烧的热化学方程式。
(2)白磷燃烧的化学方程式为P+5O=====PO ,结合题图中白磷及其完全燃烧产物的
4 2 4 10
结构,根据“反应热=反应物键能总和-生成物键能总和”与燃烧热概念可得等式:6a+5c
-(4x+12b)=-d,据此可得x=(d+6a+5c-12b)。
答案 (1)CH OH(g)+O(g)===CO (g)+2HO(l)
3 2 2 2
ΔH=-764.7 kJ·mol-1
(2)(d+6a+5c-12b)
11.(2021·广东广州六校联考)(1)一定条件下,二氧化碳可合成低碳烯烃,缓解温室效应、
充分利用碳资源。
已知:①C H(g)+2O(g)===2CO (g)+2H(g) ΔH
2 4 2 2 2 1
②2H(g)+O(g)===2H O(l) ΔH
2 2 2 2
③HO(l)===H O(g) ΔH
2 2 3
④2CO(g)+6H(g) C H(g)+4HO(g) ΔH
2 2 2 4 2 4
则ΔH=__________________________________ (用ΔH、ΔH、ΔH 表示)。
4 1 2 3
(2)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的
物种用“ad”表示。
由图可知合成氨反应N
2
(g)+H
2
(g)⇌NH
3
(g)的ΔH=________kJ·mol-1。该历程中反应速
率最慢的步骤的化学方程式为____________________________。
(3)用HS和天然气生产CS 的反应为CH(g)+2HS(g) CS(l)+4H(g)。
2 2 4 2 2 2
已知:Ⅰ.CH (g)+4S(s) CS(g)+2HS(g) ΔH=a kJ·mol-1
4 2 2 1
Ⅱ.S(s)+H(g) HS(g) ΔH=b kJ·mol-1
2 2 2
Ⅲ.CS (l) CS(g) ΔH=c kJ·mol-1
2 2 3
则反应CH(g)+2HS(g) CS(l)+4H(g)的ΔH=__________ kJ·mol-1(用含a、b、c
4 2 2 2的代数式表示)。
(4)己知:①CHO(g)+O(g)===CO (g)+HO(g) ΔH=-480 kJ·mol-1;
2 2 2 2 1
②相关化学键的键能数据如下表所示:
化学键 O===O H—H O—H
键能/(kJ·mol-1) 498 436 464
则CO(g)+2H(g) CHO(g)+HO(g) ΔH=________。
2 2 2 2
解析 (1)分析题给热化学方程式,由②×2+③×4-①可得反应 2CO(g)+6H(g)
2 2
C H(g)+4HO(g),根据盖斯定律,则有ΔH=2ΔH+4ΔH-ΔH。
2 4 2 4 2 3 1
(2)由图可知,N(g)+H(g)具有的总能量比NH (g)具有总能量高46 kJ·mol-1,则合成氨
2 2 3
反应N(g)+H(g) NH (g)的ΔH=-46 kJ·mol-1。一般情况,正反应的活化能越大,反
2 2 3
应速率越慢,图中过程N +3H →NH +2H 的活化能最大,该步反应最慢。
ad ad ad ad
(3)由Ⅰ-Ⅱ×4-Ⅲ可得反应CH(g)+2HS(g) CS(l)+4H(g),根据盖斯定律,该
4 2 2 2
反应的ΔH=(a-4b-c)kJ·mol-1。
(4)①CHO(g)+O(g)===CO (g)+HO(g) ΔH =-480 kJ·mol-1;根据表中键能,写出
2 2 2 2 1
H 和O 反应:②2H(g)+O(g)===2H O(g) ΔH =-486 kJ·mol-1。由②-①可得反应:
2 2 2 2 2 2
CO(g)+2H(g) CHO(g)+HO(g),根据盖斯定律,该反应的ΔH=(-486 kJ·mol-1)-
2 2 2 2
(-480 kJ·mol-1)=-6 kJ·mol-1。
答案 (1)2ΔH+4ΔH-ΔH
2 3 1
(2)-46 N +3H ===NH +2H
ad ad ad ad
(3)a-4b-c
(4)-6 kJ·mol-1