文档内容
训练(十八) 氯及其重要化合物
1.(2021·湖南常德检测)下列说法正确的是( )
①氯气的性质活泼,它与氢气混合后立即发生爆炸 ②实验室制取氯气时,为了防止环
境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于久置氯水的 ④
检验HCl气体中是否混有Cl,方法是将气体通入硝酸银溶液 ⑤除去HCl气体中的Cl,可
2 2
将气体通入饱和食盐水中
A.①②③ B.②③④
C.③ D.③⑤
C [采用“排除法”分析:氯气与氢气混合,达到爆炸极限,在光照的条件下才能发生
爆炸,①错,氢氧化钙溶液中溶质含量少,实验中常用氢氧化钠溶液吸收多余的氯气,②错,
排除A、B项;HCl气体与AgNO 溶液可产生沉淀,④错;将气体通入饱和食盐水中,除去的
3
是HCl气体,而不是Cl,⑤错,排除D项。]
2
2.(2021·吉林延边二中检测)从海带中提取碘单质,成熟的工艺流程如下。下列关于海水
制碘的说法,不正确的是( )
干海带――→海带灰――→悬浊液――→滤液――→碘水――→
I 的CCl 溶液――→I
2 4 2
A.实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌
B.含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C.在碘水中加入几滴淀粉溶液,溶液变蓝色
D.碘水加入CCl 得到I 的CCl 溶液,该操作为“萃取”
4 2 4
A [灼烧固体时应在坩埚中,A项错误;HO 能将I-氧化为I,B项正确。淀粉溶液遇到
2 2 2
单质碘(I),溶液变成蓝色,C项正确;I 在CCl 中的溶解度大于在水中的溶解度,碘水加入
2 2 4
CCl ,萃取碘水中的I,经分液得到I 的CCl 溶液,D项正确。]
4 2 2 4
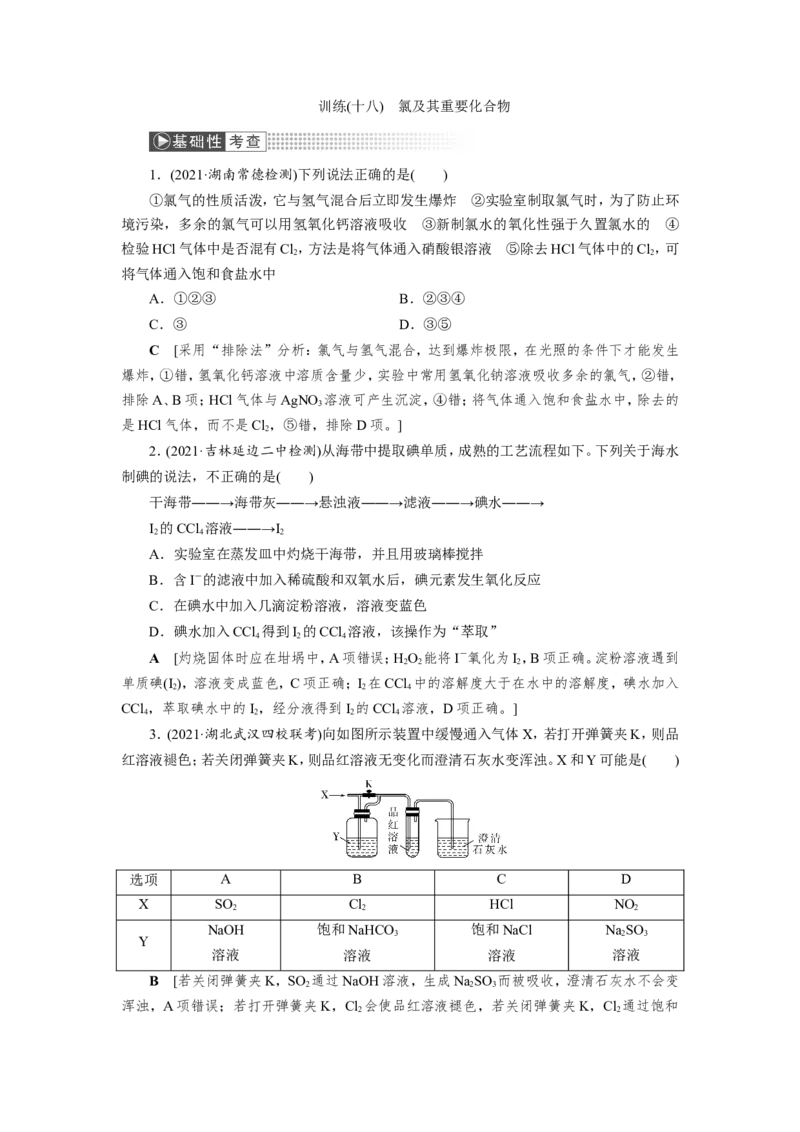
3.(2021·湖北武汉四校联考)向如图所示装置中缓慢通入气体X,若打开弹簧夹K,则品
红溶液褪色;若关闭弹簧夹K,则品红溶液无变化而澄清石灰水变浑浊。X和Y可能是( )
选项 A B C D
X SO Cl HCl NO
2 2 2
NaOH 饱和NaHCO 饱和NaCl NaSO
3 2 3
Y
溶液 溶液 溶液 溶液
B [若关闭弹簧夹K,SO 通过NaOH溶液,生成NaSO 而被吸收,澄清石灰水不会变
2 2 3
浑浊,A项错误;若打开弹簧夹K,Cl 会使品红溶液褪色,若关闭弹簧夹K,Cl 通过饱和
2 2NaHCO 溶液,产生CO,会使澄清石灰水变浑浊,B项正确;若打开弹簧夹K,HCl不会使品
3 2
红溶液褪色,若关闭弹簧夹K,HCl通过饱和NaCl溶液,HCl被吸收,澄清石灰水不会变浑浊,
C项错误;若关闭弹簧夹K,NO 通过NaSO 溶液时,NO 先与水反应生成HNO 和NO,然后
2 2 3 2 3
HNO 将NaSO 氧化,得到NaSO 和NO,NO不能使澄清石灰水变浑浊,D项错误。]
3 2 3 2 4
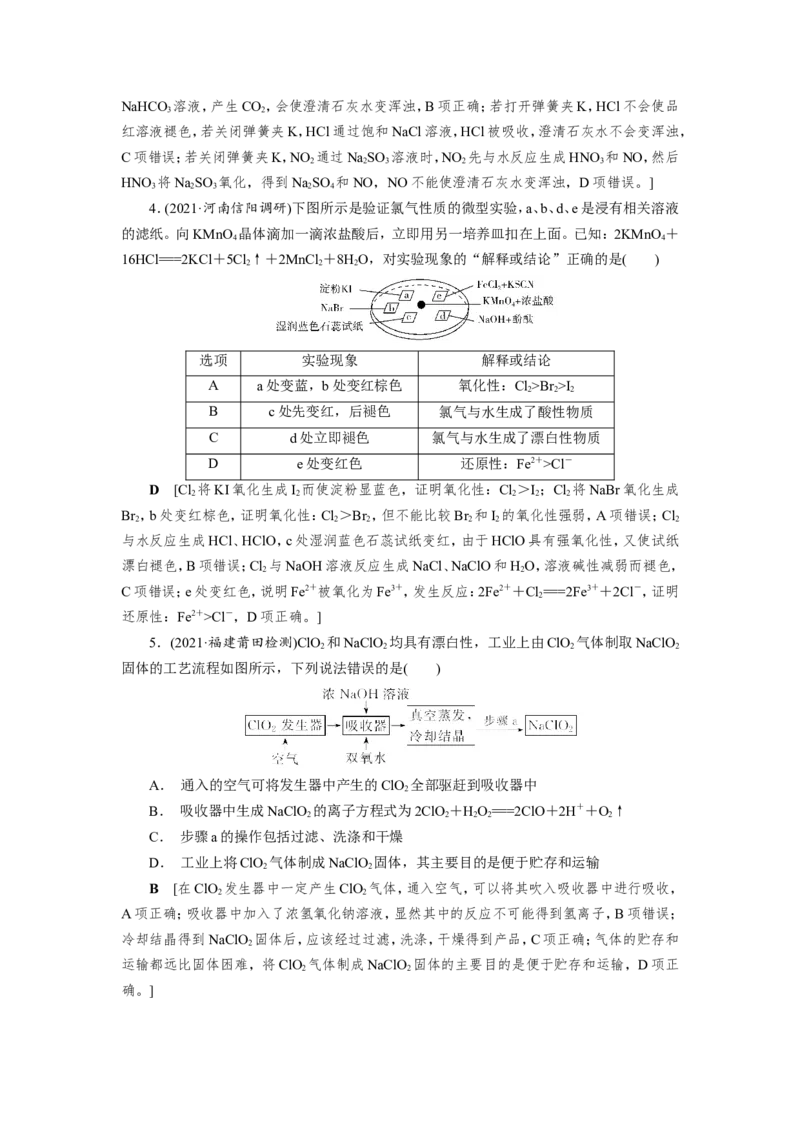
4.(2021·河南信阳调研)下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液
的滤纸。向KMnO 晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO +
4 4
16HCl===2KCl+5Cl↑+2MnCl +8HO,对实验现象的“解释或结论”正确的是( )
2 2 2
选项 实验现象 解释或结论
A a处变蓝,b处变红棕色 氧化性:Cl>Br >I
2 2 2
B c处先变红,后褪色 氯气与水生成了酸性物质
C d处立即褪色 氯气与水生成了漂白性物质
D e处变红色 还原性:Fe2+>Cl-
D [Cl 将KI氧化生成I 而使淀粉显蓝色,证明氧化性:Cl>I;Cl 将NaBr氧化生成
2 2 2 2 2
Br ,b处变红棕色,证明氧化性:Cl>Br ,但不能比较Br 和I 的氧化性强弱,A项错误;Cl
2 2 2 2 2 2
与水反应生成HCl、HClO,c处湿润蓝色石蕊试纸变红,由于HClO具有强氧化性,又使试纸
漂白褪色,B项错误;Cl 与NaOH溶液反应生成NaCl、NaClO和HO,溶液碱性减弱而褪色,
2 2
C项错误;e处变红色,说明Fe2+被氧化为Fe3+,发生反应:2Fe2++Cl===2Fe3++2Cl-,证明
2
还原性:Fe2+>Cl-,D项正确。]
5.(2021·福建莆田检测)ClO 和NaClO 均具有漂白性,工业上由ClO 气体制取NaClO
2 2 2 2
固体的工艺流程如图所示,下列说法错误的是( )
A. 通入的空气可将发生器中产生的ClO 全部驱赶到吸收器中
2
B. 吸收器中生成NaClO 的离子方程式为2ClO +HO===2ClO+2H++O↑
2 2 2 2 2
C. 步骤a的操作包括过滤、洗涤和干燥
D. 工业上将ClO 气体制成NaClO 固体,其主要目的是便于贮存和运输
2 2
B [在ClO 发生器中一定产生ClO 气体,通入空气,可以将其吹入吸收器中进行吸收,
2 2
A项正确;吸收器中加入了浓氢氧化钠溶液,显然其中的反应不可能得到氢离子,B项错误;
冷却结晶得到NaClO 固体后,应该经过过滤,洗涤,干燥得到产品,C项正确;气体的贮存和
2
运输都远比固体困难,将ClO 气体制成NaClO 固体的主要目的是便于贮存和运输,D项正
2 2
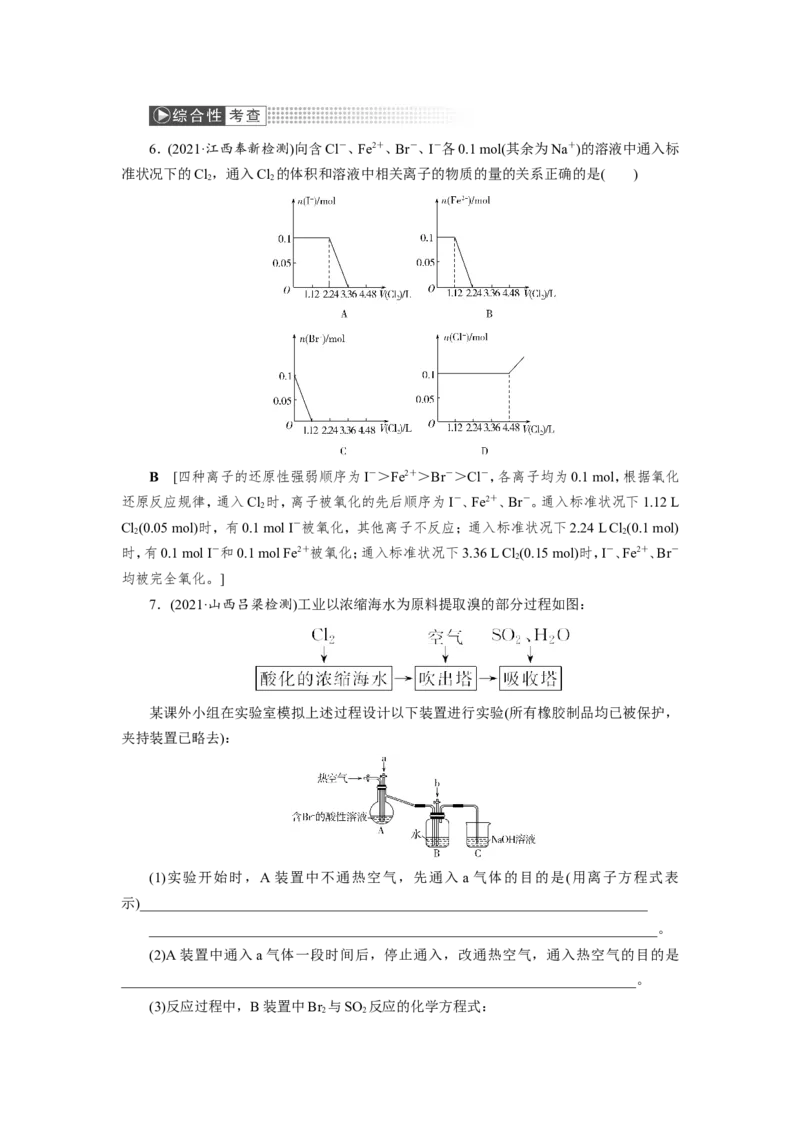
确。]6.(2021·江西奉新检测)向含Cl-、Fe2+、Br-、I-各0.1 mol(其余为Na+)的溶液中通入标
准状况下的Cl,通入Cl 的体积和溶液中相关离子的物质的量的关系正确的是( )
2 2
B [四种离子的还原性强弱顺序为I->Fe2+>Br->Cl-,各离子均为0.1 mol,根据氧化
还原反应规律,通入Cl 时,离子被氧化的先后顺序为I-、Fe2+、Br-。通入标准状况下1.12 L
2
Cl(0.05 mol)时,有0.1 mol I-被氧化,其他离子不反应;通入标准状况下2.24 L Cl (0.1 mol)
2 2
时,有0.1 mol I-和0.1 mol Fe2+被氧化;通入标准状况下3.36 L Cl (0.15 mol)时,I-、Fe2+、Br-
2
均被完全氧化。]
7.(2021·山西吕梁检测)工业以浓缩海水为原料提取溴的部分过程如图:
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,
夹持装置已略去):
(1)实验开始时,A 装置中不通热空气,先通入 a 气体的目的是(用离子方程式表
示)________________________________________________________________________
________________________________________________________________________。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气,通入热空气的目的是
_________________________________________________________________________。
(3)反应过程中,B装置中Br 与SO 反应的化学方程式:
2 2________________________________________________________________________。
(4)C装置的作用是__________________________________________。
解析 (1)欲使溴离子变成溴单质,则通入的a气体能和溴离子发生反应生成溴单质,氯
气能和溴离子发生置换反应生成溴单质,离子方程式为Cl+2Br-===2Cl-+Br 。
2 2
(2)溴易挥发,升高温度促进其挥发,所以通入热空气的目的是吹出Br 。
2
(3)溴有强氧化性,能和二氧化硫在水中发生氧化还原反应,反应的化学方程式为SO +
2
Br +2HO===H SO +2HBr。
2 2 2 4
(4)氯气不可能完全反应,氯气和溴离子反应生成溴单质,未反应的二氧化硫、氯气和溴
都有毒,不能直接排空,且这几种物质都能和碱反应,所以C装置是尾气处理装置,即C的作
用是吸收未反应的Cl、Br 和SO 。
2 2 2
答案 (1)Cl +2Br-===2Cl-+Br
2 2
(2)将溴从蒸馏烧瓶A中吹出
(3)SO +Br +2HO===H SO +2HBr
2 2 2 2 4
(4)吸收未反应完的Cl、Br 、SO 等有毒气体,防止污染空气
2 2 2