文档内容
1.(2023·天津模拟)晶体具有各向异性,如蓝晶石(AlO·SiO)在不同方向上的硬度不同;又
2 3 2
如石墨在与层垂直的方向上的电导率是与层平行的方向上的电导率的。晶体的各向异性主要
表现在( )
①硬度 ②导热性 ③导电性 ④光学性质
A.①③ B.②④
C.①②③ D.①②③④
2.(2023·杭州高三模拟)下列关于物质的聚集状态的说法不正确的是( )
A.X射线衍射实验可以区分晶体和非晶体,也可以获得分子的键长和键角的数值
B.自然形成的水晶柱是晶体,从水晶柱上切削下来的粉末不是晶体
C.缺角的NaCl晶体在饱和NaCl溶液中慢慢生长为规则的多面体,体现了晶体的自范性
D.液晶具有液体的流动性,在导热性、光学性质等物理性质方面具有类似晶体的各向异性
3.下列说法错误的是( )
A.只含分子的晶体一定是分子晶体
B.碘晶体升华时破坏了共价键
C.几乎所有的酸都属于分子晶体
D.稀有气体中只含原子,但稀有气体的晶体属于分子晶体
4.如图是金属晶体内部的电子气理论示意图。电子气理论可以用来解释金属的性质,其中
正确的是( )
A.金属能导电是因为金属阳离子在外加电场作用下定向移动
B.金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导
C.金属具有延展性是因为在外力的作用下,金属中各原子层间会出现相对滑动,但自由电
子可以起到润滑剂的作用,使金属不会断裂
D.合金与纯金属相比,由于增加了不同的金属或非金属,使电子数目增多,所以合金的延
展性比纯金属强,硬度比纯金属小
5.根据下表中给出的有关数据,判断下列说法错误的是( )
AlCl SiCl 晶体硼 金刚石 晶体硅
3 4
熔点/℃ 190 -68 2 300 >3 550 1 415沸点/℃ 178 57 2 550 4 827 2 355
A.SiCl 是分子晶体
4
B.晶体硼是共价晶体
C.AlCl 是分子晶体,加热能升华
3
D.金刚石中的C—C比晶体硅中的Si—Si弱
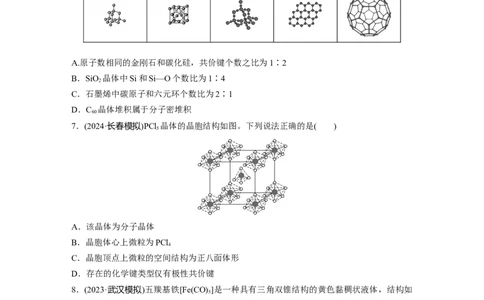
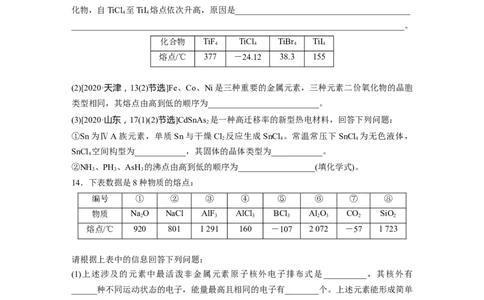
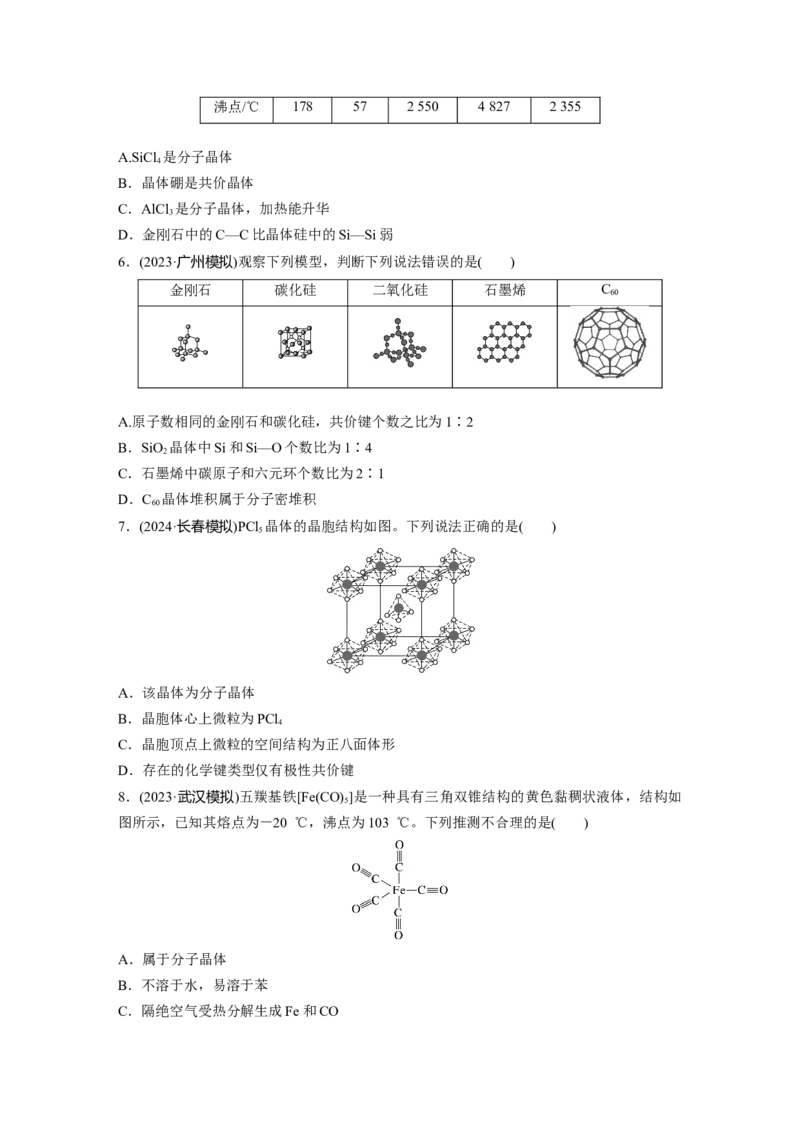
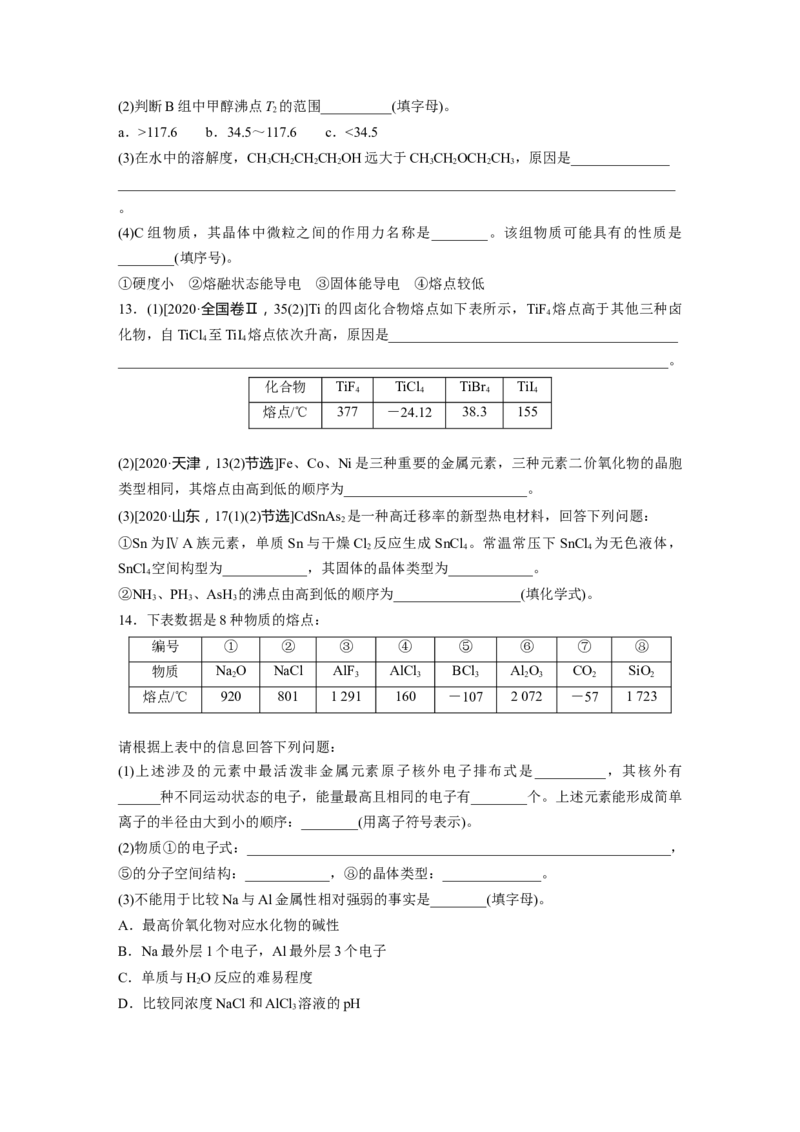
6.(2023·广州模拟)观察下列模型,判断下列说法错误的是( )
金刚石 碳化硅 二氧化硅 石墨烯 C
60
A.原子数相同的金刚石和碳化硅,共价键个数之比为1∶2
B.SiO 晶体中Si和Si—O个数比为1∶4
2
C.石墨烯中碳原子和六元环个数比为2∶1
D.C 晶体堆积属于分子密堆积
60
7.(2024·长春模拟)PCl 晶体的晶胞结构如图。下列说法正确的是( )
5
A.该晶体为分子晶体
B.晶胞体心上微粒为PCl
4
C.晶胞顶点上微粒的空间结构为正八面体形
D.存在的化学键类型仅有极性共价键
8.(2023·武汉模拟)五羰基铁[Fe(CO) ]是一种具有三角双锥结构的黄色黏稠状液体,结构如
5
图所示,已知其熔点为-20 ℃,沸点为103 ℃。下列推测不合理的是( )
A.属于分子晶体
B.不溶于水,易溶于苯
C.隔绝空气受热分解生成Fe和COD.每个Fe(CO) 粒子中含20个σ键
5
9.(2023·山东淄博模拟)铝的卤化物AlX(X=Cl、Br、I)气态时以Al X 双聚形态存在,下列
3 2 6
说法错误的是( )
性质 AlF AlCl AlBr AlI
3 3 3 3
熔点/℃ 1 290 192.4 97.8 189.4
沸点/℃ 1 272 180 256 382
A.AlF 晶体类型与其他三种不同
3
B.1 mol Al Cl 中所含配位键数目为4N
2 6 A
C.Al X 中Al、X原子价电子层均满足8e-结构
2 6
D.AlCl 熔点高于AlBr 的原因是Cl的电负性大于Br,具有一定离子晶体特征
3 3
10.(2022·山东,5)AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体
中只存在N—Al、N—Ga。下列说法错误的是( )
A.GaN的熔点高于AlN
B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化
D.晶体中所有原子的配位数均相同
11.X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中的含量仅次于
Y,W可以形成自然界中硬度最大的共价晶体。下列叙述错误的是( )
A.XY晶体的熔点高于WX 晶体的熔点
2 4
B.固态XY 是分子晶体
2 2
C.ZW是共价晶体,其硬度比Z晶体的大
D.Z、W是同一主族的元素,Z、W与元素Y形成的晶体都是共价晶体
12.下表给出了三组物质的相关性质数据:
A组(熔点/℃) B组(沸点/℃) C组(晶格能/ kJ·mol-1)
金刚石:3 550 CHOH:T NaCl:a
3 2
石墨:3 850 CHCHCHCHOH:117.6 NaBr:b
3 2 2 2
碳化硅:T CHCHOCH CH:34.5 MgO:c
1 3 2 2 3
回答下列问题:
(1)A组中的碳化硅属于________晶体,碳化硅的沸点T________(填“大于”“小于”或
1
“ 等 于 ” )3 350 , 石 墨 沸 点 高 于 金 刚 石 的 原 因 是
_________________________________________
______________________________________________________________________________。(2)判断B组中甲醇沸点T 的范围__________(填字母)。
2
a.>117.6 b.34.5~117.6 c.<34.5
(3)在水中的溶解度,CHCHCHCHOH远大于CHCHOCH CH,原因是______________
3 2 2 2 3 2 2 3
_______________________________________________________________________________
。
(4)C组物质,其晶体中微粒之间的作用力名称是________。该组物质可能具有的性质是
________(填序号)。
①硬度小 ②熔融状态能导电 ③固体能导电 ④熔点较低
13.(1)[2020·全国卷Ⅱ,35(2)]Ti的四卤化合物熔点如下表所示,TiF 熔点高于其他三种卤
4
化物,自TiCl 至TiI 熔点依次升高,原因是_________________________________________
4 4
______________________________________________________________________________。
化合物 TiF TiCl TiBr TiI
4 4 4 4
熔点/℃ 377 -24.12 38.3 155
(2)[2020·天津,13(2)节选]Fe、Co、Ni是三种重要的金属元素,三种元素二价氧化物的晶胞
类型相同,其熔点由高到低的顺序为__________________________。
(3)[2020·山东,17(1)(2)节选]CdSnAs 是一种高迁移率的新型热电材料,回答下列问题:
2
①Sn为ⅣA族元素,单质Sn与干燥Cl 反应生成SnCl 。常温常压下SnCl 为无色液体,
2 4 4
SnCl 空间构型为____________,其固体的晶体类型为____________。
4
②NH 、PH 、AsH 的沸点由高到低的顺序为__________________(填化学式)。
3 3 3
14.下表数据是8种物质的熔点:
编号 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
物质 NaO NaCl AlF AlCl BCl Al O CO SiO
2 3 3 3 2 3 2 2
熔点/℃ 920 801 1 291 160 -107 2 072 -57 1 723
请根据上表中的信息回答下列问题:
(1)上述涉及的元素中最活泼非金属元素原子核外电子排布式是__________,其核外有
______种不同运动状态的电子,能量最高且相同的电子有________个。上述元素能形成简单
离子的半径由大到小的顺序:________(用离子符号表示)。
(2)物质①的电子式:____________________________________________________________,
⑤的分子空间结构:____________,⑧的晶体类型:______________。
(3)不能用于比较Na与Al金属性相对强弱的事实是________(填字母)。
A.最高价氧化物对应水化物的碱性
B.Na最外层1个电子,Al最外层3个电子
C.单质与HO反应的难易程度
2
D.比较同浓度NaCl和AlCl 溶液的pH
3(4)③比④熔点高出很多,其原因是________________________________________________
______________________________________________________________________________。
①和②都属于离子晶体,但①比②的熔点高,请解释原因:__________________________
______________________________________________________________________________。