文档内容
考点 22 化学平衡状态与化学平衡
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
化学平衡状态 2022湖北卷13题,3分;
2023北京卷4题,3分;2023广东卷15题,4分;2023山东卷
14题,4分;2022海南卷8题,2分;2022北京卷12题,3
影响化学平衡移动的因素
分;2022浙江6月选考19题,2分;2021北京卷10题,3分;
2021辽宁卷11题,3分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,
高考对化学平衡的考查,往往通过化学平衡的特征及化学平衡常数的计算和理解进行,化学平衡常数
是高考热点。高考围绕勒夏特列原理的理解,通过实验、判断、图象、计算等形式对化学平衡移动进行综
合考查。
【备考策略】
在复习中一是要注意对基础知识的理解,特别是要理解好化学平衡的含义;二是要注意在做题时总结
解题的基本规律,同时也要提高利用这些原理分析生产、生活和科学研究领域中具体问题的能力。
【命题预测】
预计2024年高考试题命题的创新性、探究性会进一步提升,着重考查化学化学平衡移动在社会生产、
生活、科学等领域的应用, 考查问题多样化的平衡图象问题、设计新颖的平衡计算及通过图象、表格等
获取信息、数据等试题的情境上、取材上都有所创新,且与元素化合物知识结合也日趋紧密
考法 1 化学平衡状态
1.可逆反应
(1)定义
在同一条件下,既可以向正反应方向进行,同时又可以向逆反应方向进行的化学反应。
(2)特点
①二同:A.相同条件下;B.正、逆反应同时进行。②一小:反应物与生成物同时存在;任一组分的转化率都小于(填“大于”或“小于”)100%。
(3)表示
在方程式中用“ ”表示。
2.化学平衡状态
(1)概念
一定条件下的可逆反应中,正反应速率与逆反应速率相等,反应体系中所有参加反应的物质的质量或
浓度保持不变的状态。
(2)建立
(3)平衡特点
3.判断化学平衡状态的两种方法
(1)动态标志:v =v ≠0
正 逆
①同种物质:同一物质的生成速率等于消耗速率。
②不同物质:必须标明是“异向”的反应速率关系。如aA+bBcC+dD,=时,反应达到平衡状
态。
(2)静态标志:各种“量”不变
①各物质的质量、物质的量或浓度不变。
②各物质的百分含量(物质的量分数、质量分数等)不变。
③温度、压强(化学反应方程式两边气体体积不相等)或颜色(某组分有颜色)不变。
总之,若物理量由变量变成了不变量,则表明该可逆反应达到平衡状态;若物理量为“不变量”,则
不能作为平衡标志。
1.化学平衡状态的特征概括为逆、等、动、定、变,即:2.不能作为“标志”的四种情况
(1)反应组分的物质的量之比等于化学方程式中相应物质的化学计量数之比。
(2)恒温恒容下的体积不变的反应,体系的压强或总物质的量不再随时间而变化,如2HI(g)
H(g)+I(g)。
2 2
(3)全是气体参加的体积不变的反应,体系的平均相对分子质量不再随时间而变化,如2HI(g)
H(g)+I(g)。
2 2
(4)全是气体参加的反应,恒容条件下体系的密度保持不变。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)在化学平衡建立过程中,v 一定大于v ( )
正 逆
(2)恒温恒容下进行的可逆反应:2SO (g)+O(g) 2SO (g),当SO 的生成速率与SO 的消耗速率
2 2 3 3 2
相等时,反应达到平衡状态( )
(3)在一定条件下,向密闭容器中充入1 mol N 和3 mol H 充分反应,生成2 mol NH ( )
2 2 3
(4)任何可逆反应都有一定限度,达到了化学平衡状态即达到了该反应的限度( )
(5)化学反应达到限度时,正逆反应速率相等( )
(6)化学反应的限度可以通过改变条件而改变( )
(7)当一个化学反应在一定条件下达到限度时,反应即停止( )
答案:(1)× (2) × (3)× (4)√ (5)√ (6)√ (7)×
例1 下列描述的化学反应状态,不一定是平衡状态的是( )
A.H(g)+Br (g) 2HBr(g),恒温、恒容下,反应体系中气体的颜色保持不变
2 2
B.2NO (g) NO(g),恒温、恒容下,反应体系中气体的压强保持不变
2 2 4
C.CaCO (s) CO(g)+ CaO(s),恒温、恒容下,反应体系中气体的密度保持不变
3 2
D.N(g)+3H(g) 2NH (g),反应体系中H 与N 的物质的量之比保持3:1
2 2 3 2 2【答案】D
【解析】A项,H(g)+Br (g) 2HBr(g) 恒温、恒容下,反应体系中气体的颜色保持不变,说明溴
2 2
单质的浓度不再变化,达到了平衡,选项A不符合题意;B项,2NO (g) NO(g)是前后气体系数和
2 2 4
变化的反应,当恒温、恒容下,反应体系中气体的压强保持不变,达到了平衡,选项B不符合题意;C项,
CaCO (s) CO(g)+CaO(s) 恒温、恒容下,反应体系中气体的密度等于气体质量和体积的比值,质量变
3 2
化,体积不变,所以密度变化,当气体密度保持不变的状态是平衡状态,选项C不符合题意;D项,
3H(g)+N(g) 2NH (g) 反应体系中H 与N 的物质的量之比保持3:1,不能证明正逆反应速率相等,
2 2 3 2 2
不一定是平衡状态,选项D符合题意。
例2 一定温度下,反应NO(g) 2NO (g)的焓变为ΔH。现将1 mol N O 充入一恒压密闭容器
2 4 2 2 4
中,下列示意图正确且能说明反应达到平衡状态的是( )
A.①② B.②④ C.③④ D.①④
【答案】D
【解析】ΔH是恒量,不能作为判断平衡状态的标志;该反应是充入 1 mol N O ,正反应速率应是逐
2 4
渐减小直至不变,③曲线趋势不正确。
对点1 将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒温下使
其达到分解平衡NH COONH(s) 2NH (g)+CO (g),判断该分解反应已经达到化学平衡的是( )
2 4 3 2
A.2v(NH )=v(CO ) B.密闭容器中混合气体的密度不变
3 2
C.密闭容器中混合气体平均分子量不变 D.密闭容器中氨气的体积分数不变
【答案】B
【解析】当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生
的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变
化到定值时,说明可逆反应到达平衡状态。A项,没有指明正、逆速率,无法判断正逆反应速率是否相等,
故A错误;B项,随反应进行混合气体的质量增大,容器的容积不变,反应混合气体的密度增大,当密度
不再变化,说明到达平衡状态,故B正确;C项,该反应中气体只有NH 和CO,且二者的物质的量之始
3 2
终为2:1,则气体的平均分子量为定值,无法根据混合气体的平均分子量判断平衡状态,故C错误;D项,
反应混合气体只有NH 和CO,且二者物质的量之比始终为2:1,氨体积分数始终不变,所以不能说明到
3 2达平衡,故D错误;故选B。
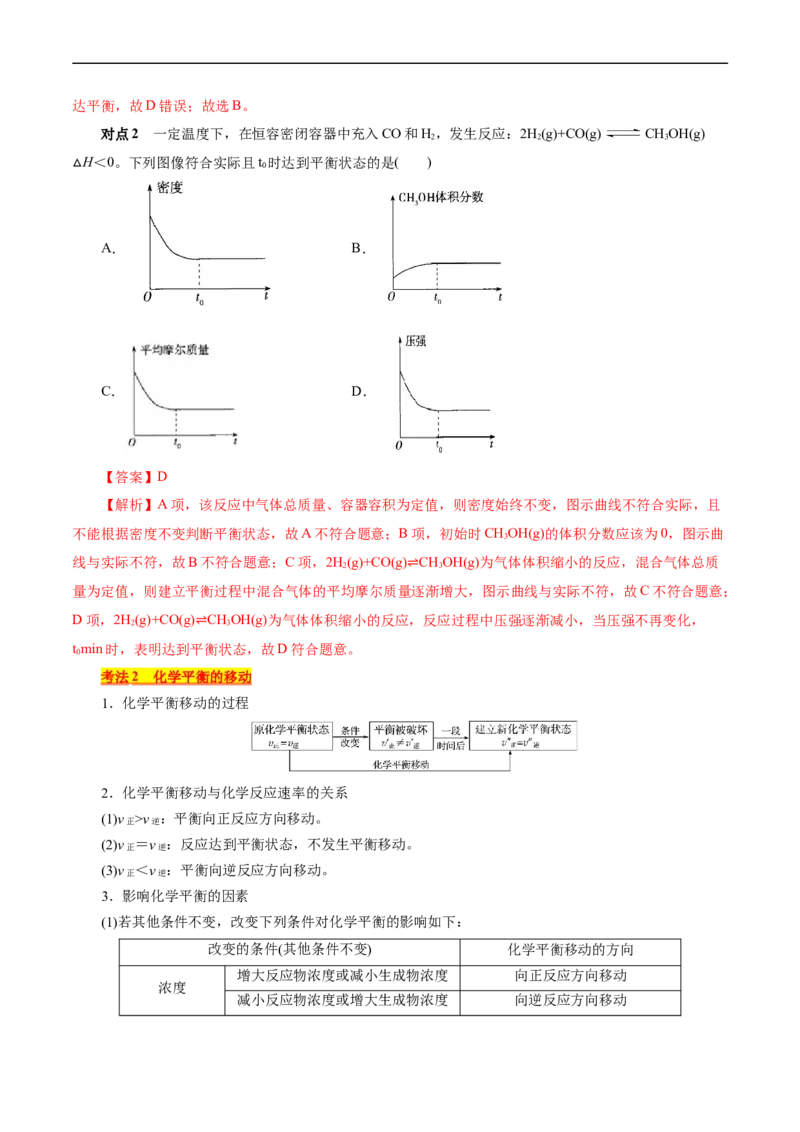
对点2 一定温度下,在恒容密闭容器中充入CO和H,发生反应:2H(g)+CO(g) CHOH(g)
2 2 3
H<0。下列图像符合实际且t 时达到平衡状态的是( )
0
△
A. B.
C. D.
【答案】D
【解析】A项,该反应中气体总质量、容器容积为定值,则密度始终不变,图示曲线不符合实际,且
不能根据密度不变判断平衡状态,故A不符合题意;B项,初始时CHOH(g)的体积分数应该为0,图示曲
3
线与实际不符,故B不符合题意;C项,2H(g)+CO(g) CHOH(g)为气体体积缩小的反应,混合气体总质
2 3
量为定值,则建立平衡过程中混合气体的平均摩尔质量⇌逐渐增大,图示曲线与实际不符,故C不符合题意;
D项,2H(g)+CO(g) CHOH(g)为气体体积缩小的反应,反应过程中压强逐渐减小,当压强不再变化,
2 3
t
0
min时,表明达到平⇌衡状态,故D符合题意。
考法 2 化学平衡的移动
1.化学平衡移动的过程
2.化学平衡移动与化学反应速率的关系
(1)v >v :平衡向正反应方向移动。
正 逆
(2)v =v :反应达到平衡状态,不发生平衡移动。
正 逆
(3)v <v :平衡向逆反应方向移动。
正 逆
3.影响化学平衡的因素
(1)若其他条件不变,改变下列条件对化学平衡的影响如下:
改变的条件(其他条件不变) 化学平衡移动的方向
增大反应物浓度或减小生成物浓度 向正反应方向移动
浓度
减小反应物浓度或增大生成物浓度 向逆反应方向移动反应前后气体 增大压强 向气体分子总数减小的方向移动
压强(对有气体 体积改变 减小压强 向气体分子总数增大的方向移动
参加的反应) 反应前后气体
改变压强 平衡不移动
体积不变
升高温度 向吸热反应方向移动
温度
降低温度 向放热反应方向移动
催化剂 同等程度改变v 、v ,平衡不移动
正 逆
(2)勒·夏特列原理
如果改变影响化学平衡的条件之一(如温度、压强以及参加反应的物质的浓度),平衡将向着能够减弱
这种改变的方向移动。
(3)“惰性气体”对化学平衡的影响
①恒温恒容条件
原平衡体系―――――→体系总压强增大―→体系中各组分的浓度不变―→平衡不移动。
②恒温恒压条件
原平衡体系―――――→容器容积增大,各反应气体的分压减小→
1.化学平衡移动的分析判断方法
2.解答化学平衡移动类试题的思维建模请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)化学平衡发生移动,化学反应速率一定改变;化学反应速率改变,化学平衡也一定发生移动( )
(2)升高温度,平衡向吸热反应方向移动,此时v 减小,v 增大( )
放 吸
(3)C(s)+CO(g) 2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率v(CO)和CO 的平衡
2 2 2
转化率均增大( )
(4)化学平衡正向移动,反应物的转化率不一定增大( )
(5)向平衡体系FeCl +3KSCN Fe(SCN) +3KCl中加入适量KCl固体,平衡逆向移动,溶液的颜
3 3
色变浅( )
(6)对于2NO (g) NO(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的颜色
2 2 4
变浅( )
答案:(1)× (2) × (3)√ (4)√ (5)× (6)×
例1 (2023•北京卷,4)下列事实能用平衡移动原理解释的是( )
A.HO 溶液中加入少量MnO 固体,促进HO 分解
2 2 2 2 2
B.密闭烧瓶内的NO 和NO 的混合气体,受热后颜色加深
2 2 4
C.铁钉放入浓HNO 中,待不再变化后,加热能产生大量红棕色气体
3
D.锌片与稀HSO 反应过程中,加入少量CuSO 固体,促进H 的产生
2 4 4 2
【答案】B
【解析】A项,MnO 会催化 HO 分解,与平衡移动无关,A项错误;B项,NO 转化为NO 的反应
2 2 2 2 2 4
是放热反应,升温平衡逆向移动, NO 浓度增大,混合气体颜色加深,B项正确;C项,铁在浓硝酸中钝
2
化,加热会使表面的氧化膜溶解,铁与浓硝酸反应生成大量红棕色气体,与平衡移动无关,C项错误;D
项,加入硫酸铜以后,锌置换出铜,构成原电池,从而使反应速率加快,与平衡移动无关,D项错误;故
选B。例2 (2022•海南省选择性考试,8)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭
2 2 2 3 2
容器中达到平衡,下列说法正确的是( )
A.增大压强,v > v ,平衡常数增大
正 逆
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2
C.恒容下,充入一定量的HO(g),平衡向正反应方向移动
2
D.恒容下,充入一定量的CH=CH (g),CH=CH (g)的平衡转化率增大
2 2 2 2
【答案】C
【解析】A项,该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率
增大的幅度大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A
正 逆
不正确;B项,催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B不
3 2
正确;C项,恒容下,充入一定量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;D项,
2 2
恒容下,充入一定量的CH=CH (g),平衡向正反应方向移动,但是CH=CH (g)的平衡转化率减小,D
2 2 2 2
不正确;故选C。
对点1 将NO 装入带活塞的密闭容器中,当反应2NO (g) NO(g)达到平衡后,改变下列一
2 2 2 4
个条件,其中叙述错误的是( )
A.升高温度,气体颜色加深,则此正反应为吸热反应
B.慢慢压缩气体体积,平衡向右移动,混合气体颜色较原来深
C.慢慢压缩气体使体积减小一半,压强增大,但小于原来的两倍
D.恒温恒容时,充入惰性气体,压强增大,平衡不会移动
【答案】A
【解析】A项,NO (g)红棕色、NO(g)无色。升高温度使气体颜色加深,则平衡左移。据平衡移动原
2 2 4
理,逆反应吸热,正反应放热,A项错误;B项,压缩气体体积即加压,平衡向右移动,使体积减小、
c(N O )
n(N O)增大,故c(NO)增大。又据K= 2 4 ,c(NO )增大,混合气体颜色较原来深,B项正确;C项,
2 4 2 4 2
c2 (NO )
2
压缩气体使体积减小,则压强增大。若体积减半时平衡没有移动,则压强加倍。实际平衡右移,使压强小
于原来的两倍,C项正确;D项,恒温恒容时,充入惰性气体,虽然容器内总压强变大,但没有改变
c(NO )、c(NO),正、逆反应速率均不变,化学平衡不会移动,D项正确。
2 2 4
对点2 将等物质的量的N 、H 充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:N(g)
2 2 2
+3H(g) 2NH (g) ΔH<0。当改变某个条件并维持新条件直至达到新的平衡时,下表中关于新平
2 3
衡与原平衡的比较正确的是( )