文档内容
【基础知识】离子反应
考点四 离子共存
【必备知识】
离子共存:指离子之间 不发生任何反应 , 不能大量共存。
一、离子反应类型
1、复分解反应型
①因生成沉淀(或微溶性物质)不能大量共存
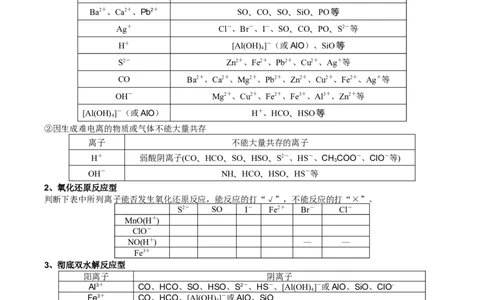
离子 不能大量共存的离子
Ba2+、Ca2+、Pb2+ SO、CO、SO、SiO、PO等
Ag+ Cl-、Br-、I-、SO、CO、PO、S2-等
H+ [Al(OH) ]-(或AlO)、SiO等
4
S2- Zn2+、Fe2+、Pb2+、Cu2+、Ag+等
CO Ba2+、Ca2+、Mg2+、Pb2+、Zn2+、Cu2+、Fe2+、Ag+等
OH- Mg2+、Cu2+、Fe2+、Fe3+、Al3+、Zn2+等
[Al(OH) ]-(或AlO) H+、HCO、HSO等
4
②因生成难电离的物质或气体不能大量共存
离子 不能大量共存的离子
H+ 弱酸阴离子(CO、HCO、SO、HSO、S2-、HS-、CH COO-、ClO-等)
3
OH- NH、HCO、HSO、HS-等
2、氧化还原反应型
判断下表中所列离子能否发生氧化还原反应,能反应的打“√”,不能反应的打“×”。
S2- SO I- Fe2+ Br- Cl-
MnO(H+)
ClO-
NO(H+) — —
Fe3+
3、彻底双水解反应型
阳离子 阴离子
Al3+ CO、HCO、SO、HSO、S2-、HS-、[Al(OH) ]-或AlO、SiO、ClO-
4
Fe3+ CO、HCO、[Al(OH) ]-或AlO、SiO
4
4、络合反应型
Fe3+与SCN-、C HO-
6 5
二、解题注意事项
在做有关离子共存题目时,应注意题干中的“关键词”,如
①“一定大量共存”还是“可能大量共存”。
②“透明溶液”还是“无色透明溶液”,CuSO 溶液为蓝色透明溶液,NaCl为无色透明溶液。
4
常见有颜色的离子:Cu2+、Fe3+、Fe2+、CrO、Cr3+、CrO2-、MnO、[Fe(SCN) ]3-等。
2 7 6
③限定&隐含条件
指出下列溶液的酸碱性① 使石蕊变红: 性
② 使甲基橙/红变红: 性
③ 使pH试纸显蓝色: 性
④ 使酚酞变蓝: 性
⑤ 常温下,c(H+)或K /c(OH-)>10-7mol·L-1: 性
W
⑥ c(H+)/c(OH-)<1: 性
⑦ 与Mg反应放出H : 性,且不含NO
2
⑧ 与Al反应放出H : 性
2
⑨ 由水电离出c(H+) < 10-7 mol·L-1: 性
⑩ 与NH HCO 反应能产生气体的溶液: 性
4 3
⑪ 加入铵盐,加热,产生氨气: 性
⑫ 含有大量Al3+、Fe3+的溶液,隐含溶液呈 性。
⑬ 含有大量S2-、SO的溶液,隐含不是 性,用离子方程式解释:
。
⑭ 含有大量AlO的溶液,隐含是碱性。
⑮ 含有大量S O的溶液,隐含溶液呈 性,用离子方程式解释:
2
。
⑯ 含有大量Cr O2-的溶液,隐含溶液呈 性;含有大量CrO的溶液,隐含溶液呈 性。用离
2 7
子方程式解释: 。
例、下列溶液中,离子一定能大量共存的有 。
(1)使酚酞溶液变红的溶液:Na+、Cl-、SO、Fe3+
(2)使紫色石蕊溶液变红的溶液:Fe2+、Mg2+、NO、Cl-
(3)常温下,c(H+)=1×10-13 mol·L-1的溶液中:NH、Al3+、SO、NO
(4)碳酸氢钠溶液:K+、SO、Cl-、H+
(5)含大量Fe3+的溶液中:NH、Na+、Cl-、SCN-
(6)强碱溶液中:Na+、K+、[Al(OH) ]-(或AlO)、CO
4
(7)常温下,pH=1的溶液中:K+、Fe2+、Cl-、NO
(8)加入铝粉有氢气产生的溶液中:K+、Na+、CO、SO
(9)由水电离出的c (H+)=1×10-12 mol·L-1的溶液:Na+、K+、Cl-、NO
水
(10)c(H+)∶c(OH-)=1∶10-2的溶液:K+、Ba2+、ClO-、CO
(11)澄清透明的溶液中:Fe3+、Mg2+、Br-、Cl-
(12)向含有Fe2+、Cl-、Na+、H+的溶液中滴入HO
2 2
(13)强碱溶液中:S2-、SO、K+
(14)加入Mg能放出H 的溶液中:NO、NH、Cl-、K+、SO
2
(15)中性溶液中:Fe3+、Al3+、NO、I-、Cl-、S2-
(16)使甲基橙变红的溶液中:Ca2+、NH +、CH COO-、Cl-
4 3
(17)=1×10-13 mol·L-1的溶液:Na+、K+、SiO、CO
【题组练习】
1、(2022·湖北,4)下列各组离子在给定溶液中能大量共存的是( )
A.在0.1 mol·L-1氨水中:Ag+、Cu2+、NO、SO
B.在0.1 mol·L-1氯化钠溶液中:Fe3+、I-、Ba2+、HCO
C.在0.1 mol·L-1醋酸溶液中:SO、NH、Br-、H+
D.在0.1 mol·L-1硝酸银溶液中:K+、Cl-、Na+、CO
2、(2022·重庆卷)下列操作中,不会影响溶液中K+、Al3+、Fe3+、Ba2+、Cl-、NO 等离子大量共存的是()
A.加入ZnSO B.加入Fe粉 C.通入NH D.通入CO
4 3 2
3、(2022·天津卷)25℃时,下列各组离子中可以在水溶液中大量共存的是( )
A.H+、NH、ClO-、Cl- B.H+、Mg2+、I-、NO
C.Na+、Al3+、HCO、SO D.K+、Na+、SO、OH-
4、(2021·湖南,12)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
粒子组 判断和分析
A Na+、Al3+、Cl-、NH ·H O 不能大量共存,因发生反应:Al3++4NH ·H O===[Al(OH) ]-+4NH
3 2 3 2 4
B H+、K+、SO、SO 不能大量共存,因发生反应:2H++SO===S↓+SO ↑+HO
2 2 2 2
C Na+、Fe3+、SO、HO 能大量共存,粒子间不反应
2 2
D H+、Na+、Cl-、MnO 能大量共存,粒子间不反应
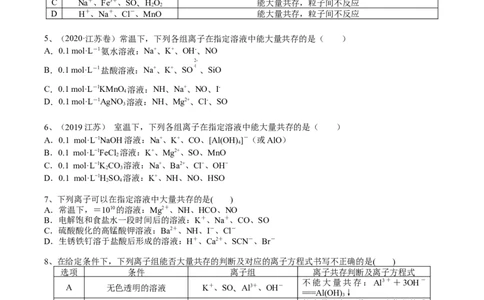
5、(2020·江苏卷)常温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1氨水溶液:Na+、K+、OH-、NO
B.0.1 mol·L-1盐酸溶液:Na+、K+、SO 、SiO
C.0.1 mol·L-1KMnO 溶液:NH、Na+、NO、I-
4
D.0.1 mol·L-1AgNO 溶液:NH、Mg2+、Cl-、SO
3
6、(2019江苏) 室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L−1NaOH溶液:Na+、K+、CO、[Al(OH) ]-(或AlO)
4
B.0.1 mol·L−1FeCl 溶液:K+、Mg2+、SO、MnO
2
C.0.1 mol·L−1KCO 溶液:Na+、Ba2+、Cl−、OH−
2 3
D.0.1 mol·L−1HSO 溶液:K+、NH、NO、HSO
2 4
7、下列离子可以在指定溶液中大量共存的是( )
A.常温下,=1010的溶液:Mg2+、NH、HCO、NO
B.电解饱和食盐水一段时间后的溶液:K+、Na+、CO、SO
C.硫酸酸化的高锰酸钾溶液:Ba2+、NH、I-、Cl-
D.生锈铁钉溶于盐酸后形成的溶液:H+、Ca2+、SCN-、Br-
8、在给定条件下,下列离子组能否大量共存的判断及对应的离子方程式书写不正确的是( )
选项 条件 离子组 离子共存判断及离子方程式
不能大量共存:Al3++3OH-
A 无色透明的溶液 K+、SO、Al3+、OH-
===Al(OH) ↓
3
能大量共存,通CO 时发生的反
B 通入少量CO Na+、OH-、K+、NO 2
2 应为2OH-+CO===CO+HO
2 2
C 滴加石蕊溶液变红的溶液 Fe2+、Na+、Cl-、NO 能大量共存
D 溶液呈蓝色 K+、Na+、Cl-、SO 能大量共存
9、下列各组澄清溶液中的离子能大量共存,且加入试剂后发生反应的离子方程式书写正确的是( )
选项 离子 试剂 离子方程式
A NH、Na+、Fe3+、S2- 少量铜粉 2Fe3++Cu===2Fe2++Cu2+
B NH、Fe3+、Br-、SO 过量NaS 2Fe3++S2-===2Fe2++S↓
2
C K+、Na+、ClO-、SO 足量SO SO +2ClO-+HO===SO+2HClO
2 2 2
K+、Na+、CO、[Al(OH) ]-(或 H++[Al(OH) ]-===Al(OH) ↓+HO
D 4 少量HCl 4 3 2
AlO) (或AlO-+H++HO===Al(OH) ↓)
2 2 310、下列各组离子能大量共存的是( )
A.Fe3+、Na+、SCN-、SO B.K+、Na+、ClO-、I-
C.Al3+、Ca2+、HCO、NO D.NH、Cu2+、CHCOO-、NO
3
11、下列各组离子中,在指定环境中一定能大量共存的是( )
A.加入酚酞变红的溶液中:S2-、SO、SO、SO、Na+
2
B.能使 试纸变深红的溶液中:K+、SO、CrO、S2-
C.c(H+) = 10-13 mol·L-1溶液中:Mg2+、Cu2+、SO、NO
D.澄清透明的中性溶液:Fe3+、Ba2+、NO、Cl-
12、常温下,下列各组离子在指定溶液中可能大量共存的是( )
A.c(Fe3+) = 0.1 mol·L-1的溶液中:Cu2+、NH、NO、SCN-
B. 的溶液中:Ca2+、Ba2+、HCO、NO
C.使酚酞变红色的溶液:Na+、K+、[Al(OH) ]-(或AlO)、Cr O2-
4 2 7
D.由水电离的c(H+) = 10-12 mol·L-1的溶液中:Na+、NH、I-、SO
13、在酸性溶液中能大量共存且为无色透明溶液的是( )
A.K+、Cl-、MnO、SO B.Na+、SO、Cl-、NO
C.Fe2+、NO、SO、SO D.Na+、K+、HSO、SO
14、孔雀石的主要成分是Cu (OH) CO(含Fe O 、FeCO 、Al O 、SiO 杂质),工业上用孔雀石制备硫酸铜
2 2 3 2 3 3 2 3 2
的第一步用过量硫酸溶解并过滤。常温下,分别取滤液并向其中加入指定物质,反应后的溶液中大量存在
的一组离子正确的是( )
A.加入过量氨水:NH、SO、OH-、Fe3+
B.加入过量稀HNO 溶液:Fe3+、H+、Cu2+、SO、NO、Al3+
3
C.加入过量NaOH溶液:Na+、Fe3+、SO、OH-、[Al(OH) ]-(或AlO)-
4
D.加入过量NaHCO 溶液:Na+、Al3+、SO、HCO
3