文档内容
选择题标准练(二)
1.化学与生产、生活及社会发展密切相关。下列说法错误的是( )
A.德尔塔病毒能在空气中以气溶胶的形式传播,气溶胶属于胶体
B.液化石油气和焦炉煤气均属于清洁燃料,其主要成分相同
C.“煤改气”可以减少SO 等有害物质的排放量,有利于打赢蓝天保卫战
2
D.写春联用的笔(主要是动物毛发)和墨(炭墨烟和动物胶)的原料中都含有蛋白质
答案 B
解析 德尔塔病毒能在空气中以气溶胶的形式传播,气溶胶是以气体为分散剂形成的胶体,
故A正确;动物毛发和动物胶中都含有蛋白质,故D正确。
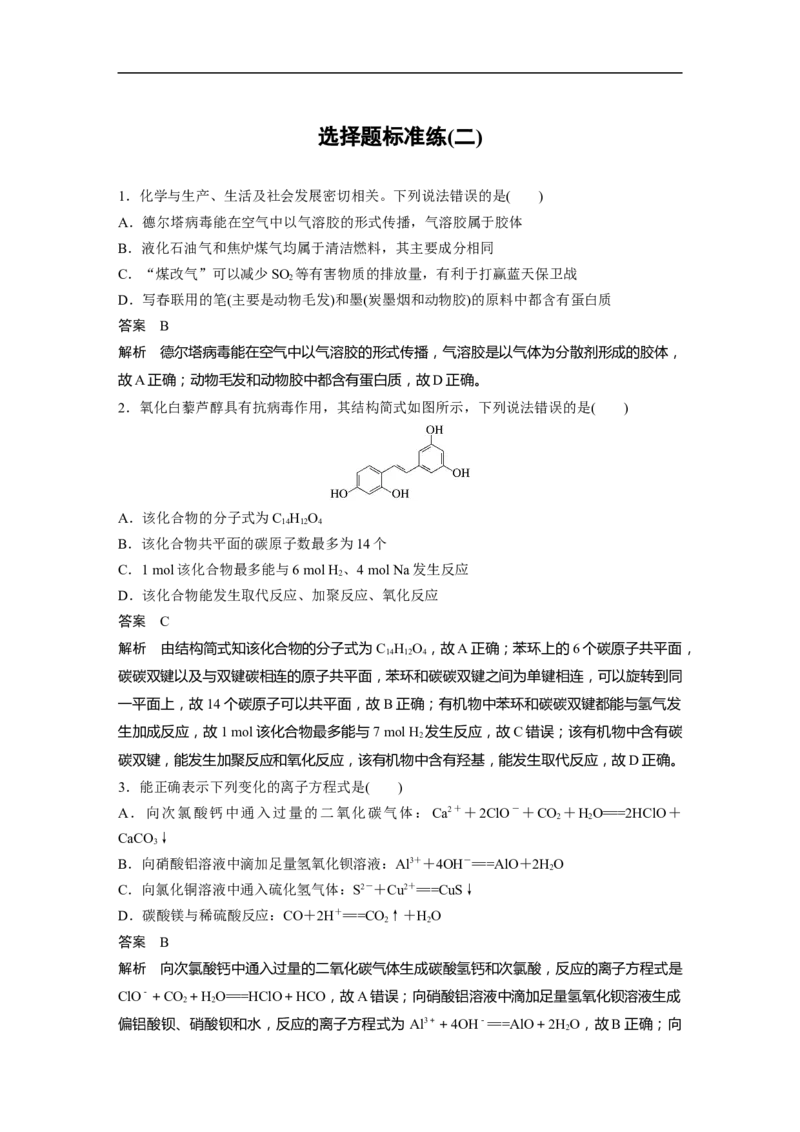
2.氧化白藜芦醇具有抗病毒作用,其结构简式如图所示,下列说法错误的是( )
A.该化合物的分子式为C H O
14 12 4
B.该化合物共平面的碳原子数最多为14个
C.1 mol该化合物最多能与6 mol H 、4 mol Na发生反应
2
D.该化合物能发生取代反应、加聚反应、氧化反应
答案 C
解析 由结构简式知该化合物的分子式为C H O ,故A正确;苯环上的6个碳原子共平面,
14 12 4
碳碳双键以及与双键碳相连的原子共平面,苯环和碳碳双键之间为单键相连,可以旋转到同
一平面上,故14个碳原子可以共平面,故B正确;有机物中苯环和碳碳双键都能与氢气发
生加成反应,故1 mol该化合物最多能与7 mol H 发生反应,故C错误;该有机物中含有碳
2
碳双键,能发生加聚反应和氧化反应,该有机物中含有羟基,能发生取代反应,故D正确。
3.能正确表示下列变化的离子方程式是( )
A.向次氯酸钙中通入过量的二氧化碳气体:Ca2++2ClO-+CO +HO===2HClO+
2 2
CaCO ↓
3
B.向硝酸铝溶液中滴加足量氢氧化钡溶液:Al3++4OH-===AlO+2HO
2
C.向氯化铜溶液中通入硫化氢气体:S2-+Cu2+===CuS↓
D.碳酸镁与稀硫酸反应:CO+2H+===CO↑+HO
2 2
答案 B
解析 向次氯酸钙中通入过量的二氧化碳气体生成碳酸氢钙和次氯酸,反应的离子方程式是
ClO-+CO+HO===HClO+HCO,故A错误;向硝酸铝溶液中滴加足量氢氧化钡溶液生成
2 2
偏铝酸钡、硝酸钡和水,反应的离子方程式为 Al3++4OH-===AlO+2HO,故B正确;向
2氯化铜溶液中通入硫化氢气体生成硫化铜沉淀和盐酸:HS+Cu2+===CuS↓+2H+,故C错
2
误;碳酸镁与稀硫酸反应生成硫酸镁、二氧化碳和水,反应的离子方程式是 MgCO +2H+
3
===Mg2++CO↑+HO,故D错误。
2 2
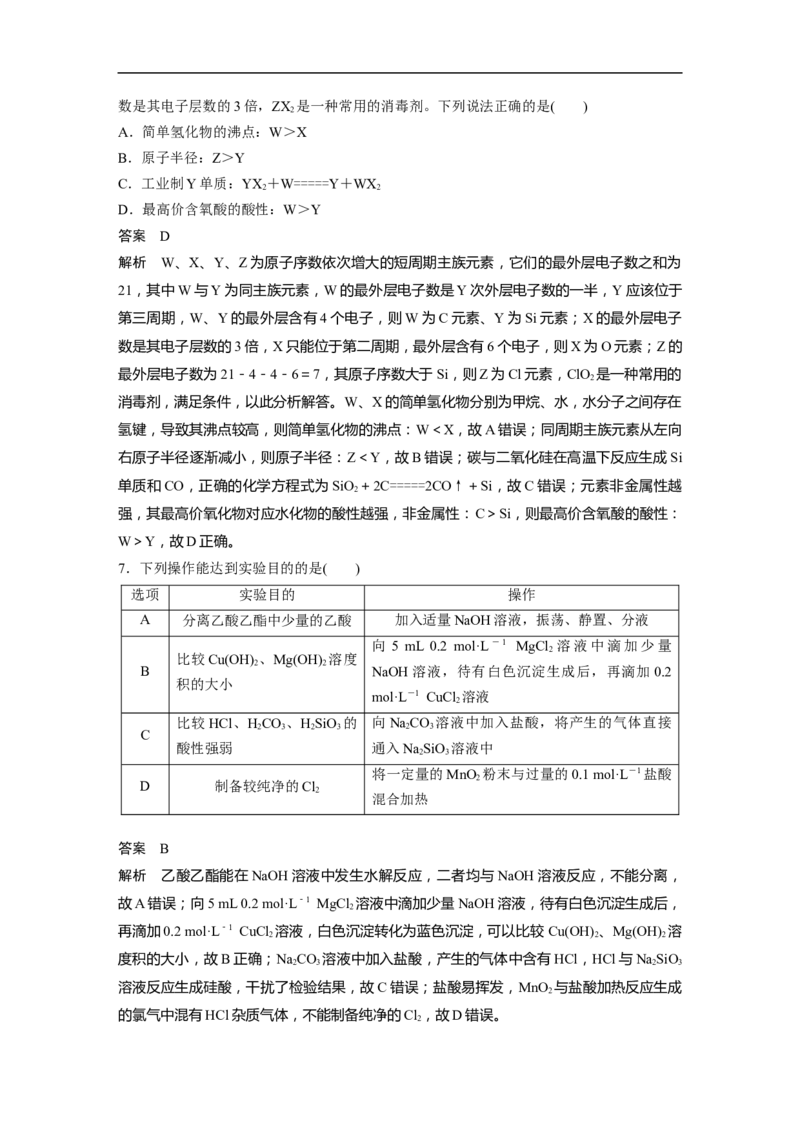
4.在一种微生物细菌作用下苯酚可以转化为CO ,目前,某研究团队利用电化学原理来模
2
拟处理废水中的苯酚(C HOH),其工作原理如图所示。下列说法错误的是( )
6 5
A.a极为正极,M为阳离子交换膜
B.b极的电极反应式为C HOH-28e-+11HO===6CO↑+28H+
6 5 2 2
C.NaCl溶液的作用是增强导电性
D.电池工作过程中,a极室的pH升高
答案 A
解析 由题图可知,此装置为原电池,a极发生还原反应,Cr O转化为Cr(OH) 同时生成氢
2 3
氧根离子,则 M为阴离子交换膜,使氢氧根离子通过,故A错误;b极苯酚发生氧化反应
生成CO ,电极反应式为C HOH-28e-+11HO===6CO↑+28H+,故B正确;电池工作
2 6 5 2 2
过程中,a极室发生反应:Cr O+6e-+7HO===2Cr(OH) +8OH-,a极室的pH升高,故D
2 2 3
正确。
5.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,2.24 L苯中含有的分子数为0.1N
A
B.0.1 mol·L-1 KS溶液中含有的K+数为0.2N
2 A
C.32 g由S、S 组成的混合物中,含S原子数为N
4 8 A
D.1 L 1.0 mol·L-1 FeCl 溶液与足量Cu反应,转移的电子数目为3N
3 A
答案 C
解析 标准状况下,苯为液态,不能用标准气体摩尔体积计算2.24 L苯的物质的量,故A
错误;溶液体积未知,无法计算K+的数目,故B错误;S 、S 均由S原子构成,故32 g混
4 8
合物中含有的S原子的物质的量为1 mol,含S原子数为N ,故C正确;1 L 1.0 mol·L-1
A
FeCl 溶液中含有氯化铁的物质的量为1 mol,FeCl 与Cu反应生成氯化铜和FeCl ,1 mol氯
3 3 2
化铁反应转移的电子数目为N ,故D错误。
A
6.W、X、Y、Z为原子序数依次增大的短周期主族元素,它们的最外层电子数之和为21,
其中W与Y为同主族元素,W的最外层电子数是Y次外层电子数的一半,X的最外层电子数是其电子层数的3倍,ZX 是一种常用的消毒剂。下列说法正确的是( )
2
A.简单氢化物的沸点:W>X
B.原子半径:Z>Y
C.工业制Y单质:YX +W=====Y+WX
2 2
D.最高价含氧酸的酸性:W>Y
答案 D
解析 W、X、Y、Z为原子序数依次增大的短周期主族元素,它们的最外层电子数之和为
21,其中W与Y为同主族元素,W的最外层电子数是Y次外层电子数的一半,Y应该位于
第三周期,W、Y的最外层含有4个电子,则W为C元素、Y为Si元素;X的最外层电子
数是其电子层数的3倍,X只能位于第二周期,最外层含有6个电子,则X为O元素;Z的
最外层电子数为21-4-4-6=7,其原子序数大于Si,则Z为Cl元素,ClO 是一种常用的
2
消毒剂,满足条件,以此分析解答。W、X的简单氢化物分别为甲烷、水,水分子之间存在
氢键,导致其沸点较高,则简单氢化物的沸点:W<X,故A错误;同周期主族元素从左向
右原子半径逐渐减小,则原子半径:Z<Y,故B错误;碳与二氧化硅在高温下反应生成Si
单质和CO,正确的化学方程式为SiO +2C=====2CO↑+Si,故C错误;元素非金属性越
2
强,其最高价氧化物对应水化物的酸性越强,非金属性:C>Si,则最高价含氧酸的酸性:
W>Y,故D正确。
7.下列操作能达到实验目的的是( )
选项 实验目的 操作
A 分离乙酸乙酯中少量的乙酸 加入适量NaOH溶液,振荡、静置、分液
向 5 mL 0.2 mol·L-1 MgCl 溶液中滴加少量
2
比较Cu(OH) 、Mg(OH) 溶度
2 2
B NaOH溶液,待有白色沉淀生成后,再滴加0.2
积的大小
mol·L-1 CuCl 溶液
2
比较HCl、HCO 、HSiO 的 向NaCO 溶液中加入盐酸,将产生的气体直接
2 3 2 3 2 3
C
酸性强弱 通入NaSiO 溶液中
2 3
将一定量的MnO 粉末与过量的0.1 mol·L-1盐酸
2
D 制备较纯净的Cl
2
混合加热
答案 B
解析 乙酸乙酯能在NaOH溶液中发生水解反应,二者均与NaOH溶液反应,不能分离,
故A错误;向5 mL 0.2 mol·L-1 MgCl 溶液中滴加少量NaOH溶液,待有白色沉淀生成后,
2
再滴加0.2 mol·L-1 CuCl 溶液,白色沉淀转化为蓝色沉淀,可以比较 Cu(OH) 、Mg(OH) 溶
2 2 2
度积的大小,故B正确;NaCO 溶液中加入盐酸,产生的气体中含有HCl,HCl与NaSiO
2 3 2 3
溶液反应生成硅酸,干扰了检验结果,故C错误;盐酸易挥发,MnO 与盐酸加热反应生成
2
的氯气中混有HCl杂质气体,不能制备纯净的Cl,故D错误。
2