文档内容
选择题标准练(四)
(选择题1~10题,每小题3分,11~15题,每小题4分,共50分)
1.中国传统文化博大精深,蕴含着丰富的化学知识。下列说法正确的是( )
A.“白釉青花一火成,花从釉里透分明”,釉里红创烧于元代景德镇,红色是因为含有氧化铜
B.“凡酸坏之酒,皆可蒸烧”,该过程利用了物质的溶解性不同
C.苏轼的《格物粗谈》中记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”,推测文
中的“气”在水中能形成分子间氢键
D.“杨梅及苏木污衣,以硫磺烟熏之,然后洗,其红自落”利用了硫黄的漂白性
答案 D
解析 红色是因为含铜彩料在高温条件下生成了氧化亚铜,A错误;“凡酸坏之酒,皆可蒸烧”,该过程
利用了物质的沸点不同,B错误;文中的“气”即乙烯,在水中不能形成分子间氢键,C错误。
2.2024年央视春晚首次应用5G⁃A技术,AI含量高,硬科技霸屏,下列有关说法错误的是( )
A.舞蹈《瓷影》所诠释的青花瓷,其主要原材料为含水的铝硅酸盐
B.晚会采用的LED屏,其发光材料通常是以Si N 为基础,用Al取代部分Si,用O取代部分N后所得的陶
3 4
瓷制作而成
C.5G⁃A技术所需高频通讯材料之一的LCP(液晶高分子)在一定加热状态下一般会变成液晶,液晶既具有液
体的流动性,又表现出类似晶体的各向异性
D.芯片中二氧化硅优异的半导体性能,使得晚会上各种AI技术得以完美体现
答案 D
解析 芯片主要成分是硅单质,故D错误。
3.下列化学用语错误的是( )
‥ ‥
A.NaClO的电子式:Na·O·Cl·
· · ·
‥ ‥
B.2p 能级电子云轮廓图:
x
C.基态Fe3+价层电子轨道表示式:
D.F原子的结构示意图:
答案 A‥ ‥
解析 NaClO是离子化合物,电子式为Na+[ ·O·Cl· ]-,A项错误;p能级电子云轮廓图为哑铃形,B项正确;
· · ·
‥ ‥
基态Fe3+有5个未成对电子,价层电子排布式为3d5,价层电子轨道表示式: ,C项
正确;F为第9号元素,原子的结构示意图: ,D 项正确。
4.设N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.3.1 g白磷(P ,正四面体结构)中含有0.15N 个P—P
4 A
B.3.2 g氧气充分反应,转移的电子数目一定为0.4N
A
C.标准状况下,2.24 L I 与2.24 L H 充分反应,生成的HI分子数目为0.2N
2 2 A
D.5.6 g铁粉与100 mL 4 mol·L-1的硝酸充分反应,产生的H 分子数目为0.1N
2 A
答案 A
3.1 g
解析 P 中含有6个P—P,3.1 g白磷的物质的量为 =0.025 mol,含有0.025×6N =0.15 N 个
4 124 g·mol-1 A A
P—P,A正确;O 和Na反应生成Na O 过程中,O元素化合价由0价下降到-1价,3.2 g氧气的物质的量
2 2 2
为0.1 mol,转移的电子数目为0.2N ,B错误;H 和I 的反应是可逆反应,且标准状况下单质碘是固体,
A 2 2
无法计算生成碘化氢的分子数,C错误;铁粉和硝酸反应不能生成氢气,D错误。
5.下列有关物质结构和性质的说法正确的是( )
A.晶体中有阳离子,不一定有阴离子
B.H O+中的H—O—H键角比水中的小
3
C.共价键的键能越大,分子晶体的熔点越高
D.非金属元素都位于元素周期表中的p区
答案 A
解析 晶体中含有阳离子不一定含有阴离子,如金属晶体中含有阳离子和自由电子,没有阴离子,故A正
6-1×2
确;H O中O原子价层电子对数为2+ =4,有2个孤电子对,H O+中O原子价层电子对数为3+
2 2 3
(6-1)-1×3
=4,有1个孤电子对,排斥力较小,使H O+中的H—O—H键角比水中的大,故B错误;分
2 3
子晶体的熔、沸点与分子间作用力、氢键有关系,与共价键强弱无关,故C错误;非金属氢元素位于s区,
故D错误。
6.能正确表示下列变化的离子方程式是( )
A.甲醇碱性燃料电池负极方程式:CH OH-6e-+H O===CO ↑+6H+
3 2 2
B.铁粉与过量稀硝酸反应:Fe+NO-
+4H+===Fe3++NO↑+2H O
3 2
C.亚硫酸氢钠的水解:HSO-
+H O
SO2-
+H O+
3 2 3 3
D.硫酸铜溶液中通入硫化氢:Cu2++S2-===CuS↓
答案 B解析 由于是碱性燃料电池,负极生成的CO 以碳酸根离子存在,故正确的负极反应式为CH OH-6e-
2 3
+8OH-===CO2-
+6H O,A错误;铁粉与过量稀硝酸反应,由于硝酸过量,生成三价铁离子,稀硝酸的还原
3 2
产物为NO,B正确;亚硫酸是二元弱酸,根据盐类水解的规律,亚硫酸氢根离子水解生成亚硫酸,其水
解方程式为HSO-
+H O H SO +OH-,C错误;硫化氢气体不能拆成离子形式,正确的离子方程式为
3 2 2 3
H S+Cu2+===CuS↓+2H+,D错误。
2
7.短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W简单离子在
同周期离子中半径最小,Q与Z同主族。下列说法错误的是( )
A.X能与多种元素形成共价键
B.最简单氢化物沸点:Z
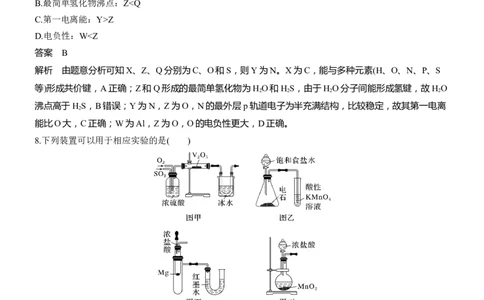
Z D.电负性:Wv(Ⅰ)>v(Ⅲ) D.三个过程的反应焓变:ΔH(Ⅱ)>ΔH(Ⅰ)>ΔH(Ⅲ) 答案 D 解析 催化剂通过降低活化能而改变反应速率,但不影响焓变,A项错误;该反应为放热反应,升高温度 平衡逆向移动,降低苯的平衡转化率,B项错误;根据图2可知,过程Ⅱ的活化能最大,因此反应速率最 慢,C项错误;过程Ⅰ、Ⅱ,都是反应物的总能量小于生成物的总能量,均为吸热反应,并且过程Ⅱ吸热 多,过程Ⅲ放热,因此ΔH(Ⅱ)>ΔH(Ⅰ)>ΔH(Ⅲ),D项正确。 14.使用合适的催化剂进行乙酸直接加氢可制备乙醇,反应原理如下: 主反应:CH COOH(g)+2H (g)===CH CH OH(g)+H O(g) ΔH<0 3 2 3 2 2 副反应:CH COOH(g)+CH CH OH(g)===CH COOCH CH (g)+H O(g) ΔH<0(热效应小可忽略) 3 3 2 3 2 3 2 在密闭容器中控制n (H )∶n (CH COOH)=10。2 MPa下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与 起始 2 起始 3 250 ℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为S(乙醇)= n(乙醇) 。下列说法正确的是( ) n(乙醇)+2n(乙酸乙酯)A.反应2CH COOH(g)+2H (g)===CH COOCH CH (g)+2H O(g) ΔH>0 3 2 3 2 3 2 B.300 ℃、0.5 MPa下,反应足够长时间,S(乙醇)<90% C.图中曲线③表示250 ℃,乙醇选择性随压强变化的曲线 D.曲线②变化的原因是随温度升高,副反应正向进行的程度减小 答案 B 解析 主反应为气体体积减小的放热反应,增大压强,平衡正向移动,乙醇的选择性上升,则250 ℃下, 乙醇选择性随压强变化的曲线是①;主反应和副反应均为放热反应,温度升高,主反应和副反应的平衡均 逆向移动,主反应逆向移动的程度大于副反应,曲线②表示2 MPa时乙醇选择性随温度变化的曲线;同理, ③表示2 MPa时乙酸乙酯选择性随温度变化的曲线,④表示250 ℃时乙酸乙酯选择性随压强变化的曲线。 根据盖斯定律,反应2CH COOH(g)+2H (g)===CH COOCH CH (g)+2H O(g)可由主反应+副反应得到,由于 3 2 3 2 3 2 主反应和副反应都为放热反应,故反应2CH COOH(g)+2H (g)===CH COOCH CH (g)+2H O(g) ΔH<0,A 3 2 3 2 3 2 错误;由图可知,250 ℃、0.5 MPa下乙醇的选择性约为90%,升高温度主反应逆向进行,故300 ℃、0.5 MPa下反应足够的时间S(乙醇) <90%,B正确;根据分析,曲线③表示2 MPa时乙酸乙酯选择性随温度变 化的曲线,C错误;曲线②表示2 MPa时乙醇选择性随温度变化的曲线,副反应的热效应小可忽略,原因 是随温度升高,主反应逆向进行,D错误。 15.25 ℃时,用0.1 mol·L-1NaOH溶液滴定20.00 mL 0.1 mol·L-1HA溶液,体系中-lg c(A-)、-lg c(HA)、NaOH 溶液的体积与溶液pH的关系如图所示。下列说法正确的是( ) A.图中曲线①表示-lg c(A-)与pH的关系 B.25 ℃ HA电离平衡常数的数量级为10-4 C.a点溶液中,2c(H+)+c(HA)=c(A-)+2c(OH-) D.b点时,V[NaOH(aq)]=20 mL 答案 C解析 由题图分析可知,曲线①表示-lg c(HA)与pH的关系,曲线②表示-lg c(A-)与pH的关系,当 c(H+ )·c(A- ) c(HA)=c(A-)时,K(HA)= =10-4.76,A、B错误;a点溶液为等物质的量浓度的HA和NaA溶液, a c(HA) 存在电荷守恒和元素守恒分别为c(H+)+c(Na+)=c(OH-)+c(A-)、2c(Na+)=c(A-)+c(HA),联立两式可得:2c(H+) +c(HA)=2c(OH-)+c(A-),C正确;若V[NaOH(aq)]=20 mL,则HA恰好完全反应,溶质为NaA,溶液显碱性, pH>7,结合图示b点时溶液pH=7可知,V[NaOH(aq)]<20 mL,D错误。