文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(福建专用)
黄金卷06
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Fe-56 Co-59 Cu-64
第Ⅰ卷
一、单项选择题:共10题,每题4分,共40分。每题只有一个选项最符合题意。
1.从古至今,人类的生活、生产都离不开材料的应用。下列说法正确的是
A.三星堆祭祀坑内发现了大量丝绸朽化后的残留物,丝绸的主要成分是蛋白质
B.人民币票面文字处采用了含 的磁性油墨, 常用作红色颜料
C.北斗卫星上使用的硅太阳能电池阵,利用 将太阳能转化为电能
D.“奋斗者号”潜水器使用的固体浮力材料,由空心玻璃微球填充在高强度树脂中制成,属于无机非
金属材料
2.铜可以溶解在氨水和过氧化氢的混合溶液中: 。
设 为阿伏加德罗常数的值,下列有关说法不正确的是
A. 基态铜原子的最外层电子数为
B.每生成 转移的电子数为
C. 含有 键数目为
D.等物质的量的 与 所含有的质子数相等
3.铜、银位于周期表中第ⅠB族。铜、硫酸铜、硝酸银、银氨溶液是实验室常用的含铜或银的化学试剂。
从废定影液[主要含有 、 、 、 等微粒]中回收Ag和 的主要步骤:向该废定影液
中加入氢氧化钠调节pH在7.5~8.5之间,然后再加入稍过量 溶液沉银,过滤、洗涤及干燥,灼烧制Ag;滤液中通入 氧化 ,用苯萃取分液。下列化学反应表示正确的是
A.硫酸铜溶液中加入小粒金属钠:
B.用铜电极电解硫酸铜溶液:
C.稀硝酸洗涤做过银镜反应的试管:
D.多余的 用硝酸处理:
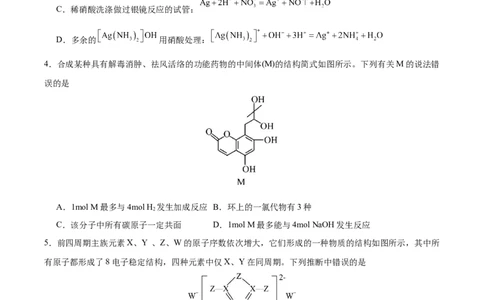
4.合成某种具有解毒消肿、祛风活络的功能药物的中间体(M)的结构简式如图所示。下列有关M的说法错
误的是
A.1mol M最多与4mol H 发生加成反应 B.环上的一氯代物有3种
2
C.该分子中所有碳原子一定共面 D.1mol M最多能与4mol NaOH发生反应
5.前四周期主族元素X、Y 、Z、W的原子序数依次增大,它们形成的一种物质的结构如图所示,其中所
有原子都形成了8电子稳定结构,四种元素中仅X、Y在同周期。下列推断中错误的是
A.简单离子半径:W> Z> Y
B.Z单质可溶于由X、Z形成的化合物中
C.第一电离能:Y> X
D.Y与氧元素形成的化合物不止三种
6.某实验小组探究Fe2+与HO 反应中滴加KSCN溶液变红色后又褪色的原因,提出如下假设:
2 2
a.Fe3+被HO 还原 b.SCN-被O 氧化 c.SCN-被HO 氧化。
2 2 2 2 2
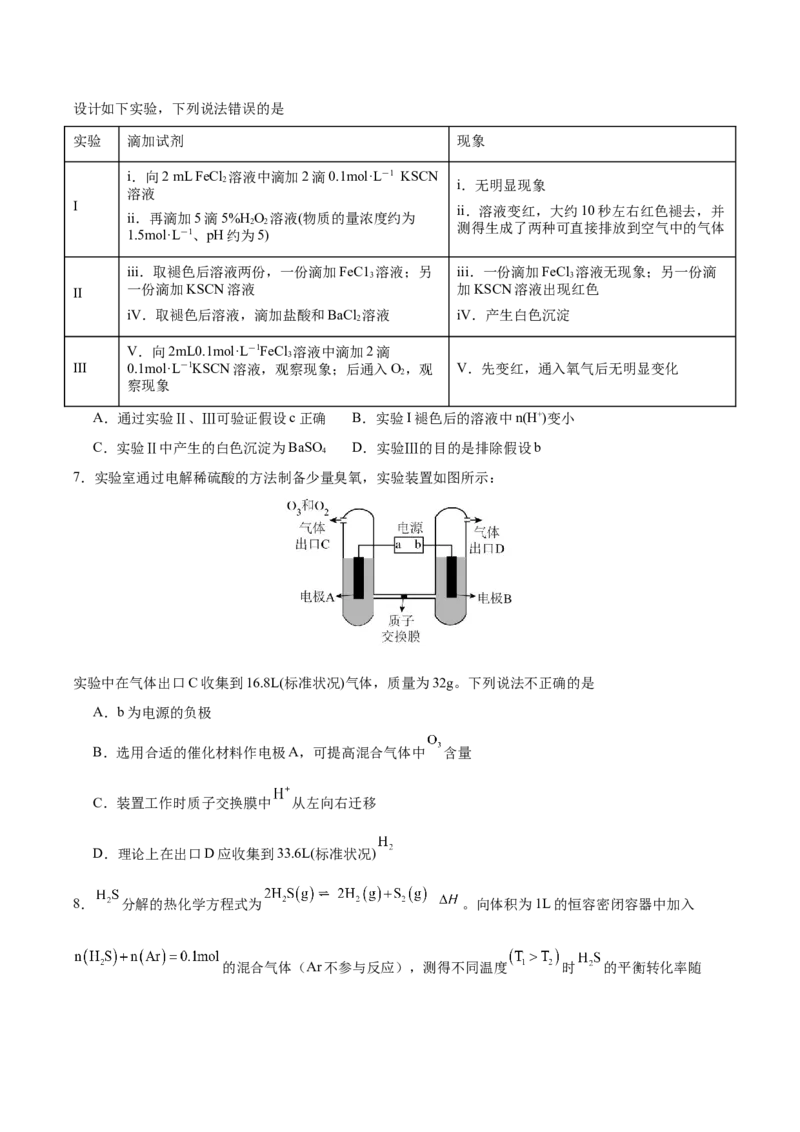
试卷第2页,共3页设计如下实验,下列说法错误的是
实验 滴加试剂 现象
i.向2 mL FeCl 溶液中滴加2滴0.1mol·L-1 KSCN
2 i.无明显现象
溶液
I
ii.溶液变红,大约10秒左右红色褪去,并
ii.再滴加5滴5%H O 溶液(物质的量浓度约为
2 2 测得生成了两种可直接排放到空气中的气体
1.5mol·L-1、pH约为5)
iii.取褪色后溶液两份,一份滴加FeC1 溶液;另 iii.一份滴加FeCl 溶液无现象;另一份滴
3 3
一份滴加KSCN溶液 加KSCN溶液出现红色
II
iV.取褪色后溶液,滴加盐酸和BaCl 溶液 iV.产生白色沉淀
2
V.向2mL0.1mol·L-1FeCl 溶液中滴加2滴
3
III 0.1mol·L-1KSCN溶液,观察现象;后通入O,观 V.先变红,通入氧气后无明显变化
2
察现象
A.通过实验Ⅱ、Ⅲ可验证假设c正确 B.实验I褪色后的溶液中n(H+)变小
C.实验Ⅱ中产生的白色沉淀为BaSO D.实验Ⅲ的目的是排除假设b
4
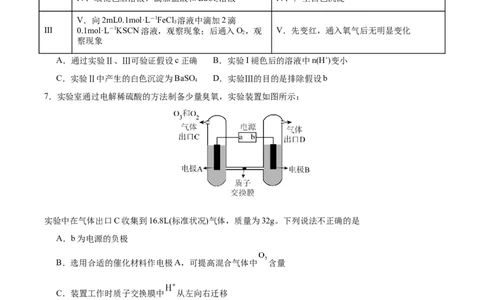
7.实验室通过电解稀硫酸的方法制备少量臭氧,实验装置如图所示:
实验中在气体出口C收集到16.8L(标准状况)气体,质量为32g。下列说法不正确的是
A.b为电源的负极
B.选用合适的催化材料作电极A,可提高混合气体中 含量
C.装置工作时质子交换膜中 从左向右迁移
D.理论上在出口D应收集到33.6L(标准状况)
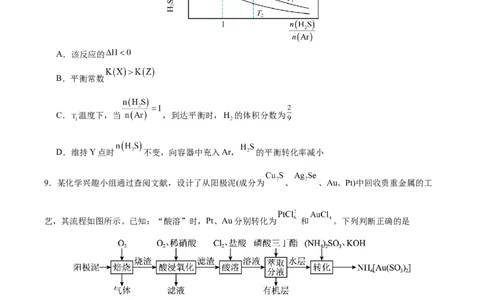
8. 分解的热化学方程式为 。向体积为1L的恒容密闭容器中加入
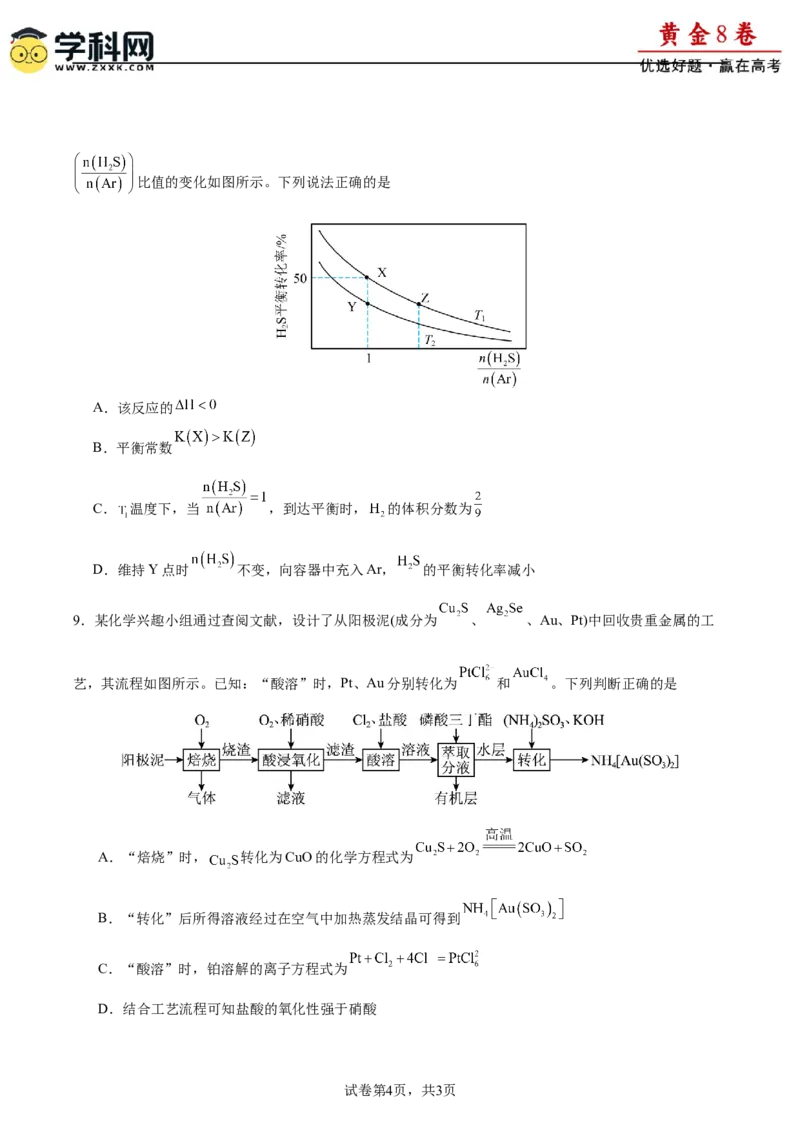
的混合气体(Ar不参与反应),测得不同温度 时 的平衡转化率随比值的变化如图所示。下列说法正确的是
A.该反应的
B.平衡常数
C. 温度下,当 ,到达平衡时, 的体积分数为
D.维持Y点时 不变,向容器中充入Ar, 的平衡转化率减小
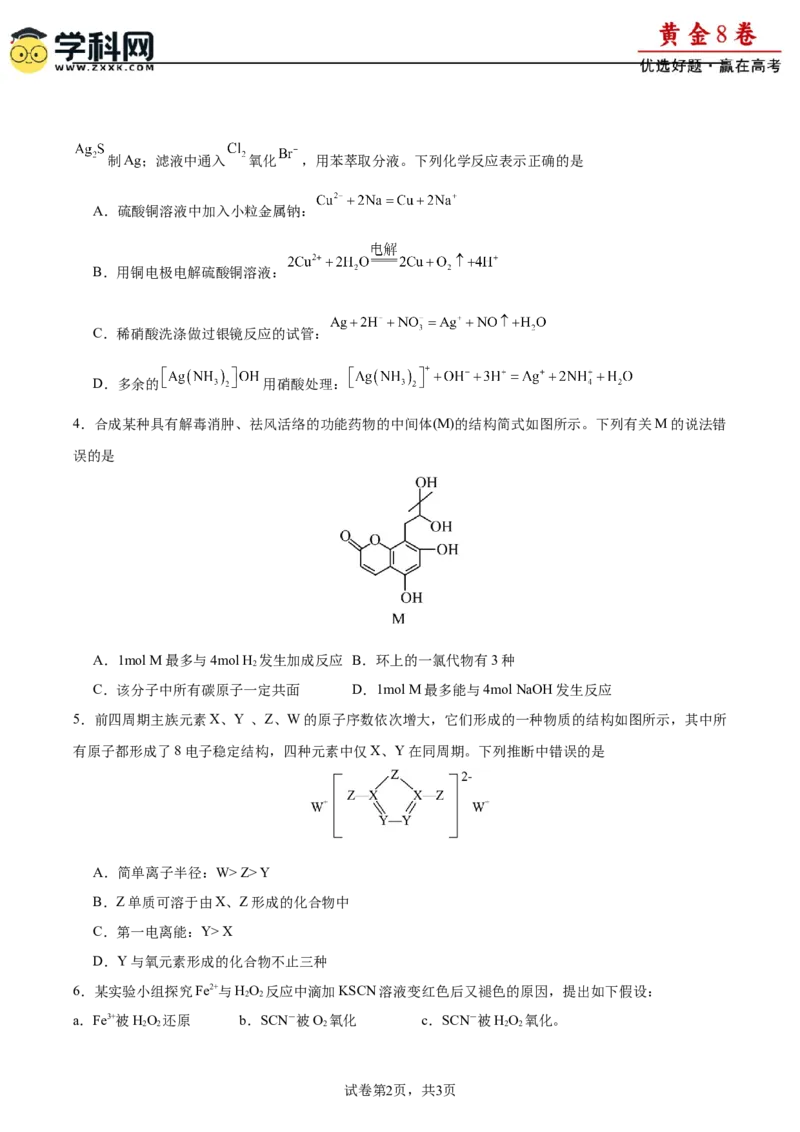
9.某化学兴趣小组通过查阅文献,设计了从阳极泥(成分为 、 、Au、Pt)中回收贵重金属的工
艺,其流程如图所示。已知:“酸溶”时,Pt、Au分别转化为 和 。下列判断正确的是
A.“焙烧”时, 转化为CuO的化学方程式为
B.“转化”后所得溶液经过在空气中加热蒸发结晶可得到
C.“酸溶”时,铂溶解的离子方程式为
D.结合工艺流程可知盐酸的氧化性强于硝酸
试卷第4页,共3页10.一定温度下,烧杯中有25mL对二甲苯和5mL水,加入bmol HA后充分搅拌并完全溶解,静置平衡后
HA在对二甲苯(PX)中浓度为 ,在水(W)中浓度为 。已知:
①实验条件下HA在两相间的分配系数: (只与温度有关):
②HA不能在对二甲苯中电离,在水中电离平衡常数 。
忽略溶液混合时体积的变化,下列说法错误的是
A.水溶液中
B.若向平衡体系中再加入对二甲苯, 减小
C.若向平衡体系中再加入20mL水,平衡后
D.若向平衡体系中再加入NaOH固体,使 ,平衡后
第Ⅱ卷
二、非选择题:共4题,共60分。
11.(14分)BiS(硫化铋)在光催化剂、锂离子电池等领域具有重要潜在价值,一种由辉铋矿(主要成分为
2 3
BiS,含SiO、Cu S等杂质)为原料提纯制备BiS 的工艺流程如图所示:
2 3 2 2 2 3
已知:①25℃时,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 Fe2+ Fe3+ Bi3+ Cu2+
开始沉淀时(c=0.01mol/L)的pH 7.5 2.2 4.5 5.2
沉淀完全时(c=1.0×10-5mol/L)的pH 9.0 3.2 5.5 6.7
②在本工艺条件下,还原性顺序为Fe>Cu>Bi。
(1)滤液1中含有FeCl 、FeCl 、CuCl 和BiCl ,滤渣1的成分是S和 ,加入盐酸保持溶液pH<1.4,
3 2 2 3否则铋元素以碱式氯化铋(BiOCl)的形式混入滤渣1使产率降低,生成BiOCl的离子方程式为 。
(2)“碱溶”步骤中加入NH •H O的目的是将Cu(OH) 转化为可溶性的 (填离子符号)。
3 2 2
(3)“转化”步骤中硫代乙酰胺(CHCSNH )在酸性溶液中会水解为乙酰胺(CHCONH )和硫化氢;硫化氢会进
3 2 3 2
一步发生反应:2Bi3+(aq)+3H S BiS(s)+6H+(aq) K,则K (Bi S)= (用含K,HS的K 、K 的式
2 2 3 sp 2 3 2 a1 a2
子表示)。
(4)若取10kg铋含量为85%的辉铋矿,经上述流程(铋元素在整个流程中损失率为5%),计算最终可制得
BiS 固体的质量约为9.9kg,实测干燥的BiS 产量高于计算值的原因是 。
2 3 2 3
(5)新型二维半导体芯片材料——硒氧化铋晶胞结构如图所示。
①该晶体的化学式为 。
②该晶胞沿z轴方向的投影图为 (填标号)。
A. B. C. D.
③该晶体中,每个 周围紧邻的 共有 个。
12.(16分)资料显示,酸性介质中, 和 反应转化为 和 。小组探究利用该反应测定
含量的条件。
实验 序号 物质a 实验现象
Ⅰ 溶液 无明显变化
加热至沸腾, 后溶液变为
Ⅱ 溶液
紫色
Ⅲ 溶液 加热至沸腾,生成大量棕黑色
试卷第6页,共3页沉淀,静置,上层溶液未变紫
色
(1) 中∠HOH键角 (填“大于”“小于”或“等于”) 中∠HOH键角,原因
为 。
(2)实验Ⅱ中反应的离子方程式是 。
(3)实验Ⅰ的条件下 能将 氧化为 ,推测实验Ⅰ未出现紫色的原因: 。
(4)经检验,棕黑色沉淀为 ,针对实验Ⅲ中的现象,提出以下假设:
假设1: 的浓度较低,不足以将 氧化为
假设2:溶液中存在还原剂 ,将生成的 ,还原为
①甲同学分析上述实验设计,认为假设1不成立,理由是 。
②针对假设2,乙同学设计实验Ⅳ证实了推测合理。
请写出实验操作和现象: 。
③实验Ⅲ中生成 的离子方程式是 ,从化学反应原理的角度分析实验Ⅲ未得到紫色溶液的
原因: 。
(5)资料表明 可作为 和 反应转化为 的催化剂。丙同学设计实验Ⅲ的对比实验进行了证
实。向 中滴加2滴 溶液,再加入 固体,加热至沸腾,
观察到溶液变为紫色。
13.(15分)NH 是重要的化工原料,可以制备丙烯腈、尿素、硝酸等产品。回答下列问题:
3
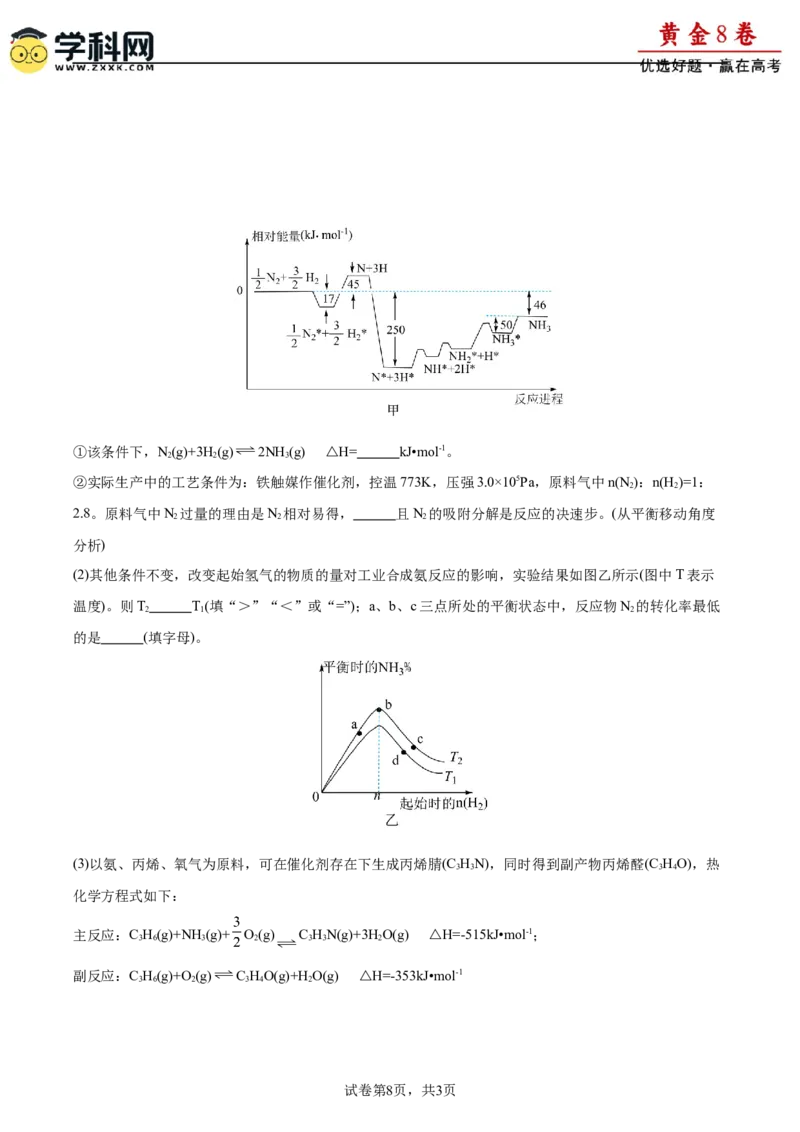
(1)合成氨反应的能量变化如图甲所示(吸附在催化剂表面的物质用“*”表示)。①该条件下,N(g)+3H(g) 2NH (g) △H= kJ•mol-1。
2 2 3
②实际生产中的工艺条件为:铁触媒作催化剂,控温773K,压强3.0×105Pa,原料气中n(N ):n(H )=1:
2 2
2.8。原料气中N 过量的理由是N 相对易得, 且N 的吸附分解是反应的决速步。(从平衡移动角度
2 2 2
分析)
(2)其他条件不变,改变起始氢气的物质的量对工业合成氨反应的影响,实验结果如图乙所示(图中T表示
温度)。则T T(填“>”“<”或“=”);a、b、c三点所处的平衡状态中,反应物N 的转化率最低
2 1 2
的是 (填字母)。
(3)以氨、丙烯、氧气为原料,可在催化剂存在下生成丙烯腈(C HN),同时得到副产物丙烯醛(C HO),热
3 3 3 4
化学方程式如下:
主反应:C H(g)+NH (g)+ O(g) C HN(g)+3H O(g) △H=-515kJ•mol-1;
3 6 3 2 3 3 2
副反应:C H(g)+O(g) C HO(g)+H O(g) △H=-353kJ•mol-1
3 6 2 3 4 2
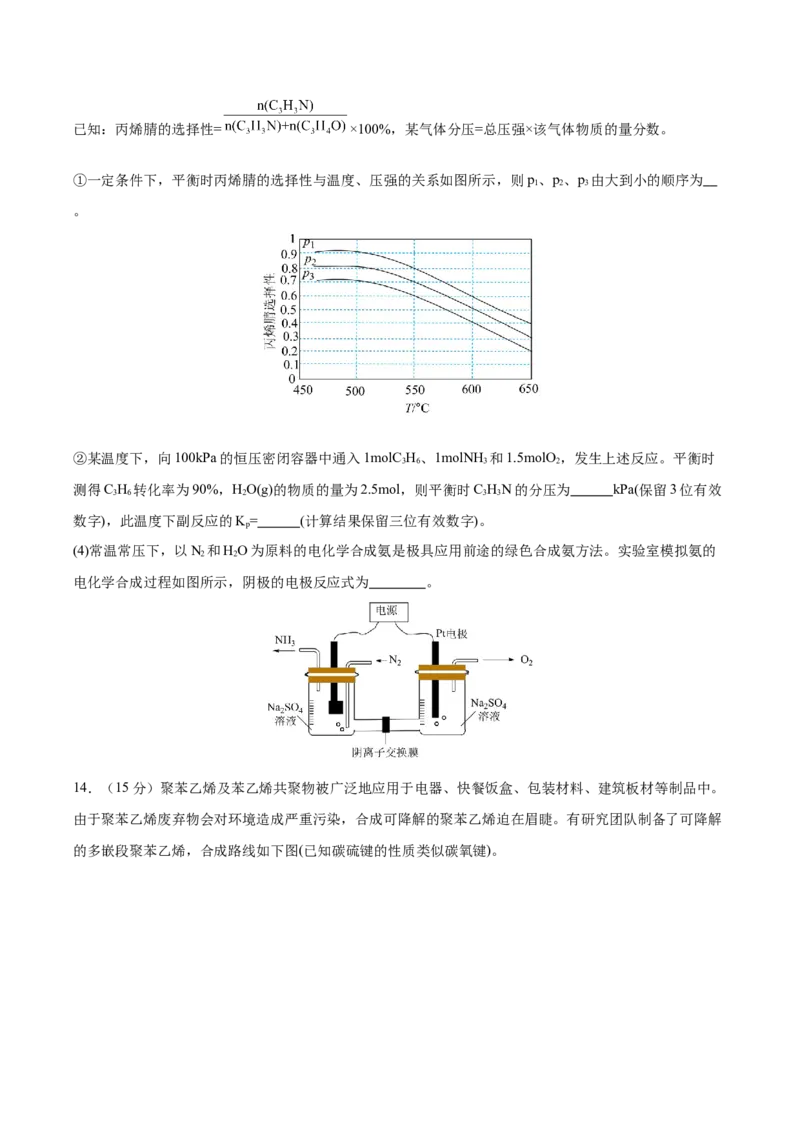
试卷第8页,共3页已知:丙烯腈的选择性= ×100%,某气体分压=总压强×该气体物质的量分数。
①一定条件下,平衡时丙烯腈的选择性与温度、压强的关系如图所示,则p、p、p 由大到小的顺序为
1 2 3
。
②某温度下,向100kPa的恒压密闭容器中通入1molC H、1molNH 和1.5molO,发生上述反应。平衡时
3 6 3 2
测得C H 转化率为90%,HO(g)的物质的量为2.5mol,则平衡时C HN的分压为 kPa(保留3位有效
3 6 2 3 3
数字),此温度下副反应的K= (计算结果保留三位有效数字)。
p
(4)常温常压下,以N 和HO为原料的电化学合成氨是极具应用前途的绿色合成氨方法。实验室模拟氨的
2 2
电化学合成过程如图所示,阴极的电极反应式为 。
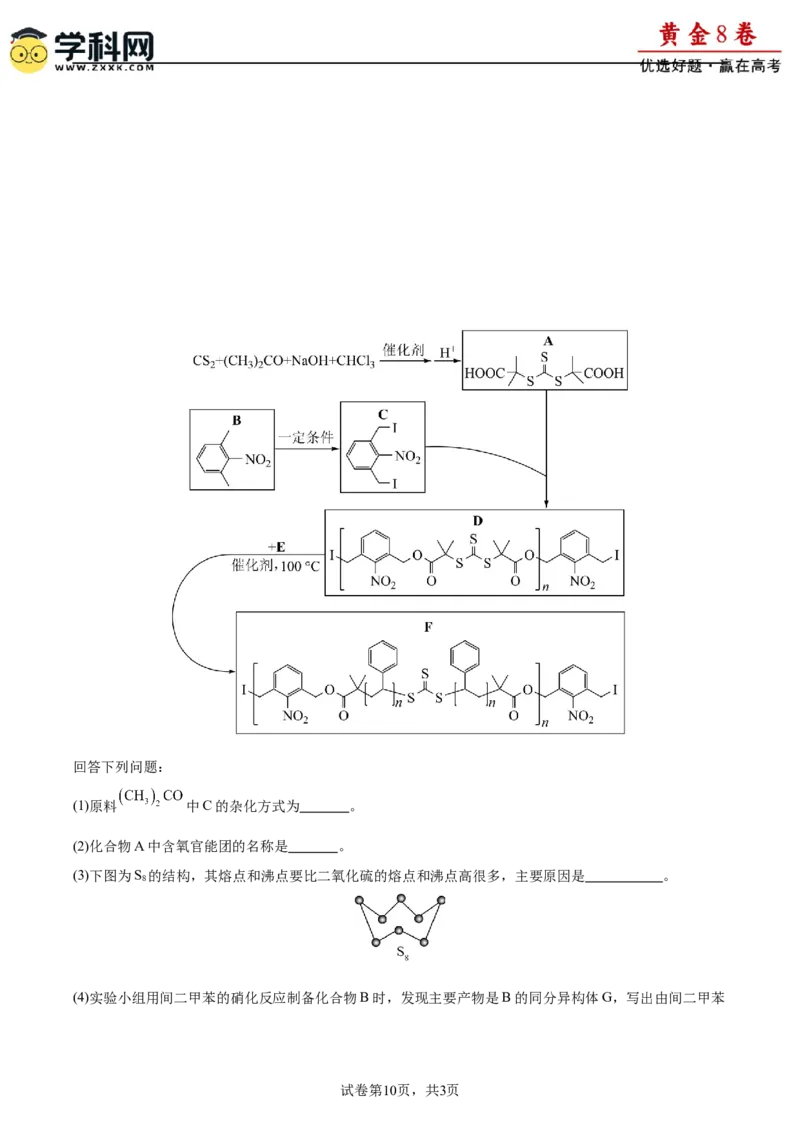
14.(15分)聚苯乙烯及苯乙烯共聚物被广泛地应用于电器、快餐饭盒、包装材料、建筑板材等制品中。
由于聚苯乙烯废弃物会对环境造成严重污染,合成可降解的聚苯乙烯迫在眉睫。有研究团队制备了可降解
的多嵌段聚苯乙烯,合成路线如下图(已知碳硫键的性质类似碳氧键)。回答下列问题:
(1)原料 中C的杂化方式为 。
(2)化合物A中含氧官能团的名称是 。
(3)下图为S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因是 。
8
(4)实验小组用间二甲苯的硝化反应制备化合物B时,发现主要产物是B的同分异构体G,写出由间二甲苯
试卷第10页,共3页生成G的化学方程式 。
(5)E的结构简式为 。
(6)高聚物F比聚苯乙烯易降解的原因是 ,F在弱酸性水溶液中降解的产物主要有 。
(7)满足下列条件的化合物B的同分异构体有 种。
①含有酯基;②含有 结构;③含有苯环;④能发生银镜反应。