文档内容
硫及其化合物(2)同步练习
(答题时间:25分钟)
一、选择题
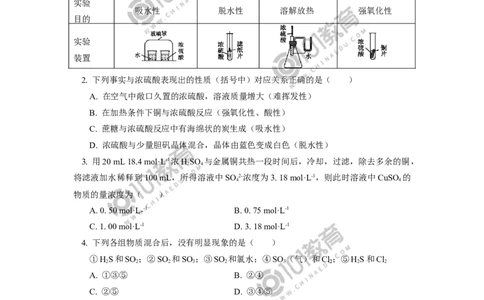
1. 某同学设想用如图所示装置来验证浓硫酸的某些性质,其中不能达到实验目的的是(
)
选项 A B C D
实验
吸水性 脱水性 溶解放热 强氧化性
目的
实验
装置
2. 下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( )
A. 在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性)
B. 在加热条件下铜与浓硫酸反应(强氧化性、酸性)
C. 蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性)
D. 浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色(脱水性)
3. 用20 mL 18.4 mol·L-1浓HSO 与金属铜共热一段时间后,冷却,过滤,除去多余的铜,
2 4
将滤液加水稀释到100 mL,所得溶液中SO 2-浓度为3. 18 mol·L-1,则此时溶液中CuSO 的
4 4
物质的量浓度为( )
A. 0. 50 mol·L--1 B. 0. 75 mol·L-1
C. 1. 00 mol·L-1 D. 3. 18 mol·L-1
4. 下列各组物质混合后,没有明显现象的是( )
①HS和SO ;②SO 和SO ;③SO 和氯水;④SO (气)和Cl;⑤HS和Cl
2 2 2 3 2 3 2 2 2
A. ①③⑤ B. ②④
C. ②⑤ D. ③④⑤
5. 硫黄在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色,
乙转化为丙。在丙溶液中加入NaS生成气体丁,把丁通入乙溶液中得到沉淀戊。甲、乙、
2
丙、丁、戊均含有硫元素,则它们分别是( )
A. SO 、HSO 、HSO 、HS、S
3 2 4 2 3 2
B. SO 、HSO 、HSO 、SO 、SO
2 2 3 2 4 2 3
C. SO 、HSO 、HSO 、SO 、NaSO
3 2 4 2 3 2 2 2 3
D. SO 、HSO 、HSO 、HS、S
2 2 3 2 4 2
6. 已知A是一种不溶于水的固体,在一定条件下有下列转化关系(部分产物及 HO省
2
第1页略)
试回答:
(1)写出物质的化学式:A________,E________。
(2)写出由B和C反应生成A,由F的浓溶液生成C的化学方程式:
B+C A_____________________________________________________,
F(浓) C___________________________________________________。
(3)写出D和F的稀溶液反应的离子方程式_________________________________
__________________。
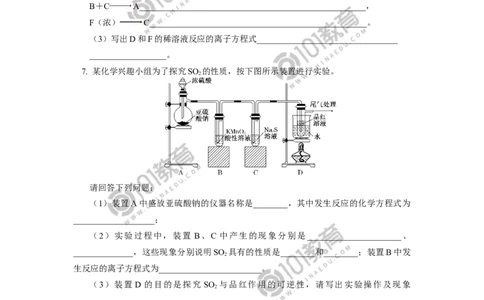
7. 某化学兴趣小组为了探究SO 的性质,按下图所示装置进行实验。
2
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为
___________________;
(2)实验过程中,装置 B、C 中产生的现象分别是______________________、
______________,这些现象分别说明SO 具有的性质是________和________;装置B中发
2
生反应的离子方程式为________________________。
(3)装置 D 的目的是探究 SO 与品红作用的可逆性,请写出实验操作及现象
2
________________________________。
(4)尾气可采用________溶液吸收。
第2页硫及其化合物(2)同步练习参考答案
1.【答案】D
【解析】盛有水的烧杯中水的量减少可以证明浓硫酸具有吸水性,故A正确;滤纸片
脱水炭化可以证明浓硫酸具有脱水性,故B正确;U形管中的水面右高左低,说明浓硫酸
溶解时放出大量的热,使锥形瓶中压强增大,故C正确;Cu与浓HSO 常温下不反应,加
2 4
热反应生成硫酸铜、二氧化硫和水,故D错误。
2.【答案】B
【解析】在空气中敞口久置的浓硫酸,会吸收空气中的水分而使溶液的质量增大,表
现的是浓硫酸的吸水性,故A错误;在加热条件下铜与浓硫酸反应生成硫酸铜、二氧化硫
和水,硫元素化合价部分变化,体现浓硫酸的强氧化性和酸性,故 B正确;蔗糖与浓硫酸
反应中有海绵状的炭生成,体现浓硫酸的脱水性,故 C错误;浓硫酸与少量胆矾晶体混合,
晶体由蓝色变成白色,体现浓硫酸的吸水性,故D错误。
3.【答案】A
【解析】浓HSO 的总物质的量为0. 02 L×18. 4 mol·L-1=0. 368 mol,反应后剩余SO 2-
2 4 4
的物质的量n(SO 2-)=0. 1 L×3. 18 mol·L-1=0. 318 mol,则表现氧化性的HSO 的物质的量
4 2 4
n(HSO )=0. 368 mol-0. 318 mol=0. 05 mol。设该反应中Cu的物质的量为x mol,由得失
2 4
0.05mol
0.1L
电子守恒有等式:2x=2×0. 05,x=0. 05,故c(CuSO )= =0. 50 mol·L-1。
4
4.【答案】B
【解析】SO 和SO 中硫元素为相邻价态,不能发生氧化还原反应。SO 和Cl 都具有
2 3 3 2
氧化性,相互间不能发生反应。
5.【答案】D
【解析】题目中所述的变化过程可表示为:
由题意可推出:甲是SO ,乙是HSO ,丙是HSO ,丁是HS,戊是S。
2 2 3 2 4 2
6.【答案】(1)S SO (2)2HS+SO ===3S↓+2HO
3 2 2 2
Cu+2HSO (浓) CuSO +SO ↑+2HO
2 4 4 2 2
(3)FeS+2H+===Fe2++HS↑
2
【解析】由A+H B,A+O C知:A元素的化合价既能升高,也能降低,
2 2
故A为非金属元素,B为氢化物,C为氧化物,且B+C A,则A为硫,进一步推知
B为HS,C为SO ,D为FeS,E为SO ,F为HSO 。
2 2 3 2 4
7.【答案】(1)蒸馏烧瓶 NaSO +HSO (浓)===Na SO +SO ↑+HO (2)溶液
2 3 2 4 2 4 2 2
−
由紫红色变为无色 无色溶液中出现黄色浑浊 还原性 氧化性 5SO +2MnO4 +
2
第3页2−
2HO===2Mn2++5SO4 +4H+ (3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精
2
灯加热,溶液恢复为红色 (4)NaOH
【解析】(1)根据仪器的特征,该仪器是蒸馏烧瓶;亚硫酸钠和浓硫酸反应生成硫酸
钠、SO 和水,化学方程式为NaSO +HSO (浓)===Na SO +SO ↑+HO。
2 2 3 2 4 2 4 2 2
(2)酸性高锰酸钾有强氧化性,二氧化硫有还原性,所以二氧化硫能被酸性高锰酸钾
溶液氧化而褪色,同时说明二氧化硫有还原性,SO 的氧化性能将S2-氧化成S,则实验过
2
程中,装置B、C中发生的现象分别是溶液由紫红色变为无色、无色溶液中出现黄色浑浊,
这些现象分别说明SO 具有的性质是还原性和氧化性;装置B中发生反应的离子方程式为
2
− 2−
5SO +2MnO4 +2HO===2Mn2++5SO4 +4H+。(3)二氧化硫具有漂白性,能使品红溶
2 2
液褪色,但加热褪色后的品红溶液,溶液的颜色能复原,所以探究 SO 与品红作用的可逆
2
性的实验操作及现象是品红溶液褪色后,关闭分液漏斗的活塞,点燃酒精灯加热,溶液恢
复为红色(4)该实验的尾气是SO ,可用NaOH溶液吸收。
2
第4页