文档内容
1.2.1 电解质的电离
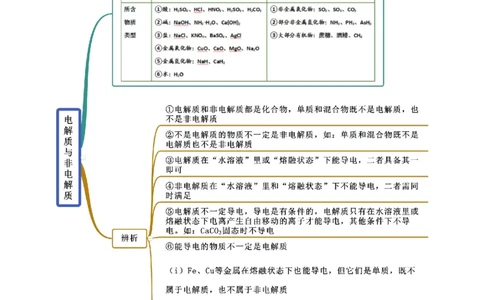
知识点一 电解质与非电解质【例1】(2020·辽阳市集美中学月考)下列物质中既能导电,又属于电解质的一组物质是( )
A.石墨、醋酸溶液、食盐晶体 B.熔融状态的KOH、熔融状态的NaCl
C.稀HSO 、NaOH溶液、纯HNO D.液氨、石灰水、水银
2 4 3
【答案】B
【解析】A、石墨能导电是单质不是电解质,醋酸溶液能导电是乙酸和水的混合物,其中醋酸属于弱电解
质,食盐晶体是电解质但不导电,故A错误;
B、熔融状态的KOH、熔融状态的NaCl均属于强电解质能导电,故B正确;
C、稀硫酸和NaOH溶液是混合物,不是电解质也不是非电解质,,纯硝酸不导电,故C错误;
D、液氨不导电,是非电解质,石灰水是混合物,水银是单质,都不是电解质也不是非电解质,故D错误;
故答案选B。
1. 水溶液里或熔融状态下能导电的化合物是电解质,能导电的物质中含有自由电子或自由移动的阴阳离子,
水溶液中或熔融状态完全电离的电解质为强电解质,据此判断
2. 注意判断电解质时不能依据能否导电进行判断,关键是看引起导电的原因是不是自身发生的电离,如果
在溶液中或熔融状态下能够自身电离出离子,则就属于电解质,否则不是
【一隅三反】
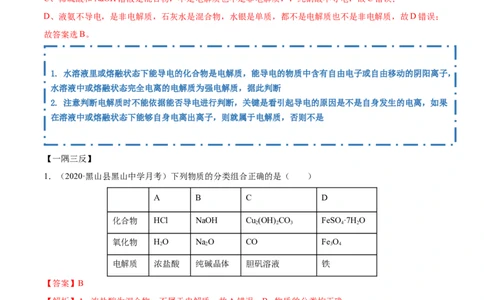
1.(2020·黑山县黑山中学月考)下列物质的分类组合正确的是( )
A B C D
化合物 HCl NaOH Cu (OH) CO FeSO ·7H O
2 2 3 4 2
氧化物 HO NaO CO Fe O
2 2 3 4
电解质 浓盐酸 纯碱晶体 胆矾溶液 铁
【答案】B
【解析】A. 浓盐酸为混合物,不属于电解质,故A错误;B. 物质的分类均正确;
C. 胆矾溶液为混合物,不属于电解质;D. 铁为单质,不属于电解质;故答案选B。
2.(2019·安徽省潜山第二中学高一期中)有关电解质的说法正确的是( )
A.NH 通入水中形成溶液能导电,故NH 是电解质
3 3
B.NaCl在电流的作用下电离出Na+和Cl—
C.BaSO 不溶于水,其水溶液导电能力弱,故BaSO 是弱电解质
4 4
D.液态HCl不导电,但HCl是电解质
【答案】D【解析】A.氨气与水反应生成的一水合氨部分电离出阴阳离子而使溶液导电,氨气本身不能电离,属于
非电解质,故A错误;
B.电解质的电离不需要外加电流,故B错误;
C.在水溶液里和熔融状态下都不导电的化合物是非电解质,硫酸钡在水溶液中溶解度较小,导致硫酸钡
溶液离子浓度较小,溶液导电能力较弱,但溶解的部分完全电离,所以硫酸钡是强电解质,故C错误;
D.在熔融或水溶液中能导电的化合物为电解质,HCl为共价化合物,液态不导电,但在水中电离,HCl
是电解质,故D正确;故选D。
3.(2020·甘肃城关·兰大附中高一期中)现有以下物质:① NaCl溶液 ② 干冰(固态的二氧化碳) ③冰醋
酸(纯净的醋酸) ④铜 ⑤BaSO 固体⑥蔗糖⑦酒精⑧熔融的KNO 其中属于电解质的是
4 3
A.①③⑤⑧ B.②③④⑤⑥⑦ C.③⑤⑧ D.全部
【答案】C
【解析】溶于水或在熔融状态下能够导电的化合物是电解质,电解质必须是纯净物,酸、碱、盐、活泼金
属氧化物等均属于电解质;则①NaCl溶液是混合物,不是电解质,也不是非电解质;②干冰(固态的二氧
化碳)是非电解质;③冰醋酸(纯净的醋酸)是电解质;④铜是单质,不是电解质,也不是非电解质;
⑤BaSO 固体是电解质;⑥蔗糖是非电解质;⑦酒精是非电解质;⑧熔融的KNO 属于电解质,因此其中
4 3
属于电解质的是③⑤⑧;答案选C。
4.(2020·辽阳市集美中学月考)现有下列十种物质:①蔗糖 ②熔融 ③盐酸 ④铜丝
⑤ 固体 ⑥液氯 ⑦ 固体 ⑧乙醇 ⑨氯水 ⑩液态
(1)上述物质中可导电的是______(填序号,下同)。
(2)上述物质中不能导电,但属于电解质的是______。
(3)上述物质中属于非电解质的是______。
【答案】②③④⑨ ⑤⑦⑩ ①⑧
【解析】(1)④铜丝中含有自由电子,属于电子导电;②熔融 、③盐酸、⑨氯水中都含有自由移动的
离子,属于离子导电,故选②③④⑨。答案为:②③④⑨;
(2)②熔融 、⑤ 固体、⑦ 固体、⑩液态 都是电解质,但②熔融 能导电,
故选⑤⑦⑩。答案为:⑤⑦⑩;
(3)①蔗糖、⑧乙醇,不管是在水溶液还是在熔融液中,都不能导电,属于非电解质,故选①⑧。答案为:
①⑧。知识点二 强弱电解质
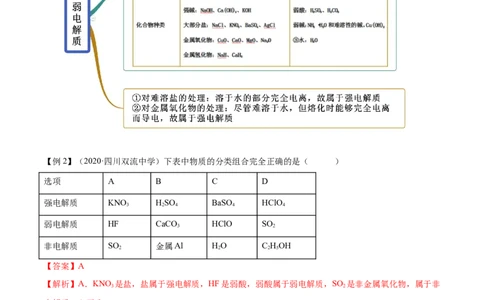
【例2】(2020·四川双流中学)下表中物质的分类组合完全正确的是( )
选项 A B C D
强电解质 KNO HSO BaSO HClO
3 2 4 4 4
弱电解质 HF CaCO HClO SO
3 2
非电解质 SO 金属Al HO C HOH
2 2 2 5
【答案】A
【解析】A.KNO 是盐,盐属于强电解质,HF是弱酸,弱酸属于弱电解质,SO 是非金属氧化物,属于非
3 2
电解质,A正确;
B.HSO 是强酸,强酸属于强电解质,CaCO 是盐,盐属于强电解质,Al是单质,既不是电解质,也不
2 4 3
是非电解质,B错误;
C.BaSO 是盐,盐属于强电解质,HClO是弱酸,弱酸属于弱电解质,HO是电解质,C错误;
4 2
D.HClO 是强酸,强酸属于强电解质,SO 是非金属氧化物,属于非电解质,C HOH是有机物,在水溶
4 2 2 5
液和熔融状态下都不能电离,是非电解质,D错误。答案选A。
【一隅三反】1.(2020·全国高二课时练习)下列属于强电解质的是
A.硫酸钡 B.食盐水 C.二氧化硅 D.醋酸
【答案】A
【解析】按强电解质的定义可知,强电解质指在水中完全电离的电解质,包含强酸、强碱、大部分盐等。
所以对四个选项进行物质分类考查:A.可知硫酸钡是强电解质,A项正确;
B.食盐水为混合物,不在强电解质的概念内,B项错误;C.二氧化硅是非电解质,C项错误;
D.醋酸在水中不完全电离,为弱电解质,D项错误。故答案选A。
2.(2019·浙江省杭州第二中学高三其他)下列属于强电解质的物质是
A.盐酸 B.NH C.HClO D.CaCO
3 3
【答案】D
【解析】A.盐酸为混合物,不属于电解质,A错误;
B.氨气溶液于水后,与水反应后才能使溶液导电,且液氨也不导电,为非电解质,B错误;
C.次氯酸为弱电解质,C错误;D.碳酸钙为强电解质,在熔融状态下可以导电,D正确;答案为D。
3.(2020·浙江高三开学考试)下列物质属于弱电解质的是( )
A.HCOOH B.SO C.BaSO D.Br
3 4 2
【答案】A
【解析】A.HCOOH在水溶液中只能部分电离,为弱电解质,故A符合题意;
B.SO 在水溶液中与水反应生成的硫酸能导电,而三氧化硫自身不能发生电离,不导电,是非电解质,故
3
B不符合题意;
C.BaSO 在熔融状态下能完全电离,属于强电解质,故C不符合题意;
4
D.电解质首先必须是化合物,Br 是单质,不是电解质也不是非电解质,故D不符合题意;答案选A。
2
4.(2020·辽阳市集美中学月考)下列物质中,①碘化氢 ②KF ③液氨 ④KClO ⑤液氯 ⑥浓
HSO ⑦干冰 ⑧NH NO ⑨澄清石灰水 ⑩CaCO 酒精。是强电解质的一组物质是
2 4 4 3 3
A.②④⑥⑧⑩ B.①②④⑧⑩ C.①②④⑥⑪⑧ D.①④⑥⑧⑩
【答案】B
【解析】①碘化氢完全电离是强电解质;②KF完全电离是强电解质;
③液氨是非电解质;④KClO完全电离是强电解质;
⑤液氯是是单质,不是电解质,也不是非电解质;⑥浓HSO 是混合物,不是电解质,也不是非电解质;
2 4
⑦干冰是二氧化碳,属于非电解质;
⑧NH NO 完全电离是强电解质;⑨澄清石灰水是混合物,不是电解质,也不是非电解质;
4 3
⑩CaCO
3
完全电离是强电解质;⑪酒精是非电解质;即是强电解质的一组物质是①②④⑧⑩,答案选B。
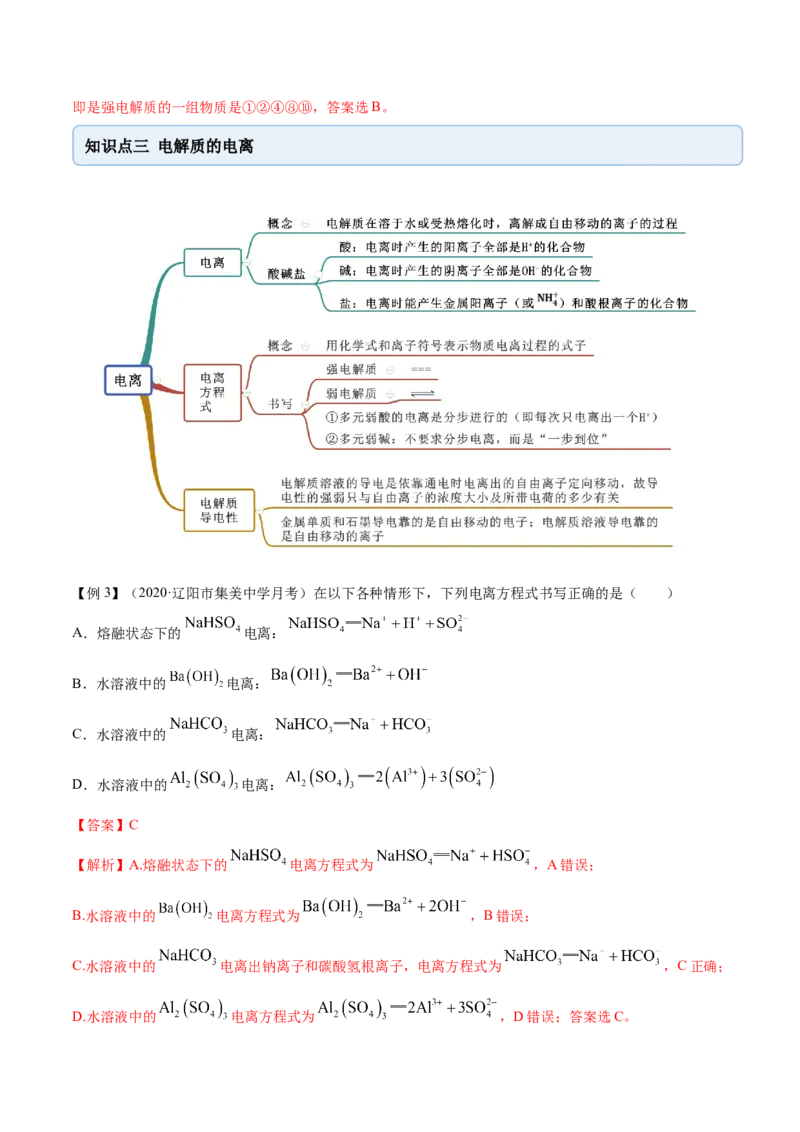
知识点三 电解质的电离
【例3】(2020·辽阳市集美中学月考)在以下各种情形下,下列电离方程式书写正确的是( )
A.熔融状态下的 电离:
B.水溶液中的 电离:
C.水溶液中的 电离:
D.水溶液中的 电离:
【答案】C
【解析】A.熔融状态下的 电离方程式为 ,A错误;
B.水溶液中的 电离方程式为 ,B错误;
C.水溶液中的 电离出钠离子和碳酸氢根离子,电离方程式为 ,C正确;
D.水溶液中的 电离方程式为 ,D错误;答案选C。根据电离方程式的书写规律判断。电离方程式左边是化学式,右边是离子符号,强电解质用等号,弱电解
质用可逆符号,电荷数标在元素符号右上角,原子或原子团个数写在离子符号前
【一隅三反】
1.(2020·大安市第一中学校月考)下列电离方程式正确的是( )
A.MgSO =Mg+2 + B.Ba(OH) =Ba2+ + (OH) -
4 2 2
C.Al (SO )=2Al3+ + 3 D.KClO = K+ + Cl— + 3O2-
2 4 3 3
【答案】 C
【解析】A.Mg+2书写错误,镁离子的符号应该是Mg2+,故A错误;
B. Ba(OH) 的电离方程式为: Ba(OH) = Ba2++ 2OH-,故B错误;
2 2
C.Al (SO ) 的电离方程式为:Al (SO )=2Al3+ + 3 ,故C正确;
2 4 3 2 4 3
D.KClO 的电离方程式为:KClO= K++ ClO -,故D错误;故答案:C。
3 3 3
2.(2019·宁夏兴庆·银川一中)下列各式中,属于正确的电离方程式的是 ( )
A.HCO CO2-+2H+ B.HCO -+H O HO++CO2-
2 3 3 3 2 3 3
C.NaHSO(熔融)=Na++H+ +SO2- D.NH ++HO NH ·H O+H+
4 4 4 2 3 2
【答案】B
【解析】A、多元弱酸分步电离,正确的电离方程式为HCO HCO -+H+、HCO - CO2-+H+,
2 3 3 3 3
故A错误;
B、碳酸氢根电离成碳酸根离子和氢离子,故B正确;
C、NaHSO 在熔融下电离时不产生氢离子,正确的电离方程式为NaHSO(熔融)=Na++HSO -,故C错误;
4 4 4
D、NH ++HO NH ·H O+H+为铵根离子水解的离子方程式,故D错误;故选B。
4 2 3 2
3.下列电离方程式中正确的是
A.HNO===H++N5++3O2− B.Ca(OH) ===Ca2++(OH−)
3 2 2
C.AlCl ===Al+3+3Cl− D.Al (SO )===2Al3++3SO2—
3 2 4 3 4
【答案】D
【解析】A.电离方程式左边是化学式,右边是离子符号。硝酸是强电解质,其电离方程式为HNO=H+
3
+NO−,故A错误;
3B. 氢氧化钙是强电解质,其电离方程式为Ca(OH) =Ca2++2OH-,故B错误;
2
C. 氯化铝是强电解质,其电离方程式为AlCl =Al3++3Cl−,故C错误;
3
D. 硫酸铝是强电解质,其电离方程式为Al (SO )=2Al3++3SO2—,故D正确;
2 4 3 4
综上所述,本题选D。
4.(2018·上海高一课时练习)下列电离方程式错误的是( )
A.(NH )SO 溶于水:(NH )SO ═2NH ++SO2﹣
4 2 4 4 2 4 4 4
B.HPO 溶于水:HPO ═3H++PO3﹣
3 4 3 4 4
C.HF溶于水:HF H++F﹣
D.NaHS溶于水:NaHS═Na++HS﹣,HS﹣ H++S2﹣
【答案】B
【解析】A.盐(NH )SO 在溶液中完全电离,用等号表示,其电离方程式为(NH )SO =2NH++SO2﹣,正确;
4 2 4 4 2 4 4 4
B.HPO 是弱酸,在溶液中部分电离,主要以电解质分子存在,存在电离平衡,用可逆号表示,多元弱酸
3 4
要分步电离,其第一步的电离方程式为:HPO H++H PO ﹣,错误;
3 4 2 4
C.HF属于弱酸,在溶液中部分电离,用可逆号表示,其电离方程式为:HF H++F﹣,正确;
D.NaHS是强电解质,在溶液中完全电离成Na+和HS﹣,HS﹣是弱酸的酸根离子,存在电离平衡,在溶液
中部分电离,所以电离方程式为:NaHS=Na++HS﹣,HS﹣ H++S2﹣,正确。故选B。
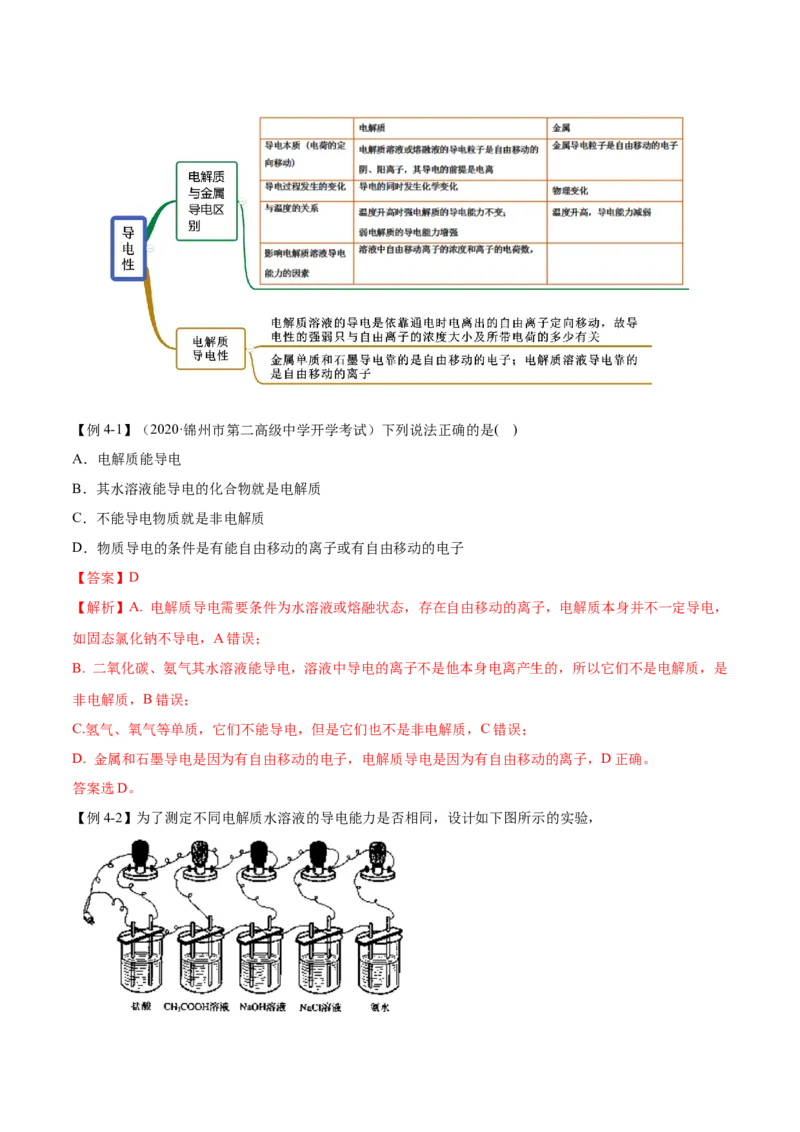
知识点四 电解质的导电性【例4-1】(2020·锦州市第二高级中学开学考试)下列说法正确的是( )
A.电解质能导电
B.其水溶液能导电的化合物就是电解质
C.不能导电物质就是非电解质
D.物质导电的条件是有能自由移动的离子或有自由移动的电子
【答案】D
【解析】A. 电解质导电需要条件为水溶液或熔融状态,存在自由移动的离子,电解质本身并不一定导电,
如固态氯化钠不导电,A错误;
B. 二氧化碳、氨气其水溶液能导电,溶液中导电的离子不是他本身电离产生的,所以它们不是电解质,是
非电解质,B错误;
C.氢气、氧气等单质,它们不能导电,但是它们也不是非电解质,C错误;
D. 金属和石墨导电是因为有自由移动的电子,电解质导电是因为有自由移动的离子,D正确。
答案选D。
【例4-2】为了测定不同电解质水溶液的导电能力是否相同,设计如下图所示的实验,请回答下列问题:
(1)本实验取了盐酸、CHCOOH(CH COOH为一元有机酸)溶液、NaOH溶液、NaCl溶液和氨水五种溶
3 3
液,若要再增加一种溶液,你认为选取下列__________最为合适。
A.NaSO B.Ca(NO ) C.Ba(OH) D.KNO E.MgSO
2 4 3 2 2 3 4
(2)为了排除无关因素的干扰,本实验应控制多种实验条件,如烧杯的规格相同、烧杯内溶液的体积相
等、相同的电极材料、各电极间的距离相等、溶液的浓度相同、灯泡的功率相同等,除此外,你认为还应
控制的条件(或因素)是_______________.
(3)本实验通过观察到_____________________现象,间接说明上述不同电解质溶液导电能力是不同的。
(4)通过本实验,证实了在相同的条件下,不同的电解质溶液导电能力是不同的,从而可以直接推出的
结论是_____________________________________
【答案】(1)D
(2)五种溶液的物质的量浓度相同
(3)灯光亮度不一
(4)不同电解质在水中的电离程度是不同的
【解析】(1)影响导电能力大小的因素之一为:离子所带电荷;盐酸,CHCOOH溶液,NaOH溶液,
3
NaCL溶液和氨水五种溶液中电解质电离出的离子都带一个单位的电荷,硝酸钾电离出的离子带一个单位
的电荷,故选D;
(2)影响导电能力大小的因素之一为离子的浓度,所以还应控制的条件(或因素)是五种溶液的物质的
量浓度相同。
(3)灯泡的亮度与导电能力有关,通过实验观察到的现象是灯光的亮度不一,间接说明上述不同电解质
溶液导电能力是不同的;
(4)本实验的外在条件相同,只有电解质不同,所以得出的结论是:不同电解质在水中的电离程度是不
同的。
【一隅三反】
1.(2020·黑山县黑山中学月考)化学兴趣小组在家中进行化学实验,按照如图连接好线路发现灯泡不亮,
按照右图连接好线路发现灯泡亮,由此得出的结论正确的是( )A.NaCl是非电解质 B.NaCl溶液是电解质
C.NaCl在水溶液中电离出了可以自由移动的离子D.NaCl溶液中,水电离出大量的离子
【答案】C
【解析】A. NaCl属于盐,所以是电解质,A错误;
B. NaCl溶液是混合物所以不是电解质,B错误;
C. 氯化钠固体溶于水后在水分子的作用下,发生电离,电离为可以移动的离子使溶液导电,C正确;
D. 氯化钠溶于水是氯化钠发生了电离,水的电离实际很微弱,D错误;故答案选C。
2.(2020·辽阳市集美中学月考)某学生利用如图所示装置对电解质溶液导电性进行实验探究。下列说法
中正确的是( )
A.闭合开关K后,电流计指针不发生偏转,证明酒精溶液是非电解质
B.闭合开关K,往溶液中通入氯气,随着气体通入,电流计示数增大,故氯气是电解质
C.取用 的蔗糖溶液替换酒精溶液,电流计的示数相同
D.闭合开关K,往烧杯中加 固体,虽然固体溶解,由于不反应,故电流计指针不发生偏转
【答案】C
【解析】A.当开关K闭合后,电流计指针不发生偏转,说明不能形成闭合回路,证明酒精溶液不导电,酒
精是非电解质,A错误;
B.闭合开关K,往溶液中通入氯气,氯气与水反应生成 和次氯酸,这两种酸电离出阴、阳离子,随着
气体通入,离子浓度增大,导电性增强,电流计示数增大,而氯气是单质,氯气既不是电解质也不是非电
解质,溶液导电是两种酸电离的缘故,所以不能得出氯气是电解质的结论,B错误;
C.酒精溶液和蔗糖溶液均不导电,取用 的蔗糖溶液替换该酒精溶液,电流计的示数相同,C正
确;
D.闭合开关K,往烧杯中加入 固体,氯化钠溶于水,电离出阴、阳离子,混合溶液能导电,所以电
流计指针发生偏转,D错误。故选C。
3.(2020·辽阳市集美中学月考)下列关于电解质电离的叙述中正确的是( )
A. 在水中溶解度很小,其导电能力很弱,所以 是弱电解质
B. 在水中溶解度很小,但溶解的 全部电离,所以 是强电解质
C.氯气( )和氨气( )的水溶液导电性都很好,所以它们都是电解质
D.水难电离纯水几乎不导电,水是非电解质
【答案】B
【解析】A. 是强电解质,因为其在水中溶解的部分全部电离,A错误;
B. 是强电解质,因为其在水中溶解的部分全部电离,B正确;
C. 是单质,既不属于电解质,又不属于非电解质, 自身不能电离出离子,不是电解质, 的水
溶液之所以能够导电是因为 与水反应生成了弱电解质 ,C错误;
D.水是弱电解质,D错误;答案选B。