文档内容
第二节 离子反应
第2课时 离子反应
基础巩固
1.下列有关反应中不属于离子反应的是( )
A.NaCO 溶液与澄清石灰水的反应
2 3
B.氢氧化铜与稀硫酸的反应
C.锌与氯化铜溶液的反应
D.二氧化碳与生石灰作用生成碳酸钙的反应
【答案】D
【解析】
离子反应指的是有离子参加或生成的反应。酸、碱、盐在溶液中相互之间的反应都有离子参加,活泼金
属可以把较不活泼的金属从它们的盐溶液中置换出来(K、Ca、Na除外),在这些反应中也都有离子参加,
因此这些反应都属于离子反应。二氧化碳与生石灰的反应没有离子参加,不属于离子反应。
2.加入适量的HSO 溶液,可使溶液中下列离子数量显著减少的是( )。
2 4
A.Cl- B.Ba2+
C.NO-
D.Na+
3
【答案】B
[【解析】加入HSO 溶液后,SO2- 与Ba2+生成沉淀。
2 4 4
3.(2021·洮南市第一中学高一月考)下列各项中两组物质间的反应,可以用同一个离子方程式表示的是
A. 和NaOH; 和
B. 和 ; 和
C. 溶液和少量稀盐酸; 溶液和过量稀盐酸
D. 和NaOH; 和
【答案】A
【解析】
A. 和NaOH反应的离子方程式为H++OH-=H O, 和 反应的离子方程式为H++OH-
2
=H O,故A符合题意;
2
B. 和 反应的离子方程式为2H++SO +2OH-+Ba2+=2H O+BaSO, 和 反应的
2 4
离子方程式为SO +Ba2+=BaSO ,故B不符合题意;
4
C. 溶液和少量稀盐酸反应的离子方程式为CO +H+=HCO , 溶液和过量稀盐酸反应的
离子方程式为CO +2H+=CO +H O,故C不符合题意;
2 2
D. 和NaOH反应的离子方程式为H++OH-=H O, 和 反应的离子方程式为
2
+2H+=Cu2++2H O,故D不符合题意;
2
学科网(北京)股份有限公司故选A。
4.离子方程式CO2-
+2H+ CO↑+H O表示 ( )
3 2 2
A.碳酸盐与盐酸之间的反应
B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与强酸之间的反应
【答案】C。
【解析】
CO2-只代表可溶性的碳酸盐,从此点分析选项A和B都是不正确的;H+只代表强酸而不是一切酸(如弱酸
3
HS、HF、CHCOOH等均不能用H+表示)。
2 3
5.(2022·湖南邵阳·高一期中)下列离子方程式正确的是
A.稀硝酸溶液与氢氧化钠溶液反应:H++OH-=H O
2
B.碳酸钙与盐酸反应: +2H+=CO ↑+H O
2 2
C.稀硫酸与锌反应:HSO +Zn=Zn2++ +H ↑
2 4 2
D.稀硫酸与氢氧化钡溶液混合产生沉淀:Ba2++ =BaSO ↓
4
【答案】A
【解析】A.稀硝酸溶液与氢氧化钠溶液发生中和反应生成硝酸钠和水,硝酸钠、硝酸和氢氧化钠均溶于
水,所以反应的离子方程式为:H++OH-=H O,故A正确;
2
B.碳酸钙不溶于水,在离子方程式里不能拆成离子,故B错误;
C.硫酸是溶于水能电离的电解质,在离子方程式里要写成离子,故C错误;
D.稀硫酸与氢氧化钡溶液反应,不但生成硫酸钡沉淀,还生成水,故D错误;
故选A。
6.下列有关离子反应的说法中正确的是( )。
A.参加离子反应的一定都是电解质
B.任何一种离子的浓度在反应中一定减小
C.没有气体、沉淀、水生成的反应也可能是离子反应
D.所有酸碱中和反应的离子方程式均相同
【答案】C
【解析】
电解质在溶液中的反应是离子反应,但参加离子反应的物质不一定都是电解质,如在置换反应中,单质不是电
解质,A项错误。在离子反应中有些离子浓度不变,如BaCl 与NaSO 的反应中Cl-和Na+均不变,B项错误。
2 2 4
产生沉淀、气体、水只是复分解类型中的部分离子反应,还有一些复分解反应或其他类型的离子反应,可能
没有沉淀、气体或水生成,C项正确。强酸与强碱的稀溶液反应生成可溶性盐和水均可用H++OH- HO
2
来表示,但一些中和反应不能用上述离子方程式表示,如Ba(OH) 稀溶液与稀硫酸的反应,应写为Ba2++2OH-
2
+2H++SO2- BaSO↓+2H O,D项错误。
4 4 2
7.NaHCO 和NaHSO 的溶液混合后,实际参加反应的离子是( )
3 4
A.H+和CO
学科网(北京)股份有限公司B.HCO和HSO
C.Na+、HCO和H+
D.HCO和H+
【答案】D
【解析】
NaHCO 和NaHSO 的电离方程式分别如下:
3 4
NaHCO ===Na++HCO;NaHSO===Na++H++SO,故D项正确。
3 4
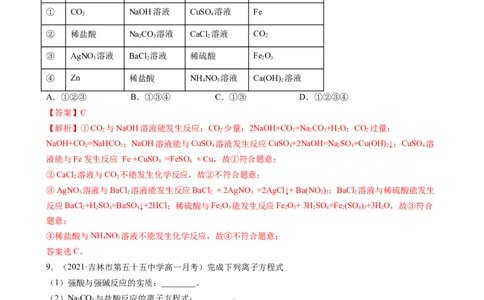
8.下列四组物质,从左至右都能发生化学反应的是(如:a+b-反应 b+c-反应 c+d-反应)
a b c d
① CO NaOH溶液 CuSO 溶液 Fe
2 4
② 稀盐酸 NaCO 溶液 CaCl 溶液 CO
2 3 2 2
③ AgNO 溶液 BaCl 溶液 稀硫酸 Fe O
3 2 2 3
④ Zn 稀盐酸 NH NO 溶液 Ca(OH) 溶液
4 3 2
A.①②③ B.①③④ C.①③ D.①②③④
【答案】C
【解析】①CO 与NaOH溶液能发生反应:CO 少量:2NaOH+CO =Na CO+H O;CO 过量:
2 2 2 2 3 2 2
NaOH+CO =NaHCO;NaOH溶液能与CuSO 溶液发生反应CuSO +2NaOH=Na SO +Cu(OH) ↓;CuSO 溶
2 3 4 4 2 4 2 4
液能与Fe发生反应 Fe +CuSO =FeSO + Cu,故①符合题意;
4 4
②CaCl 溶液与CO 不能发生化学反应,故②不符合题意;
2 2
③AgNO 溶液与BaCl 溶液能发生反应BaCl + 2AgNO =2AgCl↓+ Ba(NO );BaCl 溶液与稀硫酸能发生
3 2 2 3 3 2 2
反应BaCl +H SO =BaSO ↓+2HCl;稀硫酸与Fe O 能发生反应Fe O+ 3H SO =Fe (SO )+3H O,故③符合
2 2 4 4 2 3 2 3 2 4 2 4 3 2
题意;
④稀盐酸与NH NO 溶液不能发生化学反应,故④不符合题意;
4 3
答案选C。
9.(2021·吉林市第五十五中学高一月考)完成下列离子方程式
(1)强酸与强碱反应的实质:________。
(2)NaCO 与盐酸反应的离子方程式:________。
2 3
(3)CaCO 与盐酸反应的离子方程式:________。
3
(4)铝片与硫酸铜溶液:________。
(5)硫酸钠与氯化钡:________。
【答案】
(1)OH-+H+=H O
2
(2) +2H+=H O+CO↑
2 2
(3)CaCO +2H+=Ca2++CO ↑+H O
3 2 2
(4)2Al+3Cu2+=2Al3++3Cu
学科网(北京)股份有限公司(5)Ba2++ =BaSO ↓
4
【解析】
(1)强酸与强碱反应的实质是酸电离产生的H+与碱电离产生的OH-结合生成HO,反应的离子方程式为:
2
OH-+H+=H O。
2
(2)NaCO 与盐酸反应产生NaCl、HO、CO,反应的离子方程式为: +2H+=H O+CO↑。
2 3 2 2 2 2
(3)CaCO 与盐酸反应CaCl 、HO、CO,反应的离子方程式为:CaCO +2H+=Ca2++CO ↑+H O。
3 2 2 2 3 2 2
(4)由于Al的活动性比Cu强,所以铝片与硫酸铜在溶液中发生置换反应产生硫酸铝、铜,反应的离子
方程式为:2Al+3Cu2+=2Al3++3Cu。
(5)硫酸钠与氯化钡在溶液中发生复分解反应产生BaSO 沉淀和NaCl,反应的离子方程式为:Ba2++
4
=BaSO ↓。
4
10.(1)实验室用碳酸钙与盐酸反应制取CO 气体,反应的离子方程式为 ;
2
用澄清石灰水检验CO 气体的离子方程式是 。
2
(2)将表面附有铁锈(主要成分是Fe O)的铁钉放入稀硫酸中,开始反应的离子方程式是
2 3
;反应片刻后,可观察到有气体产生,反应的离子方程式是 。
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控
制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO )治疗胃酸过多的离子方程式为 。
3
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH) ],反应的离子方程式为
3
。
【答案】(1)CaCO+2H+ Ca2++CO ↑+H O
3 2 2
Ca2++2OH-+CO CaCO ↓+H O
2 3 2
(2)Fe O+6H+ 2Fe3++3H O Fe+2H+ Fe2++H ↑
2 3 2 2
(3)①HCO-
+H+ CO↑+H O ②Al(OH) +3H+ Al3++3H O
3 2 2 3 2
【解析】
在书写离子方程式时,碳酸钙、Fe O、单质铁、CO、H、HO等用化学式表示。Ca(OH) 微溶于水,溶液
2 3 2 2 2 2
(澄清石灰水)状态用离子符号表示,悬浊液(石灰乳)状态用化学式表示。
能力提升
11.(2021·山西实验中学)下列实验过程中产生的现象与如图所示坐标图形相符合的是
A.稀盐酸加到一定量NaHCO 溶液中(横坐标是稀盐酸的体积,纵坐标为HCO 数目)
3
学科网(北京)股份有限公司B.稀盐酸滴加到AgNO 溶液中(横坐标是稀盐酸的体积,纵坐标为溶液的导电能力)
3
C.NaOH溶液滴入Ba(HCO ) 溶液中(横坐标是NaOH溶液的体积,纵坐标为沉淀质量)
3 2
D.稀硫酸滴加到Ba(OH) 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
2
【答案】D
【解析】
A.稀盐酸滴加到一定量NaHCO 溶液中,c(HCO )不断减少,减少到0后不会再增大,故A不符合题意;
3
B.稀盐酸滴加到AgNO 溶液中虽然生成氯化银沉淀,但是同时生成了硝酸,溶液中的离子浓度不会减
3
少到0后再增大(若两种溶液的浓度相同,则恰好反应时溶液中的离子浓度变为原来的一半),所以溶
液的导电能力也不会减小到0后再增大,故B不符合题意;
C.NaOH溶液滴入Ba(HCO ) 溶液中生成碳酸钡沉淀,沉淀质量从0逐渐增大到最大值后不变,故C不
3 2
符合题意;
D.稀硫酸滴加到Ba(OH) 溶液中发生的离子反应为2H++SO2-+Ba2++2OH-=2H O+BaSO↓,溶液中的离子
2 4 2 4
浓度逐渐减小,两者恰好反应时离子浓度达到最小值,继续加入氢氧化钡溶液,离子浓度又逐渐增大到
最大值(最大值由氢氧化钡溶液中的离子浓度决定)后不变,所以溶液的导电能力先减小后增大到不变,
故D符合题意;
本题答案D。
12.某同学在实验室中进行如下实验:
编号 Ⅰ Ⅱ Ⅲ
实验
现象 没有明显变化,溶液仍为无色 有沉淀生成,溶液为蓝色 有无色气体放出
以下结论不正确的是( )。
A.Ⅰ中无明显变化,但两溶液混合发生了离子反应
B.Ⅱ中的沉淀应是白色
C.Ⅲ中的离子方程式为2H++Zn Zn2++H ↑
2
D.Ⅲ中发生的反应不是离子反应
【答案】D
【解析】
Ⅰ中无明显变化,但发生反应H++OH- HO,A项正确。Ⅱ中BaCl 与CuSO 溶液反应生成白色的BaSO
2 2 4 4
沉淀,B项正确。Ⅲ中Zn与稀盐酸反应的离子方程式为Zn+2H+ Zn2++H ↑,C项正确。
2
13.(2021·淮北市树人高级中学高一开学考试)在甲、乙两烧杯溶液中,分别含有大量Cu2+、K+、H+、
Cl-、 、OH-6种离子中的3种,已知甲烧杯的溶液呈碱性,则乙烧杯溶液中大量存在的离子是
A.K+、H+、 B. 、OH-、Cl-
C.K+、 、Cl- D.Cu2+、H+、Cl-
学科网(北京)股份有限公司【答案】D
【解析】甲烧杯的溶液呈碱性,则一定含有OH-,与OH-不能大量共存的Cu2+、H+在乙组;与Cu2+、H+不
能大量共存的 在甲组;再从溶液呈电中性分析,甲组中还含有K+,乙组中还含有Cl-,从而得出乙
组中含有Cu2+、H+、Cl-,故选D。
14.(2021·安徽·泾县中学高一阶段练习)某兴趣小组的同学向一定体积的Ba(OH) 溶液中逐滴加入稀盐
2
酸,并测得混合溶液的导电能力随时间变化的曲线如图所示,回答下列问题。
(1)Ba(OH) 的电离方程式为___________。
2
(2)AB段发生的反应的离子方程式为___________。
(3)B处Ba(OH) 溶液与稀盐酸恰好完全中和,此时溶液中主要存在的离子有___________(填离子符号)。
2
(4)下列化学反应的实质与Ba(OH) 溶液与稀盐酸反应的实质相同的是___________(填字母)。
2
A.Ba(OH) 和HSO
2 2 4
B.NaOH和HSO
2 4
C.KOH与HNO
3
【答案】(1)Ba(OH) =Ba2++2OH-
2
(2)H++OH-=H O
2
(3)Ba2+、Cl-
(4)BC
【解析】(1)Ba(OH) 为强电解质,完全电离,其电离方程式为Ba(OH) =Ba2++2OH-;答案为Ba(OH) =Ba2+
2 2 2
+2OH-。
(2)溶液导电能力与离子浓度成正比,A、B段酸碱发生中和反应生成氯化钡和水,溶液体积增大导致离子
浓度减小,溶液导电能力降低,其离子方程式为H++OH-═H O;答案为H++OH-═H O。
2 2
(3)B处Ba(OH) 溶液与稀盐酸恰好完全中和,即Ba(OH) +2HCl=BaCl +2H O,则B点溶质为BaCl ,
2 2 2 2 2
BaCl 是强电解质而完全电离,即BaCl =Ba2++2Cl-,所以B点溶液中主要存在的离子有Ba2+、Cl-;答案为
2 2
Ba2+、Cl-。
(4)Ba(OH) 溶液与稀盐酸反应为强酸强碱发生中和反应生成可溶性的盐和水;
2
A.Ba(OH) 和HSO 为强酸强碱的中和反应,但二者生成难溶性盐,故A不符合题意;
2 2 4
B.NaOH和HSO 为强酸强碱的中和反应,且生成可溶性盐,故B符合题意;
2 4
C.KOH与HNO 为强酸强碱的中和反应,且生成可溶性盐,故C符合题意;
3
答案为BC。
学科网(北京)股份有限公司学科网(北京)股份有限公司学科网(北京)股份有限公司