文档内容
第三节 化学反应的方向
一、化学反应自发进行方向的判据
(一)焓判据——自发反应与焓变的关系:
多数能自发进行的化学反应是放热反应,但有很多吸热反应也能自发进行。因此,只根据焓变
来判断反应进行的方向是不全面的。反应焓变是与反应进行方向有关的因素之一,但不是决定反应
能否自发进行的唯一因素。
(二)熵判据
1、熵
(1)定义:熵是衡量体系混乱度大小的物理量。
(2)符号和单位:S,常用单位:J/(mol·K)
(3)影响熵大小的因素:混乱度越大→体系越无序→熵值越大
①与物质的量的关系:物质的量越大→粒子数越多→熵值越大
②对于同一物质,当物质的量相同时,S(g)>S(l)>S(s)
③不同物质熵值的关系:I、物质组成越复杂→熵值越大
II、对于原子种类相同的物质:分子中原子数越多→熵值越大
2、熵变
(1)定义:发生化学反应时物质熵的变化称为熵变,符号为ΔS
(2)计算公式:ΔS=生成物总熵-反应物总熵
3、熵判据——自发反应与熵变的关系
多数能自发进行的化学反应是熵增的反应。熵变是与反应进行方向有关的因素之一,但不是决
定反应能否自发进
行的唯一因素。因此,只根据熵变来判断反应进行的方向是不全面的。
二、自由能与化学反应的方向
(一)自由能与化学反应的方向:在等温、等压条件下的封闭体系中(不考虑体积变化做功以外的
其他功),自由能(符号为ΔG,单位为kJ/mol)的变化综合反映了体系的焓变和熵变对自
发过程的影响:即ΔG=ΔH-TΔS。这时,化学反应总是向着自由能减小的方向进行,直到
体系达到平衡。即:
ΔG=ΔH-TΔS<0,反应能自发进行;
ΔG=ΔH-TΔS=0,反应处于平衡状态;ΔG=ΔH-TΔS>0,反应不能自发进行。
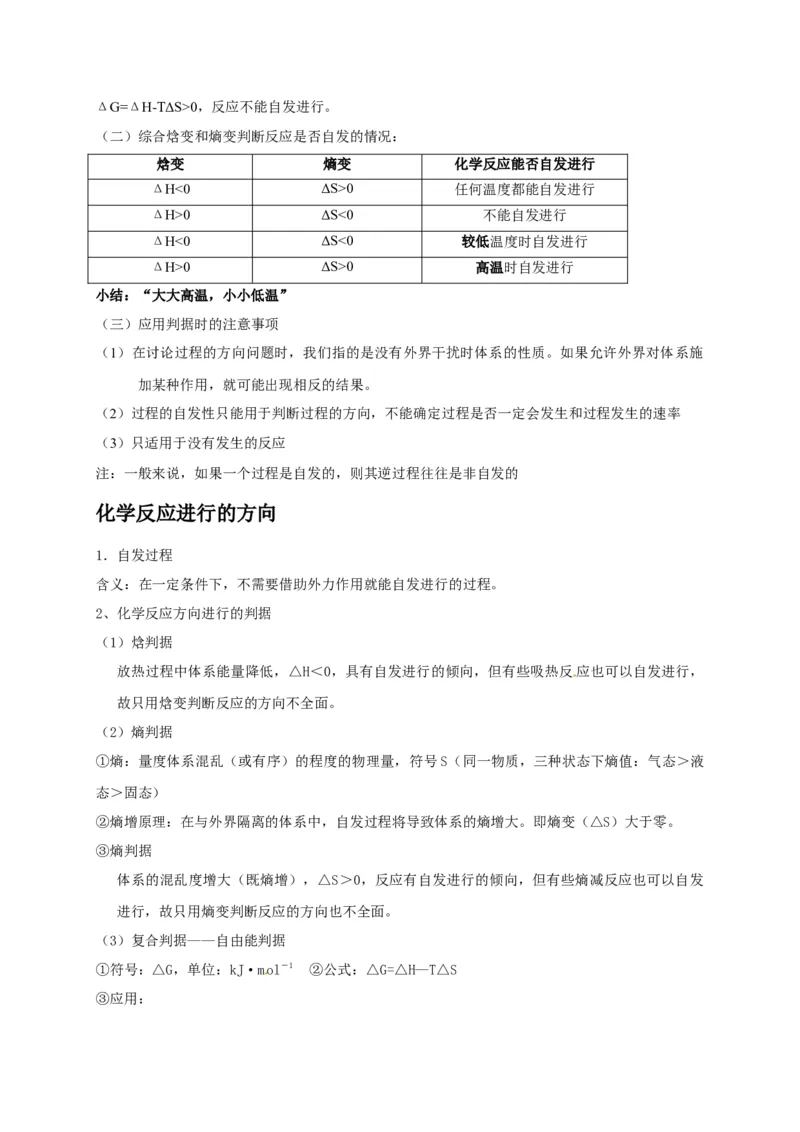
(二)综合焓变和熵变判断反应是否自发的情况:
焓变 熵变 化学反应能否自发进行
ΔH<0 ΔS>0 任何温度都能自发进行
ΔH>0 ΔS<0 不能自发进行
ΔH<0 ΔS<0 较低温度时自发进行
ΔH>0 ΔS>0 高温时自发进行
小结:“大大高温,小小低温”
(三)应用判据时的注意事项
(1)在讨论过程的方向问题时,我们指的是没有外界干扰时体系的性质。如果允许外界对体系施
加某种作用,就可能出现相反的结果。
(2)过程的自发性只能用于判断过程的方向,不能确定过程是否一定会发生和过程发生的速率
(3)只适用于没有发生的反应
注:一般来说,如果一个过程是自发的,则其逆过程往往是非自发的
化学反应进行的方向
1.自发过程
含义:在一定条件下,不需要借助外力作用就能自发进行的过程。
2、化学反应方向进行的判据
(1)焓判据
放热过程中体系能量降低,△H<0,具有自发进行的倾向,但有些吸热反应也可以自发进行,
故只用焓变判断反应的方向不全面。
(2)熵判据
①熵:量度体系混乱(或有序)的程度的物理量,符号S(同一物质,三种状态下熵值:气态>液
态>固态)
②熵增原理:在与外界隔离的体系中,自发过程将导致体系的熵增大。即熵变(△S)大于零。
③熵判据
体系的混乱度增大(既熵增),△S>0,反应有自发进行的倾向,但有些熵减反应也可以自发
进行,故只用熵变判断反应的方向也不全面。
(3)复合判据——自由能判据
①符号:△G,单位:kJ·mol-1 ②公式:△G=△H—T△S
③应用:△G<0 能自发进行
△G=0 平衡状态
△G>0 不能自发进行
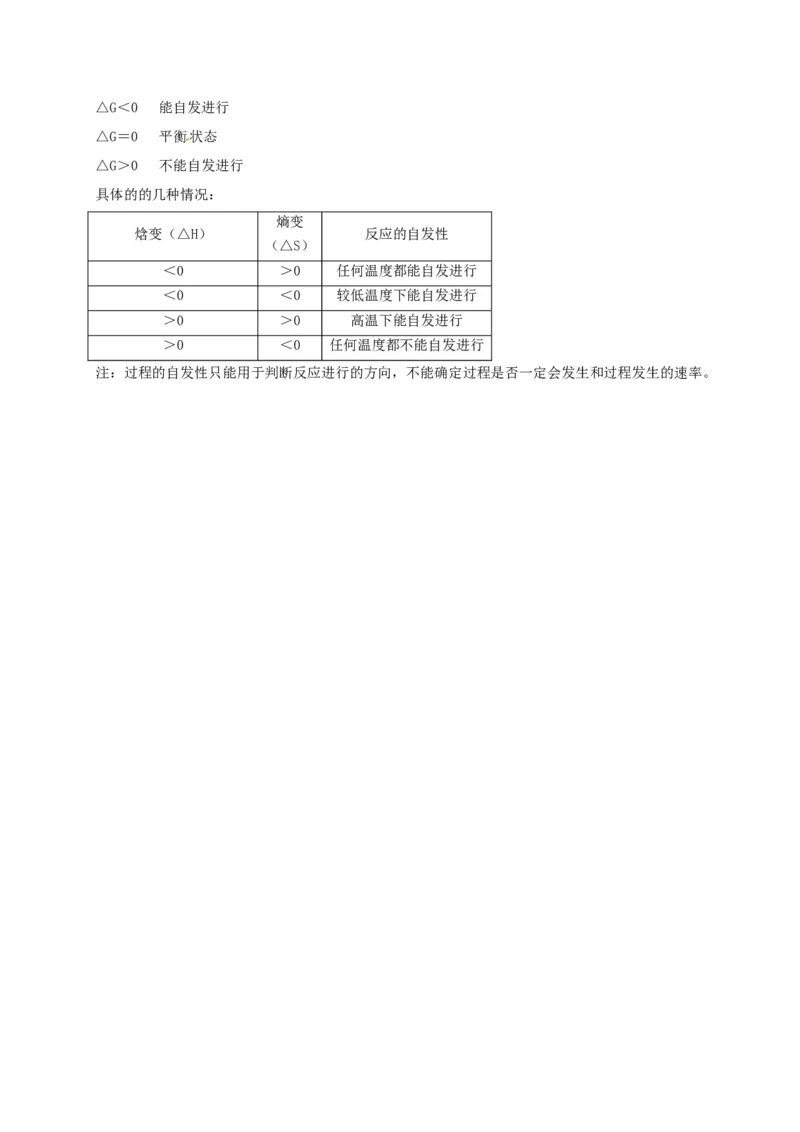
具体的的几种情况:
熵变
焓变(△H) 反应的自发性
(△S)
<0 >0 任何温度都能自发进行
<0 <0 较低温度下能自发进行
>0 >0 高温下能自发进行
>0 <0 任何温度都不能自发进行
注:过程的自发性只能用于判断反应进行的方向,不能确定过程是否一定会发生和过程发生的速率。