文档内容
第六章单元测试题
一、选择题(下列各题只有一个选项符合题意,每小题3分,共60分)
1.下列说法中错误的是( )
A.化学反应中的能量变化通常表现为热量的变化
B.化学键的断裂和形成是化学反应中能量变化的主要原因
C.需要加热才能发生的反应一定是吸热反应
D.如果一个反应是放热反应,说明反应物总能量大于生成物总能量
2.如图是铜﹣锌原电池示意图。下列有关该原电池的描述中正确的是( )
A.锌片作正极,不断溶解
B.铜片作负极,有气泡产生
C.负极反应:Zn2++2e﹣═Zn
D.正极反应:2H++2e﹣═H ↑
2
3.一定条件下,在2L密闭容器中发生反应:2A(s)+3B(g)═2C(g)+4D(g),测得5min内,A
的物质的量减小了10mol,则0~5min内该反应的平均速率为( )
A.v(A)=1.0mol/(L•min) B.v(B)=1.5mol/(L•min)
C.v(C)=2.0mol/(L•min) D.v(D)=0.5mol/(L•min)
4.电化学气敏传感器可用于监测环境中NH 的含量,其工作理示意图如图。下列说法正确的
3
是( )
A.b电极反应式为:O +2H O+4e﹣═4OH﹣
2 2
B.溶液中OH﹣向电极b移动
C.NH 的还原产物为N
3 2
D.电流方向:由a经外电路到b
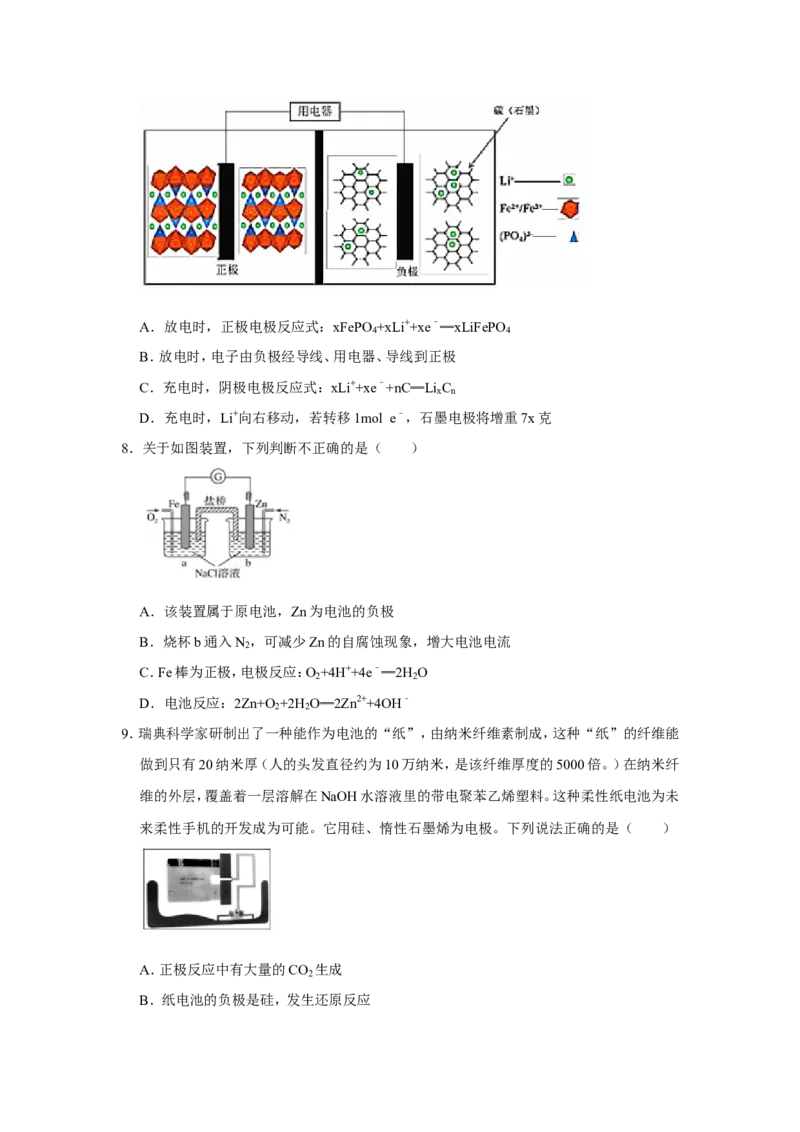
5.新华网报道,我国固体氧化物燃料电池技术研发取得新突破。科学家利用该科技实现了H S废气资源回收能量,并H S得到单质硫的原理如图所示。下列说法正确的是( )
2 2
A.电极a为电池正极
B.电路中每流过4mol电子,正极消耗1molO
2
C.电极b上的电极反应:O +4e﹣+4H+═2H O
2 2
D.电极a上的电极反应:2H S+2O2﹣﹣2e﹣═S +2H O
2 2 2
6.自然界中臭氧形成反应3O(g)→2O(g)+Q的能量变化如图所示。下列说法中错误的是(
2 3
)
A.2O →3O 为放热反应
3 2
B.氧气比臭氧稳定
C.反应物的能量低于生成物
D.总反应的Q=E ﹣E
3 1
7.高能LiFePO 电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过
4
程中只让Li+通过。结构如图所示。原理如下:(1﹣x)LiFePO +xFePO +Li C
4 4 x n
LiFePO +nC。
4
下列说法不正确的是( )A.放电时,正极电极反应式:xFePO +xLi++xe﹣═xLiFePO
4 4
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阴极电极反应式:xLi++xe﹣+nC═Li C
x n
D.充电时,Li+向右移动,若转移1mol e﹣,石墨电极将增重7x克
8.关于如图装置,下列判断不正确的是( )
A.该装置属于原电池,Zn为电池的负极
B.烧杯b通入N ,可减少Zn的自腐蚀现象,增大电池电流
2
C.Fe棒为正极,电极反应:O +4H++4e﹣═2H O
2 2
D.电池反应:2Zn+O +2H O═2Zn2++4OH﹣
2 2
9.瑞典科学家研制出了一种能作为电池的“纸”,由纳米纤维素制成,这种“纸”的纤维能
做到只有20纳米厚(人的头发直径约为10万纳米,是该纤维厚度的5000倍。)在纳米纤
维的外层,覆盖着一层溶解在NaOH水溶液里的带电聚苯乙烯塑料。这种柔性纸电池为未
来柔性手机的开发成为可能。它用硅、惰性石墨烯为电极。下列说法正确的是( )
A.正极反应中有大量的CO 生成
2
B.纸电池的负极是硅,发生还原反应C.在石墨电极表面有O 生成
2
D.电池放电时,溶液的pH值变小
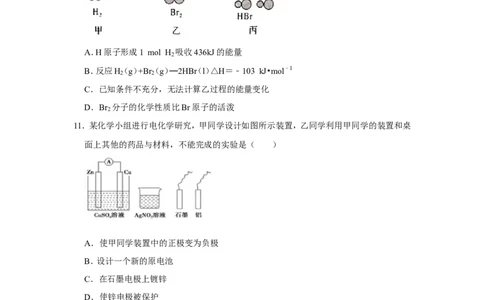
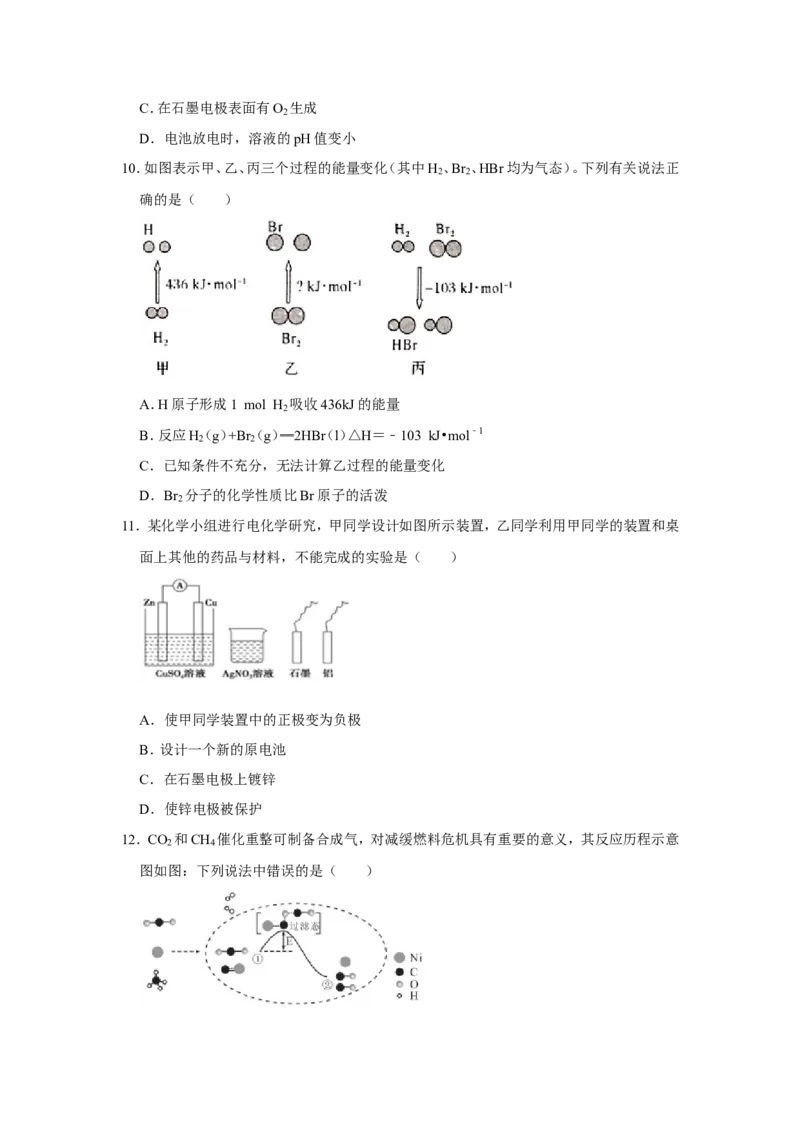
10.如图表示甲、乙、丙三个过程的能量变化(其中H 、Br 、HBr均为气态)。下列有关说法正
2 2
确的是( )
A.H原子形成1 mol H 吸收436kJ的能量
2
B.反应H(g)+Br(g)═2HB(r l)△H=﹣103 kJ•mol﹣1
2 2
C.已知条件不充分,无法计算乙过程的能量变化
D.Br 分子的化学性质比Br原子的活泼
2
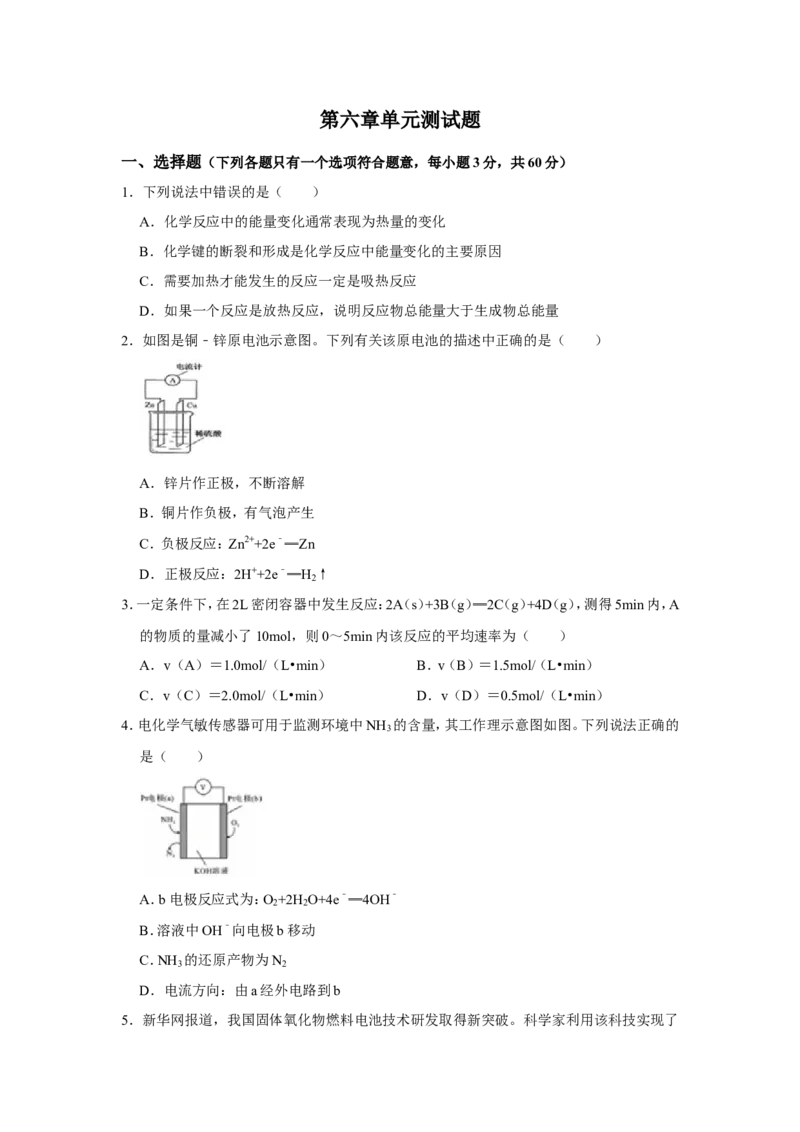
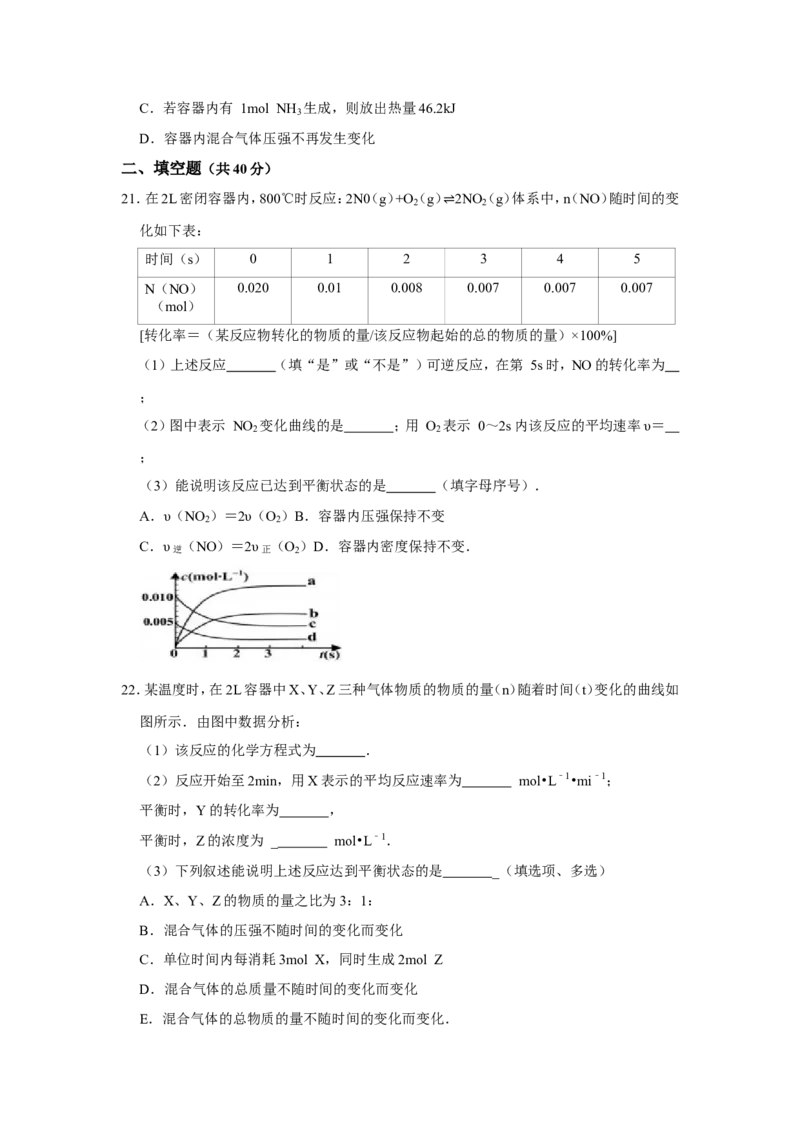
11.某化学小组进行电化学研究,甲同学设计如图所示装置,乙同学利用甲同学的装置和桌
面上其他的药品与材料,不能完成的实验是( )
A.使甲同学装置中的正极变为负极
B.设计一个新的原电池
C.在石墨电极上镀锌
D.使锌电极被保护
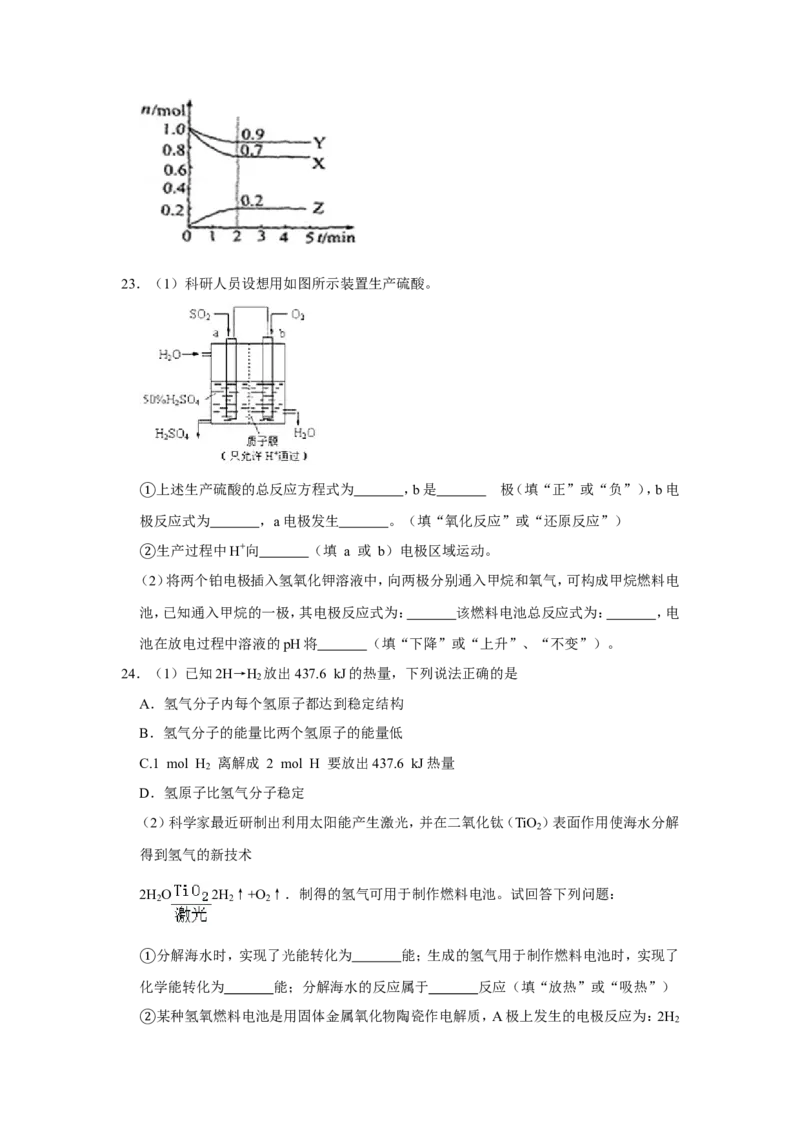
12.CO 和CH 催化重整可制备合成气,对减缓燃料危机具有重要的意义,其反应历程示意
2 4
图如图:下列说法中错误的是( )A.过程 一 是吸热反应
B.Ni是该①反应②的催化剂
C.过程 一 既有碳氧键的断裂,又有碳氧键的形成
D.反应①的总化②学方程式可表示为:CH
4
+CO
2
2CO+2H
2
13.在一固定体积的容器中,发生制水煤气反应C(s)+H O(g)═CO(g)+H(g),可使反应速
2 2
率增大的措施是( )
增大压强
①升高温度
②通入He
③增加碳的量
④用等量炭粉代替焦炭
⑤A. B. C. D.
14.下列①关②于⑤化学反应速率的②说③法正④确⑤的是( )①②③⑤ ②③④
A.对于化学反应来说,反应速率越大,反应现象越明显
B.常温下铁片和硫酸反应,产生氢气的速率随硫酸浓度的增加而增加
C.温度、催化剂、压强的变化都能导致反应物活化分子百分数改变
D.对于一个可逆反应,若化学平衡发生移动,则速率一定发生了改变
15.在只有气体参加的反应中,改变下列条件,能使反应物中单位体积内活化分子数和活化
分子百分数同时增大的是( )
A.增大反应物的浓度 B.增大压强
C.升高温度 D.移去生成物
16.在一密闭容器中进行如下反应:2SO(气)+O(气) 2SO(气),已知反应过程中某一时
2 2 3
刻SO 、O 、SO 的浓度分别为0.2mol/L、0.1mol/L、0⇌.2mol/L,当反应达平衡时,可能存在
2 2 3
的数据是( )
A.SO 为0.4mol/L、O 为0.2mol/L
2 2
B.SO 为0.25mol/L
2
C.SO 、SO 均为0.15mol/L
2 3
D.SO 为0.4mol/L
3
17.下列四组实验中,反应速率最快的是( )
组别 A B C D
条件H O 的溶液体积/mL 10 10 10 10
2 2
H O 溶液质量分数/% 6 6 3 6
2 2
温度/℃ 20 40 40 40
MnO 质量/g 0.05 0.05 0.05 0
2
A.A B.B C.C D.D
18.已知:CH(g)+2NO(g) N(g)+CO(g)+2H O(g)△H<0,在 1 L 密闭容器中分别加
4 2 2 2 2
入 0.50 mol CH 和 1.0 ⇌mol NO ,保持温度不变,测得 n(CH )随时间变化的有关实验
4 2 4
数据如表所示:下列说法不正确的是( )
时间/min 0 10 20 30 40 50
n(CH )/mo 0.5 0.35 0.25 0.17 0.10 0.10
4
l
A.0~20 min 内,NO 的反应速率为 0.025mol•L﹣1•min﹣1
2
B.随着反应的进行,反应物的浓度降低,反应速率减慢
C.由实验数据可知,该反应在 40min 时才达平衡状态
D.达平衡时,二氧化氮的转化率与甲烷的转化率相等
19.在一定条件下,将NH 放入固定容积的密闭容器中使其发生分解反应,达到平衡状态后,
3
改变其中一个条件X,Y随X的变化符合图中曲线的是( )
当X表示温度时,Y表示NH 的物质的量
3
①当X表示压强时,Y表示NH
3
的转化率
②当X表示反应时间时,Y表示混合气体的密度
③当X表示NH
3
的物质的量时,Y表示某一生成物的物质的量
④
A.只有 正确 B.只有 正确
C.只有① 正确 D. ①② 都正确
20.已知:N①
2
(g②)+③3H
2
(g) 2NH
3
△H=﹣924kJ•m①ol② ﹣1.③在④恒容密闭容器内,投入2molN
2
和6molH 发生反应,当⇌反应达到平衡状态时,下列说法不正确的是( )
2
A.其他条件不变,升高温度,平衡被破坏,逆反应速率增大,正反应速率减小
B.一定存在2v(H
2
)
正
=3v(NH
3
)
正C.若容器内有 1mol NH 生成,则放出热量46.2kJ
3
D.容器内混合气体压强不再发生变化
二、填空题(共40分)
21.在2L密闭容器内,800℃时反应:2N0(g)+O(g) 2NO(g)体系中,n(NO)随时间的变
2 2
化如下表: ⇌
时间(s) 0 1 2 3 4 5
N(NO) 0.020 0.01 0.008 0.007 0.007 0.007
(mol)
[转化率=(某反应物转化的物质的量/该反应物起始的总的物质的量)×100%]
(1)上述反应 (填“是”或“不是”)可逆反应,在第 5s时,NO的转化率为
;
(2)图中表示 NO 变化曲线的是 ;用 O 表示 0~2s内该反应的平均速率υ=
2 2
;
(3)能说明该反应已达到平衡状态的是 (填字母序号).
A.υ(NO )=2υ(O )B.容器内压强保持不变
2 2
C.υ逆 (NO)=2υ正 (O
2
)D.容器内密度保持不变.
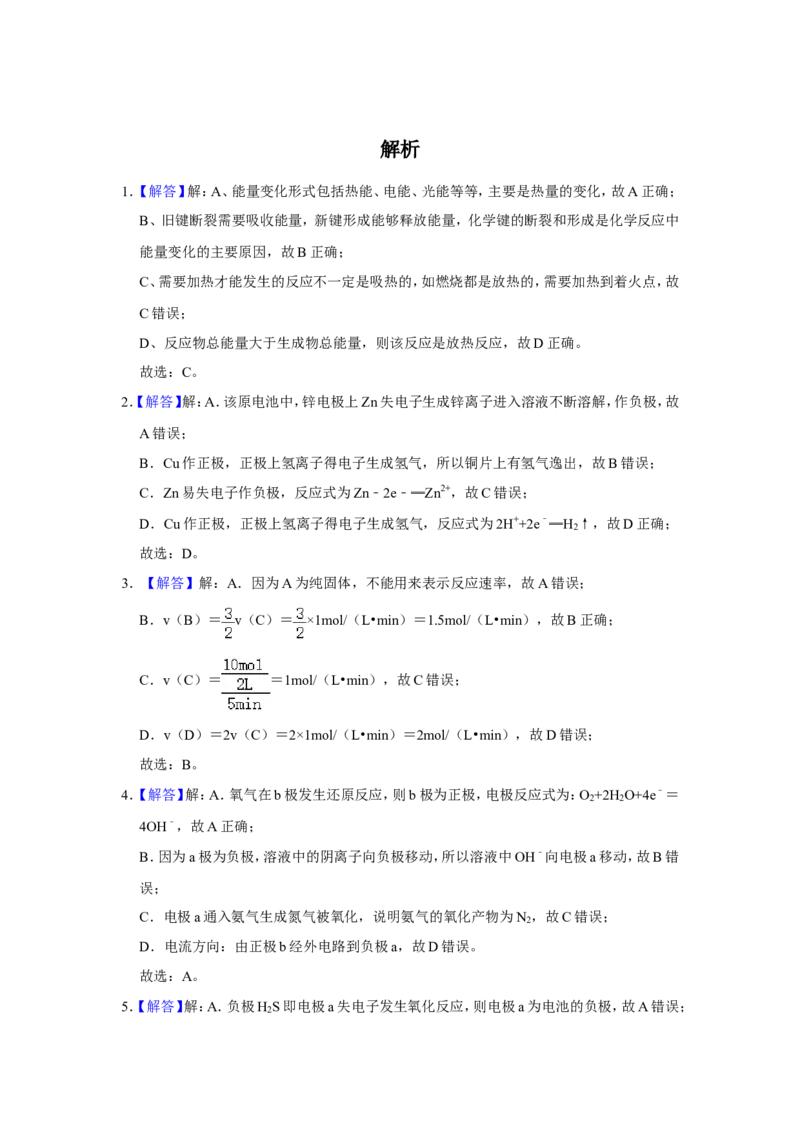
22.某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如
图所示.由图中数据分析:
(1)该反应的化学方程式为 .
(2)反应开始至2min,用X表示的平均反应速率为 mol•L﹣1•mi﹣1;
平衡时,Y的转化率为 ,
平衡时,Z的浓度为 _ mol•L﹣1.
(3)下列叙述能说明上述反应达到平衡状态的是 _(填选项、多选)
A.X、Y、Z的物质的量之比为3:1:
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2mol Z
D.混合气体的总质量不随时间的变化而变化
E.混合气体的总物质的量不随时间的变化而变化.23.(1)科研人员设想用如图所示装置生产硫酸。
上述生产硫酸的总反应方程式为 ,b是 极(填“正”或“负”),b电
①极反应式为 ,a电极发生 。(填“氧化反应”或“还原反应”)
生产过程中H+向 (填 a 或 b)电极区域运动。
(②2)将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,可构成甲烷燃料电
池,已知通入甲烷的一极,其电极反应式为: 该燃料电池总反应式为: ,电
池在放电过程中溶液的pH将 (填“下降”或“上升”、“不变”)。
24.(1)已知2H→H 放出437.6 kJ的热量,下列说法正确的是
2
A.氢气分子内每个氢原子都达到稳定结构
B.氢气分子的能量比两个氢原子的能量低
C.1 mol H 离解成 2 mol H 要放出437.6 kJ热量
2
D.氢原子比氢气分子稳定
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO )表面作用使海水分解
2
得到氢气的新技术
2H O 2H ↑+O ↑.制得的氢气可用于制作燃料电池。试回答下列问题:
2 2 2
分解海水时,实现了光能转化为 能;生成的氢气用于制作燃料电池时,实现了
①化学能转化为 能;分解海水的反应属于 反应(填“放热”或“吸热”)
某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为:2H
2
②+2O2‾﹣4e‾=2H O,则B极的电极反应式为:
2
(3)已知某电池的总反应为:Zn+2MnO +2NH Cl═ZnCl +2NH ↑+Mn O +H O,写出该电
2 4 2 3 2 3 2
池的电极反应方程式:负极 正极解析
1.【解答】解:A、能量变化形式包括热能、电能、光能等等,主要是热量的变化,故A正确;
B、旧键断裂需要吸收能量,新键形成能够释放能量,化学键的断裂和形成是化学反应中
能量变化的主要原因,故B正确;
C、需要加热才能发生的反应不一定是吸热的,如燃烧都是放热的,需要加热到着火点,故
C错误;
D、反应物总能量大于生成物总能量,则该反应是放热反应,故D正确。
故选:C。
2.【解答】解:A.该原电池中,锌电极上Zn失电子生成锌离子进入溶液不断溶解,作负极,故
A错误;
B.Cu作正极,正极上氢离子得电子生成氢气,所以铜片上有氢气逸出,故B错误;
C.Zn易失电子作负极,反应式为Zn﹣2e﹣═Zn2+,故C错误;
D.Cu作正极,正极上氢离子得电子生成氢气,反应式为2H++2e﹣═H ↑,故D正确;
2
故选:D。
3.【解答】解:A.因为A为纯固体,不能用来表示反应速率,故A错误;
B.v(B)= v(C)= ×1mol/(L•min)=1.5mol/(L•min),故B正确;
C.v(C)= =1mol/(L•min),故C错误;
D.v(D)=2v(C)=2×1mol/(L•min)=2mol/(L•min),故D错误;
故选:B。
4.【解答】解:A.氧气在b极发生还原反应,则b极为正极,电极反应式为:O +2H O+4e﹣=
2 2
4OH﹣,故A正确;
B.因为a极为负极,溶液中的阴离子向负极移动,所以溶液中OH﹣向电极a移动,故B错
误;
C.电极a通入氨气生成氮气被氧化,说明氨气的氧化产物为N ,故C错误;
2
D.电流方向:由正极b经外电路到负极a,故D错误。
故选:A。
5.【解答】解:A.负极H S即电极a失电子发生氧化反应,则电极a为电池的负极,故A错误;
2B.正极O 即电极b得电子发生还原反应,电极反应为:O +4e﹣=2O2﹣,所以电路中每流
2 2
过4mol电子,正极消耗1molO
2
,故B正确;
C.电极b为O 得电子发生还原反应,电极反应为:O +4e﹣=2O2﹣,故C错误;
2 2
D.电极a失电子发生氧化反应,则电极反应为:2H S+2O2﹣﹣4e﹣═S +2H O,故D错误。
2 2 2
故选:B。
6.【解答】解:A.由能量变化图可知,O 能量高于O 能量,所以2O →3O 为放热反应,故A
3 2 3 2
正确;
B.由能量变化图可知,O 能量高于O 能量,能量越低越稳定,所以氧气比臭氧稳定,故B
3 2
正确;
C.由能量变化图可知,反应物的能量低于生成物,故C正确;
D.3O (g)→2O (g)+Q,Q=E ﹣E ,故D错误;
2 3 2 1
故选:D。
7.【解答】解:A.放电正极上FePO 得到电子发生还原反应生成LiFePO ,正极电极反应式:
4 4
xFePO +xLi++xe﹣═xLiFePO ,故A正确;
4 4
B.原电池中电子流向是负极﹣导线﹣用电器﹣导线﹣正极,则放电时,电子由负极经导
线、用电器、导线到正极,故B正确;
C.根据总反应:(1﹣x)LiFePO +xFePO +Li C LiFePO +nC,则充电时,阴极C变化
4 4 x n 4
为Li C ,电极反应式:xLi++xe﹣+nC═Li C ,故C正确;
x n x n
D.充电时,Li+向阴极即右移动,电极反应式:xLi++xe﹣+nC═Li C ,则石墨电极增重的质
x n
量就是锂离子的质量,根据关系式:
xLi+~~~xe﹣
1mol 1mol
可知若转移1mole﹣,就增重1molLi+,即7g,故D错误;
故选:D。
8.【解答】解:A、该装置属于Zn空气电池,Zn比Fe活泼,Zn为负极,Fe为正极,故A正确;
B、b烧杯中通氮气,有利于驱除溶液中的溶解氧,减少Zn与b中溶解氧发生的自腐蚀,增
大电池电流,故B正确;
C、Fe为正极,正极上氧气得电子发生还原反应生成氢氧根离子,反应为 O +2H O+4e﹣
2 2
═4OH﹣,故C错误;
D、因盐桥隔离了Zn2+和OH﹣,电池反应为2Zn+O +2H O═2Zn2++4OH﹣,故D正确。
2 2故选:C。
9.【解答】解:A.正极反应若产生大量CO ,则会膨胀损坏电池,所以不可能有大量的CO 生
2 2
成,故A错误;
B.纸电池的负极是硅,发生氧化反应,故B错误;
C.正极为惰性石墨烯,而产生氧气的反应应是OH﹣的失去电子,为氧化反应,不可能在
正极生成,故C错误;
D.电池放电时,总反应为Si+2NaOH+H O=Na SiO +2H ↑,则消耗氢氧化钠,所以溶液
2 2 3 2
的pH值变小,故D正确;
故选:D。
10.【解答】解:A.1 mol H 分解生成H原子吸收436kJ的能量,则H原子形成1 mol H 放
2 2
出436kJ的能量,故A错误;
B.H 、Br 、HBr均为气态,则由图可得,H(g)+Br(g)═2HB(r g)△H=﹣103 kJ•mol﹣1,
2 2 2 2
故B错误;
C.HBr的键能未知,无法由焓变等于断裂化学键吸收的能量减去成键释放的能量计算乙
过程的能量变化,故C正确;
D.断裂化学键吸收能量,则Br 分子的化学性质比Br原子的稳定,故D错误;
2
故选:C。
11.【解答】解:A、装置甲是原电池,锌做负极,铜作正极,若将锌换成石墨,电解质换成硝酸
银溶液时,即铜变成负极,故A不选;
B、将铝、石墨和硝酸银组成一个新的原电池,故B不选;
C、因为只有硫酸铜和硝酸银2种电解质溶液,并且铜离子和银离子的氧化性都比锌离子
强,所以不可能析出锌,故C选;
D、将锌与铝组合形成原电池,锌作正极被保护,故D不选。
故选:C。
12.【解答】解:A、反应物的能量高于生成物的能量,此反应为放热反应,故A错误;
B、Ni在此反应中先消耗、后生成,故为催化剂,故B正确;
C、由反应物、生成物可知, → 既有碳氧键的断裂,又有碳氧键的形成,故C正确;
D、此反应的反应物为CO
2
和①CH②4 ,Ni做催化剂,产物为CO和氢气,故化学方程式为
CH +CO 2CO+2H ,故D正确。
4 2 2
故选:A。
13.【解答】解: 增大压强,可增大反应速率,故正确;
①升高温度,可增大反应速率,故正确;
②固定体积通入He,反应浓度不变,反应速率不变,故错误;
③增加碳的量,增加固体物质的浓度不影响化学反应速率,故错误。
④用等量炭粉代替焦炭,固体表面积增大,可增大反应速率,故正确;
⑤故选:A。
14.【解答】解:A.反应速率与反应现象无关,如中和反应的速率很快,但现象不明显,故A错
误;
B、随硫酸浓度增大,铁与浓硫酸反应的机理发生改变,铁与浓硫酸反应不产生氢气,而发
生钝化,故B错误;
C、温度、正催化剂,均可提高反应物中的活化分子百分数;而压强和浓度只改变活化分子
的浓度,不改变百分数,故C错误;
D、化学平衡的移动是因为正、逆反应的速率不等导致,所以化学平衡发生移动,则速率一
定发生了改变,故D正确;
故选:D。
15.【解答】解:增大反应物的浓度和增大压强,只能增大活化分子数,不能增大活化分子百分
数,而升高温度、加入催化剂既能增大活化分子数,又能增大活化分子百分数,移去生成
物,活化分子数目减少,只有C正确。
故选:C。
16.【解答】解:2SO (g)+O (g) 2SO (g),
2 2 3
某时刻(mol/L) 0.2 0.1 ⇌ 0.2
极限转化(mol/L) 0.4 0.2 0
极限转化(mol/L) 0 0 0.4
A.SO 和O 的浓度增大,说明反应向逆反应方向进行建立平衡,若SO 完全反应,则SO
2 2 3 2
和O 的浓度浓度分别为0.4mol/L、0.2mol/L,但SO 不可能完全转化,故A错误;
2 3
B.SO 为0.25mol/L,SO 的浓度增大,说明反应向逆反应方向进行建立平衡,若SO 完全
2 2 3
反应,则SO 的浓度浓度为0.4mol/L,实际浓度为0.25mol/L小于0.4mol/L,故B正确;
2
C.反应物、生产物的浓度不可能同时减小,只能一个减小,另一个增大,故C错误;
D.SO 为0.4mol/L,SO 的浓度增大,说明该反应向正反应方向进行建立平衡,若SO 和
3 3 2
氧气完全反应,SO 的浓度的浓度为0.4mol/L,达到平衡的实际浓度应该小于0.4mol/L,
3
故D错误;
故选:B。17.【解答】解:对比四组实验,B 实验中温度、浓度最高,并且加入了催化剂,所以 B反应速
率最快,
故选:B。
18.【解答】解:A.由表中数据可知20min内,△n(CH )=0.25mol,则消耗0.5molNO ,反应
4 2
速率为v= = =0.025mol•L﹣1•min﹣1,故A正确;
B.反应速率与浓度呈正比,浓度越小,反应速率越小,故B正确;
C.由表中数据可知40min时处于平衡状态,但不一定在40min时才达到平衡,故C错误;
D.加入 0.50 mol CH 和 1.0 mol NO ,二者按1:2参加反应,则转化率相等,故D正确。
4 2
故选:C。
19.【解答】解: 反应吸热,升高温度,平衡向正反应方向移动,NH 的物质的量减小,故正
3
确; ①
增大压强,平衡向逆反应方向移动,NH 的转化率减小,故正确;
3
②达到平衡后,因混合气体的质量和体积不变,混合气体的密度将不变,故错误;
③增加NH
3
的物质的量时,平衡向正方向移动,某一生成物的物质的量增加,故错误。
④故选:B。
20.【解答】解:A、升高温度正、逆反应速率都增大,故A错误;
B、任意时刻都符合,速率之比等于物质的量之比,所以一定存在 2v(H )正=3 v(NH )
2 3
正,故B正确;
C、由反应的热化学方程式可知,有2mol NH 生成,则放出热量 92.4 kJ,所以若容器内
3
有1mol NH 生成,则放出热量46.2kJ,故C正确;
3
D、容器内混合气体压强不再发生变化时,说明气体的物质的量不变,反应达平衡状态,故
D正确;
故选:A。
21.【解答】解:(1)从图象分析,随反应时间的延长,各物质的浓度不再不变,且反应物没有
完全反应,所以反应为可逆反应,5s时反应达到平衡状态,NO物质的量变化了0.02mol﹣
0.007mol=0.013mol,转化率= ×100%= ×100%=65%,
故答案为:是; 65%;
(2)根据一氧化氮物质的量的变化知,该反应向正反应方向移动,则二氧化氮的物质的量在不断增大,且同一时间段内,一氧化氮减少的物质的量等于二氧化氮增加的物质的量,
所以表示NO 的变化的曲线是b,
2
0~2s内v(NO)= =0.0030mol(/ L.min),同一化学反应同一时间
段内,各物质的反应速率之比等于其计量数之比,所以氧气的反应速率为
0.0015mol/(L•s),
故答案为:b;0.0015mol/(L•s);
(3)A.反应速率之比等于化学方程式计量数之比,υ(NO )=2υ(O )是正反应速率之比,
2 2
无法判断正逆反应速率是否相等,故A错误;
B.反应前后气体体积不同,压强不变说明正逆反应速率相等,各组分浓度不变,故B正确;
C.v逆 (NO)=2v正 (O
2
)时,说明NO正逆反应速率相等,反应达到平衡状态,故C正确;
D.恒容容器,反应物生成物都是气体质量不变,所以密度不变不一定平衡,故D错误;
故选BC,
故答案为:BC.
22.【解答】Ⅱ.(1)根据图象分析,物质的量增大的是生成物,减小的是反应物,所以反应物
是X、Y,生成物是Z;X、Y、Z物质的量的变化量分别为:0.3 mol、0.1mol、0.2mol,根据参
加反应的物质的量之比等于其计量数之比得计量数,所以X、Y、Z的计量数之比为3:1:
2.故答案为:3X+Y 2Z;
(2)反应开始至2mi⇌n,Z物质的量的变化量为0.2mol,
由 3X+Y 2Z
开始1.0 ⇌ 1.0 0
转化0.3 0.1 0.2
平衡0.7 0.9 0.2
所以用X表示的平均反应速率为v(X)= = =0.075mol/mol•L﹣1•mi﹣1;
平衡时,Y的转化率为 ×100%=10%;
平衡时,Z的浓度为 =0.1mol/L;
故答案为:0.075;10%;0.1;
(3)A.X、Y、Z的物质的量之比与反应起始时的物质的量和平衡时转化的程度有关,不能说明上述反应达到平衡状态,故A错误;
B.反应前后气体的计量数之和不相等,混合气体的压强不随时间的变化而变化,说明上
述反应达到平衡状态,故B正确;
C.无论反应是否平衡,单位时间内每消耗3molX,同时生成2molZ,故C错误;
D.反应遵循质量守恒定律,无论是否平衡,混合气体的总质量不随时间的变化而变化,不
能说明上述反应达到平衡状态,故D错误;
E.化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,混合气体的总物质
的量不随时间的变化而变化,可以说明上述反应达到平衡状态,故E正确.
故答案为:B、E.
23.【解答】解:(1) 原电池中,二氧化硫被O 氧化生成硫酸,总反应为2SO +O +2H O=
2 2 2 2
2H
2
SO
4
,通入二氧①化硫的a电极是负极、发生失去电子的氧化反应,通入氧气的b电极是
正极,正极电极反应式为O +4e﹣+4H+=2H O,
2 2
故答案为:2SO
2
+O
2
+2H
2
O=2H
2
SO
4
; 正;O
2
+4e﹣+4H+=2H
2
O;氧化反应;
电池工作时,电解质溶液中阳离子移向正极b,阴离子移向负极a,所以生产过程中
②H+向b电极区域运动,故答案为:b;
(2)由CH 和O 组合形成的碱性燃料电池中,CH 发生失去电子的氧化反应,为负极,电
4 2 4
极反应式为CH +10OH﹣﹣8e﹣=CO 2﹣+7H O,正极为O 所在电极,电极反应式为O +4e
4 3 2 2 2
﹣+2H O=4OH﹣,所以燃料电池总反应式为CH +2O +2OH﹣=CO 2﹣+3H O,由于原电池
2 4 2 3 2
消耗OH﹣,溶液碱性减弱,pH降低,
故答案为:CH +10OH﹣﹣8e﹣=CO 2﹣+7H O; CH +2O +2OH﹣=CO 2﹣+3H O;下降。
4 3 2 4 2 3 2
24.【解答】解:(1)A.氢气分子内每个氢原子都达到2电子稳定结构,故A正确;
B.2H→H 放出437.6 kJ的热量,则氢气分子的能量比两个氢原子的能量低,故B正确;
2
C.1 mol H 离解成 2 mol H 要吸收437.6 kJ热量,故C错误;
2
D.氢原子比氢气分子活泼,故D错误;
故答案为:AB;
(2) 分解海水时,实现了光能转化为化学能;生成的氢气用于制作燃料电池时,实现了
化学①能转化为电能;分解海水的反应属于吸热反应,
故答案为:化学;电;吸热;
某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为:
②2H +2O2‾﹣4e‾=2H O,则B极的电极反应式为O +4e‾=2O2‾,
2 2 2
故答案为:O +4e‾=2O2‾;
2(3)电池的总反应为Zn+2MnO +2NH Cl═ZnCl +2NH ↑+Mn O +H O,该电池的负极反
2 4 2 3 2 3 2
应为Zn﹣2e‾=Zn2+,正极反应为2NH ++2MnO +2e‾=2NH ↑+Mn O +H O,
4 2 3 2 3 2
故答案为:Zn﹣2e‾=Zn2+;2NH ++2MnO +2e‾=2NH ↑+Mn O +H O。
4 2 3 2 3 2