文档内容
3.4.2沉淀溶解平衡的应用(分层作业)
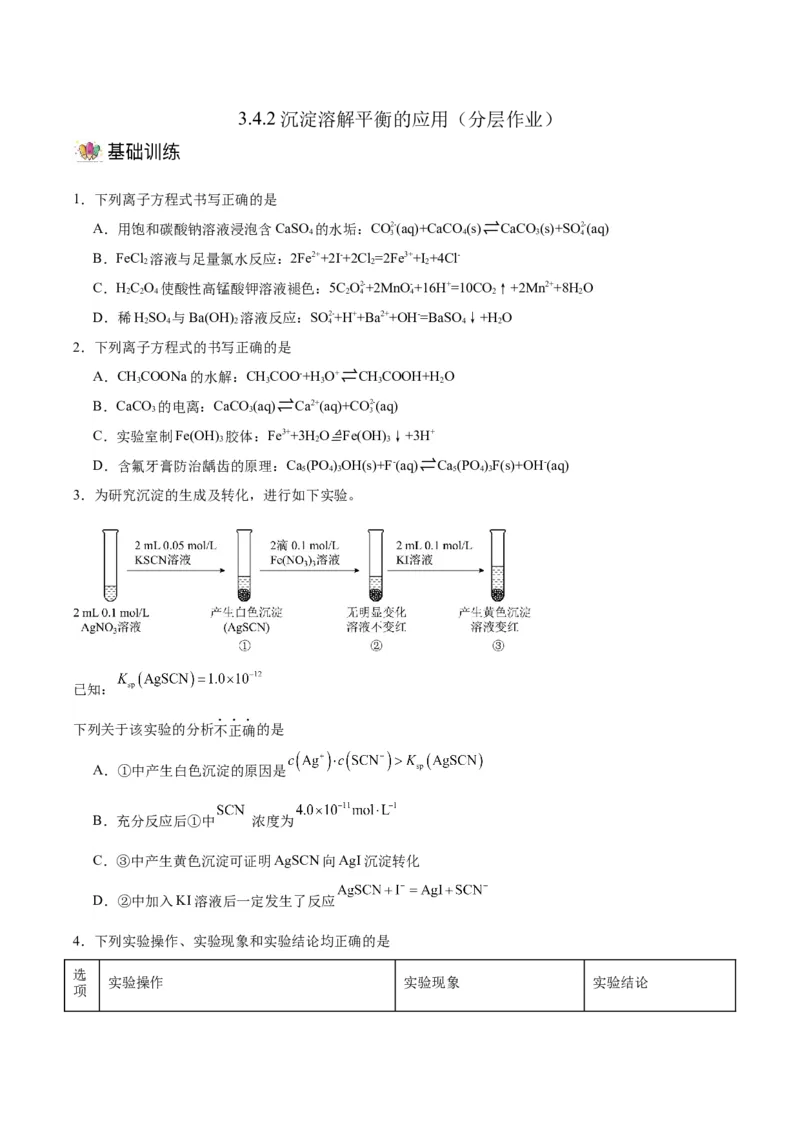
1.下列离子方程式书写正确的是
A.用饱和碳酸钠溶液浸泡含CaSO 的水垢:CO2- (aq)+CaCO (s)⇌CaCO (s)+SO2- (aq)
4 3 4 3 4
B.FeCl 溶液与足量氯水反应:2Fe2++2I-+2Cl=2Fe3++I +4Cl-
2 2 2
C.HC O 使酸性高锰酸钾溶液褪色:5C O2- +2MnO- +16H+=10CO ↑+2Mn2++8H O
2 2 4 2 4 4 2 2
D.稀HSO 与Ba(OH) 溶液反应:SO2- +H++Ba2++OH-=BaSO ↓+H O
2 4 2 4 4 2
2.下列离子方程式的书写正确的是
A.CHCOONa的水解:CHCOO-+H O+⇌CHCOOH+H O
3 3 3 3 2
B.CaCO 的电离:CaCO (aq)⇌Ca2+(aq)+CO2- (aq)
3 3 3
C.实验室制Fe(OH)
3
胶体:Fe3++3H
2
O≜Fe(OH)
3
↓+3H+
D.含氟牙膏防治龋齿的原理:Ca (PO )OH(s)+F-(aq)⇌Ca (PO )F(s)+OH-(aq)
5 4 3 5 4 3
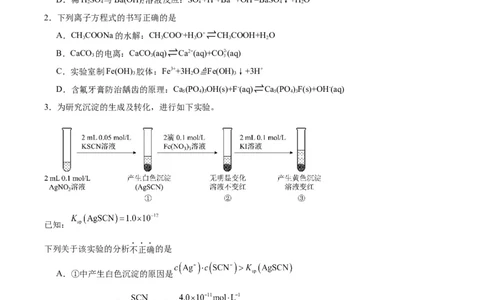
3.为研究沉淀的生成及转化,进行如下实验。
已知:
下列关于该实验的分析不正确的是
A.①中产生白色沉淀的原因是
B.充分反应后①中 浓度为
C.③中产生黄色沉淀可证明AgSCN向AgI沉淀转化
D.②中加入KI溶液后一定发生了反应
4.下列实验操作、实验现象和实验结论均正确的是
选
实验操作 实验现象 实验结论
项常温下,用pH计分测0.1mol/LNaA溶液和
A pH(NaA)H CO
0.1mol/LNaCO 溶液的pH 2 3 2 3
2 3
向盛有KI 溶液的两试管中分别加入淀粉溶液 前者溶液变蓝,后者有黄色 KI 溶液中还含有 和
B 3 3
和AgNO 溶液 沉淀产生 I-
3
HS-水解程度小于电离
C 向NaHS溶液中滴入酚酞 溶液变红
程度
向2mL1mol/LNaOH溶液中加入几滴1mol/L
先有白色沉淀生成;后有红
D MgCl 溶液,生成白色沉淀,再加入几滴
2 褐色沉淀生成
1mol/L FeCl 溶液
3
A.A B.B C.C D.D
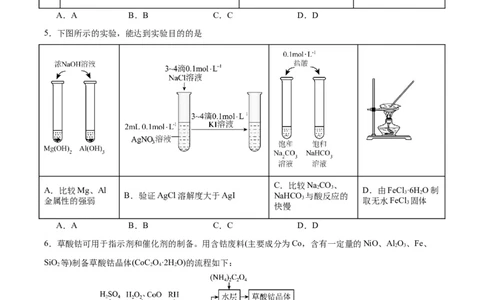
5.下图所示的实验,能达到实验目的的是
C.比较NaCO、
A.比较Mg、Al 2 3 D.由FeCl ·6H O制
B.验证AgCl溶解度大于AgI NaHCO 与酸反应的 3 2
金属性的强弱 3 取无水FeCl 固体
快慢 3
A.A B.B C.C D.D
6.草酸钴可用于指示剂和催化剂的制备。用含钴废料(主要成分为Co,含有一定量的NiO、Al O、Fe、
2 3
SiO 等)制备草酸钴晶体(CoC O·2H O)的流程如下:
2 2 4 2
已知:①草酸钴晶体难溶于水。
②RH为有机物(难电离)、Mn+代表金属离子,Mn++nRH⇌MR +nH+。
n
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH) Fe(OH) Co(OH) Al(OH) Ni(OH)
3 2 2 3 2开始沉淀 2.7 7.6 7.6 4.0 7.5
完全沉淀 3.7 9.6 9.2 5.2 8.0
④滤液中Co元素以Co2+形式存在。
回答下列问题:
(1)为提高浸出速率,除将含钴废料粉碎外,还可采取的措施有 (写出两条)。
(2)“浸出液”中加入HO 后发生反应的离子方程式为 。
2 2
(3)加入氧化钴调节溶液的pH,调节的pH范围是 。
(4)操作①在实验室所用的主要仪器为 。
(5)可否考虑先将Co2+转化为CoCO,再利用应CoCO(aq)+C O2- (aq)⇌CoC O(s)+CO2- (aq),将CoCO 化为
3 3 2 4 2 4 3 3
CoC O (填“能”或“不能”),说明理由: 。[K (CoCO)=1.5×10-
2 4 sp 3
13,K (CoC O)=6.0×10-8]
sp 2 4
7.25℃时,CuS和ZnS悬浊液中对应离子浓度的对数值1g(S2-)与1gc(M2+)的关系如图所示。下列说法不正
确的是
A.25℃时,ZnS的溶解度更大
B.25℃时,K (CuS)约为1×10-35
sp
C.在ZnS悬浊液中加入Cu2+,可以发生反应ZnS(S)+Cu2+(aq)⇌CuS(S)+Zn2+(aq)
D.已知温度升高,CuS的溶解度增大,则图中对应线段向下平移
8.利用平衡移动原理,分析一定温度下Mg2+在不同pH的NaCO 体系中的可能产物。
2 3
已知:
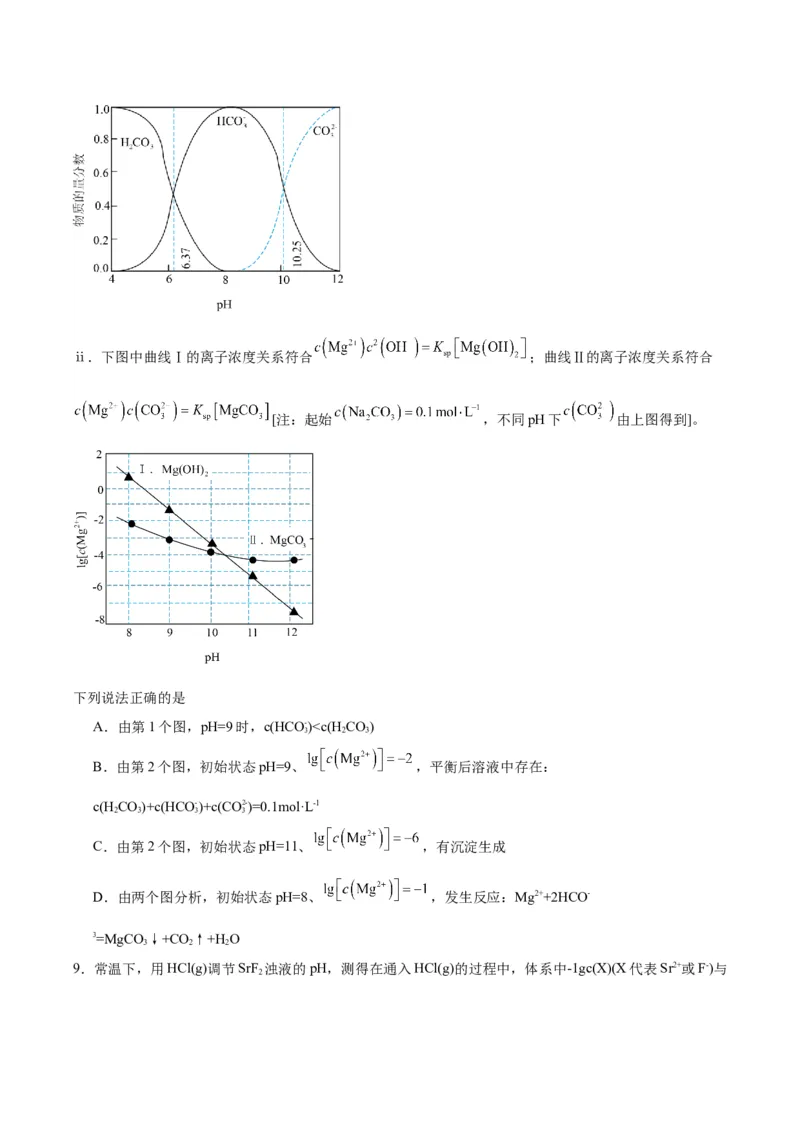
ⅰ.下图中曲线表示NaCO 体系中各含碳粒子的物质的量分数与pH的关系。
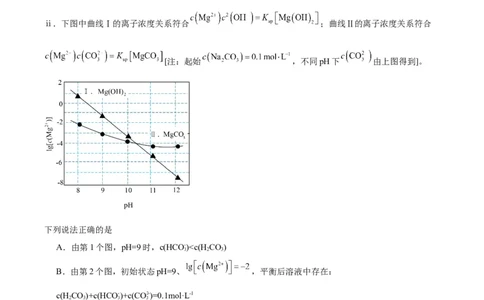
2 3ⅱ.下图中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同pH下 由上图得到]。
下列说法正确的是
A.由第1个图,pH=9时,c(HCO- )c( )
3
C.T℃时,向10mL水中加入CaCO 和PbCO 至二者均饱和,溶液中 =3×10-5
3 3
D.T℃时,向CaCO 沉淀中加入1mol•L-1的NaSO 溶液,CaCO 沉淀会转化为CaSO 沉淀
3 2 4 3 4
15.电镀污泥[主要含 、 、 、 等]中铬镍资源再利用生产红矾钠(
)和粗镍,该工业流程如图。
已知:
① 、 、 、 的 依次为 、 、 、 ;
②Cr及其化合物的性质与Al类似;
③溶液中金属离子开始沉淀、沉淀完全和沉淀开始溶解的pH如下表所示:
金属离子开始沉淀时( )的pH 7.2 4.9 3.7 2.2
沉淀完全时( )的pH 8.7 6.8 4.7 3.2
沉淀开始溶解的pH ― 12.0 7.8
请回答下列问题:
(1)若污泥中Cr以 的形式存在,则“①浸出”时发生反应的化学方程式为 。
(2)“②除杂”时,若镍离子浓度为0.05mol/L,则溶液中 浓度范围为 mol/L。
(3)“转溶”时,氢氧化钠加入量不宜过多,其原因为 (用离子方程式表示)。
(4)“④氧化”步骤中包括先将 、 沉淀,过滤后溶液中继续加入NaOH溶液和 。沉淀 、
时,pH应控制的范围为 ,加入 发生反应的离子方程式为 。
(5)操作Ⅲ为 。