文档内容
3.4.2沉淀溶解平衡的应用(分层作业)
1.下列离子方程式书写正确的是
A.用饱和碳酸钠溶液浸泡含CaSO 的水垢:CO2- (aq)+CaCO (s)⇌CaCO (s)+SO2- (aq)
4 3 4 3 4
B.FeCl 溶液与足量氯水反应:2Fe2++2I-+2Cl=2Fe3++I +4Cl-
2 2 2
C.HC O 使酸性高锰酸钾溶液褪色:5C O2- +2MnO- +16H+=10CO ↑+2Mn2++8H O
2 2 4 2 4 4 2 2
D.稀HSO 与Ba(OH) 溶液反应:SO2- +H++Ba2++OH-=BaSO ↓+H O
2 4 2 4 4 2
【答案】A
【解析】A.用饱和碳酸钠溶液浸泡含CaSO 的水垢发生沉淀转化CO2- (aq)+CaCO (s)⇌CaCO (s)+SO
4 3 4 3
2- (aq),故A正确;
4
B.FeCl 溶液与足量氯水反应生成氯化铁和碘单质,反应的离子方程式为2Fe2++4I-+3Cl=2Fe3++2I +6Cl-,
2 2 2
故B错误;
C.HC O 使酸性高锰酸钾溶液褪色,反应的离子方程式为5HC O+2MnO- +6H+=10CO ↑+2Mn2++8H O,
2 2 4 2 2 4 4 2 2
故C错误;
D.稀HSO 与Ba(OH) 溶液反应生成硫酸钡沉淀、水,反应的离子方程式为SO2- +2H++Ba2++2OH-
2 4 2 4
=BaSO ↓+2H O,故D错误;
4 2
选A。
2.下列离子方程式的书写正确的是
A.CHCOONa的水解:CHCOO-+H O+⇌CHCOOH+H O
3 3 3 3 2
B.CaCO 的电离:CaCO (aq)⇌Ca2+(aq)+CO2- (aq)
3 3 3
C.实验室制Fe(OH)
3
胶体:Fe3++3H
2
O≜Fe(OH)
3
↓+3H+
D.含氟牙膏防治龋齿的原理:Ca (PO )OH(s)+F-(aq)⇌Ca (PO )F(s)+OH-(aq)
5 4 3 5 4 3
【答案】D
【解析】A.题干所示为醋酸钠遇酸的反应,水解反应为CHCOO-+H O⇌CHCOOH+OH-,选项A错误;
3 2 3
B.题干所示为是CaCO 的沉淀溶解平衡,电离方程式为CaCO =Ca2++CO2- ,选项B错误;
3 3 3
C.题干所示为不是沉淀而是胶体,应该为Fe3++3H
2
O≜Fe(OH)
3
↓(胶体)+3H+,选项C错误;
D.含氟牙膏防治龋齿的原理是产生保护层,反应为:Ca (PO )OH(s)+F-(aq)⇌Ca (PO )F(s)+OH-(aq),选
5 4 3 5 4 3
项D正确;
答案选D。
3.为研究沉淀的生成及转化,进行如下实验。已知:
下列关于该实验的分析不正确的是
A.①中产生白色沉淀的原因是
B.充分反应后①中 浓度为
C.③中产生黄色沉淀可证明AgSCN向AgI沉淀转化
D.②中加入KI溶液后一定发生了反应
【答案】D
【解析】A.向硝酸银溶液中滴加硫氰化钾,银离子浓度与硫氰根离子浓度幂之积大于硫氰化银的溶度积,
生成白色沉淀,A正确;
2×10−3L×0.1mol/L−2×10−3L×0.05mol/L
B.生成沉淀后溶液中剩余的银离子的浓度为:c(Ag+)=
2×10−3L+2×10−3L
1.0×10−12
=0.025mol/L,则溶液中SCN-浓度为 =4.0×10−11mol·L-1,B正确;
0.025mol/L
C.向AgSCN悬浊液中滴加硝酸铁,溶液未变红,加入KI以后,碘离子与AgSCN中的银离子发生反应生
成更难溶的AgI,实现了AgSCN向AgI的转化,C正确;
D.硝酸根离子在酸辛条件下具有强氧化性,而KI具有强还原性,所以加入KI以后,也可能是硝酸根离
子将碘离子氧化为碘单质,也会出现上述现象,D错误;
故选D。
4.下列实验操作、实验现象和实验结论均正确的是
选
实验操作 实验现象 实验结论
项
常温下,用pH计分测0.1mol/LNaA溶液和
A pH(NaA)H CO
0.1mol/LNaCO 溶液的pH 2 3 2 3
2 3向盛有KI 溶液的两试管中分别加入淀粉溶液 前者溶液变蓝,后者有黄色 KI 溶液中还含有 和
B 3 3
和AgNO 溶液 沉淀产生 I-
3
HS-水解程度小于电离
C 向NaHS溶液中滴入酚酞 溶液变红
程度
向2mL1mol/LNaOH溶液中加入几滴1mol/L
先有白色沉淀生成;后有红
D MgCl 溶液,生成白色沉淀,再加入几滴
2 褐色沉淀生成
1mol/L FeCl 溶液
3
A.A B.B C.C D.D
【答案】B
【解析】A.NaCO 溶液的pH大,可知阴离子的水解程度大,则对应HCO- 的酸性弱,即酸性为HA>
2 3 3
HCO- ,故A错误;
3
B.由操作和现象可知溶液中含碘单质、碘离子,则操作、现象、结论均合理,故B正确;
C.NaHS溶液中HS-的水解程度大于电离程度,溶液显碱性,溶液变红,故C错误;
D.NaOH过量,均有沉淀的生成,不能比较K (Fe(OH) )、K (Mg(OH) )的大小,故D错误;
sp 3 sp 2
故选:B。
5.下图所示的实验,能达到实验目的的是
C.比较NaCO、
A.比较Mg、Al 2 3 D.由FeCl ·6H O制
B.验证AgCl溶解度大于AgI NaHCO 与酸反应的 3 2
金属性的强弱 3 取无水FeCl 固体
快慢 3
A.A B.B C.C D.D
【答案】A
【解析】A.氢氧化镁不与氢氧化钠反应故不溶解,氢氧化铝与氢氧化钠反应而溶解,则氢氧化铝具有弱
酸性,氢氧化镁碱性大于氢氧化铝,最高价氧化物对应水化物的碱性越强,则金属性越强,故说明金属性
Mg>Al ,A正确;
B.硝酸银与氯化钠反应时硝酸银过量,则滴入的KI会与过量的硝酸银反应出现碘化银沉淀,难以证明是氯化银转化为碘化银,故难以验证AgCl溶解度大于AgI,B错误;
C.应选择等体积、等物质的量浓度的碳酸钠和碳酸氢钠与盐酸反应,而碳酸钠和碳酸氢钠的溶解度不同、
饱和碳酸钠和饱和碳酸氢钠溶液的物质的量浓度不同, C错误;
D.氯化铁易水解,加盐酸可抑制氯化铁水解,要由FeCl ·6H O制取无水FeCl 固体,应在坩埚中、HCl的
3 2 3
氛围中加热FeCl ·6H O脱水得到无水FeCl 固体,D错误;
3 2 3
故选A。
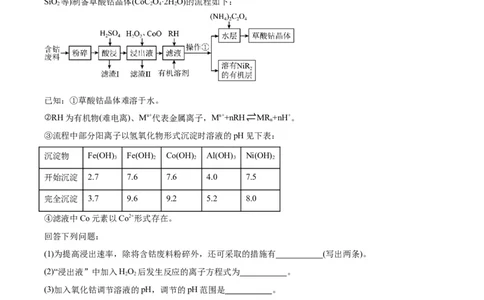
6.草酸钴可用于指示剂和催化剂的制备。用含钴废料(主要成分为Co,含有一定量的NiO、Al O、Fe、
2 3
SiO 等)制备草酸钴晶体(CoC O·2H O)的流程如下:
2 2 4 2
已知:①草酸钴晶体难溶于水。
②RH为有机物(难电离)、Mn+代表金属离子,Mn++nRH⇌MR +nH+。
n
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH) Fe(OH) Co(OH) Al(OH) Ni(OH)
3 2 2 3 2
开始沉淀 2.7 7.6 7.6 4.0 7.5
完全沉淀 3.7 9.6 9.2 5.2 8.0
④滤液中Co元素以Co2+形式存在。
回答下列问题:
(1)为提高浸出速率,除将含钴废料粉碎外,还可采取的措施有 (写出两条)。
(2)“浸出液”中加入HO 后发生反应的离子方程式为 。
2 2
(3)加入氧化钴调节溶液的pH,调节的pH范围是 。
(4)操作①在实验室所用的主要仪器为 。
(5)可否考虑先将Co2+转化为CoCO,再利用应CoCO(aq)+C O2- (aq)⇌CoC O(s)+CO2- (aq),将CoCO 化为
3 3 2 4 2 4 3 3
CoC O (填“能”或“不能”),说明理由: 。[K (CoCO)=1.5×10-
2 4 sp 3
13,K (CoC O)=6.0×10-8]
sp 2 4
【答案】(1)适当提高酸浸温度、适当增加硫酸浓度、搅拌等
(2)2Fe2++H O+2H+=2Fe3++2H O
2 2 2
(3)5.2≤pH<7.5(4)分液漏斗
(5) 不能 该反应的平衡常数K=2.5×10-6,转化程度小,不能实现转化
【解析】(1)根据影响化学反应速率的因素及影响结果可知,为提高浸出速率,除将含钴废料粉碎外,
还可以适当提高酸浸温度、适当增加硫酸浓度、搅拌等,故答案为:适当提高酸浸温度、适当增加硫酸浓
度、搅拌等。
(2)由分析可知,“浸出液”中加入HO 主要是亚铁离子被HO 氧化变为铁离子,便于后续调节pH值
2 2 2 2
将其转化为Fe(OH) 沉淀,反应的离子方程式为2Fe2++H O+2H+=2Fe3++2H O,故答案为:2Fe2+
3 2 2 2
+H O+2H+=2Fe3++2H O。
2 2 2
(3)由分析可知,加入氧化钴,发生CoO+2H+=Co2++H O,根据阳离子以氢氧化物形式沉淀时溶液的pH
2
可知,调节溶液的pH为5.2≤pH<7.5,使Fe3+和Al3+完全转化为沉淀Fe(OH) 、Al(OH) ,同时不能影响到镍
3 3
和钴,故答案为:5.2≤pH<7.5。
(4)由分析可知,操作①为萃取分液,所用的主要仪器为分液漏斗,故答案为:分液漏斗。
(5)根据题干数据可知,CoCO(aq)+C O2- (aq)=CoC O(s)+CO2- (aq)该反应的平衡常数
3 2 4 2 4 3
c(CO2− ) c(CO2− ) c(Ca2+ ) K (CaCO )
K= 3 = 3 × = sp 3 =2.5×10-6,转化程度小,不能实现该转化,
c(C O2− ) (C O2− ) c(Ca2+ ) K (CaC O )
2 4 2 4 sp 2 4
故答案为:不能;该反应的平衡常数K=2.5×10-6,转化程度小,不能实现转化。
7.25℃时,CuS和ZnS悬浊液中对应离子浓度的对数值1g(S2-)与1gc(M2+)的关系如图所示。下列说法不正
确的是
A.25℃时,ZnS的溶解度更大
B.25℃时,K (CuS)约为1×10-35
sp
C.在ZnS悬浊液中加入Cu2+,可以发生反应ZnS(S)+Cu2+(aq)⇌CuS(S)+Zn2+(aq)
D.已知温度升高,CuS的溶解度增大,则图中对应线段向下平移【答案】D
【解析】A.CuS和ZnS化学组成相同,相同条件下K (ZnS)>K (CuS)可以体现ZnS的溶解度更大,A项
sp sp
正确;
B.CuS对应离子浓度的对数值的关系曲线上的任意一点可以求K (CuS)=c(Cu2+)·c(S2-),
sp
K (CuS)=c(Cu2+)·c(S2-)=10-10×10-25=10-35,B项正确;
sp
C.K (ZnS)>K (CuS),反映ZnS比CuS溶解能力大,CuS更难溶于水,可以发生溶解度小的沉淀转化为
sp sp
溶解度更小的沉淀,ZnS(S)+Cu2+(aq)⇌CuS(S)+Zn2+(aq)能发生,C项正确;
D.温度升高,CuS的溶解度增大,K (CuS)增大,则图中对应线段向上平移,D项错误;
sp
答案选D。
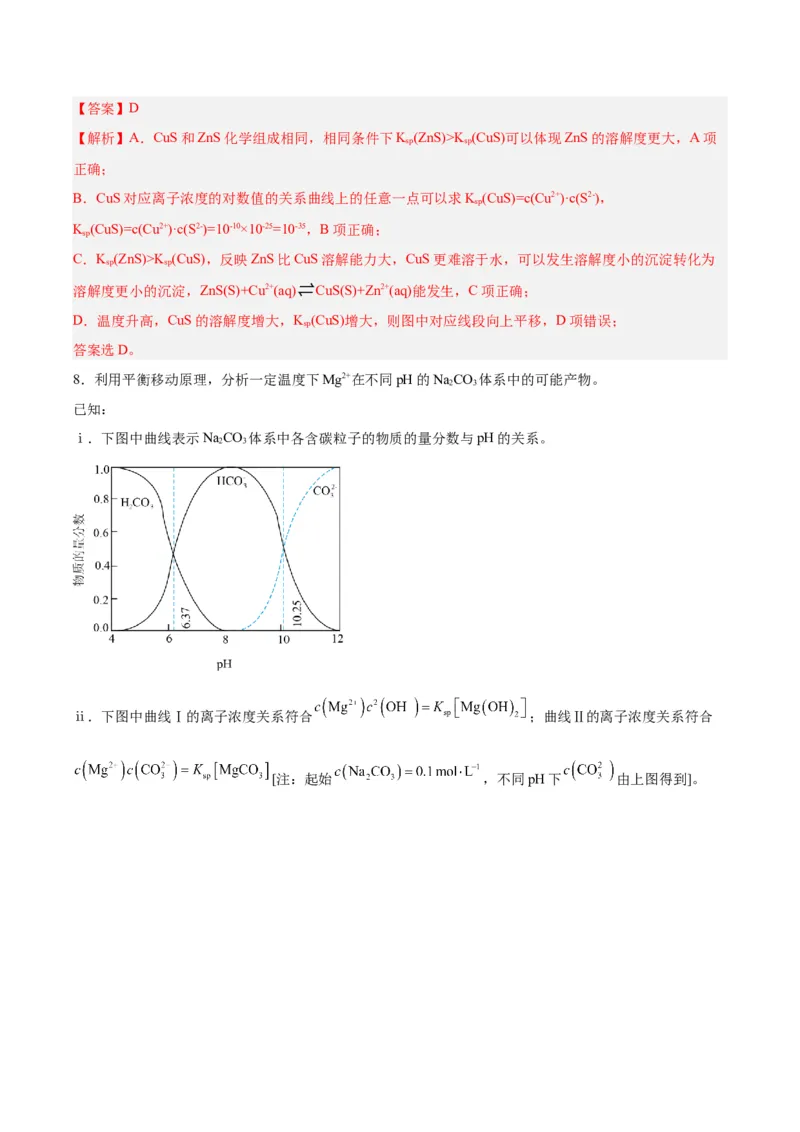
8.利用平衡移动原理,分析一定温度下Mg2+在不同pH的NaCO 体系中的可能产物。
2 3
已知:
ⅰ.下图中曲线表示NaCO 体系中各含碳粒子的物质的量分数与pH的关系。
2 3
ⅱ.下图中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同pH下 由上图得到]。下列说法正确的是
A.由第1个图,pH=9时,c(HCO- )c( )
3
C.T℃时,向10mL水中加入CaCO 和PbCO 至二者均饱和,溶液中 =3×10-5
3 3
D.T℃时,向CaCO 沉淀中加入1mol•L-1的NaSO 溶液,CaCO 沉淀会转化为CaSO 沉淀
3 2 4 3 4
【答案】CD
【解析】A.由Ksp(CaSO )=4.90×10-5得c(Ca2+)c(SO2- )=4.90×10-5,两边取负对数得:-lgc(Ca2+)-lgc(SO2- )=5-
4 4 41g4.9,曲线在pN轴和pM轴上截距相等为5-lg4.9,与图中最接近的曲线为a,A正确;
B.由A知曲线b为Ksp (CaCO )=2.8×10-9曲线,d点表示CaCO 的饱和溶液,且c(Ca2+)>c(CO2- ),B正确;
3 3 3
C.在二者饱和溶液中,Ksp(CaCO )与Ksp(PbCO )在计算中使用相同的c(CO2- ),所以
3 3 3
K (CaCO ) c(Ca2+ )c(CO2− ) c(Ca2+ ) 2.8×10−9
sp 3 = 3 = = =0.3×105,C错误;
K (PbCO ) c(Pb2+ )c(CO2− ) c(Pb2+ ) 8.4×10−4
sp 3 3
D.向CaCO 沉淀中加入1mol/L的NaSO 溶液时,因为Ksp (CaCO ) < Ksp(CaSO ),CaCO 沉淀不会转化
3 2 4 3 4 3
为CaSO 沉淀,D错误;
4
答案选CD。
15.电镀污泥[主要含 、 、 、 等]中铬镍资源再利用生产红矾钠(
)和粗镍,该工业流程如图。
已知:
① 、 、 、 的 依次为 、 、 、 ;
②Cr及其化合物的性质与Al类似;
③溶液中金属离子开始沉淀、沉淀完全和沉淀开始溶解的pH如下表所示:
金属离子
开始沉淀时( )的pH 7.2 4.9 3.7 2.2
沉淀完全时( )的pH 8.7 6.8 4.7 3.2
沉淀开始溶解的pH ― 12.0 7.8
请回答下列问题:
(1)若污泥中Cr以 的形式存在,则“①浸出”时发生反应的化学方程式为 。(2)“②除杂”时,若镍离子浓度为0.05mol/L,则溶液中 浓度范围为 mol/L。
(3)“转溶”时,氢氧化钠加入量不宜过多,其原因为 (用离子方程式表示)。
(4)“④氧化”步骤中包括先将 、 沉淀,过滤后溶液中继续加入NaOH溶液和 。沉淀 、
时,pH应控制的范围为 ,加入 发生反应的离子方程式为 。
(5)操作Ⅲ为 。
(6)若实验取干污泥250g,其中含Cr11.2%,实验所得晶体为59.6g,则Cr元素回收率为 (结果
保留一位小数)。
【答案】(1)CrO+3HSO=Cr(SO)+3HO
2 3 2 4 2 44 2
(2)5.8×10-14~2.0×10-13.5
(3)Al(OH)+OH-=AlO- +2HO 、Cr(OH)+OH-=CrO- +2HO
3 2 2 3 2 2
(4) 4.7~4.9 2Cr3++3HO+10OH-=2CrO2- +8HO
2 2 4 2
(5)过滤、洗涤、干燥、灼烧
(6)74.3%
【解析】(1)污泥中Cr以CrO 的形式存在,则“①浸出”时发生反应为CrO 和稀硫酸生成水、
2 3 2 3
Cr(SO),化学方程式为CrO+3HSO=Cr(SO)+3HO;
2 44 2 3 2 4 2 44 2
(2)“②除杂”时,加磷酸钠将Cr3+、Fe3+、Al3+转化为沉淀分离,而镍离子没有沉淀进入滤液Ⅱ,结合
K (AlPO ) 5.8×10−19
sp 4
K 可知,Al3+沉淀完全所需PO3- 浓度较大,为c(PO3- )= = mol/L=5.8×10-14mol/L
sp 4 4 c(Al3+
)
1.0×10−5
√K (Ni (PO ) ) √5.0×10−31
,若镍离子浓度为0.05mol/L,则需要c(PO3- )=❑ sp 3 4 2 =❑ mol/L=2.0×10-13.5mol/L,
4 C3 (Ni2+
)
0.053
故溶液中PO3- 浓度范围为5.8×10-14~2.0×10-13.5mol/L;
4
(3)已知,Cr及其化合物的性质与Al类似;则“转溶”时,氢氧化钠加入量不宜过多,否则Al(OH) 会
3
和过量氢氧根离子转化为AlO- 、Cr(OH) 会和过量氢氧根离子转化为CrO- ,反应分别为:Al(OH)+OH-=AlO-
2 3 2 3
2+2HO 、Cr(OH)+OH-=CrO- +2HO;
2 3 2 2
(4)“④氧化”步骤中包括先将Fe3+、Al3+沉淀,而Cr3+不转化为沉淀,过滤后溶液中继续加入NaOH溶
液和HO 氧化三价铬,结合图表可知,沉淀Fe3+、Al3+时,pH应控制的范围为4.7~4.9;加入HO 在碱性
2 2 2 2
条件下将三价铬转化为CrO2- ,过氧化氢被还原为水,离子方程式为2Cr3++3HO+10OH-=2CrO2- +8HO;
4 2 2 4 2(5)由分析可知,操作Ⅲ为过滤、洗涤、干燥、灼烧;