文档内容
第四章 物质结构 元素周期律
第三节 化学键
第二课时 共价键
【学习目标】1.以氯化氢的形成过程为例,从微观角度分析宏观物质的形成过程,认识共价键的形
成,建立共价键的概念,进一步建立化学键的概念,培养宏观辨识与微观探析的化学核心素养。
2.通过阅读思考,讨论交流,理解共价键的形成过程和形成条件,能用电子式对共价键进行表征,能
熟练地用电子式表示共价化合物的形成过程,知道共价键的分类方法、涵义及分子存在一定的空间结构。
【学习重点】共价键、共价化合物的概念及判断;用电子式表示共价化合物及共价化合物的形成过程
【学习难点】用电子式表示共价化合物的形成过程。
【课前预习】
旧知回顾:1.离子键是指 带相反电荷离子之间的相互作用 。其形成条件是 ① 活泼的金属 元素(如
周期表中第 IA 、 IIA 族)和 活泼的非金属 元素(如周期表中第 VIA 、 VIIA 族)之间的化合物.如:
NaCl 、 MgO 、 CaCl , ②活泼的金属 阳 离子或 铵根 离子和 酸根 离子。
2
2.在元素符号周围用“·”或“×”来表示 原子的最外层电子 的式子叫电子式。如氧化镁、氯化钾的电
子式
分别为 M g 2 + [∶O∶ ] 2- M g 2+ K + [∶Cl∶ ] - ,用电子式表示氯化镁的形成过程为:
。
新知预习:1.氯分子的形成过程,氯原子的最外层有7个电子,要达到8电子稳定结构,都需要获得
1 个电子 ,所以氯原子间难以发生电子的得失。如果2个氯原子各提供1个电子,形成 共用电子对 ,2个
氯原子就都形成了8电子稳定结构,从而形成氯分子。
2.由同种原子形成共价键,两个原子吸引电子的能力 相同 ,共用电子对 不偏向 任何一个原子,成
键的原子因此而 不显电性 ,这样的共价键叫做 非极性 共价键,简称非极性键。在化合物分子中,不同
种原子形成共价键时,因为原子吸引电子的能力 不同 ,共用电子对偏向 吸引电子能力强的一方,所以
吸引电子力强的一方显 负电性 ,吸引电子能力弱的原子一方显 正电性 。像这样共用电子对偏移的共
价键叫做 极性 共价键,简称极性键。
3.化学键的形成与 原子结构 有关,它主要通过原子的 价电子 间的转移或共用来实现。一般的化学
物质主要由 离子键 或 共价键 结合而成。分子具有一定的空间结构,如CO 是 直线 形,HO呈 V
2 2
形,CH 呈 正四面体 形等。
4
【课中探究】情景导入:在通常情况下,将水加热到100 ℃时,水便会沸腾,而要使水分解成氢气和氧气,却需要
将水加热至1 000 ℃这样的高温时,才会有部分水分解。这是为什么呢?通过上节可的学习,我们知道钠
在氯气中燃烧会生成氯化钠,它是由钠离子和氯离子间的静电作用形成的。H 和Cl 在点燃或光照的情况
2 2
下可生成HCl,它的形成过程和NaCl会是一样的吗?我们将通过本节课的学习来揭晓答案。
一、共价键
活动一、Cl 、HCl 的形成过程
2
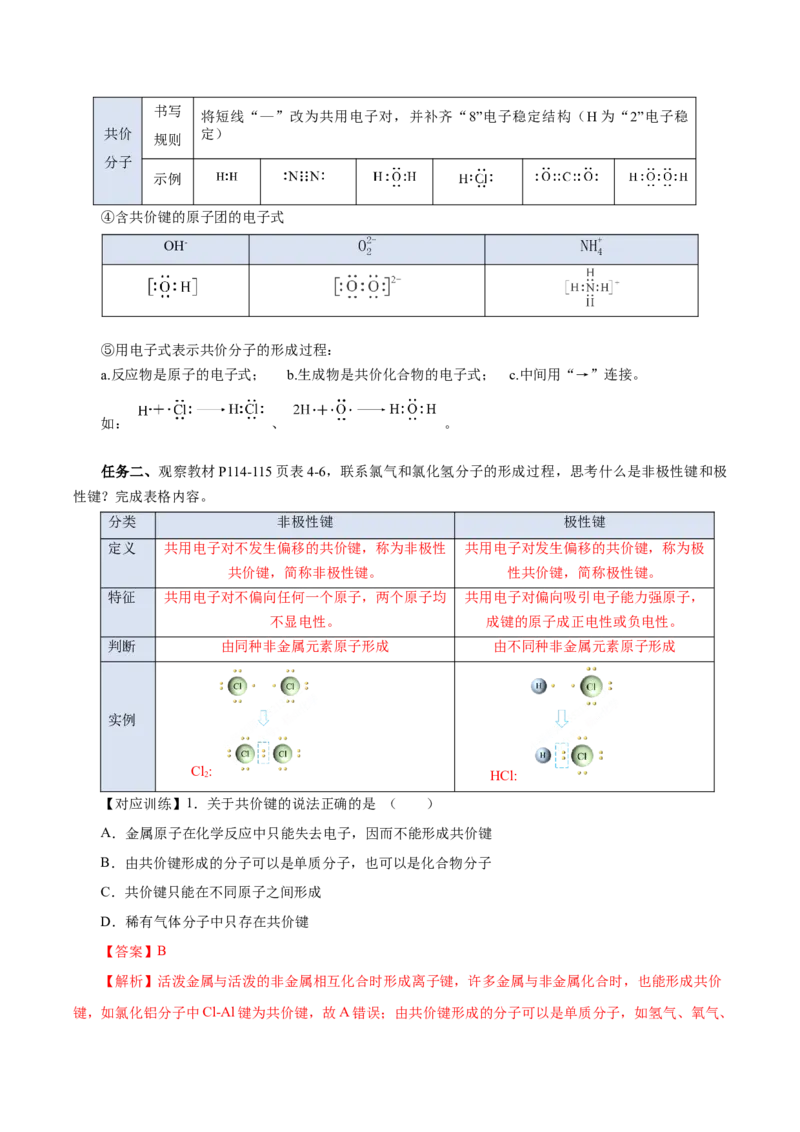
任务一、阅读教材P114页1、2自然段,思考从微观角度如何理解Cl 分子的形成过程?
2
【答案要点】①氯原子的最外层有7个电子,要达到稳定的8电子结构,需获得1个电子;
②2个氯原子各提供1个电子→2个氯原子间形成共用电子对→2个氯原子均达到8电子稳定结构→形
成稳定的氯气分子。
③用图示表示:
任务二、阅读教材P114页内容,思考从微观角度如何理解HCl分子的形成过程?
【答案要点】①H原子需获得1个电子达到稳定结构,Cl原子需获得1个电子达到稳定结构。
②H原子和Cl原子各提供1个电子组成一对共用电子,使两原子最外电子层都达到稳定结构并产生强
烈的相互作用,从而形成了HCl分子。
③图示表示: 。
④形象表示:
⑤电子式表示HCl的形成过程: 。
【对应训练】如果用“·”表示最外层的电子,原子形成NaCl和HCI的的过程可表示如下:有关说法正确的是( )
A.H易失电子显+1价而形成稳定结构 B.NaCl固体中主要存在NaCl分子
C.HCl的水溶液中主要存在HCl分子 D.H与Cl共用一对电子形成HCl
【答案】D
【解析】A.HCl是共价化合物,H和Cl之间存在共用电子对,共用电子对偏向Cl,使得H显+1价,
Cl显-1价,A错误;B.NaCl是由Na+和Cl-形成的离子化合物,不存在“NaCl分子”的说法,B错误;
C.HCl是强电解质,在水中完全电离,故HCl的水溶液中不存在HCl分子,C错误;D.如图所示,H与
Cl共用一对电子形成HCl,D正确;故选D。
活动二、共价键的概念及成因
任务一、阅读教材P114页内容,思考共价键的定义和实质分别是什么?
【答案要点】①定义:原子间通过共用电子对所形成的相互作用叫做共价键。共价键的成键微粒主要
是非金属元素的原子(稀有气体除外)。
②成键实质:共用电子对对两个原子的电性作用。
任务二、讨论交流:共价键形成的原因是什么?从物质类别看共价键可能存在于哪些物质中?
【答案要点】①成键原因:通过共用电子对,各原子最外层电子数一般达到“2”或“8”的稳定状态,
两原子核都吸引共用电子对,使之处于平衡状态,体系总能量降低。
②存在:a.非金属单质分子(稀有气体除外),如H、O、Cl、C等;
2 2 2
b.非金属形成的化合物中,如HO、CO、HSO 、CH 等;
2 2 2 4 4
c.原子团(根)中,如OH-、 、 等。,侵权必究
SO2- NH+
4 4
【对应训练】1.关于NaCl和HCl,说法正确的是( )
A.NaCl和HCl分子中都含有Cl-
B.NaCl是离子化合物,HCl是共价化合物
C.两种化合物不同元素原子间都存在共用电子对
D.两种化合物类型不同,所以不能相互转化
【答案】B
【解析】NaCl是离子化合物,不能称为“分子”,NaCl晶体中含有Na+、Cl-,两种离子间的作用为
离子键,不存在共用电子对;HCl是共价化合物,分子中不存在Cl-;NaCl和HCl可以相互转化,NaCl与
浓硫酸共热可生成HCl,HCl与NaOH中和可生成NaCl。
2.下列化合物分子内只有共价键的是( )
A.BaCl B.NaOH C.(NH )SO D.HSO
2 4 2 4 2 4
【答案】D【解析】Ba是活泼金属,与活泼非金属反应生成的BaCl 是离子化合物,钡、氯间的化学键是离子
2
键。NaOH中,Na+与OH-间以离子键结合,OH-中O原子与H原子以共价键结合。(NH )SO 中,NH与
4 2 4
SO间以离子键结合,NH中N与H,SO中S与O以共价键结合。HSO 中,H和O之间与S和O之间都
2 4
以共价键结合。
3.下列说法正确的是( )
A.某物质的水溶液能导电,则该物质中一定含有离子键
B.MgCl 晶体中存在共价键和离子键
2
C.NH 和Cl 两种分子中,每个原子的最外层都具有8电子稳定结构
3 2
D.HS和CO 两种分子中均含有共价键
2 2
【答案】D
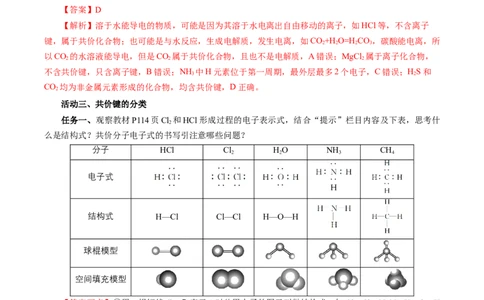
【解析】溶于水能导电的物质,可能是因为其溶于水电离出自由移动的离子,如HCl等,不含离子
键,属于共价化合物;也可能是与水反应,生成电解质,发生电离,如CO+H O=HCO,碳酸能电离,所
2 2 2 3
以CO 的水溶液能导电,但是CO 属于共价化合物,且也不是电解质,A错误;MgCl 属于离子化合物,
2 2 2
不含共价键,只含离子键,B错误;NH 中H元素位于第一周期,最外层最多2个电子,C错误;HS和
3 2
CO 均为非金属元素形成的化合物,均含共价键,D正确。
2
活动三、共价键的分类
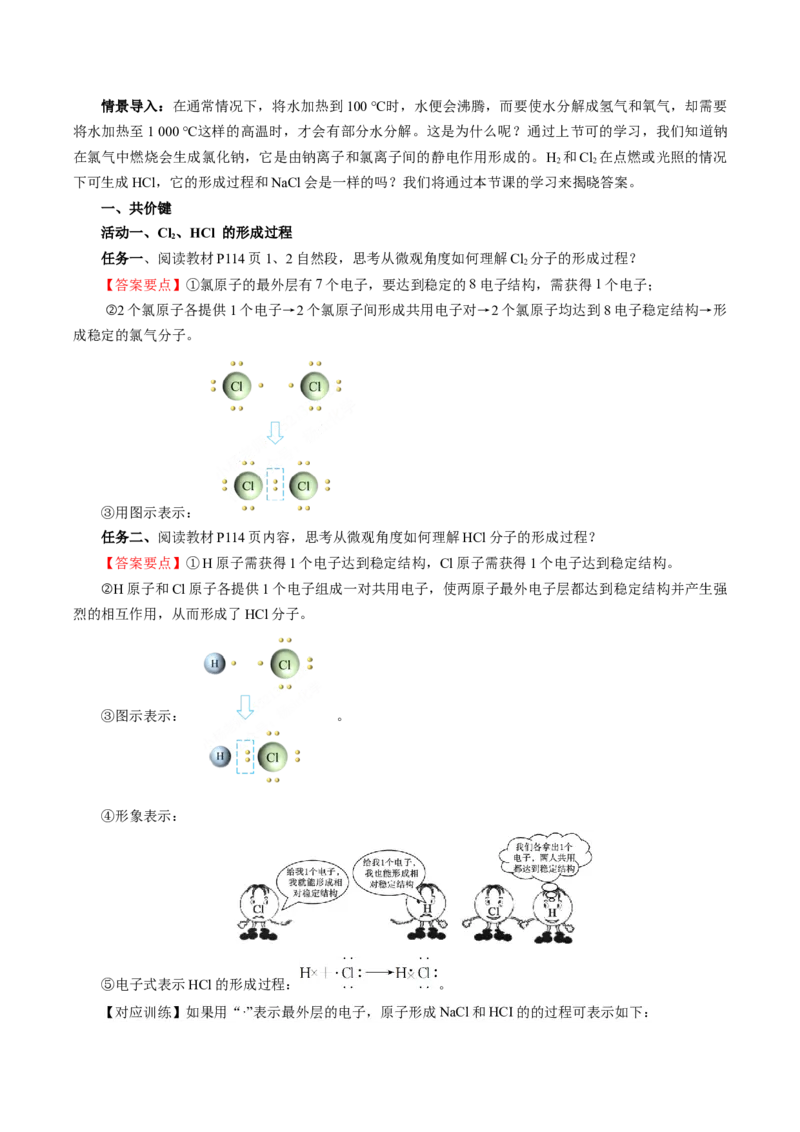
任务一、观察教材P114页Cl 和HCl形成过程的电子表示式,结合“提示”栏目内容及下表,思考什
2
么是结构式?共价分子电子式的书写引注意哪些问题?
分子 HCl Cl HO NH CH
2 2 3 4
电子式
结构式 H—Cl Cl—Cl H—O—H
球棍模型
空间填充模型
【答案要点】①用一根短线“—”表示1对共用电子的图示叫做结构式,如Cl—Cl、N≡N、H—O—H
、H—Cl、O=C=O、H—O—O—H等。
②根据原子最外层电子(单电子)数,确定共用电子对数。
原子 H C/Si N/P O/S F/Cl
最外层电子数 1 4 5 6 7
需共用电子对 1 4 3 2 1
③用“.”或“×”在两原子间表示共用电子对和原子的周围表示出未成对电子数。书写
将短线“—”改为共用电子对,并补齐“8”电子稳定结构(H为“2”电子稳
共价 定)
规则
分子
示例
④含共价键的原子团的电子式
OH- O2- NH+
2 4
⑤用电子式表示共价分子的形成过程:
a.反应物是原子的电子式; b.生成物是共价化合物的电子式; c.中间用“→”连接。
如: 、 。
任务二、观察教材P114-115页表4-6,联系氯气和氯化氢分子的形成过程,思考什么是非极性键和极
性键?完成表格内容。
分类 非极性键 极性键
定义 共用电子对不发生偏移的共价键,称为非极性 共用电子对发生偏移的共价键,称为极
共价键,简称非极性键。 性共价键,简称极性键。
特征 共用电子对不偏向任何一个原子,两个原子均 共用电子对偏向吸引电子能力强原子,
不显电性。 成键的原子成正电性或负电性。
判断 由同种非金属元素原子形成 由不同种非金属元素原子形成
实例
Cl:
2 HCl:
【对应训练】1.关于共价键的说法正确的是 ( )
A.金属原子在化学反应中只能失去电子,因而不能形成共价键
B.由共价键形成的分子可以是单质分子,也可以是化合物分子
C.共价键只能在不同原子之间形成
D.稀有气体分子中只存在共价键
【答案】B
【解析】活泼金属与活泼的非金属相互化合时形成离子键,许多金属与非金属化合时,也能形成共价
键,如氯化铝分子中Cl-Al键为共价键,故A错误;由共价键形成的分子可以是单质分子,如氢气、氧气、氮气等,也可以是化合物分子,如氯化氢、硫化氢、水等,故B正确;共价键能在同种原子之间形成,如
氢气、氧气、氮气等,故C错误;稀有气体原子就是分子,不存在化学键,故D错误;答案选B。
2.下列说法中正确的是 ( )
A.书写共价化合物的电子式只需把结构式中的一个单键改成一对电子即可
B.已知 ,可见,成键的一方不提供电子也可能形成化学键
C.将某种化合物溶于水,若能导电说明这种化合物是离子化合物
D.只要是离子化合物其熔点就比共价化合物的熔点高
【答案】B
【解析】Cl 的结构式是Cl—Cl,Cl 的电子式是ClCl,只把结构式中的一个单键改成一对电子则得
2 2
ClCl,并不是Cl 的电子式,此例可证明A错。B中H+没有电子,成键电子完全由水分子提供,B正确。
2
某些共价化合物如HCl,溶于水也能导电,C错。共价化合物中有一部分熔点比离子化合物要高,如二氧
化硅的熔点比氯化钠高。
二、共价化合物
活动一、共价化合物的概念及结构
任务一、阅读教材P114页最后两个自然段,回答什么是共价化合物?共价化合物的导电性有何特
点?
【答案要点】①定义:原子间以共用电子对形成的化合物称为共价化合物。如HO、CO、HSO 等。
2 2 2 4
②导电性:熔融状态时不导电(即熔融无法破坏共价键),溶于水后可能导电(如HCl、HSO 等
2 4
酸),可能不导电(如乙醇)。杨sir化学,侵权必究
任务二、讨论交流、观察分析教材P114页表4-6,思考共价化合物与物质类别有何关系?其组成与结
构有何特点?
【答案要点】①常见类型:非金属氢化物,如NH 、HCl、HS等;非金属氧化物,如CO、CO 、SO
3 2 2 2
等;酸,如HCl、HNO、HSO ;大多数有机化合物,如CH、CHCHOH等。
3 2 4 4 3 2
②特点:只能在水溶液中电离而导电(如液态氯化氢不导电);共价化合物只含共价键(若含有离子
键则为离子化合物);含共价键的化合物不一定是共价化合物(如NaO);由非金属元素形成的化合物不
2 2
一定是共价化合物(如铵盐)。
任务三、阅读教材P115页第二自然段,思考化学键的概念及类型分别是什么?
【答案要点】①概念:使离子相结合或原子相结合的作用力。
离子键 —得失电子、阴阳离子、静电作
用
②类型: 化学键
极性键 —不同原子、共用电子对偏移
共价键
非极性键—相同原子、共用电子对不偏移【对应训练】1.下列说法正确的是( )
A.共价化合物一定含有共价键,也可能含有离子键
B.由非金属元素组成的化合物一定是共价化合物
C.HO的性质很稳定,与水分子间存在氢键有关
2
D.离子化合物中可能含有共价键
【答案】D
【解析】A.共价化合物中仅含有共价键,不含离子键,A错误;B.由非金属元素组成的化合物不一
定是共价化合物,如氯化铵,是有非金属元素组成的离子化合物,B错误;C.氢键不影响化学性质,所
以水分子稳定与水分子间存在氢键无关,而与共价键键能有关,C错误;D.离子化合物中可能含有共价
键,如氢氧化钠是由离子键和共价键构成的离子化合物,D正确;故选D。
2.下列关于化学键的说法中正确的是( )
A.离子晶体中只有离子键
B.共价化合物分子中一定不含离子键
C.硫、氢、氧只能形成一种化合物
D.离子化合物中一定含有金属元素
【答案】B
【解析】有些离子晶体中只有离子键,例如氯化钠,有些离子晶体中既有离子键又有共价键,例如氯
化铵,A错误;共价化合物分子中只有共价键、一定不含离子键,B正确;硫、氢、氧能形成多种化合
物,例如HSO 、HSO 等,C错误;离子化合物中不一定含有金属元素,例如氯化铵,D错误。
2 4 2 3
活动二、分子间作用力和氢键
任务一、阅读教材P115页最后自然段,回答从化学键的角度看,化学反应的实质是什么?有化学键
的断裂或形成一定是化学反应吗?
【答案要点】①化学反应的本质是旧化学键的断裂和新化学键的形成过程。如下图:
②有化学键断裂或形成的变化不一定是化学变化。如 NaCl溶于水、结晶析出,均未发生化学变化。如下图:
任务二、阅读教材P116页“资料卡片”,思考分子间作用力和氢键的概念、特点及影响因素分别是
什么?
【答案要点】①把分子聚集在一起的作用力,叫分子间作用力,又称范德华力。分子间作用力比化学
键弱得多,主要影响物质的熔点、沸点等物理性质。一般来说,对于组成和结构相似的物质,相对分子质
量越大,范德华力越大,克服范德华力所需消耗的能量越大,物质的熔、沸点就越高。如:I > Br >
2 2
Cl > F。
2 2
②氢键是分子间存在的一种比范德华力强的分子间作用力。通常是N、O、F与H形成。氢键会使物
质的熔点和沸点升高。因为固体熔化或液体汽化时必须破坏分子间的氢键,消耗较多能量。
【对应训练】1.现有下列物质:①Cl ②Na O ③NaOH ④HCl ⑤H O ⑥MgF ⑦NH Cl
2 2 2 2 2 2 4
(1)只由离子键构成的物质是________(填序号,下同)
(2)只由极性键构成的物质是_________
(3)由极性键和非极性键构成的物质是__________
(4)由离子键和非极性键构成的物质是__________
(5)属于离子化合物的物质是__________
(6)属于共价化合物的物质的是__________
(7)下列变化(填字母)A碘的升华B烧碱熔化C氯化钠溶于水D氯化氢溶于水E氧气溶于水F氯
化铵受热分解,未发生化学键破坏的是___________;仅发生离子键破坏的是_________;仅发生共价键破
坏的是____________;既发生离子键又发货所能共价键破坏的是_________。
【答案】⑥ ④ ⑤ ② ②③⑥⑦ ④⑤ AE BC D F
【解析】考查化学键与物质类别,①只含非极性键,②含有离子键和非极性键,③含有离子键和极性
键,④只含非极性键,⑤含有极性键和非极性键,⑥只含离子键,⑦含有离子键和极性键,(1)只由离
子键构成的物质是⑥;(2)只由极性键构成的物质是④;(3)由离子键和非极性键构成的物质的⑤;
(4)由离子键和非极性键构成物质是②;(5)属于离子化合物是②③⑥⑦;(6)属于共价化合物的是
④⑤;(7)A、碘升华破坏的是分子间作用力;B、烧碱熔化破坏的是离子键;C、氯化钠溶于水破坏的
是离子键;D、氯化氢溶于水破坏的是极性键;E、氧气溶于水,未破坏化学键;F、NH Cl分解破坏的是
4离子键和共价键,未发生化学键破坏的是AE;只发生离子键破坏的是B和C;只发生共价键破坏的是D;
既发生离子键破坏又发生共价键破坏的是F。
2.下列说法正确的是( )
A.HF比HCl稳定,是由于HF分子间存在氢键
B.物质中化学键被破坏,一定发生化学变化
C.晶体MgCl 和NaO中的化学键类型相同
2 2
D.NaHSO 熔化时破坏离子键和共价键
4
【答案】C
【解析】A.HF比HCl稳定,是由于H-F键的键能大于H-Cl,与氢键无关,故A错误;B.化学反应
的本质是既有旧键的断裂又有新键的形成,故化学键被破坏不一定发生化学反应,故B错误;C.晶体
MgCl 和NaO中都只有离子键,故化学键相同,故C正确;D.NaHSO 熔化时只能破坏离子键,不能破
2 2 4
坏共价键,故D错误;故选C。
【课后巩固】1.(易)教材作业:P117页练习1、7、8、9
2.(易)下列叙述正确的是( )
A.离子键只存在于金属阳离子与酸根阴离子之间
B.两种非金属元素形成AB型化合物,它一定含共价键
C.物质中化学键破坏了,一定发生化学变化杨sir化学,侵权必究
D.在冰的结构中氢、氧原子间均以化学键相结合
【答案】B
【解析】A.离子键不一定存在于金属阳离子与酸根阴离子之间,如KOH、NaO、NH Cl都含有离子
2 4
键,故A错误;B.不同非金属元素之间易形成共价键,所以两种非金属元素形成AB型化合物,它一定
含共价键,故B正确;C.物质中化学键破坏了,该物质不一定发生化学反应,如电解质溶于水或熔融时
发生电离,故C错误;D.在冰的结构中水分子间存在氢键,氢键是一个水分子中的氢原子与另一个水分
子中的氧原子间形成的分子间作用力,不是化学键,故D错误;答案选B。
3.(中)下列有关说法正确的是( )
①如果某化合物只含共价键,则其一定是共价化合物
②有阴离子存在的物质中一定存在阳离子
③碳、氮形成的氢化物常温下都是气态
④非金属单质在反应中都只能作氧化剂,具有强氧化性
⑤金属氧化物一定是碱性氧化物
⑥稀有气体不活泼是因为它们原子最外层都达到8电子稳定结构A.①② B.②③④
C.①②⑥ D.②③⑤
【答案】A
【解析】①如果某化合物只含共价键,则其一定是共价化合物,故①正确;②有阴离子存在的物质中
一定存在阳离子,故②正确;③碳、氮形成的氢化物常温下不一定都是气态,比如苯、肼都是液态,故③
错误;④非金属单质在反应中既能作氧化剂,又能作还原剂,比如氯气和NaOH溶液反应,故④错误;⑤
金属氧化物不一定是碱性氧化物,比如氧化铝为两性氧化物,故⑤错误;⑥稀有气体不活泼是因为它们原
子最外层都达到8电子稳定结构,He是2电子稳定结构,故⑥错误;因此①②正确,故A正确。综上所
述,答案为A。
4.(中)下列说法正确的是( )
A.NH Cl属于离子化合物,该物质中只存在离子键
4
B.CO、CH 和HO 分子中只存在极性共价键
2 4 2 2
C.N 和C1 两种分子中,每个原子的最外层都具有8电子稳定结构
2 2
D.干冰溶于水生成碳酸的过程只需克服分子间作用力
【答案】C
【解析】A.NH Cl离子化合物,铵根离子和氯离子之间形成的是离子键,铵根离子中N原子和H原
4
子之间形成的是极性共价键,故A错误;B.HO 中含有O-H极性键和O-O非极性键,故B错误;C.N
2 2 2
和Cl 两种分子,结构式分别为N≡N、Cl-Cl,N最外层5个电子、Cl最外层7个电子,则两种分子中每个
2
原子的最外层都具有8电子稳定结构,故C正确;D.干冰是分子晶体,溶于水生成碳酸,发生化学变
化,则共价键破坏,故D错误;故选:C。
5.(中)下列物质发生所述变化时,所克服的微粒间作用力,属于同类型的是( )
A.干冰和碘的升华 B.NaBr和HI分别在水中电离
C. 和CaO的熔化 D.将氯化氢和乙醇分别加入水中
【答案】AC
【解析】干冰和I (s)的升华,均破坏分子间作用力,A符合题意;氯化钠属于离子晶体,溶解在水
2
中克服离子键;HI属于共价化合物,溶解在水中克服共价键,B不符合题意;NaSO 和CaO均属于离子
2 4
化合物,熔化时破坏的是离子键,C符合题意;氯化氢加入水中,会破坏共价键,而乙醇与水互溶,在水
中仍以分子形式存在,所以不破坏化学键,D不符合题意。
6.(中)关于氢键及范德华力,下列说法正确的是( )
A.氢键比范德华力强,所以它属于化学键
B.分子间形成的氢键使物质的熔点和沸点升高C.沸点HI>HBr>HCl>HF
D.HO是一种稳定的化合物,这是由于HO之间形成氢键所致
2 2
【答案】B
【解析】A.氢键属于分子间作用力,不属于化学键,故A项错误;B.物质熔化与沸腾时需要破坏
氢键,而破坏氢键需要一定能量,所以分子间形成氢键使物质的熔点和沸点都升高,故B项正确;C.第
VIIA族元素中,只有氟化氢分子间存在氢键,沸点较高,出现反常,因此沸点为HF>HI>HBr>HCl,故
C项错误;D.水之所以化学性质稳定是因为分子内氢氧键比较稳定,与氢键无关,故D项错误。答案为
B。
7.(难)在抗击新冠病毒中“84消毒液(有效成分是NaClO)”发挥了重要作用。工业上,制备“84消
毒液”的原理为:NaCl+H O\o(\s\up6(_____)NaClO+H ↑。下列说法正确的是( )
2 2
A.该反应每转移2 mol电子生成74.5 g的NaClO
B.“84消毒液”与酒精的消毒原理相同
C.NaClO的电子式为
D.上述制备消毒液的反应过程中有离子键、非极性共价键的断裂和形成
【答案】A
【解析】根据方程式可知Cl的化合价从-1价升高为+1价,转移2mol电子生成1molNaClO,质量为
74.5g,A正确;NaClO中Cl元素为+1价,具有强氧化性,可用于杀菌消毒,酒精因能破坏蛋白质的结构
从而可以消毒,二者原理不同,B错误;NaClO是离子化合物,钠离子和次氯酸根离子之间形成离子键,
氯原子和氧原子之间形成1对共用电子对,均满足8电子稳定结构,在次氯酸根离子中O显负价,Cl显正
价,故其电子式为 ,C错误;NaCl中钠离子和氯离子之间是离子键,水分子中含有极性共价
键,NaClO中含有离子键和极性共价键,H 中存在非极性共价键,故上述反应过程中有离子键、极性共价
2
键的断裂,没有非极性键的断裂,有离子键、极性共价键、非极性共价键的生成,D错误。
8.(中)I.下列物质:①N②CO ③NH ④Na O⑤Na O⑥NaOH⑦CaBr⑧HO⑨NH Cl⑩HBr。含有极
2 2 3 2 2 2 2 2 2 4
性键和非极性键的是_____________;含有非极性键的离子化合物是___________。(填序号,下同)
II.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO 熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI
4
分解;⑦碘升华;⑧溴蒸气被木炭吸附。未破坏化学键的是__________;仅离子键被破坏的是
_____________;仅共价键被破坏的是__________。
III.下列物质:①1H、2H、3H;②HO、DO、TO;③O、O;④14N、14C。互为同位素的是
2 2 2 2 3
__________;互为同素异形体的是__________。已知自然界氧的同位素16O、17O、18O,氢的同位素有H、
D、T,从水分子的原子组成来看,自然界的水共有__________种。杨sir化学,侵权必究
【答案】⑧ ⑤ ①⑤⑦⑧ ②③ ④⑥ ① ③ 18
【解析】I.①N 含有非极性键;②CO 含有极性键;③NH 含有极性键;④NaO含有离子键;
2 2 3 2⑤NaO 含有离子键、非极性键;⑥NaOH含有离子键、极性键;⑦CaBr 含有离子键;⑧HO 含有极性
2 2 2 2 2
键、非极性键;⑨NH Cl含有离子键、极性键;⑩HBr含有极性键,综上分析含有极性键和非极性键的是
4
⑧,含有非极性键的离子化合物是⑤,故答案为:⑧,⑤;
II.①干冰气化仅破坏分子间作用力;②硝酸钾熔化破坏离子键;③KHSO 熔融破坏离子键;④硫酸
4
溶于水破坏共价键;⑤蔗糖溶于水破坏分子间作用力;⑥HI分解破坏共价键;⑦ 碘升华破坏分子间作
用力;⑧ 蒸气被木炭吸附未破坏化学键,综上分析未破坏化学键的是①⑤⑦⑧,仅离子键被破坏的是
②③,仅共价键被破坏的是④⑥,故答案为:①⑤⑦⑧,②③,④⑥;
III. 同位素质子数相同、中子数不同的原子,所以①1H、2H、3H;②HO、DO、TO;③O、O;
2 2 2 2 3
④14N、14C中互为同位素的是①,同素异形体是同种元素组成的不同单质,所以①1H、2H、3H;②HO、
2
DO、TO;③O、O;④14N、14C中互为同素异形体的是③,自然界氧的同位素16O、17O、18O,氢的同
2 2 2 3
位素有H、D、T,在1个水分子中含有2个氢原子和1个氧原子,若水分子中的氢原子相同,则16O可分
别与H、D、T构成水,即存在三种水;17O可分别与H、D、T构成水,即存在三种水;18O可分别与H、
D、T构成水,即存在三种水;若水分子中的氢原子不同,则16O可分别与HD、DT、HT构成水,即存在
三种水;17O可分别与HD、DT、HT构成水,即存在三种水;18O可分别与HD、DT、HT构成水即存在三
种水; .综上所述,共形成3×6=18种水,故答案为:①,③,18;