文档内容
第五章 化学生产中的重要非金属元素
第二节 氮及其化合物 课时作业
第三课时 硝酸 酸雨及防治
基础达标
1.下列说法错误的是( )
A. 燃煤时加入适量石灰石,可以减少废气中的SO
2
B. 在汽车排气管上加装“催化转化器”是为了减少有害气体的排放
C. 人们已开始研究使用新的自来水消毒剂,如ClO 等,是因为氯气有毒
2
D. 工业生产硝酸时补充空气有利于原料的充分利用和减少污染物排放
2.下列有关硝酸化学性质的叙述中,正确的是( )
A.浓、稀硝酸都能使蓝色石蕊试纸最终变为红色
B.硝酸能与FeO反应,只表现氧化性
C.硝酸可与NaS反应制得HS气体
2 2
D.浓硝酸因分解放出的NO 又溶解于硝酸而呈黄色
2
3.关于硝酸的说法正确的是( )
A.硝酸电离出的H+,能被Zn、Fe等金属还原成H
2
B.浓HNO 与浓HCl按3∶1的体积比所得的混合物叫王水
3
C.硝酸与金属反应时,主要是+5价的氮元素得电子
D.常温下,向浓HNO 中投入Fe片,会产生大量的红棕色气体
3
4.下列关于硫酸、硝酸的认识中,正确的是( )
A.浓硫酸和蔗糖的反应主要体现了浓硫酸的脱水性和氧化性
B.浓硝酸在光照下颜色变黄,是因为浓硝酸具有强氧化性
C.常温下,浓硝酸和浓硫酸均可以用铝罐贮存,是因为铝与它们不反应
D.铜分别与浓硝酸、稀硝酸反应生成NO 和NO,故稀硝酸的氧化性大于浓硝酸
2
5.为研究物质性质,下列实验操作及现象描述正确的是 (
)
A.如图,①中为浓盐酸和浓硝酸中的一种,②中为浓氨水,则 大
烧杯中均观察到白烟
B.将氨水缓慢滴入AlCl 溶液中,研究Al(OH) 的两性
3 3
C.常温下,浓硫酸或浓硝酸中投入Fe片,均会产生大量的气体D.加热除去NH Cl中的少量NaHCO
4 3
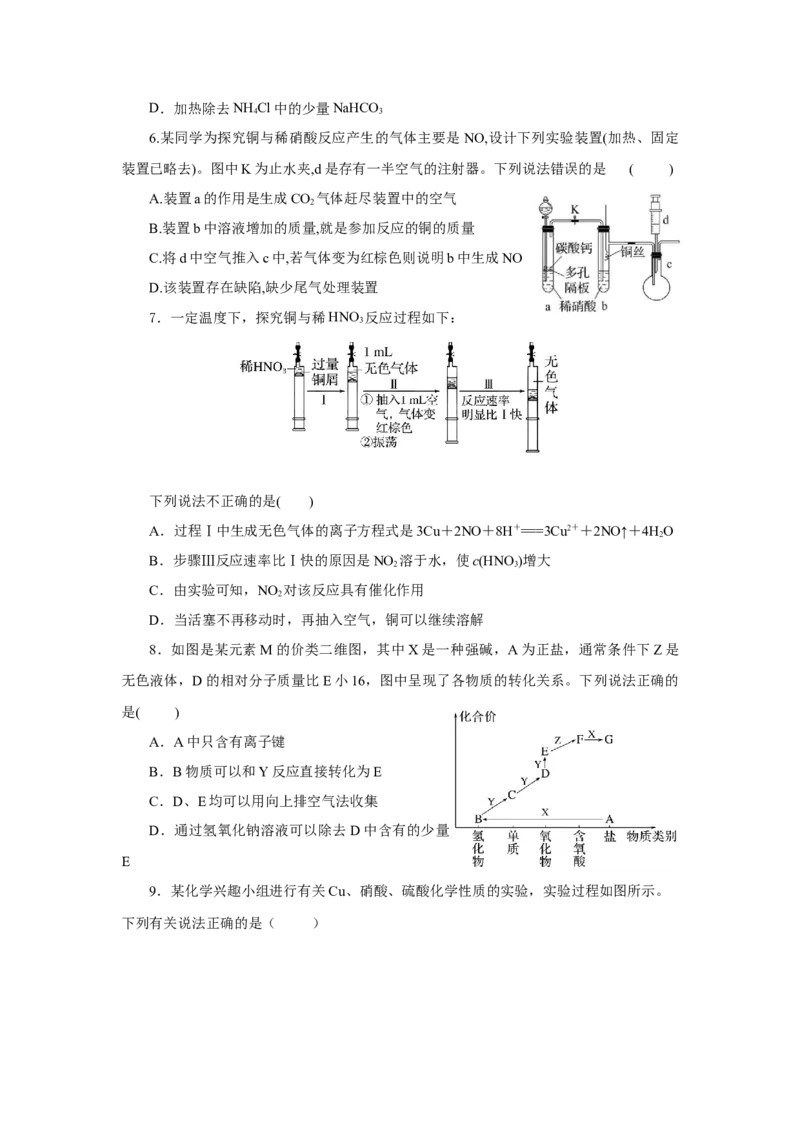
6.某同学为探究铜与稀硝酸反应产生的气体主要是NO,设计下列实验装置(加热、固定
装置已略去)。图中K为止水夹,d是存有一半空气的注射器。下列说法错误的是 ( )
A.装置a的作用是生成CO 气体赶尽装置中的空气
2
B.装置b中溶液增加的质量,就是参加反应的铜的质量
C.将d中空气推入c中,若气体变为红棕色则说明b中生成NO
D.该装置存在缺陷,缺少尾气处理装置
7.一定温度下,探究铜与稀HNO 反应过程如下:
3
下列说法不正确的是( )
A.过程Ⅰ中生成无色气体的离子方程式是3Cu+2NO+8H+===3Cu2++2NO↑+4HO
2
B.步骤Ⅲ反应速率比Ⅰ快的原因是NO 溶于水,使c(HNO)增大
2 3
C.由实验可知,NO 对该反应具有催化作用
2
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
8.如图是某元素M的价类二维图,其中X是一种强碱,A为正盐,通常条件下Z是
无色液体,D的相对分子质量比E小16,图中呈现了各物质的转化关系。下列说法正确的
是( )
A.A中只含有离子键
B.B物质可以和Y反应直接转化为E
C.D、E均可以用向上排空气法收集
D.通过氢氧化钠溶液可以除去D中含有的少量
E
9.某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示。
下列有关说法正确的是( )A.①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO
2
B.若③中加入足量稀硫酸,则在相同条件下①中产生的气体体积比③中产生的气体
体积小
C.③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
D.由上述实验可知:Cu在常温下既可与稀硝酸反应,也可与稀硫酸反应
10.通过如图流程制备硝酸铜晶体,下列说法不正确的是( )
A.将废铜片粉碎,可提高反应速率
B.若将废铜片直接“溶解”,既产生污染又降低硝酸的利用率
C.为了使硝酸铜尽可能析出,“结晶”应将溶液蒸干
D.用无水乙醇代替水“洗涤”的目的之一是减少晶体的溶解损失
能力提升
11.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法
可制得硝酸,反应过程如图:
N―――――――――――→NH ――――――→NO――――→NO ―――――→HNO
2 3 2 3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物,应处理后才能排
放。下列说法不正确的是( )
A.常温下,浓硝酸可盛放在铝制或铁制容器中
B.BaSO 固体能溶于稀硝酸,生成Ba(NO ),放出SO 气体
3 3 2 2
C.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出 NH ,将未
3
反应的原料气送回合成塔以提高原料的利用率
D.转化④中,当V(NO )∶V(O )=4∶1时,理论上NO 全部转化为HNO
2 2 2 3
12.硝酸与金属反应后所得还原产物与硝酸的浓度和金属的活泼性有关。10 mL 0.5mol·L-1 HNO 与0.048 g Mg恰好完全反应。若氮元素只被还原到一种价态,下列说法不正
3
确的是( )
A.HNO 作还原剂 B.HNO 浓度越低,N元素还原价态越低
3 3
C.反应中转移电子数为0.004 mol D.还原产物可能为NH NO
4 3
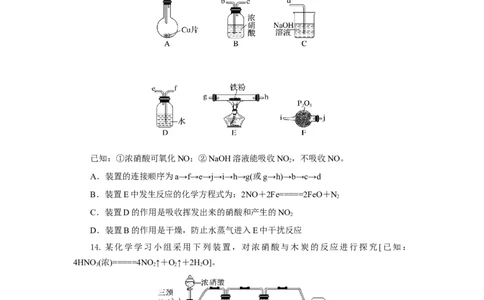
13.某兴趣小组设计用铁粉将NO还原为N(同时生成FeO)。下列说法不正确的是(
2
)
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO ,不吸收NO。
2
A.装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d
B.装置E中发生反应的化学方程式为:2NO+2Fe=====2FeO+N
2
C.装置D的作用是吸收挥发出来的硝酸和产生的NO
2
D.装置B的作用是干燥,防止水蒸气进入E中干扰反应
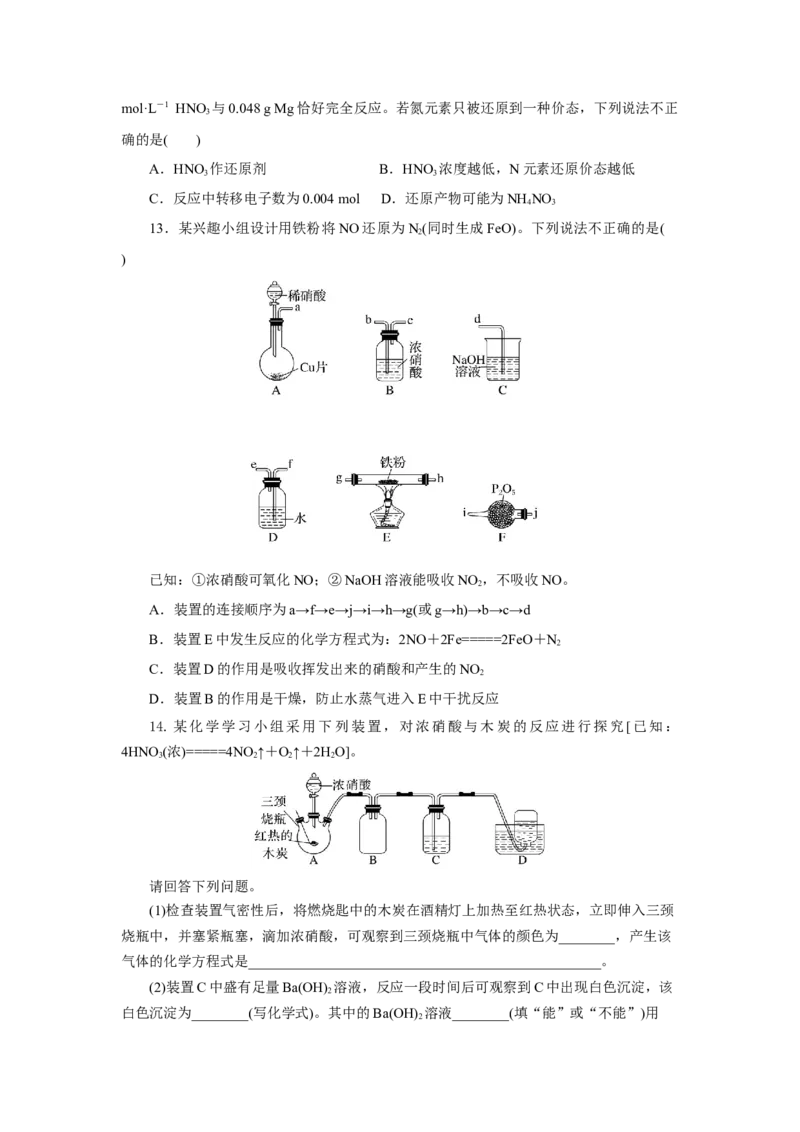
14.某化学学习小组采用下列装置,对浓硝酸与木炭的反应进行探究[已知:
4HNO(浓)=====4NO ↑+O↑+2HO]。
3 2 2 2
请回答下列问题。
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,立即伸入三颈
烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三颈烧瓶中气体的颜色为________,产生该
气体的化学方程式是__________________________________________________。
(2)装置C中盛有足量Ba(OH) 溶液,反应一段时间后可观察到C中出现白色沉淀,该
2
白色沉淀为________(写化学式)。其中的Ba(OH) 溶液________(填“能”或“不能”)用
2Ca(OH) 溶液代替,理由是
2
________________________________________________________________。
(3)装置B的作用是___________________________________________。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O。
2
①下列对该气体的检验方法合理的是__________(填字母)。
A.敞口观察集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果集气瓶中收集到的无色气体是氧气,则氧气的来源是_________________。
直击高考
15.下列有关实验操作、现象和解释或结论都正确的是 ( )
序号 实验操作 现象 解释或结论
过量的Fe粉中加入稀HNO,
① 3 溶液呈红色 稀HNO 将Fe氧化为Fe3+
充分反应后,滴入KSCN溶液 3
② 浓HNO 久置或光照 变黄色 HNO 不稳定易分解
3 3
Al箔表面被HNO 氧化,形
③ Al箔插入稀HNO 中 无现象 3
3 成致密的氧化膜
用玻璃棒蘸取浓HNO 点到蓝 试纸先变红
④ 3 浓HNO 具有酸性和强氧化性
色石蕊试纸上 色后褪色 3
A.①② B.③④ C.②③④ D.②④
16.某化学小组设计了如下有关氮的化合物的实验。请按要求回答下列问题。
(1)氨气的喷泉实验:如下图装置所示,干燥的圆底烧瓶里充满NH ,欲观察到烧瓶中
3
产生喷泉,需进行的操作是____________________________。
(2)硝酸的制备实验:如图所示a~f装置。①装置a的最佳选择为(填“图3”或“图4”)______________。
②装置b中NaO 的作用是_______________________________________________。
2 2
(3)硝酸的性质实验:
①常温下,同学甲在上图实验结束后,用pH计测装置e中溶液的pH=1.00。
ⅰ.这说明e中发生的反应可能为(写化学方程
式)_________________________________。
ⅱ.同学乙做同样实验,测得e中溶液的pH=6.00,可能原因是
_______________________。
②用如图所示装置进行硝酸与铜的反应实验。
ⅰ.请在h方框中补全该实验所需装置图并标注所需试剂
_________________________。
ⅱ.硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:
____________________。
ⅲ.g中为稀硝酸时,反应开始后,g中溶液颜色变蓝。写出g中反应的离子方程式:
___________________________________________________。
ⅳ.g中为浓硝酸时,g中溶液颜色变绿。反应较ⅱ中剧烈许多的原因是
_______________。
ⅴ.对比ⅲ与ⅳ反应后g中溶液颜色,推测其原因是ⅳ反应后g溶液中溶有NO 且达
2
饱和。为证明该推测正确,向ⅳ反应后g溶液中加入__________________,会观察到溶液颜色由绿色变为蓝色。