文档内容
zxxk.com
化学用语课后练习
题一: 分类是一种行之有效、简便易行的科学方法。下列物质的俗称、化学式、类别三者一致的是(
)
A.苛性钠 NaCO 盐 B.干冰 HO 氧化物
2 3 2
C.生石灰 Ca(OH) 碱 D.水银 Hg 单质
2
题二: 下列选项中物质的俗名、化学式、类别、用途完全对应的是( )
A.纯碱 NaCO 碱 制玻璃
2 3
B.生石灰 CaO 氧化物 补钙剂
C.食盐 NaCl 盐 除铁锈
D.火碱 NaOH 碱 生产橡胶
题三: 地壳中含量最多的金属元素和含量最多的非金属元素所形成的化合物是( )
A.Fe O B.Al O C.SiO D.CuO
3 4 2 3 2
题四: 稀土元素铕(Eu)是激光及原子能应用的重要的材料。已知氯化铕的化学式为EuCl,
3
则氧化铕的化学式为( )
A.EuO B.EuO C.EuO D.EuO
2 3 3 2 3
题五: 屠呦呦带领科研团队研发的新型抗疟疾药——青蒿素和双氢青蒿素,在全球抗击疟疾进程
中,拯救了上百万人的生命,因此获得2015年诺贝尔生理学或医学奖。青蒿素化学式为C H O,下
15 22 5
列说法不正确的是( )
A.青蒿素属于有机物
B.青蒿素中C、H、O三种元素的质量比为15:22:5
C.青蒿素中氧元素的质量分数为28.4%
D.利用化学提取和合成药物,以抑制细菌和病毒,保障人体健康
题六: 2015年,中国女科学家屠呦呦获得诺贝尔生理学或医学奖。理由是她和她的团队先驱性地
发现了青蒿素,开创了疟疾治疗新方法。下列关于青蒿素(化学式是C H O )的叙述正确的是(
15 22 5
)
A.青蒿素由三种原子构成
B.青蒿素属于有机高分子化合物
C.青蒿素中碳元素和氧元素的质量比为3:1
D.青蒿素的相对分子质量为282
题七: 下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )
A. 电解水2HO H↑ +O ↑分解反应
2 2 2
0zxxk.com
B. 硫酸铜溶液中滴加氢氧化钠溶液 CuSO +2NaOH=Cu(OH) ↓ + Na SO 复分解反应
4 2 2 4
C. 在空气中燃烧 2Mg + O 2MgO 氧化反应
2
D. 氢气还原氧化铜H + CuO = Cu+H O 置换反应
2 2
题八: 按要求写出与水有关的化学方程式。
(1)反应物有水的化合反应: ;
(2)生成物有水的化合反应: ;
(3)有水参加的分解反应: ;
(4)有水生成的分解反应: 。
题九: 天宫一号飞行器中的镍氢电池放电时所发生的化学方程式为H +2NiO(OH)=2Ni(OH) ,下
2 2
列说法正确的是( )
A. NiO(OH)是混和物 B. NiO(OH)是反应物
C. Ni(OH) 中含有两种元素 D. Ni(OH) 中Ni的化合价为+1价
2 2
题十: 关于化学方程式CH+2O ComCO+2H O的描述正确的是( )
4 2bin 2 2
A.甲烷加氧气在点燃条件下,反应生成二氧化碳和水
B.1个甲烷和2个氧气在点燃条件下,生成1个二氧化碳和2个水
C.1个CH 分子和2个O 分子在点燃条件下,生成1个CO 分子和2个HO分子
4 2 2 2
D.1gCH 和2gO 在点燃条件下,生成1g CO 和2g HO
4 2 2 2
题十一:下列关于四种粒子的结构示意图的说法中正确的是( )
A.①③属于不同种元素 B.④属于离子,离子符号为Mg+2
C.②③的化学性质相似 D.②表示的元素在化合物中通常显+1价
题十二:以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是( )
A.①的化学性质比较稳定 B.③④属于同种元素
C.④是一种阴离子 D.② 容易得到电子
1zxxk.com
题十三:下列化学用语与所表达的意义对应错误的是( )
题十四:下列化学用语表达正确的是( )
A.氯酸钾中氯元素的化合价:
B.镁离子的结构示意图:
C.两个乙醇分子:2C HOH
2 5
D.工业上炼铁的主要反应原理:3C+2Fe O 4Fe+3CO ↑
2 3 2
题十五:下列关于钠原子和钠离子的说法中,正确的是( )
A.它们的核外电子数相同
B.它们的性质完全相同
C.钠原子的质量比钠离子大得多
D.它们的质子数和中子数都相同
题十六:C-12和C-14是碳元素的两种不同的原子,二者的不同点有( )
①原子中的电子数;②原子核内的中子数;③原子核内的质子数;④原子的质量
A.①② B.③④ C.①③ D.②④
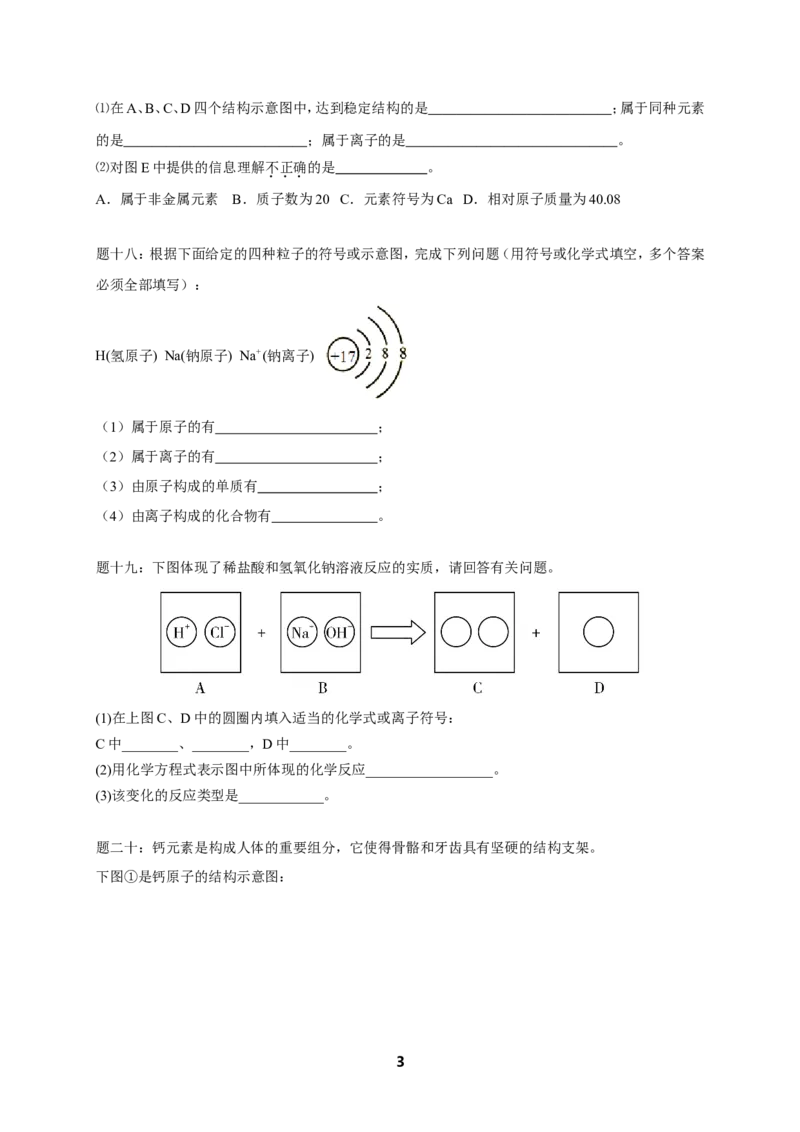
题十七:结合下列图示回答问题。
2zxxk.com
⑴在A、B、C、D四个结构示意图中,达到稳定结构的是 ;属于同种元素
的是 ;属于离子的是 。
⑵对图E中提供的信息理解不正确的是 。
A.属于非金属元素 B.质子数为20 C.元素符号为Ca D.相对原子质量为40.08
题十八:根据下面给定的四种粒子的符号或示意图,完成下列问题(用符号或化学式填空,多个答案
必须全部填写):
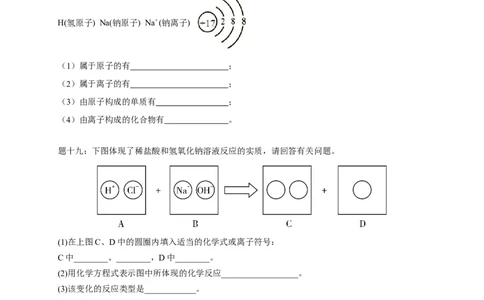
H(氢原子) Na(钠原子) Na+ (钠离子)
(1)属于原子的有 ;
(2)属于离子的有 ;
(3)由原子构成的单质有 ;
(4)由离子构成的化合物有 。
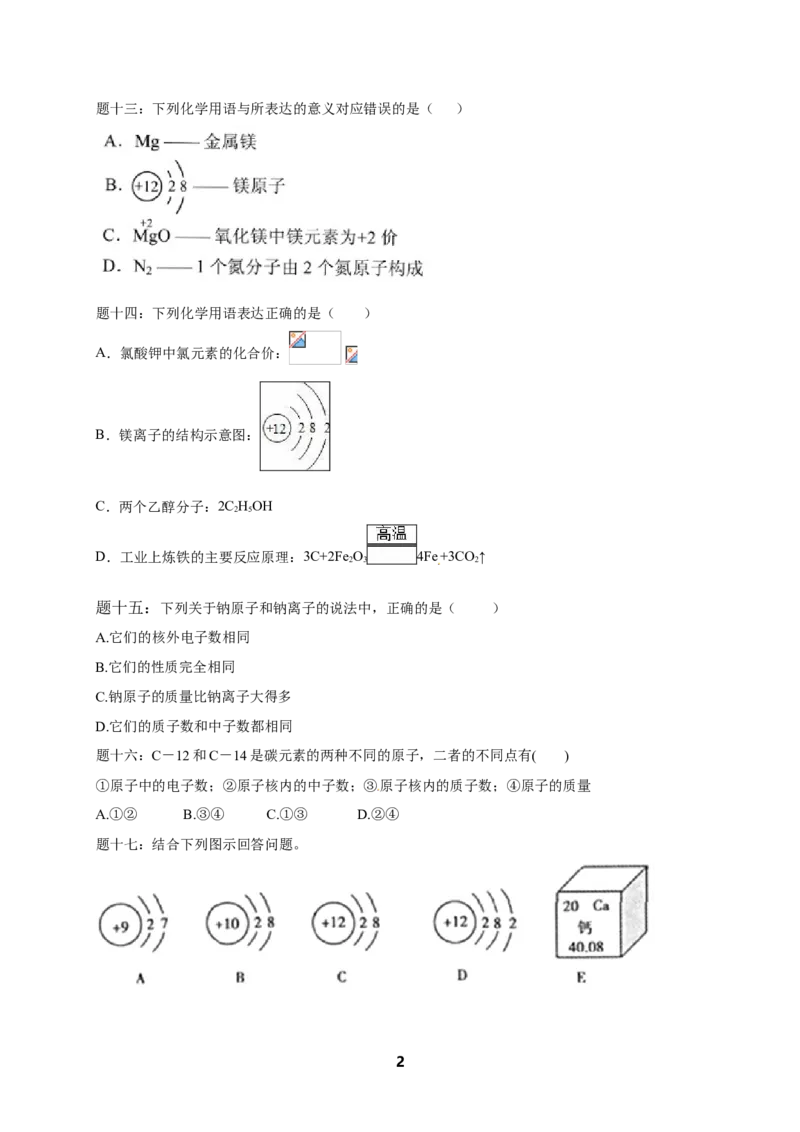
题十九:下图体现了稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题。
(1)在上图C、D中的圆圈内填入适当的化学式或离子符号:
C中________、________,D中________。
(2)用化学方程式表示图中所体现的化学反应__________________。
(3)该变化的反应类型是____________。
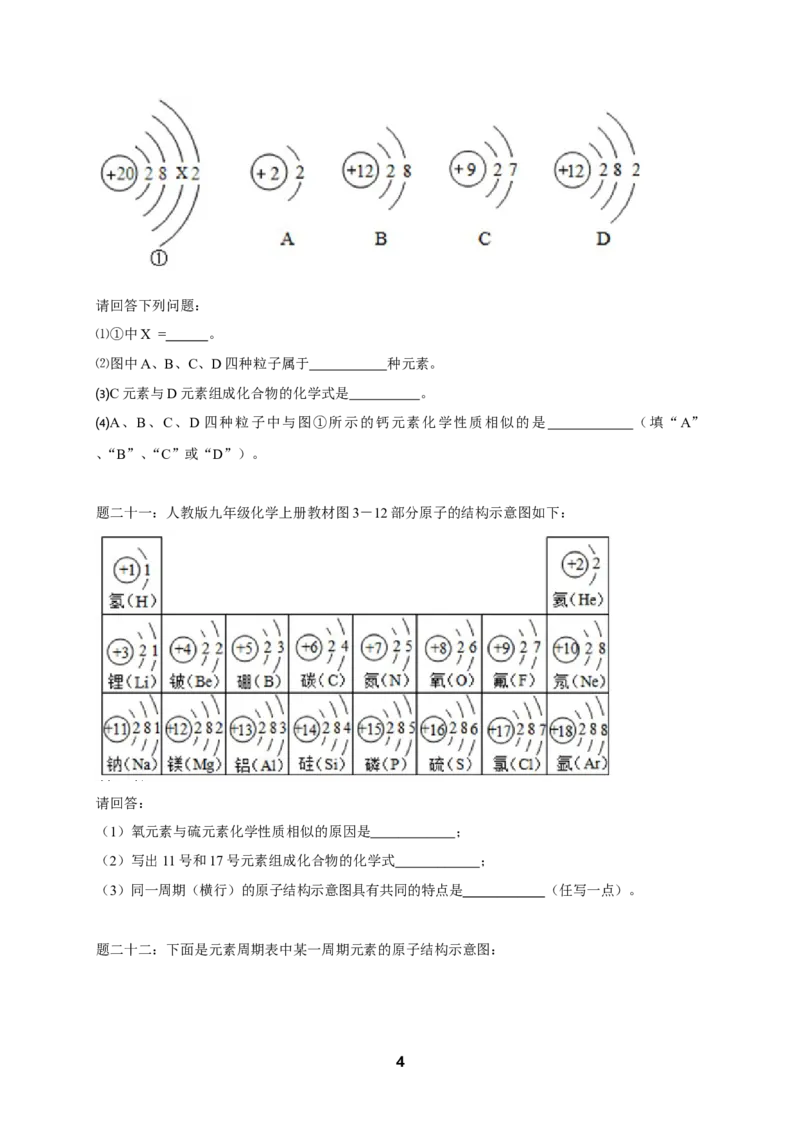
题二十:钙元素是构成人体的重要组分,它使得骨骼和牙齿具有坚硬的结构支架。
下图①是钙原子的结构示意图:
3zxxk.com
请回答下列问题:
⑴①中X = 。
⑵图中A、B、C、D四种粒子属于 种元素。
⑶C元素与D元素组成化合物的化学式是 。
⑷A、B、C、D 四种粒子中与图①所示的钙元素化学性质相似的是 (填“A”
、“B”、“C”或“D”)。
题二十一:人教版九年级化学上册教材图3-12部分原子的结构示意图如下:
请回答:
(1)氧元素与硫元素化学性质相似的原因是 ;
(2)写出11号和17号元素组成化合物的化学式 ;
(3)同一周期(横行)的原子结构示意图具有共同的特点是 (任写一点) 。
题二十二:下面是元素周期表中某一周期元素的原子结构示意图:
4zxxk.com
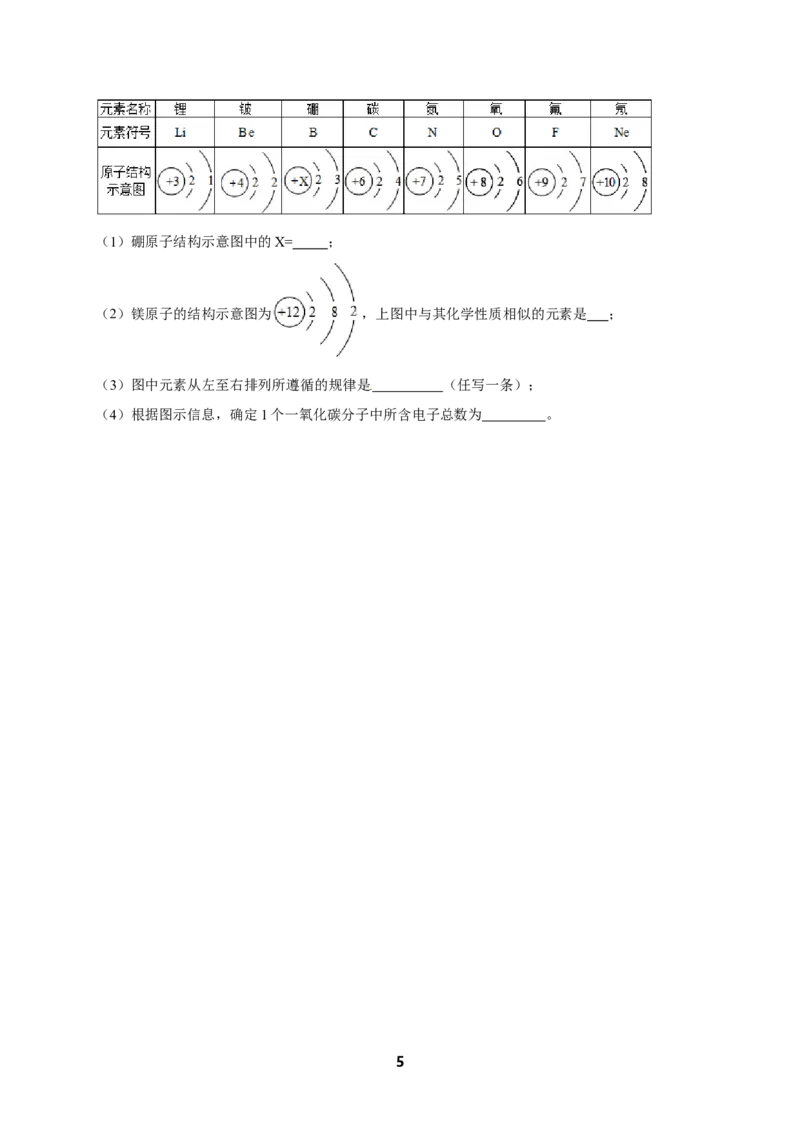
(1)硼原子结构示意图中的X= ;
(2)镁原子的结构示意图为 ,上图中与其化学性质相似的元素是 ;
(3)图中元素从左至右排列所遵循的规律是 (任写一条);
(4)根据图示信息,确定1个一氧化碳分子中所含电子总数为 。
[来源:Zxxk.Com]
5zxxk.com
化学用语课后练习参考答案
题一: D
详解:氢氧化钠俗称火碱、烧碱、苛性钠,其化学为NaOH,属于碱,A项错误;干冰是固态的二氧化碳,
其化学式为CO,属于氧化物,B项错误;生石灰是氧化钙的俗称,其化学式为CaO,属于氧化物,C项错
2
误;水银是金属汞的俗称,其化学式为Hg,属于单质,D项正确。
题二: D
详解:碳酸钠俗称纯碱,其化学式为NaCO,是由钠离子和碳酸根离子构成的化合物,属于盐,A错误;
2 3
生石灰是氧化钙的俗称,其化学式为CaO,是由钙元素和氧元素组成的化合物,属于氧化物,由于氧化
钙与水反应生成氢氧化钙,该反应放出大量的热,且生成的氢氧化钙具有腐蚀性,因此氧化钙不能用
作补钙剂,B错误。氯化钠的俗称是食盐,其化学式为NaCl,是由钠离子和氯离子构成的化合物,属于
盐;食盐不与铁锈的主要成分氧化铁反应,不能用于除铁锈,C错误;氢氧化钠俗称火碱、烧碱、苛性
钠,其化学式为NaOH,是由钠离子和氢氧根离子构成的化合物,属于碱;可用于生产橡胶,D正确。
题三: B
详解:地壳中含量最多的金属元素是铝、地壳中含量最多的非金属元素是氧,二者形成化合物的化学
式是AlO。本题应选B。
2 3
题四: B
详解:氯化铕中的氯元素的化合价为1,由化合物中正负化合价代数和为零,可得EuCl 中Eu为+3
3
价。氧化铕中铕元素显+3价,氧元素显﹣2价,则其化学式为EuO。
2 3
题五: B
详解:青蒿素是一种含碳元素的化合物,属于有机物,A项说法正确;青蒿素中碳、氢、氧三种元素的
质量比为:(12×15):(1×22):(16×5)=90:11:40,B项说法错误;青蒿素中氧元素的质量分数为
×100%≈28.4%,C项说法正确;化学的重要用途之一是利用化学反应提取和
合成药物,以抑制细菌和病毒,保障人体健康,D项说法正确。
[来源:学.科.网]
题六: D
详解:青蒿素是由青蒿素分子构成的,青蒿素分子(C H O)由C、H、O三种原子构成,A项错误;青蒿
15 22 5
素属于有机化合物,它的相对分子质量为:12×15+1×22+16×5=282,它的相对分子质量较小,不属
于有机高分子化合物,B项错误、D项正确;青蒿素中碳元素和氧元素的质量比为:(12×15):(16×5)
=9:4,C项错误。本题应选D。
题七: B
[来源:学科网]
6zxxk.com
详解:A中电解水的化学方程式是错误的,应为:2HO 2H↑+ O ↑;氧化反应不属于基本反应
2 2 2
类型,镁与氧气的反应所属的基本反应类型是化合反应,C错误;氢气还原氧化铜的化学方程式缺少
反应条件,应为:H + CuO Cu + HO,D错误;B所对应的化学式和反应类型均正确。
2 2
题八: (1)CO+HO=HCO (2)2H+O 2HO (3)2HO 2H↑+O↑
2 2 2 3 2 2 2 2 2 2
(4)2HO 2HO+O↑(或:HCO=HO+CO↑)
2 2 2 2 2 3 2 2
详解:所写化学方程式既要与水有关,又要符合要求的反应类型,书写时注意标注反应条件和生成物
的状态符号。
题九: B
详解:NiO(OH)是一种有固定组成的物质,有唯一的化学式且由不同元素组成,属于纯净物中的化合
物;NiO(OH)在“等号”的前面,属于反应物;Ni(OH) 是由Ni、O、H三种元素组成的;氢氧根的化合价
2
是1价,根据化合物中各元素正负化合价代数和为零的原则,可判断出Ni(OH) 中Ni的化合价为
2
+2价。本题应选B。
题十: C
详解:化学方程式中的“+”应读作和,A项不正确;微观方面可表示各物质的粒子个
[来源:Zxxk.Com]
数比,表示1个甲烷分子和2个氧气分子在点燃条件下,生成1个二氧化碳分子和2个水分子,B项不
正确、C项正确;化学方程式中各化学式前的数字表示各物质的粒子个数比而不是质量比,D项不正
确。
题十一: D
详解:同种元素质子数一定相同,①③的质子数都是17,两者属于同种元素,A项错误;离子中质子数
与核外电子数不等,④中质子数比电子数多2,是镁离子,符号应为Mg2+,B项错误;元素的性质与其原
子的最外层电子数关系密切,所以最外层电子数相同则化学性质相似,②③的最外层电子数分别是
1、7,化学性质不会相似,C 项错误;②所示原子最外层电子数是1,化学反应中易失掉最外层的1个电
子而形成带一个单位正电荷的阳离子,在化合物中通常显+1价,D项正确。
题十二: C
[来源:学#科#网Z#X#X#K]
详解:最外层电子数为8(第一层为最外层时为2)的结构称为稳定结构,因此①④属于稳定结构,这
两种微粒化学性质比较稳定,A正确;核内质子数相同的原子属于同种元素,③④核内质子数相同,因
此属于同种元素,B正确;④是带有一个单位正电荷的阳离子,C错误;②最外层有7个电子,大于4个,
易得到1个电子,达到8个电子的稳定结构,D正确。
7zxxk.com
题十三: B
详解:B选项所示粒子核内有12个质子,核外有10个电子,表明该粒子是Mg2+,B项错误,其余各项中
化学用语所表达的意义均正确。
题十四: C
详解:氯酸钾(KClO)中钾元素显+1价、氧元素显﹣2价,依据化合物中各元素正负化合价的代数和为
3
零的规律可计算出氯元素显+5价,A项错误;B选项图中粒子的质子数=核外电子数=12,该微粒为原
子,B项错误;CHOH是乙醇的化学式,该符号还可以表示一个乙醇分子,若表示多个该分子,应在该
2 5
分子符号前加上相应的数字,如:两个乙醇分子可表示为2CHOH,C项正确;工业上炼铁的原理为:在
2 5
高温条件下,用还原剂一氧化碳还原氧化铁等铁的氧化物,生成铁和二氧化碳,化学方程式为:
FeO+3CO 2Fe+3CO ,D项错误。
2 3 2
题十五: D
详解:钠离子比钠原子少一个电子,带有一个单位的正电荷,它们的最外层电子数和核外电子数都不
同,A项错误;由于最外层电子数不同,因此它们的化学性质不同,B项错误;钠原子变成钠离子,只是
核外电子发生变化,原子核不变(即质子数和中子数不变),由于电子的质量比质子或中子的质量小
得多,因此钠原子和钠离子的质量差别不大,C项错误、D项正确。
题十六: D
详解:元素是具有相同的核电荷数(质子数)的一类原子的总称。在原子中,质子数=核外电子数,所以
C-12和C-14的电子数和质子数均相同;原子核是由质子与中子构成
的,相对原子质量≈中子数+质子数,C-12和C-14的区别是所含的中子数不同,因而相对原子质量不
同,原子的质量也不相同。本题应选D。
题十七: ⑴BC CD C ⑵A
详解:⑴在原子结构示意图中,最外层达到8个电子(只有第一层时是2个电子)的结构称为相对稳定
结构;元素是具有相同质子数(或核电荷数)的一类原子的总称,所以决定元素种类的是质子数;质子
数和核外电子数不相等的结构示意图是离子;
⑵钙属于金属元素,左上角表示原子序数,该数值等于质子数;元素符号和相对原子质量从图中也可
以读出。
题十八: (1)H、Na (2)Na+ 、Cl (3)Na (4)NaCl
详解:四种粒子分别为氢原子、钠原子、钠离子和氯离子,这几种粒子可以形成的单质有氢气(由氢气
分子构成)和金属钠(由钠原子构成),可以形成由离子构成的化合物是氯化钠。
题十九: (1)Na+ Cl- HO (2)HCl+NaOH=NaCl+HO (3)复分解反应
2 2
8zxxk.com
详解:(1)中和反应的实质是氢氧根离子和氢离子反应生成水的过程,氯化钠是由钠离子
和氯离子构成的,所以C中的粒子为Na+、Cl-,D中的粒子为HO;(2)氢氧化钠和盐酸反应生成氯化
2
钠和水,化学方程式为:HCl+NaOH=NaCl+HO;(3)该反应是两种化合物相互交换成分生成另外两种
2
化合物的反应,属于复分解反应。
题二十: ⑴8 ⑵3 ⑶MgF ⑷D
2
详解:⑴在原子中,质子数=核外电子数,可列式得:20=2+8+X+2,可解得X=8;
⑵具有相同质子数的一类元素,统称为一种元素,可以确定B、D属于同种元素,图中A、B、C、D四种粒
子属于3种元素;
⑶C是氟元素、D是镁元素,由它们的最外层电子数可以看出:在化学变化中,氟原子易得到1个电子,
带1个单位的负电荷,通常显的化合价为-1价;镁原子失去2个电子,带2个单位的正电荷,通常显
的化合价为+2价,则F、Mg两元素形成化合物的化学式是MgF;
2
⑷元素的化学性质,取决于原子的最外层电子数,所以与图①中钙元素具有相似化学性质的是D镁元
素(A中原子的最外层电子数也是2,但第一层上的2个电子属于相对稳定结构)。
题二十一: (1)两种原子的最外层电子数相同 (2)NaCl (3)电子层数相同
详解:(1)元素的化学性质主要取决于原子的最外层电子数,氧元素与硫元素化学性质相似的原因是:
两种原子的最外层电子数相同;(2)原子序数为11的元素为钠元素,原子序数为17的元素为氯元素,
钠为+1价,氯为﹣1价,故组成化合物的化学式为NaCl;
(3)由原子结构示意图可以看出,同一周期(横行)的原子结构示意图具有的共同的特点是电子层数
相同等。
题二十二: (1)5 (2)铍 (3)最外层电子数依次增加 (4)14
详解:(1)根据原子结构示意图,圆圈内的数字表示该种原子的质子数,在原子中:质子数=核外电子
数,硼的核外电子数是2+3=5;
(2)元素的化学性质由其最外层电子数决定,一般最外层电子数相同的原子,化学性质相似;
(3)同一周期的元素的原子具有相同的电子层数,由所给信息可知,从左到右同一周期最外层电子数
依次增多;
(4)1个一氧化碳分子由1个碳原子和1个氧原子构成,1个碳原子含有6个电子,1个氧原子含有8
个电子,所以1个一氧化碳分子含有6+8=14 个电子。
9