文档内容
zxxk.com
化学计算经典精讲课后练习
“塑化剂”是一种工业原料,但不法商人把它添加到饮用品当中,
题一:
人喝了这样的饮用品,会对身体造成严重的危害。已知“塑化剂”的主要成
分是邻苯二甲酸二辛酯,化学式为C H O ,完成下列问题:
24 38 4
(1)邻苯二甲酸二辛酯属于______________。(填有机物或无机物)
(2)邻苯二甲酸二辛酯的相对分子质量是_________________。
(3)邻苯二甲酸二辛酯中碳、氢、氧三种元素的质量比是_______________。
(4)邻苯二甲酸二辛酯中碳元素的质量分数是_____________________。
(精确到0.1%)
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾
题二:
(KIO )。如图所示是超市销售的一种加碘盐标签上的部分文字说明。
3
请回答下列问题:
(1)碘酸钾中钾、碘、氧三种元素质量比为________。
(2)每袋该食盐中碘元素的质量是 mg。
(3)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg。
假设碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为 g。
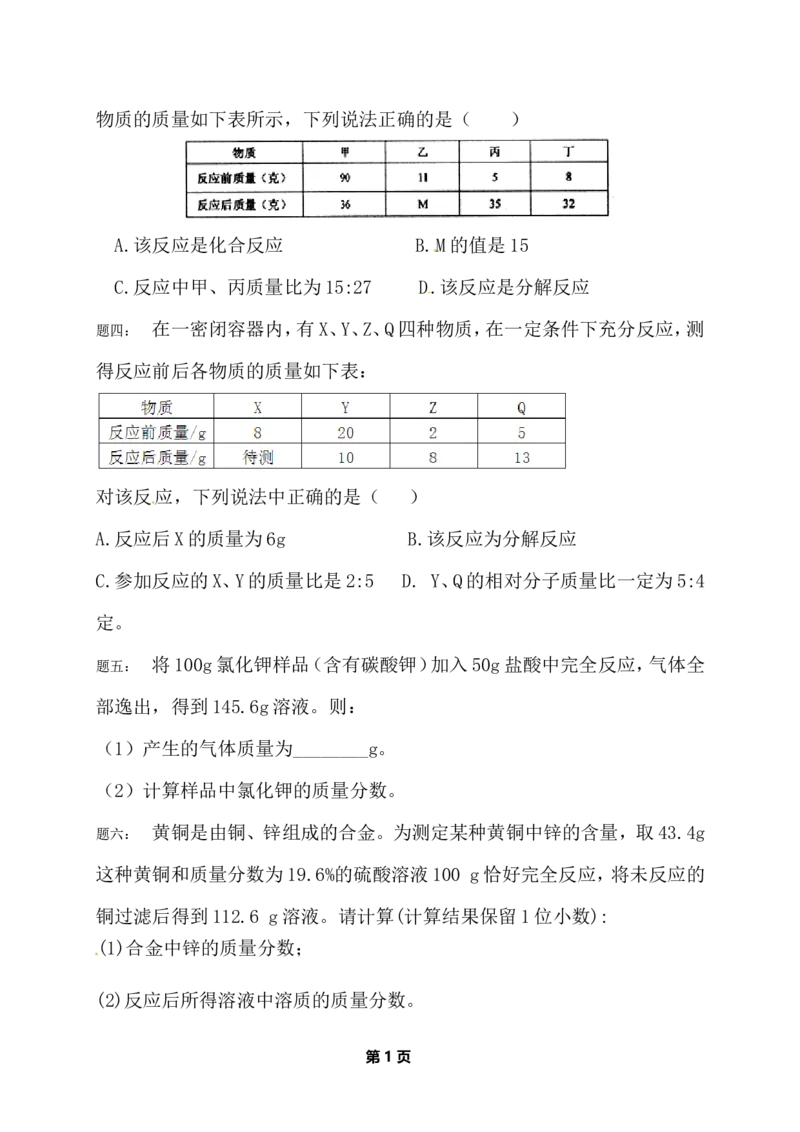
密闭容器内有四种物质,在一定条件下充分反映,测得反应前后各
题三:
第 0 页zxxk.com
物质的质量如下表所示,下列说法正确的是( )
A.该反应是化合反应 B.M的值是15
C.反应中甲、丙质量比为15:27 D.该反应是分解反应
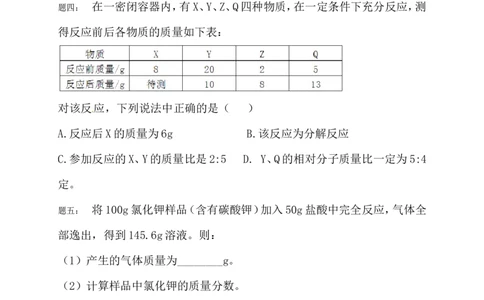
在一密闭容器内,有X、Y、Z、Q四种物质,在一定条件下充分反应,测
题四:
得反应前后各物质的质量如下表:
对该反应,下列说法中正确的是( )
A.反应后X的质量为6g B.该反应为分解反应
C.参加反应的X、Y的质量比是2:5 D. Y、Q的相对分子质量比一定为5:4
定。
将100g氯化钾样品(含有碳酸钾)加入50g盐酸中完全反应,气体全
题五:
部逸出,得到145.6g溶液。则:
(1)产生的气体质量为________g。
(2)计算样品中氯化钾的质量分数。
黄铜是由铜、锌组成的合金。为测定某种黄铜中锌的含量,取43.4g
题六:
这种黄铜和质量分数为19.6%的硫酸溶液100 g恰好完全反应,将未反应的
铜过滤后得到112.6 g溶液。请计算(计算结果保留1位小数):
(1)合金中锌的质量分数;
(2)反应后所得溶液中溶质的质量分数。
第 1 页zxxk.com
食盐在20℃时的溶解度是36g,在这个温度下,不可能得到的溶液的
题七:
质量分数是( )
A.25% B.20% C.30% D.26.5%
将一定量的溶质质量分数为 20.0%的某溶液,在一定温度下蒸发掉
题八:
10.0g水时,有2.0g不含结晶水的溶质晶体析出,此时溶液中溶质的质量分
数变为24.0%.则该溶液在此温度下的溶解度为 g
;此实验中所取的20.0%的溶液质量为 g。
取若干克氯酸钾和二氧化锰的固体混合物,在试管中加热至不再有
题九:
气体放出,将试管内的剩余固体冷却后溶于水,过滤、洗涤、干燥得到纯净固
体3.25g,还得到100g溶质质量分数为7.45%的滤液。试计算(写出必要的
计算过程):
⑴反应后产生气体的质量。
⑵原混合物中氯元素的质量分数。
28.7g的氯化钠和硝酸钠的混合物,溶于100g水中,向所得溶液中加
题十:
入134g的硝酸银溶液,恰好完全反应,得到溶液的质量是234g。计算:原混
合物中钠元素的质量分数。(已知:AgNO +NaCl=AgCl↓+NaNO ;计算结果精
3 3
确到1%)
第 2 页zxxk.com
[来源:学科网ZXXK]
第 3 页zxxk.com
化学计算经典精讲
课后练习参考答案
(1)有机物 (2)390 (3)144:19:32 (4)73.8%
题一:
解析:1.(1)由邻苯二甲酸二辛酯,化学式为C H O 可知,含有碳元素,所以
24 38 4
属于有机化合物,简称有机物;(2)由邻苯二甲酸二辛酯,化学式为C H O
24 38 4
可知,邻苯二甲酸二辛酯的相对分子质量=12×24+1×38+16×4=390;(3)由
邻苯二甲酸二辛酯,化学式为C H O 可知,邻苯二甲酸二辛酯中碳、氢、氧
24 38 4
三种元素的质量比=(12×24):(1×38):(16×4)=144:19:32;(4)邻苯二甲
酸二辛酯中碳元素的质量分数= ×100%=73.8%。
(1)39:127:48 (2)10 (3)7.5[来源:Zxxk.Com]
题二:
解析:(1)元素的质量比=相对原子质量×原子个数之比;(2)每袋食盐质量
是 500g,含碘量 20mg/kg,所以每袋该食盐中碘元素的质量 500g×20mg/
kg=10mg;500g食盐中含碘元素10 mg,那么0.15mg碘元素需要多少食盐提
供,根据对应关系成比例即可计算出为7.5g。
D
题三:
解析:根据质量守恒定律可知,反应前各物质的质量总和=反应后生成各物
质的质量总和,则得:90+11+5+8=36+M+35+32,解得M=11,B项错误;甲的质
量减少为反应物,丙、丁的质量增加为生成物,乙的质量不变,可能是催化剂,
也可能不参加反应,因此该反应属于分解反应,A项错误、D项正确;反应中
甲、丙质量比为:(90-36)g: (35-5)g=9:5,C项错误。本题应选D。
C
题四:
第 4 页zxxk.com
解析:本题应先根据反应前后质量的变化确定出反应物和生成物,再根据质
量守恒定律确定出待测的X的质量。由于反应后Y的质量减少,所以Y是反
应物,参加反应的Y的质量为20g-10g=10g;反应后Z、Q两种物质的质量增
加,说明 Z、Q 都是生成物,且生成的 Z、Q 的质量分别是:8g-2g=6g、
13g-5g=8g,由于生成物的总质量大于反应物Y的质量,根据质量守恒定律
可推断出X一定是反应物,且参加反应的X的质量是:8g+6g-10g=4g,故待
测的X的质量是:8g-4g=4g;参加反应的X、Y的质量比是4g:10g=2:5,由于
不知道化学方程中各种物质前的化学计量数,所以Y、Q的相对分子质量比
无法确
⑴4.4
题五:
⑵解:设样品中碳酸钾的质量为x
K CO +2HCl=2KCl+CO ↑+H O
2 3 2 2
138 44
x 4.4g
=
解得:x=13.8g[来源:学#科#网]
氯化钾的质量为100g-13.8g=86.2g
样品中氯化钾的质量分数为: ×100%=86.2%
答:样品中氯化钾的质量分数为86.2%。
解析:由质量守恒定律可以计算出反应产生二氧化碳的质量为:
100g+50g-145.6g=4.4g;依据化学方程式中碳酸钾与二氧化碳的质量关系,
第 5 页zxxk.com
可以利用二氧化碳的质量计算出样品中参加反应的碳酸钾的质量,进一步
计算出样品中氯化钾的质量及样品中氯化钾的质量分数。
参加反应的硫酸的质量为100g×19.6%=19.6g
题六:
设:合金中锌的质量为x,反应生成硫酸锌的质量为y。
Zn+H SO =ZnSO +H ↑
2 4 4 2
65 98 161
x 19.6g y
65:98=x:19.6g 解得:x=13g
98:161=19.6g:y 解得:y=32.2g
合金中锌的质量分数为 ×100%≈30.3%
所得溶液中溶质的质量分数为 ×100%≈28.6%
答:合金中锌的质量分数为 30.3%;反应后所得溶液中溶质的质量分数为
28.6%。
解析:黄铜中的铜不能与稀硫酸反应,锌能与稀硫酸反应,其中的锌与硫酸
恰好完全反应,根据锌与稀硫酸反应的化学方程式,由硫酸的质量可以计算
锌的质量及生成的硫酸锌的质量,从而可以计算锌的质量分数及反应后所
得溶液中溶质的质量分数。
C
题七:
解析:食盐在20℃时的溶解度是36克,20℃时食盐溶液的质量分数最大值=
×100%≈26.5%,因此,在20℃这个温度下,不可能得到的溶液的
质量分数为30%的溶液。本题应选C。
第 6 页zxxk.com
31.6;72
题八:
解析:根据题意,可知析出2.0克不含结晶水的溶质晶体后所得溶质的质量
分数变为24.0%的溶液为该温度下的饱和溶液,则该溶液在此温度下的溶解
度为s,依据 ×100%≈24%,解得:s=31.6g;设实验中所取的20.0%的
溶液质量为x,x×20%=(x-10.0g-2.0g)×24%,解得x=72g。
(1)二氧化锰的质量为3.25g。
题九:
氯化钾的质量是100g×7.45%=7.45g
设:生成氧气的质量为x。
2KClO 2KCl+3O ↑
3 2
149 96
7.45g x[来源:学*科*网Z*X*X*K]
= 解得:x=4.8g
(2)氯元素的质量为:7.45g× ×100%=3.55g
原混合物中氯元素的质量分数= ×100%≈22.9%
解析:(1)氯酸钾和二氧化锰的固体混合物,加热至不再有气体产生时溶于
水,剩余3.25g固体的成分是二氧化锰,滤液中的溶质为氯化钾,其质量为:
100g×7.45%=7.45g,根据氯化钾的质量求出氧气的质量;(2)氯化钾中氯元
素的质量即为氯酸钾中的氯元素的质量;原混合物的质量应为氯化钾的质
量与氧气的质量,再加上二氧化锰的质量之和。
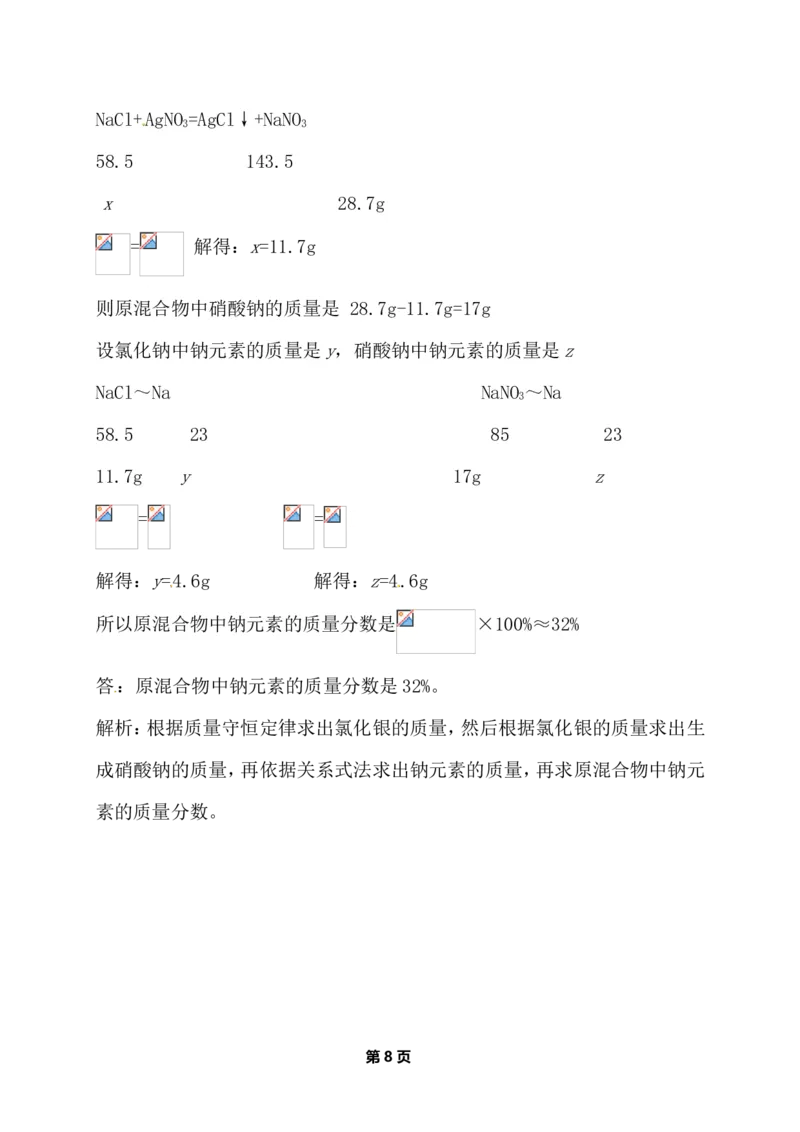
生成沉淀的质量是:(28.7g+100g+134g)-234 g=28.7 g
题十:
设混合物中氯化钠的质量是x 。
第 7 页zxxk.com
NaCl+AgNO =AgCl↓+NaNO
3 3
58.5 143.5
x 28.7g
= 解得:x=11.7g
则原混合物中硝酸钠的质量是 28.7g-11.7g=17g
设氯化钠中钠元素的质量是y,硝酸钠中钠元素的质量是z
NaCl~Na NaNO ~Na
3
58.5 23 85 23
11.7g y 17g z
= = [来源:学|科|网Z|X|X|K]
解得:y=4.6g 解得:z=4.6g
所以原混合物中钠元素的质量分数是 ×100%≈32%
答:原混合物中钠元素的质量分数是32%。
解析:根据质量守恒定律求出氯化银的质量,然后根据氯化银的质量求出生
成硝酸钠的质量,再依据关系式法求出钠元素的质量,再求原混合物中钠元
素的质量分数。
第 8 页