文档内容
zxxk.com
化学计算课后练习
题一: 我国汉代器物和秦俑彩绘用的颜料“汉紫”,直到近来人们才研究出来,其成
分为紫色的硅酸铜钡(钡为+2价;硅为+4价),它的化学式为:BaCuSi O ,则x的值为(
2 x
)
A.3 B.4 C.5 D.6
题二: 在2013年一本中考化学资料的学习工具卡上有常见的化合价记忆口诀,有
一句是“SO 、CO 负二价,NO 、OH负一价,还有NH 正一价”,请问NH 中氮
元素的化合价是( )
A.3 B.+1 C.+3 D.+5
题三: 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示
其中 代表一个碳原子, 代表一个氢原子, 代表一个氧原子。下列说法不正确的是
( )
A.乙酸是一种化合物
B.乙酸的相对分子质量为60
C.乙酸中碳元素的质量分数为60%
D.乙酸分子中的碳原子、氢原子、氧原子的个数比为1∶2∶1
题四: 屠呦呦带领科研团队研发的新型抗疟疾药——青蒿素和双氢青蒿素,在全球抗
击疟疾进程中,拯救了上百万人的生命,因此获得2015年诺贝尔生理或医学奖。青蒿素
化学式为C H O ,下列说法不正确的是( )
15 22 5
A.青蒿素属于有机物
B.青蒿素中C、H、O三种元素的质量比为15:22:5
C.青蒿素中氧元素的质量分数为28.4%
D.利用化学反应提取和合成药物,以抑制细菌和病毒,保障人体健康
0zxxk.com
题五: 随着人们生活水平的提高,小汽车走进了千家万户,车用防冻液“冬天防冻、夏
天防沸、全年防水垢、防腐蚀”的优良性能被爱车族广泛使用,现国际上普遍使用的是
乙二醇[(CH OH) ]水基型防冻液,请回答:
2 2
(1)乙二醇的相对分子质量为 ;
(2)乙二醇中C、H、O元素的质量比为 。
题六: 低钠盐适合患有高血压、肾病、心脏病的患者服用,苹果酸钠盐(C H O Na)是低
4 5 5
钠盐的一种。请回答:
(1)苹果酸钠盐的相对分子质量是 。
(2)苹果酸钠盐中各元素的质量比为C:H:O:Na= 。
(3)若某病人每天食用5.85g苹果酸钠盐,比食用相同质量的食盐(NaCl)少摄入钠元素
多少克?(计算结果保留一位小数)
题七: 偏二甲肼(C H N )与N O 反应放出的能量能把火箭送入太空。该化学方程式为
2 8 2 2 4
C H N + 2N O =2X↑+ 3N ↑+ 4H O↑。下列说法正确的是( )
2 8 2 2 4 2 2
A.X的化学式为CO B.偏二甲肼中碳的质量分数为40%
C.该反应属于分解反应 D.生成N 和H O的质量比为14:9
2 2
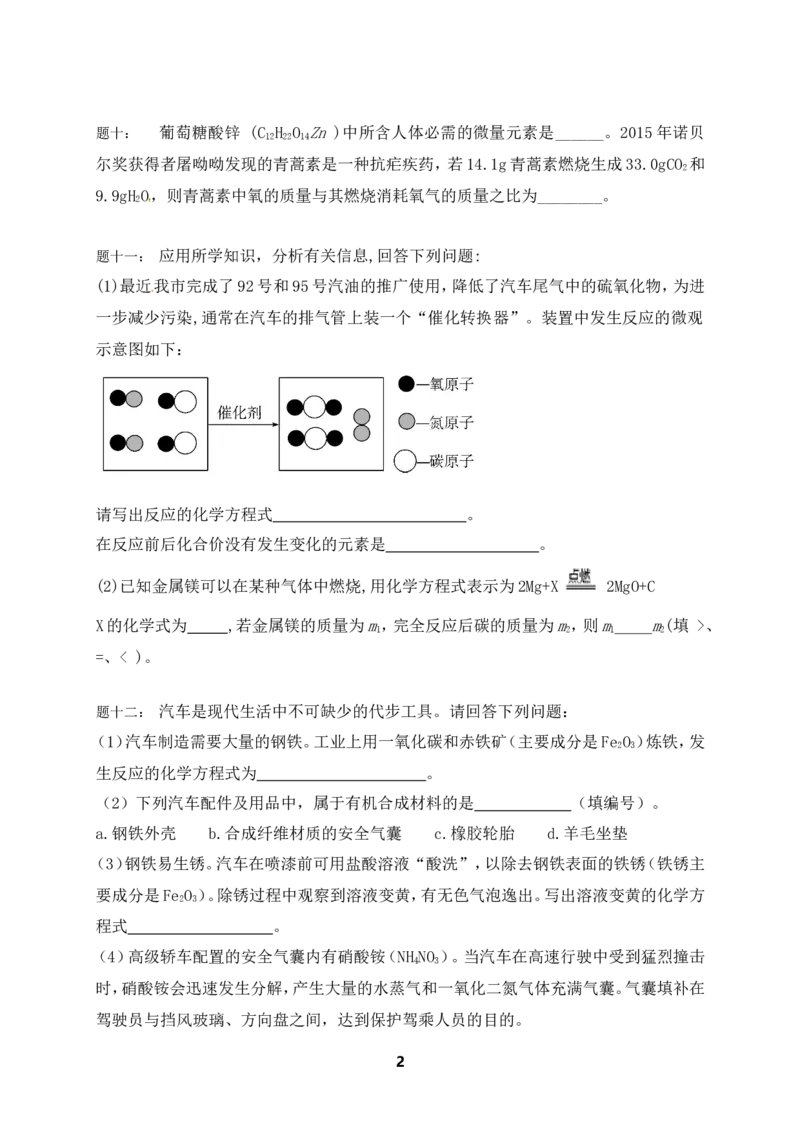
题八: 科学家最新发现,通过简单的化学反应,可以将树木纤维素转变为超级储能装
置,
如图是该反应的微观示意图,下列说法错误的是( )
[来源:学|科|网]
A.参加反应的X,Y两物质的粒子个数之比为3:4
B.该反应不属于置换反应
C.W物质中碳元素的质量分数为75%
D.化学反应前后原子的种类、个数、质量均保持不变
题九: 2.3g某物质在空气中完全燃烧,生成4.4g二氧化碳和2.7g水,则该物质中一
定
含有 元素(填元素符号),其中各元素的质量比为 。
1zxxk.com
[来源:Z.xx.k.Com]
题十: 葡萄糖酸锌 (C H O Zn )中所含人体必需的微量元素是______。2015年诺贝
12 22 14
尔奖获得者屠呦呦发现的青蒿素是一种抗疟疾药,若14.1g青蒿素燃烧生成33.0gCO 和
2
9.9gH O,则青蒿素中氧的质量与其燃烧消耗氧气的质量之比为________。
2
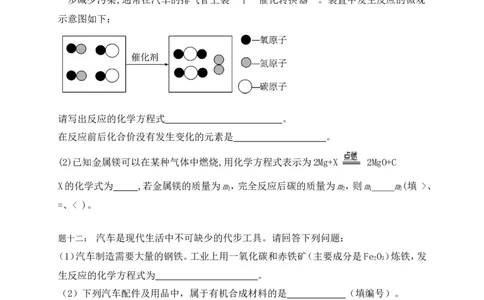
题十一: 应用所学知识,分析有关信息,回答下列问题:
(1)最近我市完成了92号和95号汽油的推广使用,降低了汽车尾气中的硫氧化物,为进
一步减少污染,通常在汽车的排气管上装一个“催化转换器”。装置中发生反应的微观
示意图如下:
请写出反应的化学方程式 。
在反应前后化合价没有发生变化的元素是 。
(2)已知金属镁可以在某种气体中燃烧,用化学方程式表示为2Mg+X 2MgO+C
X的化学式为 ,若金属镁的质量为m,完全反应后碳的质量为m,则m m(填 >、
1 2 1 2
=、< )。
[来源:学科网]
题十二: 汽车是现代生活中不可缺少的代步工具。请回答下列问题:
(1)汽车制造需要大量的钢铁。工业上用一氧化碳和赤铁矿(主要成分是Fe O )炼铁,发
2 3
生反应的化学方程式为 。
(2)下列汽车配件及用品中,属于有机合成材料的是 (填编号)。
a.钢铁外壳 b.合成纤维材质的安全气囊 c.橡胶轮胎 d.羊毛坐垫
(3)钢铁易生锈。汽车在喷漆前可用盐酸溶液“酸洗”,以除去钢铁表面的铁锈(铁锈主
要成分是Fe O )。除锈过程中观察到溶液变黄,有无色气泡逸出。写出溶液变黄的化学方
2 3
程式 。
(4)高级轿车配置的安全气囊内有硝酸铵(NH NO )。当汽车在高速行驶中受到猛烈撞击
4 3
时,硝酸铵会迅速发生分解,产生大量的水蒸气和一氧化二氮气体充满气囊。气囊填补在
驾驶员与挡风玻璃、方向盘之间,达到保护驾乘人员的目的。
2zxxk.com
①已知硝酸铵中铵根离子(NH )的化合价为+1价,则铵根中氮元素的化合价为 。
②写出硝酸铵受撞击发生分解反应的化学方程式 。
(5)酒驾会带来危害。交警在查酒驾时,先请司机打开车窗,若闻到酒精气味,则要求司
机必须接受酒精含量的测试。交警能闻到酒精的气味是因为 。
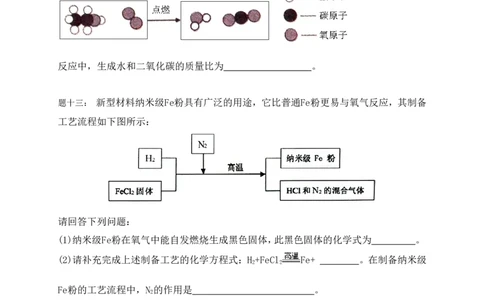
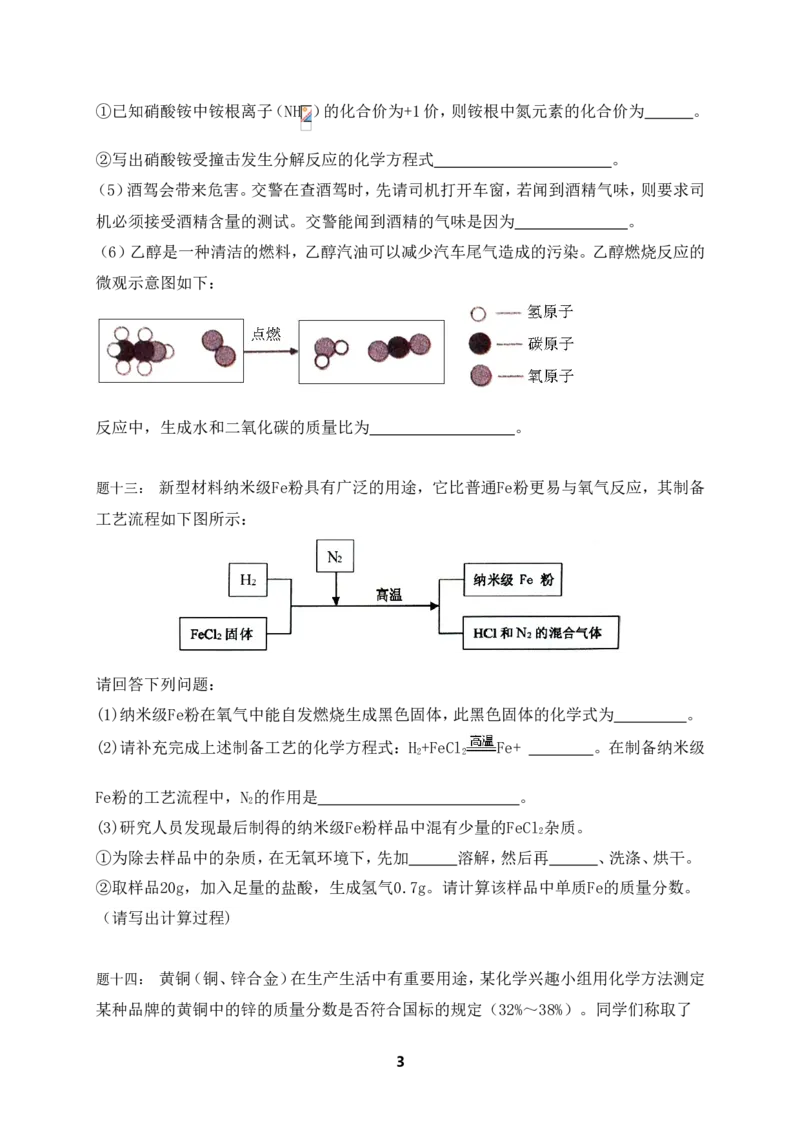
(6)乙醇是一种清洁的燃料,乙醇汽油可以减少汽车尾气造成的污染。乙醇燃烧反应的
微观示意图如下:
反应中,生成水和二氧化碳的质量比为 。
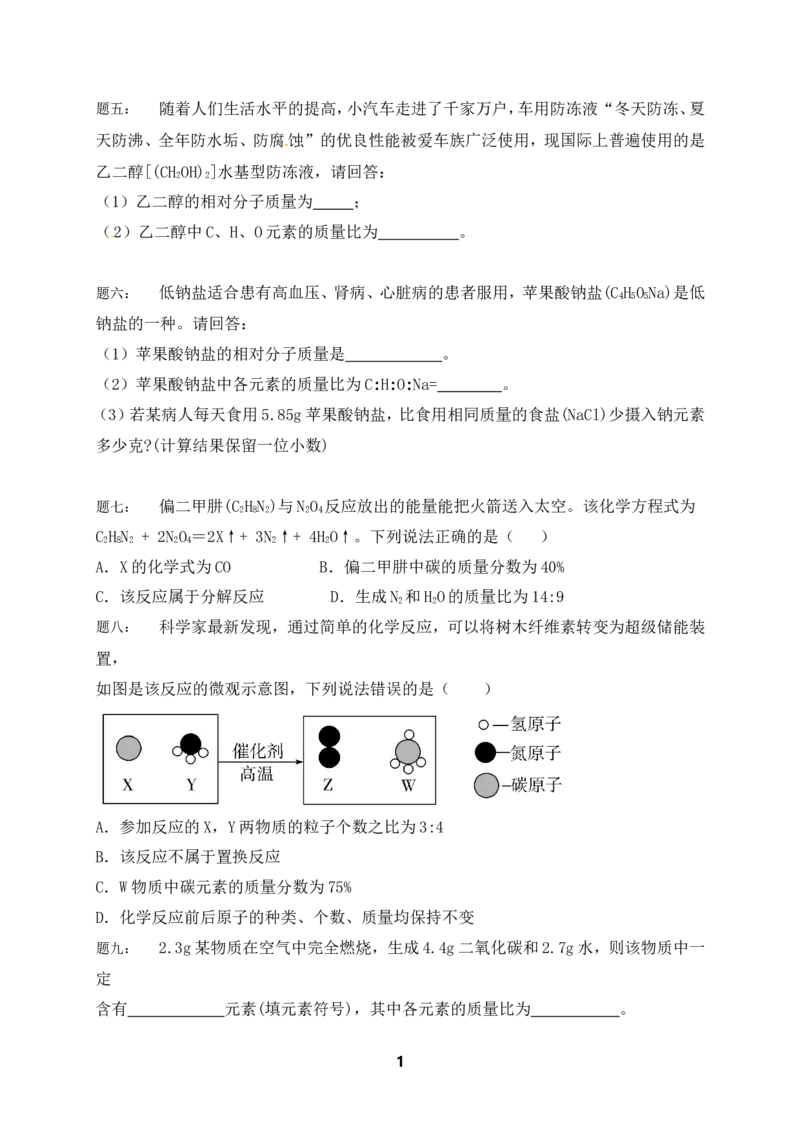
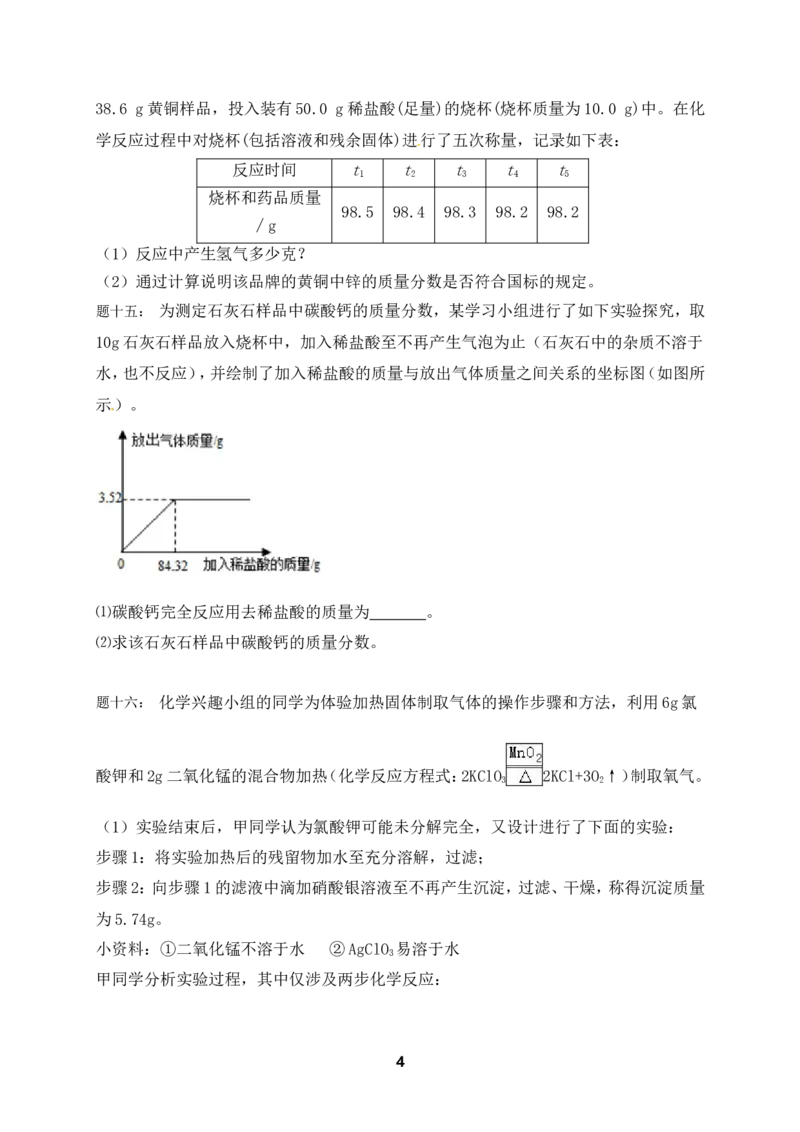
题十三: 新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备
工艺流程如下图所示:
请回答下列问题:
(1)纳米级Fe粉在氧气中能自发燃烧生成黑色固体,此黑色固体的化学式为 。
(2)请补充完成上述制备工艺的化学方程式:H +FeCl Fe+ 。在制备纳米级
2 2
Fe粉的工艺流程中,N 的作用是 。
2
(3)研究人员发现最后制得的纳米级Fe粉样品中混有少量的FeCl 杂质。
2
①为除去样品中的杂质,在无氧环境下,先加 溶解,然后再 、洗涤、烘干。
②取样品20g,加入足量的盐酸,生成氢气0.7g。请计算该样品中单质Fe的质量分数。
(请写出计算过程)
题十四: 黄铜(铜、锌合金)在生产生活中有重要用途,某化学兴趣小组用化学方法测定
某种品牌的黄铜中的锌的质量分数是否符合国标的规定(32%~38%)。同学们称取了
3zxxk.com
38.6 g黄铜样品,投入装有50.0 g稀盐酸(足量)的烧杯(烧杯质量为10.0 g)中。在化
学反应过程中对烧杯(包括溶液和残余固体)进行了五次称量,记录如下表:
反应时间 t t t t t
1 2 3 4 5
烧杯和药品质量
98.5 98.4 98.3 98.2 98.2
∕g
(1)反应中产生氢气多少克?
(2)通过计算说明该品牌的黄铜中锌的质量分数是否符合国标的规定。
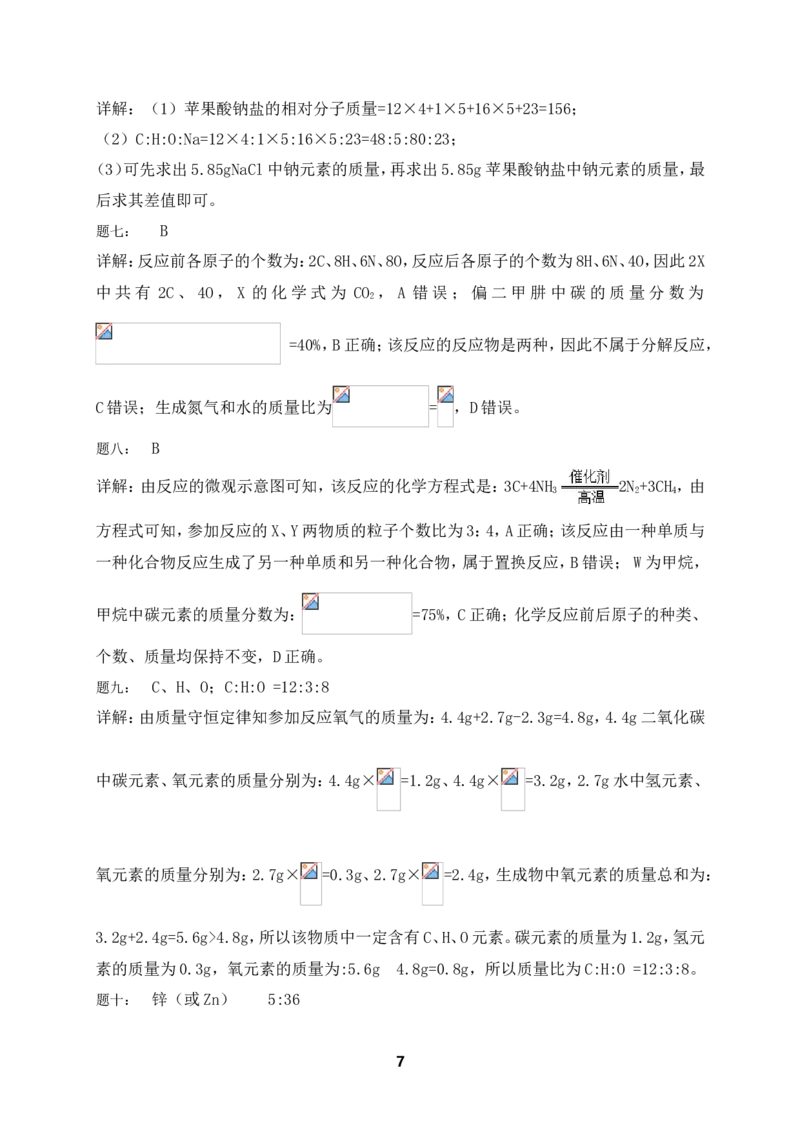
题十五: 为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究,取
10g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于
水,也不反应),并绘制了加入稀盐酸的质量与放出气体质量之间关系的坐标图(如图所
示)。
⑴碳酸钙完全反应用去稀盐酸的质量为 。
⑵求该石灰石样品中碳酸钙的质量分数。
题十六: 化学兴趣小组的同学为体验加热固体制取气体的操作步骤和方法,利用6g氯
酸钾和2g二氧化锰的混合物加热(化学反应方程式:2KClO 2KCl+3O ↑)制取氧气。
3 2
(1)实验结束后,甲同学认为氯酸钾可能未分解完全,又设计进行了下面的实验:
步骤1:将实验加热后的残留物加水至充分溶解,过滤;
步骤2:向步骤1的滤液中滴加硝酸银溶液至不再产生沉淀,过滤、干燥,称得沉淀质量
为5.74g。
小资料:①二氧化锰不溶于水 ②AgClO 易溶于水
3
甲同学分析实验过程,其中仅涉及两步化学反应:
4zxxk.com
2KClO 2KCl+3O ↑ KCl+AgNO ═AgCl↓+KNO
3 2 3 3
推出两反应间存在KClO →KCl→AgCl↓物质转化关系和质量比例关系。
3
请你利用上述关系,通过计算帮甲同学判断KClO 是否完全分解?(要求:简单写出计算
3
过程、说明判断依据,计算结果精确到0.1)
(2)乙同学对甲同学的方案提出质疑:认为通过称量加热后残留物质量,利用加热前后
质量差进行计算,同样可以达到甲同学的实验目的。你赞同乙同学的观点吗?说明理由:
; 。
5zxxk.com
化学计算
课后练习参考答案
题一: D
详解:铜元素在化合物中的化合价为+2价、氧元素为2价、钡元素为+2价、硅元素为+4
价,依据化合物中各元素正负化合价的代数和为零的规律可列式得:
(+2)+ (+2)+ (+4)×2+(2)x = 0,可解得x = 6。本题应选D。
题二: A
详解:氢元素化合价为+1价,由于铵根为+1价,设氮元素化合价为x,可列式得:
x+ (+1)×4 = +1,解得x = 3。
题三: C
详解:由乙酸的分子模型图可得出乙酸的化学式为C H O ,因此乙酸是由C、H、O三种元
2 4 2
素组成的化合物,A正确;乙酸的相对分子质量为:12×2+1×4+16×2=60,B正确;乙酸
中碳元素的质量分数是:(12×2)÷60×100%=40%,C错误;乙酸分子中的碳原子、氢原子、
氧原子的个数比为2∶4∶2 =1∶2∶1,D正确。
题四: B
详解:青蒿素是一种含碳元素的化合物,属于有机物,A项说法正确;青蒿素中碳、氢、氧
三种元素的质量比为:(12×15):(1×22):(16×5)=90:11:40,B项说法错误;青蒿素中
氧元素的质量分数为 ×100%≈28.4%,C项说法正确;化学的重要用
途之一是利用化学反应提取和合成药物,以抑制细菌和病毒,保障人体健康,D项说法正
确。
题五: (1)62 (2)12:3:16
详解:(1)相对分子质量为构成分子的各原子的相对原子质量之和,则乙二醇[(CH OH) ]
2 2
的相对分子质量为:(12+1×3+16)×2=62;
(2)化合物中各元素质量比=各原子的相对原子质量×原子个数之比,则乙二醇中碳、氢、
氧元素的质量比为(12×2):(1×3×2):(16×2)=12:3:16。
题六: (1)156 (2)48:5:80:23
(3)5.85gNaCl中钠元素的质量为5.85g×(23/58.5)×l00%=2.3g
5.85gC H O Na中钠元素的质量为5.85g×(23/156)×100%≈0.86g
4 5 5
5.85gNaCl比等质量的C H O Na多的钠元素的质量为2.3g0.86g≈1.4g
4 5 5
答:该病人每天食用5.85g苹果酸钠盐比食用相同质量的NaCl少摄入钠元素1.4g。
6zxxk.com
详解:(1)苹果酸钠盐的相对分子质量=12×4+1×5+16×5+23=156;
(2)C:H:O:Na=12×4:1×5:16×5:23=48:5:80:23;
(3)可先求出5.85gNaCl中钠元素的质量,再求出5.85g苹果酸钠盐中钠元素的质量,最
后求其差值即可。
题七: B
详解:反应前各原子的个数为:2C、8H、6N、8O,反应后各原子的个数为8H、6N、4O,因此2X
中共有 2C、4O,X 的化学式为 CO ,A 错误;偏二甲肼中碳的质量分数为
2
=40%,B正确;该反应的反应物是两种,因此不属于分解反应,
C错误;生成氮气和水的质量比为 = ,D错误。
题八: B
详解:由反应的微观示意图可知,该反应的化学方程式是:3C+4NH 2N +3CH ,由
3 2 4
方程式可知,参加反应的X、Y两物质的粒子个数比为3:4,A正确;该反应由一种单质与
一种化合物反应生成了另一种单质和另一种化合物,属于置换反应,B错误; W为甲烷,
甲烷中碳元素的质量分数为: =75%,C正确;化学反应前后原子的种类、
个数、质量均保持不变,D正确。
题九: C、H、O;C:H:O =12:3:8
详解:由质量守恒定律知参加反应氧气的质量为:4.4g+2.7g-2.3g=4.8g,4.4g二氧化碳
中碳元素、氧元素的质量分别为:4.4g× =1.2g、4.4g× =3.2g,2.7g水中氢元素、
氧元素的质量分别为:2.7g× =0.3g、2.7g× =2.4g,生成物中氧元素的质量总和为:
3.2g+2.4g=5.6g>4.8g,所以该物质中一定含有C、H、O元素。碳元素的质量为1.2g,氢元
素的质量为0.3g,氧元素的质量为:5.6g4.8g=0.8g,所以质量比为C:H:O =12:3:8。
题十: 锌(或Zn) 5:36
7zxxk.com
详解:C、H、O 属于人体中的常量元素,锌属于人体中的微量元素;根据反应前后元素的
质量不变可知青蒿素中碳的质量即二氧化碳中碳的质量,青蒿素中氢的质量即水中氢的
质量,碳的质量为33.0g =9g,氢的质量为9.9g× ,青蒿素中氧的质量为:
14.1g9g1.1g=4g,参加反应的氧气的质量为33g+9.9g14.1g=28.8g,青蒿素中氧
的质量与消耗氧气的质量之比为4:28.8=5:36。
题十一: (1)2CO+2NO 2CO +N ;氧元素 (2)CO ;>
2 2 2
详解:(1)由题图中反应的微观示意图可知,一氧化碳和一氧化氮在催化剂的作用下生成
二氧化碳和氮气,反应的化学方程式为:2CO+2NO 2CO +N ;反应中碳的化合价由一
2 2
氧化碳中的+2价变成了二氧化碳中的+4价,氮元素由一氧化氮中的+2价变成了氮气中
的零价,只有氧元素的化合价在反应前后没有发生变化(仍为2价);
(2)依据质量守恒定律:化学反应前后原子的种类、数目均不变,可推断反应物X的化学
式为CO ,化学方程式中金属镁与碳的质量比为48:12(即每48份质量的镁会生成12份
2
质量的碳),所以金属镁的质量(m)大于完全反应后生成碳的质量(m)。
1 2
题十二: (1)Fe O +3CO 2Fe+3CO (2)bc (3)Fe O +6HCl=2FeCl +3H O
2 3 2 2 3 3 2
(4)①3 ②NH NO N O↑+2H O↑ (5)分子在不断运动 (6)27:44
4 3 2 2
详解:(1)在高温条件下,一氧化碳能和氧化铁反应生成铁和二氧化碳,由此写出反应的
化学方程式;
(2)钢铁属于金属材料,合成纤维、合成橡胶属于有机合成材料,羊毛属于天然有机材料,
故选bc;
(3)铁锈的主要成分氧化铁能和盐酸反应生成黄色的氯化铁溶液和水,铁锈除去后,露
出的铁继续和盐酸反应生成氯化亚铁和氢气,本题要求写出溶液变黄的化学方程式,因
此写出第一个反应的化学方程式即可;
(4)①铵根中氢元素的化合价为+1价,设铵根中氮元素的化合价为x,则x+(+1) 4=+1,
解得x= 3;②根据提供的信息可知硝酸铵撞击后会生成水和一氧化二氮,根据一写、
二配、三注的步骤即可写出反应的化学方程式;
(5)闻到气味是因为分子在不断运动;
8zxxk.com
(6)由反应微观示意图可得乙醇燃烧的化学方程式:C H OH+3O 3H O+2CO ,
2 5 2 2 2
反应中生成水和二氧化碳的质量比为: = 。
题十三: (1)Fe O (2)2HCl;防止纳米级铁粉被氧化(3)①水;过滤
3 4
②设样品中铁的质量为x。
Fe+2HCl=FeCl +H ↑
2 2
56 2
x 0.7g
56:2=x:0.7g 解得:x=19.6g
样品中单质铁的质量分数为(19.6g/20g)×100%=98%
答:样品中单质铁的质量分数为98%。
详解:(1)铁粉燃烧生成的黑色固体是Fe O ;(2)根据化学反应前后原子种类和数目不变,
3 4
可知化学方程式中在空格应填写“2HCl”,氮气的化学性质稳定,可用作保护气,隔绝氧
气以防止纳米级铁粉被氧化;(3)FeCl 溶于水,Fe粉不溶于水,所以用先加水溶解,然后
2
再过滤的方法除去混在Fe粉中的FeCl ,再经洗涤、烘干可得到Fe粉;根据铁粉与盐酸
2
反应的化学方程式,利用铁与氢气的质量关系,根据氢气的质量可以计算出参加反应铁
的质量,进一步计算出样品中单质铁的质量分数。
题十四: (1)0.4
(2)设38.6 g黄铜样品中含锌的质量为x
Zn + 2HCl = ZnCl + H ↑
2 2
65 2
[来源:学*科*网]
x 0.4 g
= 解得:x = 13 g
该品牌的黄铜中锌的质量分数是: ×100%≈33.7 %,介于国标规定的32%~38 %
之间,说明该品牌的黄铜中锌的质量分数符合国标的规定。
答:该品牌的黄铜中的锌的质量分数为33.7%,符合国标的规定。
详解:通过分析题中数据和表格中的数据,根据反应前后烧杯和药品总质量的变化得出
反应产生氢气的质量是解题的关键。根据化学方程式中锌与氢气的质量关系计算出参加
反应的锌的质量,进一步计算出黄铜中锌的质量分数,以判断是否符合国标规定。
9zxxk.com
题十五: ⑴84.32g
⑵设10g石灰石样品中碳酸钙的质量为x
CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
100 44
x 3.52g
100:x=44:3.52g
解得:x=8g
[来源:Zxxk.Com]
该石灰石样品中碳酸钙的质量分数为 8g/10g×100%=80%。
答:该石灰石样品中碳酸钙的质量分数为80%。
详解:当产生的气体不再增多,说明样品中的碳酸钙已完全反应,根据图像可知,恰好生
成最多量气体时消耗盐酸的质量为84.32g,最多得到气体的质量为3.52g。根据气体
的质量可计算样品中碳酸钙的质量,进而计算样品中碳酸钙的质量分数。
题十六: (1)由反应的化学方程式2KClO 2KCl+3O ↑、KCl+AgNO ═AgCl↓+KNO ,
3 2 3 3
推出两反应间存在的关系为:2KClO ~2KCl~2AgCl,即KClO ~KCl~AgCl,它们的质量
3 3
关系为122.5:74.5:143.5,
设参加反应的氯酸钾的质量为x。
KClO ~KCl~AgCl
3
122.5 143.5
x 5.74g
,解得:x=4.9g
6g>4.9g,故KClO 没有完全分解。
3
(2)赞同;由质量守恒定律,固体混合物减少的质量即为生成氧气的质量,由反应的化学
方程式计算出参加反应的氯酸钾的质量,进一步判断氯酸钾是否完全分解
详解:(1)由反应的化学方程式,找出KClO →KCl→AgCl↓等物质的转化关系和质量比,
3
根据生成沉淀的质量,计算出参加反应的氯酸钾的质量,进一步判断KClO 是否完全分
3
解;(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,通过称量加热前后物质的
质量变化,所得质量差即为反应生成氧气的质量,由反应的化学方程式可计算出参加反
应的氯酸钾的质量,进一步判断氯酸钾是否完全分解。
10zxxk.com
11