文档内容
2023-2024 学年上海市黄浦区九年级(上)期末化学试卷(一模)
参考答案与试题解析
一、选择题(共20分)
1.(1分)氦是第一种在地球之外的宇宙中被发现的元素,其元素符号是( )
A.Ag B.He C.Hg D.Ne
【答案】B
【分析】利用元素符号的书写规则和对应的元素名称进行分析。
【解答】解:A.Ag表示银元素,故A错误;
B.He表示氦元素,故B正确;
C.Hg表示汞元素,故C错误;
D.Ne表示氖元素,故D错误;
故选:B。
【点评】考查学生对元素符号的识记,难度较小。
2.(1分)摆放在超市货架上的商品属于溶液的是( )
A.豆浆 B.矿泉水 C.牛奶 D.酸奶
【答案】B
【分析】利用溶液的特征是均一的、稳定的混合物分析。
【解答】解:A.豆浆是不均一、不稳定的,放置一段时间后会分层,故A错误;
B.矿泉水中含有可溶于水的矿物质,是均一的、稳定的混合物,故B正确;
C.牛奶是不均一、不稳定的液体,属于乳浊液,故C错误;
D.酸奶不是均一的、稳定的混合物,属于乳浊液,故D错误;
故选:B。
【点评】考查学生对溶液概念的理解,难度小。
3.(1分)空气里含量最多的气体是( )
A.CO B.O C.N D.H O
2 2 2 2
【答案】C
【分析】空气中各成分的体积分数分别是:氮气大约占空气体积的78%、氧气大约占空气
体积的21%、稀有气体大约占空气体积的0.94%、二氧化碳大约占空气体积的0.03%、水
蒸气和其它气体和杂质大约占0.03%。
【解答】解:A、二氧化碳大约占空气体积的0.03%,故选项错误;
第1页(共15页)B、氧气大约占空气体积的21%,故选项错误;
C、氮气大约占空气体积的78%,含量最多;故选项正确;
D、水蒸气和其它气体和杂质大约占0.03%,故选项错误;
故选:C。
【点评】本考点考查了空气中各种气体的含量,同学们要加强记忆有关的知识点,在理解
的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中。
4.(1分)某水库中氮、磷含量升高,其中的“氮”“磷”指的是( )
A.分子 B.原子 C.元素 D.单质
【答案】C
【分析】食品、药品、营养品、水库中的水等物质中的“氮、磷”等不是以单质、分子、原子、
离子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【解答】解:这里的“氮、磷”等不是以单质、分子、原子、离子等形式存在,这里所指的
“氮、磷”是强调存在的元素,与具体形态无关;
故选:C。
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解
是正确解答此类试题的关键。
5.(1分)净水机中加入活性炭,主要是利用活性炭的( )
A.难溶于水 B.稳定性 C.还原性 D.吸附性
【答案】D
【分析】根据活性炭具有吸附作用,能够吸附色素和异味进行解答。
【解答】解:活性炭具有吸附作用,能够吸附水中的色素和异味,所以活性炭可以净化饮用
水,因此利用了活性炭的吸附性。
故选:D。
【点评】本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用
途是由物质的哪种性质决定的。
6.(1分)物质的命名正确的是( )
A.NaHCO 碳酸钠 B.K S 硫酸钾
3 2
C.Al O 氧化铝 D.SiO 二氧化硫
2 3 2
【答案】C
【分析】根据由两种元素组成的化合物,读作“某化某”进行分析。
【解答】解:A、NaHCO 为碳酸氢钠,而不是碳酸钠,故A不正确;
3
第2页(共15页)B、由两种元素组成的化合物,读作“某化某”,则K S为硫化钾,故B不正确;
2
C、Al O 读作氧化铝,故C正确;
2 3
D、SiO 为二氧化硅,而不是二氧化硫,故D不正确。
2
故选:C。
【点评】本题主要考查化学式的名称等,注意完成此题,可以从题干中抽取有用的信息,结
合已有的知识进行解题。
7.(1分)红磷在氧气中燃烧的现象描述正确的是( )
A.产生蓝光 B.火星四射
C.生成黑色固体 D.产生浓厚白烟
【答案】D
【分析】根据红磷在氧气中燃烧的现象,进行分析判断。
【解答】解:红磷在氧气中燃烧,产生大量的白烟,生成一种白色固体。
故选:D。
【点评】本题难度不大,了解常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象
时,需要注意烟和雾的区别。
8.(1分)以下含有结晶水的物质是( )
A.食盐 B.胆矾 C.冰 D.干冰
【答案】B
【分析】根据含有结晶水的化合物属于结晶水合物,进行分析判断。
【解答】解:A、食盐不含结晶水,不属于结晶水合物,故A错误;
B、胆矾是五水合硫酸铜的俗称,属于结晶水合物,故B正确;
C、冰是固态的水,本身是水,不属于结晶水合物,故C错误;
D、干冰是固态的二氧化碳,不含结晶水,不属于结晶水合物,故D错误;
故选:B。
【点评】本题难度不大,明确含有结晶水的化合物属于结晶水合物是正确解答本题的关键。
9.(1分)某混合溶液中含两种固体溶质,可采取降温结晶的方法提纯其中一种含量较多的物
质,该方法是利用了两种物质具有不同的( )
A.溶解度变化趋势 B.熔点
C.密度 D.式量
【答案】A
【分析】根据物质的溶解度受温度的影响情况进行分析。
第3页(共15页)【解答】解:某混合溶液中含两种固体溶质,可采取降温结晶的方法提纯其中一种含量较
多的物质,该方法是利用了两种物质具有不同的溶解度变化趋势。
故选:A。
【点评】此题难度不大,掌握物质的溶解度受温度的影响情况等即可顺利解答。
10.(1分)3SO 和3SO 含有相同的( )
2 3
A.分子个数 B.式量
C.氧原子个数 D.物质质量
【答案】A
【分析】A、根据化学式前面数字的含义,进行分析解答;
B、根据式量为构成分子的各原子的相对原子质量之和,进行分析解答;
C、根据化学式的含义,进行分析解答;
D、根据物质的质量比=分子的式量×分子个数之比,进行分析解答;
【解答】解:A、3SO 表示3个二氧化硫分子,3SO 表示3个三氧化硫分子,因此它们的分
2 3
子个数相等,故选项符合题意;
B、3SO 的式量之和为3×(32+16×2)=192,3SO 的式量之和为3×(32+16×3)=240,因此
2 3
它们的式量不相等,故选项不符合题意;
C、分子由原子构成,在3SO 中含有6个氧原子,3SO 中含有9个氧原子,因此它们的氧
2 3
原子的个数不相等,故选项不符合题意;
D、3SO 与3SO 的质量比为[3×(32+16×2)]:[3×(32+16×3)]=4:5,因此它们的物质质量
2 3
不相等,故选项不符合题意。
故选:A。
【点评】明确物质是由分子构成的,分子是由原子构成的。
11.(1分)判断某溶液呈酸性的方法可行的是( )
A.闻气味,有无刺激性
B.根据溶质的组成中是否含有氢元素
C.滴加石蕊溶液,观察溶液颜色变化
D.滴加酚酞溶液,观察溶液颜色变化
【答案】C
【分析】根据判断溶液成酸性的方法分析,酸性溶液中含有大量的氢离子,能使紫色石蕊
试液变红,不能使无色酚酞试液变色。
【解答】解:A、闻气味,有无刺激性,不能判断溶液呈酸性,故错误;
第4页(共15页)B、根据溶质的组成中是否含有氢元素,不能判断溶液呈酸性,故错误;
C、酸性溶液中含有大量的氢离子,能使紫色石蕊试液变红,因此滴加石蕊溶液,观察溶液
颜色变化能判断溶液呈酸性,故正确;
D、酸性溶液中含有大量的氢离子,不能使无色酚酞试液变色,因此滴加酚酞溶液不能判
断溶液呈酸性,故错误。
故选:C。
【点评】此题难度不大,掌握判断溶液酸碱性的方法等即可顺利解答。
12.(1分)有关氧化物说法错误的是( )
A.属于纯净物
B.均能用于实验室制取氧气
C.含有两种元素
D.状态可能是固态、液态或气态
【答案】B
【分析】根据纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质,纯净物
分为单质和化合物以及氧化物的概念分析。
【解答】解:氧化物是由两种元素组成,其中一种是氧元素的化合物;
A、氧化物是由两种元素组成,其中一种是氧元素的化合物,属于纯净物,正确;
B、氧化物不一定能用于实验室制取氧气,如:二氧化碳,错误;
C、氧化物一定含有两种元素,正确;
D、状态可能是固态、液态或气态,如氧化铜为固体,水为液体,二氧化碳为气体;正确;
故选:B。
【点评】本题难度不大,掌握纯氧化物的概念即可正确解答本题。
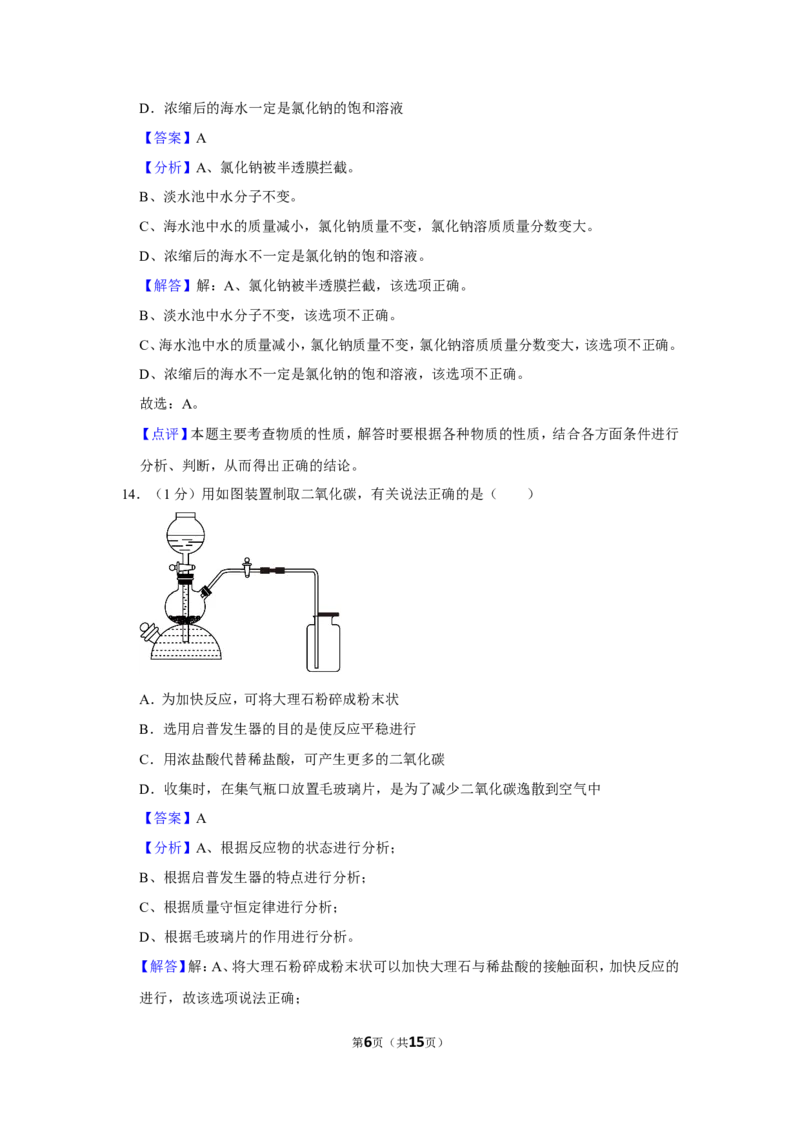
13.(1分)对海水加压,水分子通过半透膜进入淡水池,得到淡水的过程如图所示。加压一段
时间后,海水池中没有晶体析出,有关说法正确的是( )
A.氯化钠被半透膜拦截
B.淡水池中水分子变大
C.海水池中氯化钠溶质质量分数不变
第5页(共15页)D.浓缩后的海水一定是氯化钠的饱和溶液
【答案】A
【分析】A、氯化钠被半透膜拦截。
B、淡水池中水分子不变。
C、海水池中水的质量减小,氯化钠质量不变,氯化钠溶质质量分数变大。
D、浓缩后的海水不一定是氯化钠的饱和溶液。
【解答】解:A、氯化钠被半透膜拦截,该选项正确。
B、淡水池中水分子不变,该选项不正确。
C、海水池中水的质量减小,氯化钠质量不变,氯化钠溶质质量分数变大,该选项不正确。
D、浓缩后的海水不一定是氯化钠的饱和溶液,该选项不正确。
故选:A。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
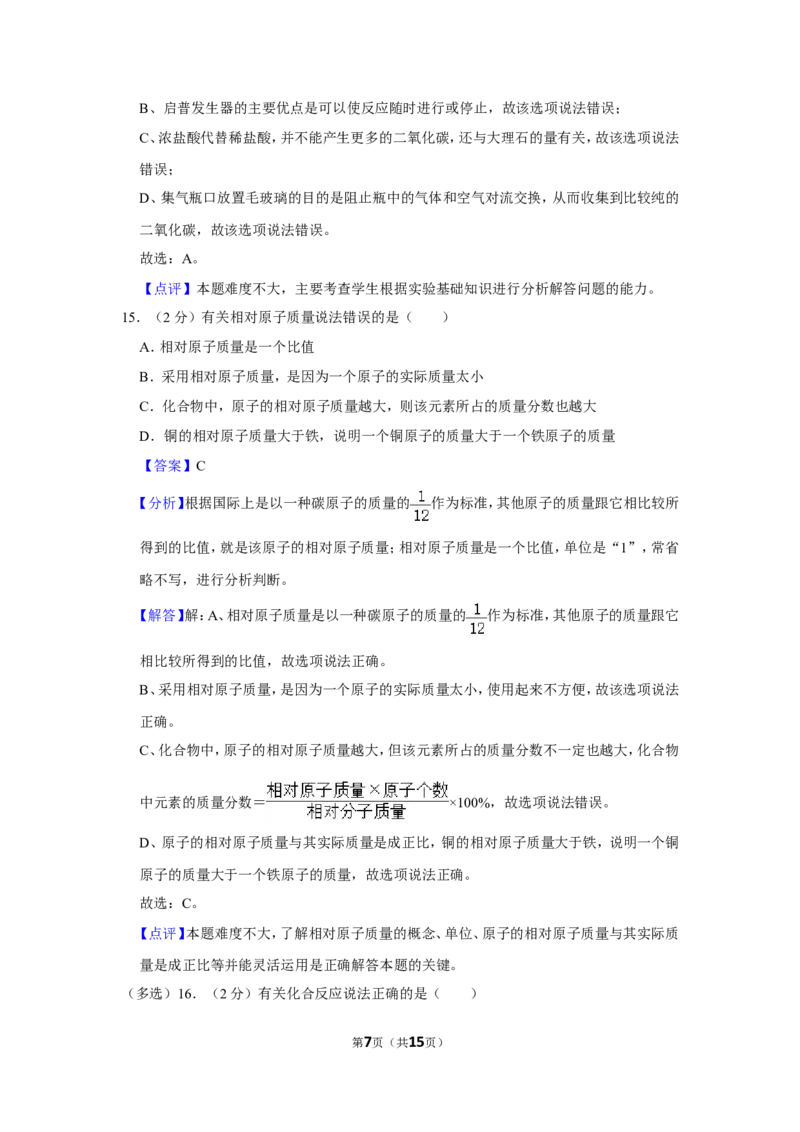
14.(1分)用如图装置制取二氧化碳,有关说法正确的是( )
A.为加快反应,可将大理石粉碎成粉末状
B.选用启普发生器的目的是使反应平稳进行
C.用浓盐酸代替稀盐酸,可产生更多的二氧化碳
D.收集时,在集气瓶口放置毛玻璃片,是为了减少二氧化碳逸散到空气中
【答案】A
【分析】A、根据反应物的状态进行分析;
B、根据启普发生器的特点进行分析;
C、根据质量守恒定律进行分析;
D、根据毛玻璃片的作用进行分析。
【解答】解:A、将大理石粉碎成粉末状可以加快大理石与稀盐酸的接触面积,加快反应的
进行,故该选项说法正确;
第6页(共15页)B、启普发生器的主要优点是可以使反应随时进行或停止,故该选项说法错误;
C、浓盐酸代替稀盐酸,并不能产生更多的二氧化碳,还与大理石的量有关,故该选项说法
错误;
D、集气瓶口放置毛玻璃的目的是阻止瓶中的气体和空气对流交换,从而收集到比较纯的
二氧化碳,故该选项说法错误。
故选:A。
【点评】本题难度不大,主要考查学生根据实验基础知识进行分析解答问题的能力。
15.(2分)有关相对原子质量说法错误的是( )
A.相对原子质量是一个比值
B.采用相对原子质量,是因为一个原子的实际质量太小
C.化合物中,原子的相对原子质量越大,则该元素所占的质量分数也越大
D.铜的相对原子质量大于铁,说明一个铜原子的质量大于一个铁原子的质量
【答案】C
【分析】根据国际上是以一种碳原子的质量的 作为标准,其他原子的质量跟它相比较所
得到的比值,就是该原子的相对原子质量;相对原子质量是一个比值,单位是“1”,常省
略不写,进行分析判断。
【解答】解:A、相对原子质量是以一种碳原子的质量的 作为标准,其他原子的质量跟它
相比较所得到的比值,故选项说法正确。
B、采用相对原子质量,是因为一个原子的实际质量太小,使用起来不方便,故该选项说法
正确。
C、化合物中,原子的相对原子质量越大,但该元素所占的质量分数不一定也越大,化合物
中元素的质量分数= ×100%,故选项说法错误。
D、原子的相对原子质量与其实际质量是成正比,铜的相对原子质量大于铁,说明一个铜
原子的质量大于一个铁原子的质量,故选项说法正确。
故选:C。
【点评】本题难度不大,了解相对原子质量的概念、单位、原子的相对原子质量与其实际质
量是成正比等并能灵活运用是正确解答本题的关键。
(多选)16.(2分)有关化合反应说法正确的是( )
第7页(共15页)A.反应物中的元素均以化合态存在
B.能证明各反应物的元素组成情况
C.生成物中各元素化合价的代数和等于零
D.生成物中的元素全部来自于反应物
【答案】CD
【分析】根据化合反应是由两种或两种以上物质生成一种物质的反应,其特点可总结为
“多变一”,进行分析判断。
【解答】解:A、化合反应是由两种或两种以上物质生成一种物质的反应,反应物中的元素
不一定均以化合态存在,如氢气在氧气中燃烧生成水,反应物均以游离态存在,故选项说
法错误。
B、化合反应是由两种或两种以上物质生成一种物质的反应,不能证明各反应物的元素组
成情况,故选项说法错误。
C、化合反应是由两种或两种以上物质生成一种物质的反应,生成物只有一种,生成物中
各元素化合价的代数和等于零,故选项说法正确。
D、化合反应是由两种或两种以上物质生成一种物质的反应,由质量守恒定律,反应前后
元素种类不变,生成物中的元素全部来自于反应物,故选项说法正确。
故选:CD。
【点评】本题难度不大,了解化合反应的特征(“多变一”)并能灵活运用是正确解答本题
的关键。
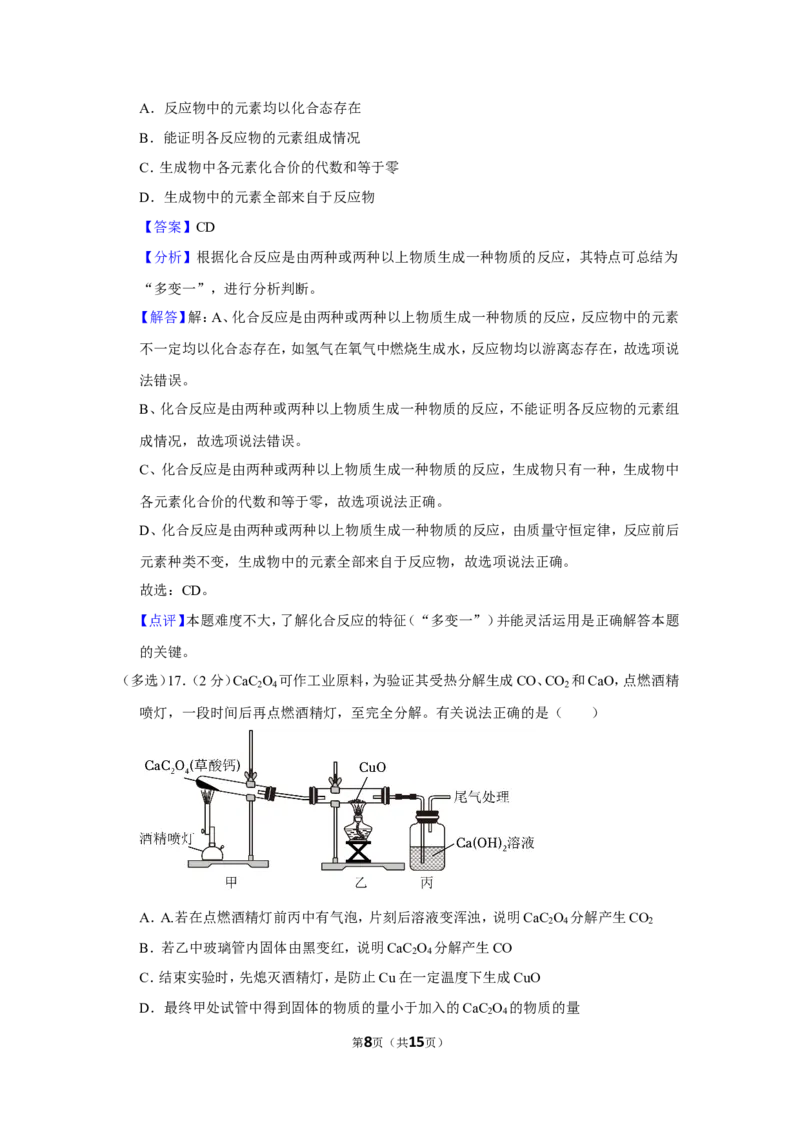
(多选)17.(2分)CaC O 可作工业原料,为验证其受热分解生成CO、CO 和CaO,点燃酒精
2 4 2
喷灯,一段时间后再点燃酒精灯,至完全分解。有关说法正确的是( )
A.A.若在点燃酒精灯前丙中有气泡,片刻后溶液变浑浊,说明CaC O 分解产生CO
2 4 2
B.若乙中玻璃管内固体由黑变红,说明CaC O 分解产生CO
2 4
C.结束实验时,先熄灭酒精灯,是防止Cu在一定温度下生成CuO
D.最终甲处试管中得到固体的物质的量小于加入的CaC O 的物质的量
2 4
第8页(共15页)【答案】AB
【分析】加热时一氧化碳和氧化铜反应生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑
浊。
【解答】解:A、若在点燃酒精灯前丙中有气泡,片刻后溶液变浑浊,说明CaC O 分解产生
2 4
CO ,该选项正确。
2
B、若乙中玻璃管内固体由黑变红,说明CaC O 分解产生CO,是因为加热时一氧化碳和
2 4
氧化铜反应生成铜和二氧化碳,该选项正确。
C、结束实验时,先熄灭酒精灯,是防止Cu在一定温度下生成CuO,同时防止液体倒吸炸
裂玻璃管,该选项不正确。
D、最终甲处试管中得到固体的物质的量等于加入的CaC O 的物质的量,是因为醋酸钙
2 4
和氧化钙的每个“分子”中含有的钙原子个数相等,该选项不正确。
故选:AB。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
二、简答题。
18.(6分)某注射液含葡萄糖(C H O )和氯化钠,可补充病患所需的糖分等,标签如表所示。
6 12 6
①葡萄糖属于 纯净物 (选填“混合物”或“纯净物”)。葡萄糖分子中C、H、O原子
的物质的量之比是 1 : 2 : 1 。我国科学家以二氧化碳等物质为原料制得葡萄糖,该过
程属于 化学变化 (选填“物理变化”或“化学变化”)。
②氯化钠中氯元素的化合价为 ﹣ 1 或﹣ 1 价 。医生建议小明每日氯化钠摄入量不超
过6g,若小明一天摄入了0.1mol氯化钠,请判断是否超标并说明理由 不超标,理由是
0.1mol 氯化钠的质量为 5.85g 。
③实验室模拟配制100mL该注射液(密度约为1g/cm3),请将实验步骤补充完整:称取
0.9 g氯化钠于200mL烧杯中、 量取 99.1mL 水倒入烧杯中 、搅拌至完全溶解后转移
入细口瓶。
【答案】①纯净物;1:2:1;化学变化;
第9页(共15页)②﹣1或﹣1价;不超标,理由是0.1mol氯化钠的质量为5.85g;
③0.9;量取99.1mL水倒入烧杯中。
【分析】①根据纯净物和混合物的概念、物质的量以及变化过程中是否有新物质生成,进
行分析解答;
②根据化合物中正负化合价的代数和为0以及物质的量的计算,进行分析解答;
③根据一定溶质质量分数的溶液的配制步骤,进行分析解答。
【解答】解:①葡萄糖是由一种物质组成,属于纯净物;一个葡萄糖分子中含有6个碳原子、
12个氢原子和6个氧原子,则葡萄糖分子中C、H、O原子的物质的量之比为6:12:6=1:
2:1;以二氧化碳等物质为原料制得葡萄糖,此过程中有新物质生成,属于化学变化;故答
案为:纯净物;1:2:1;化学变化;
②氯化钠中钠元素的化合价为+1价,则氯元素的化合价为﹣1价;氯化钠的摩尔质量为
58.5g/mol,所以0.1mol 氯化钠的质量=0.1mol×58.5g/mol=5.85g<6g,因此小明一天摄
入的氯化钠不超标;故答案为:﹣1或﹣1价;不超标,理由是0.1mol氯化钠的质量为
5.85g;
③ 100mL 该注射液中氯化钠质量为 100mL×1g/cm3×0.9%=0.9g,需要水的质量为
100mL×1g/cm3﹣0.9g=99.1g(合99.1mL);配制过程中称取0.9g氯化钠于200mL烧杯中、
量取99.1mL水倒入烧杯中、搅拌至完全溶解后转移入细口瓶;故答案为:0.9;量取
99.1mL水倒入烧杯中。
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行
分析问题、解决问题的能力。
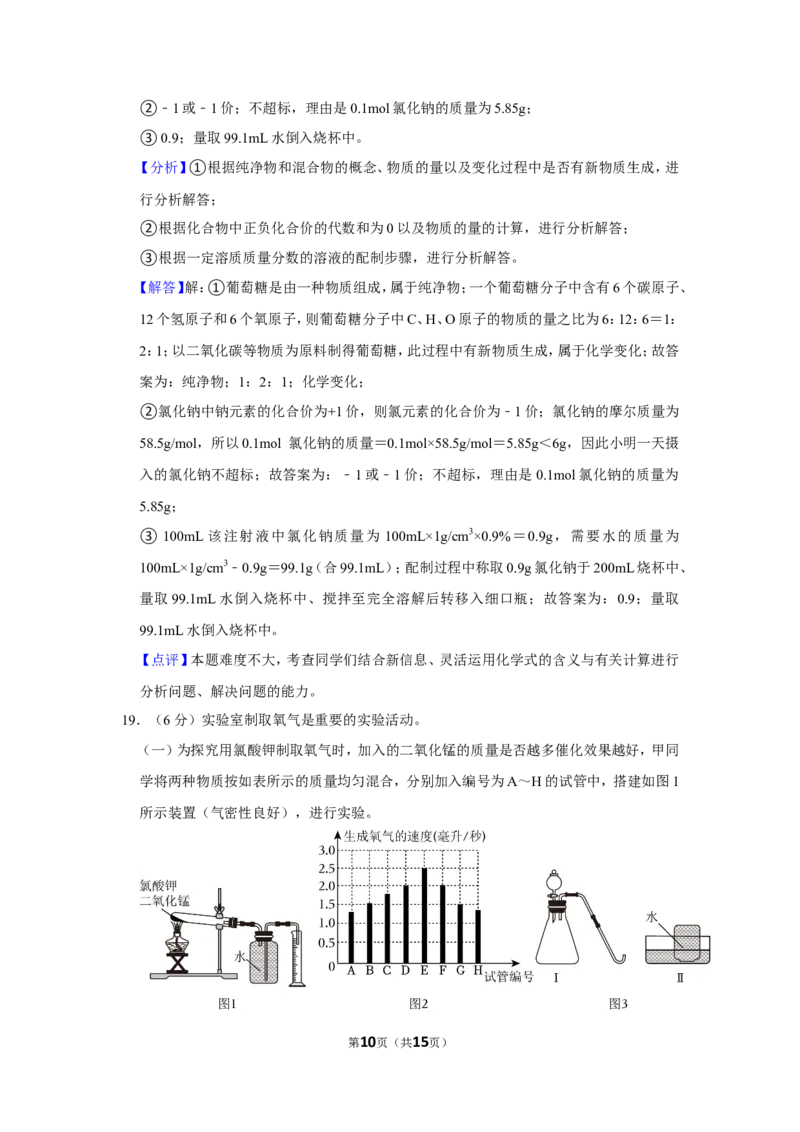
19.(6分)实验室制取氧气是重要的实验活动。
(一)为探究用氯酸钾制取氧气时,加入的二氧化锰的质量是否越多催化效果越好,甲同
学将两种物质按如表所示的质量均匀混合,分别加入编号为A~H的试管中,搭建如图1
所示装置(气密性良好),进行实验。
第10页(共15页)试管编号 A B C D E F G H
氯酸钾质量(g) 2.0 2.0 2.0 2.0 2.0 2.0 2.0 2.0
二氧化锰质量(g) 0.2 0.3 0.4 0.5 0.65 1.0 1.3 2.0
记录各自生成300mL氧气所需的时间,计算生成氧气的速度,如图2所示。
①写出试管中反应的化学方程式 2KClO 2KCl+3O ↑ 。
3 2
②如图收集氧气的方法利用了氧气具有 不易溶于水 的性质。
③分析实验结果,你得出的结论是 在一定范围内,反应速率随二氧化锰质量的增加而
增大,但超过一定值后,反应速率随二氧化锰的增加而减小 。
(二)用过氧化氢溶液与二氧化锰混合制取氧气。
④用向上排空气法收集氧气,集满后集气瓶应 正放 (选填“正放”或“倒放”)于
桌面。
⑤氧化铁也可作过氧化氢溶液制取氧气的催化剂。为比较氧化铁和二氧化锰的催化效果,
请将实验方案补充完整。
实验用品:3%过氧化氢溶液、氧化铁、二氧化锰、量筒、电子天平以及其他所需用品
实验装置:提供如图3所示装置(气密性良好)。
实验步骤及需要记录的数据: 分别向等量的 3% 过氧化氢溶液中分别加入等量的氧化铁
和二氧化锰,比较收集等体积的氧气时所需时间 。
【答案】(一)①2KClO 2KCl+3O ↑;
3 2
②不易溶于水;
③在一定范围内,反应速率随二氧化锰质量的增加而增大,但超过一定值后,反应速率随
二氧化锰的增加而减小;
(二)分别向等量的3%过氧化氢溶液中分别加入等量的氧化铁和二氧化锰,比较收集等
体积的氧气时所需时间。
【分析】(一)根据氯酸钾制取氧气的反应及表中内容进行分析;
【解答】解:(一)①氯酸钾在二氧化锰催化作用下加热生成氯化钾和氧气,反应的化学方
程式为:2KClO 2KCl+3O ↑。
3 2
第11页(共15页)②由图为排水法收集装置,氧气不易溶于水,则可用该装置收集。
③由图2可知,随着二氧化锰质量的增加,生成氧气的速度先增大后减小,则说明在一定
范围内,反应速率随二氧化锰质量的增加而增大,但超过一定值后,反应速率随二氧化锰
的增加而减小。
(二)若想比较氧化铁和二氧化锰的催化效果,则可分别取等体积的过氧化氢溶液,并分
别加入等质量的氧化铁和二氧化锰,比较收集等体积的氧气时所需时间即可。
故答案为:(一)①2KClO 2KCl+3O ↑;
3 2
②不易溶于水;
③在一定范围内,反应速率随二氧化锰质量的增加而增大,但超过一定值后,反应速率随
二氧化锰的增加而减小;
(二)分别向等量的3%过氧化氢溶液中分别加入等量的氧化铁和二氧化锰,比较收集等
体积的氧气时所需时间。
【点评】本题主要考查催化剂的性质,根据题中信息进行分析即可。
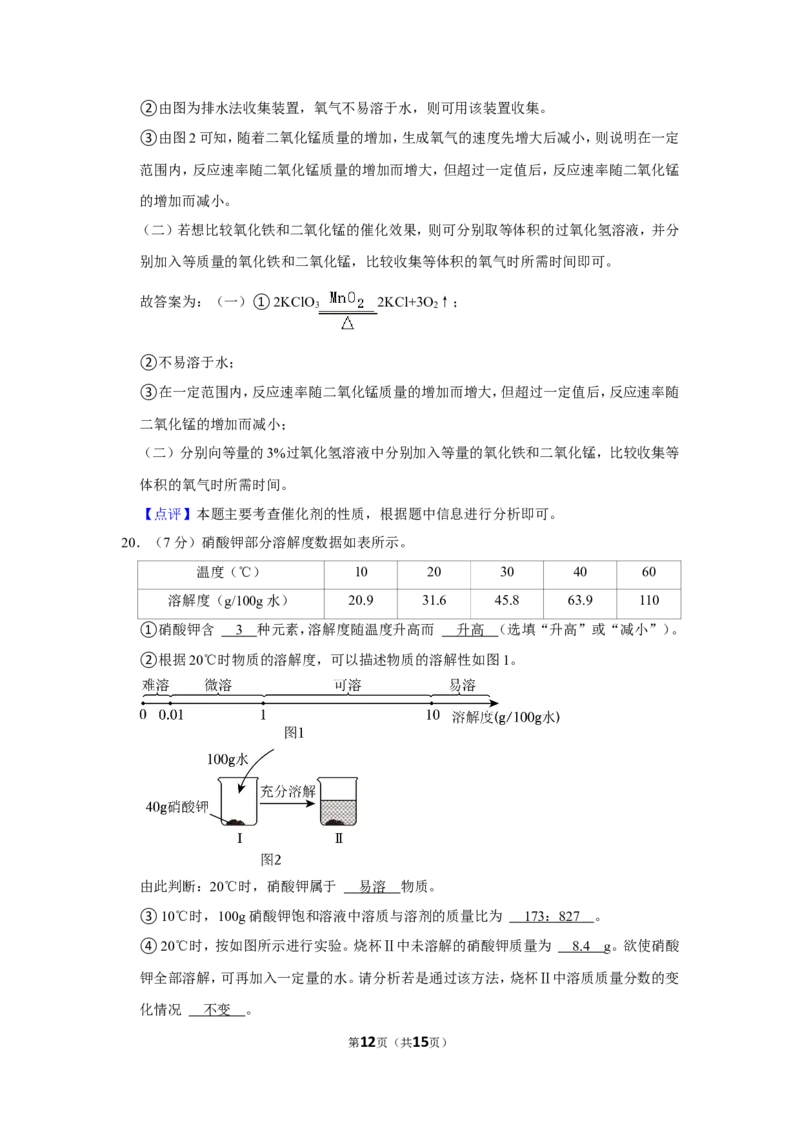
20.(7分)硝酸钾部分溶解度数据如表所示。
温度(℃) 10 20 30 40 60
溶解度(g/100g水) 20.9 31.6 45.8 63.9 110
①硝酸钾含 3 种元素,溶解度随温度升高而 升高 (选填“升高”或“减小”)。
②根据20℃时物质的溶解度,可以描述物质的溶解性如图1。
由此判断:20℃时,硝酸钾属于 易溶 物质。
③10℃时,100g硝酸钾饱和溶液中溶质与溶剂的质量比为 17 3 : 82 7 。
④20℃时,按如图所示进行实验。烧杯Ⅱ中未溶解的硝酸钾质量为 8. 4 g。欲使硝酸
钾全部溶解,可再加入一定量的水。请分析若是通过该方法,烧杯Ⅱ中溶质质量分数的变
化情况 不变 。
第12页(共15页)⑤为得到50℃、70g硝酸钾饱和溶液,同学将原烧杯Ⅱ(如图2所示)中的物质升温至
50℃,再蒸发70g水(维持在50℃),请结合数据分析实验目的能否达成 否 。
【答案】①3;升高。
②易溶。
③173:827。
④8.4;不变。
⑤否。
【分析】硝酸钾中含有钾元素、氮元素和氧元素,溶解度随温度升高而升高。
20℃时,硝酸钾溶解度大于10g,属于易溶物质。
根据提供数据可以进行相关方面的计算和判断。
【解答】解:①硝酸钾含3种元素,即钾元素、氮元素和氧元素,溶解度随温度升高而升高。
故答案为:3;升高。
②20℃时,硝酸钾溶解度大于10g,属于易溶物质。
故答案为:易溶。
③10℃时,100g硝酸钾饱和溶液中溶质质量是100g× ≈17.3g,水的质量是
100g﹣17.3g=82.7g,溶质与溶剂的质量比为17.3g:82.7g=173:827。
故答案为:173:827。
④20℃时硝酸钾溶解度是31.6g,按如图所示进行实验。烧杯Ⅱ中未溶解的硝酸钾质量为
40g﹣31.6g=8.4g。欲使硝酸钾全部溶解,可再加入一定量的水。请分析若是通过该方法,
烧杯Ⅱ中溶质质量分数的变化情况不变,是因为前后都是相同温度下的饱和溶液。
故答案为:8.4;不变。
⑤为得到50℃、70g硝酸钾饱和溶液,同学将原烧杯Ⅱ(如图2所示)中的物质升温至
50℃,再蒸发70g水(维持在50℃),不能达到实验目的,是因为蒸发70g水后,烧杯中的
物质总质量是70g,其中水的质量是30g,50℃是硝酸钾溶解度小于110g,因此50℃时,
30g水不能完全溶解40g硝酸钾。
故答案为:否。
【点评】本题主要考查溶解方面的知识,比较简单。
21.(6分)氢能是很有发展前途的新能源,用液氨(NH )储存氢气是一种新型的储氢技术,有
3
关流程如图所示。(常压下,NH 的沸点是﹣33.5℃、H 的沸点为﹣253℃)
3 2
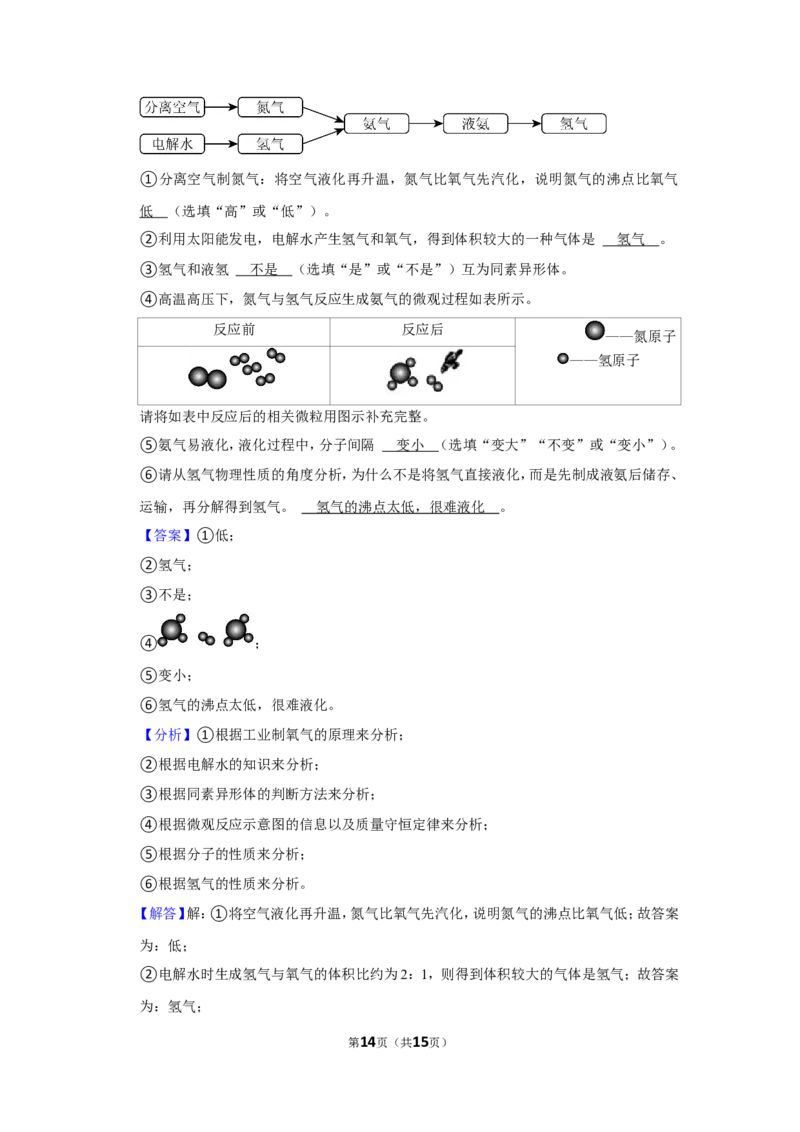
第13页(共15页)①分离空气制氮气:将空气液化再升温,氮气比氧气先汽化,说明氮气的沸点比氧气
低 (选填“高”或“低”)。
②利用太阳能发电,电解水产生氢气和氧气,得到体积较大的一种气体是 氢气 。
③氢气和液氢 不是 (选填“是”或“不是”)互为同素异形体。
④高温高压下,氮气与氢气反应生成氨气的微观过程如表所示。
反应前 反应后
——氮原子
——氢原子
请将如表中反应后的相关微粒用图示补充完整。
⑤氨气易液化,液化过程中,分子间隔 变小 (选填“变大”“不变”或“变小”)。
⑥请从氢气物理性质的角度分析,为什么不是将氢气直接液化,而是先制成液氨后储存、
运输,再分解得到氢气。 氢气的沸点太低,很难液化 。
【答案】①低;
②氢气;
③不是;
④ ;
⑤变小;
⑥氢气的沸点太低,很难液化。
【分析】①根据工业制氧气的原理来分析;
②根据电解水的知识来分析;
③根据同素异形体的判断方法来分析;
④根据微观反应示意图的信息以及质量守恒定律来分析;
⑤根据分子的性质来分析;
⑥根据氢气的性质来分析。
【解答】解:①将空气液化再升温,氮气比氧气先汽化,说明氮气的沸点比氧气低;故答案
为:低;
②电解水时生成氢气与氧气的体积比约为2:1,则得到体积较大的气体是氢气;故答案
为:氢气;
第14页(共15页)③液氢是液态的氢气,二者是同一种物质,因此氢气和液氢不是互为同素异形体;故答案
为:不是;
④高温高压下,氮气与氢气反应生成氨气,由质量守恒定律可知,还应补充一个氨分子,
故 反 应 后 的 图 示 为 ; 故 答 案 为 :
;
⑤氨气易液化,液化过程中,分子间隔变小;故答案为:变小;
⑥因为氢气的沸点太低,很难液化,而氨气的沸点较高,易于液化,因此不是将氢气直接
液化,而是先制成液氨后储存、运输,再分解得到氢气;故答案为:氢气的沸点太低,很难
液化。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布日期:2024/1/17 16:34:38;用户:郭亚红;邮箱:18317538760;学号:45050889
第15页(共15页)