文档内容
2023-2024学年上海市浦东新区九年级(上)期末化学试卷(一
模)
参考答案与试题解析
一、选择题(共20分)
1.(1分)空气中含量最多的物质是( )
A.N B.He C.O D.H O
2 2 2
【答案】A
【分析】利用空气中各成分的体积分数分析。
【解答】解:空气中各成分的体积分数为:氮气78%、氧气21%、稀有气体0.94%、二氧化碳
0.03%、其他气体和杂质0.03%。
故选:A。
【点评】考查学生对空气中各成分的体积分数的掌握情况,难度小。
2.(1分)属于化学性质的是( )
A.导电性 B.硬度 C.可燃性 D.密度
【答案】C
【分析】物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要
通过化学变化表现出来的性质。据此判断物质的性质。
【解答】解:A、导电性是不需要通过化学变化表现出来的性质,属于物理性质。
B、硬度是不需要通过化学变化表现出来的性质,属于物理性质。
C、可燃性是需要通过燃烧这一化学变化表现出来的性质,属于化学性质。
D、密度是不需要通过化学变化表现出来的性质,属于物理性质。
故选:C。
【点评】本题主要考查了物质的化学性质方面的内容,完成此题,可以依据该性质是否在
化学变化中表现出来。
3.(1分)加入水中能形成溶液的是( )
A.植物油 B.淀粉 C.蔗糖 D.大理石
【答案】C
【分析】可根据各物质在水中的溶解性及溶液的定义和特征进行分析解答。
【解答】解:一种或几种物质分散到另一种物质中,形成均一的、稳定的混合物叫做溶液,
第1页(共16页)它的基本特征是均一性和稳定性;只有被分散的物质在另一种物质中是可溶的,二者混合
后才会形成溶液。
A、植物油不能溶于水,把植物油放入水中充分搅拌只能形成乳浊液,选项错误。
B、淀粉不能溶于水,把面粉放入水中充分搅拌只能形成悬浊液,选项错误。
C、蔗糖可以溶于水,能形成溶液,选项正确。
D、大理石不溶于水,不能形成溶液,选项错误。
故选:C。
【点评】该题主要考查溶液的形成,在判断物质混合后是否能形成溶液时,可以结合生活
经验,根据物质的溶解性、溶液的定义和特征进行判断,其中了解物质的溶解性是解题的
关键。
4.(1分)在pH=12炉具清洁剂中滴加酚酞溶液,溶液变( )
A.无色 B.红色 C.蓝色 D.紫色
【答案】B
【分析】根据当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的pH
小于7时,呈酸性。酚酞试液遇酸性溶液不变色,遇碱性溶液变红,遇中性溶液不变色进行
解答。
【解答】解:pH=12的炉具清洁剂显碱性,向其中滴加酚酞溶液,能使无色酚酞试液变红。
故选:B。
【点评】解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据酸碱性溶
液与酸碱指示剂相互作用显色方面的知识分析。
5.(1分)互为同素异形体的是( )
A.氧气和臭氧 B.冰和干冰
C.氢气和液氢 D.银和水银
【答案】A
【分析】化学上把同种元素组成的不同单质互称为同素异形体,互为同素异形体的物质要
符合以下两个条件:同种元素形成,不同单质;据此进
【解答】解:A、氧气和臭氧都是由氧元素形成的不同物质,都是单质,互为同素异形体,故
选项正确。
B、冰和干冰分别是固态的水、固态的二氧化碳,均属于化合物,不属于同素异形体,故选
项错误。
C、液氢是液态的氢气,和氢气是同一种物质,不属于同素异形体,故选项错误。
第2页(共16页)D、水银是金属汞的俗称,和银是不同种元素组成的单质,不属于同素异形体,故选项错误。
故选:A。
【点评】本题难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,
②不同单质,这是解决此类题的关键之所在。
6.(1分)在氧气中燃烧产生大量白烟的物质是( )
A.铁丝 B.木炭 C.硫 D.红磷
【答案】D
【分析】根据铁丝、木炭、硫、红磷在氧气中燃烧的现象进行分析判断.
【解答】解:A、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故
选项不符合题意。
B、木炭在氧气中燃烧,发出白光,放出大量的热,生成能使澄清石灰水变浑的气体,故选
项不符合题意。
C、硫在氧气中燃烧,发出明亮的蓝紫色火焰,放出热量,产生一种具有刺激性气味的气体,
故选项不符合题意。
D、红磷在氧气中燃烧,产生大量的白烟,放出大量的热,故选项符合题意。
故选:D。
【点评】本题难度不大,掌握常见物质燃烧的现象即可正确解答;但在描述物质燃烧的现
象时,需要注意光和火焰、烟和雾的区别.
7.(1分)MoO 是一种优良的储能材料,其中Mo的化合价是( )
3
A.+4 B.+5 C.+6 D.+7
【答案】C
【分析】根据化合物中各元素的化合价代数和为0,利用化合物的化学式可计算其中未知
的元素化合价。
【解答】解:MoO 是一种优良的储能材料,氧元素的化合价为﹣2价,根据化合物中各元素
3
的化合价代数和为0原则,Mo的化合价+6价。
故选:C。
【点评】掌握化合价法则是解答本题的关键。
8.(1分)物质性质和用途对应关系正确的是( )
A.石墨质软,作电极
B.氦气很稳定,作霓虹灯
C.氧气有助燃性,作燃料
第3页(共16页)D.干冰升华吸热,用于人工降雨
【答案】D
【分析】A、根据作电极的物质应具有优良的导电性,进行分析判断;
B、根据氮气的化学性质不活泼,进行分析判断;
C、根据氧气能支持燃烧,进行分析判断;
D、根据干冰的特点,进行分析判断。
【解答】解:A、石墨具有优良的导电性,可用作电极,故选项说法错误;
B、氮气的化学性质不活泼,可用作保护气,故选项说法错误;
C、氧气能支持燃烧,但不具有可燃性,不能作燃料,故选项说法错误;
D、干冰升华吸热,用于人工降雨,故选项说法正确;
故选:D。
【点评】本题难度不大,物质的性质决定物质的用途,掌握碳单质和常见气体的性质和用
途是正确解答本题的关键。
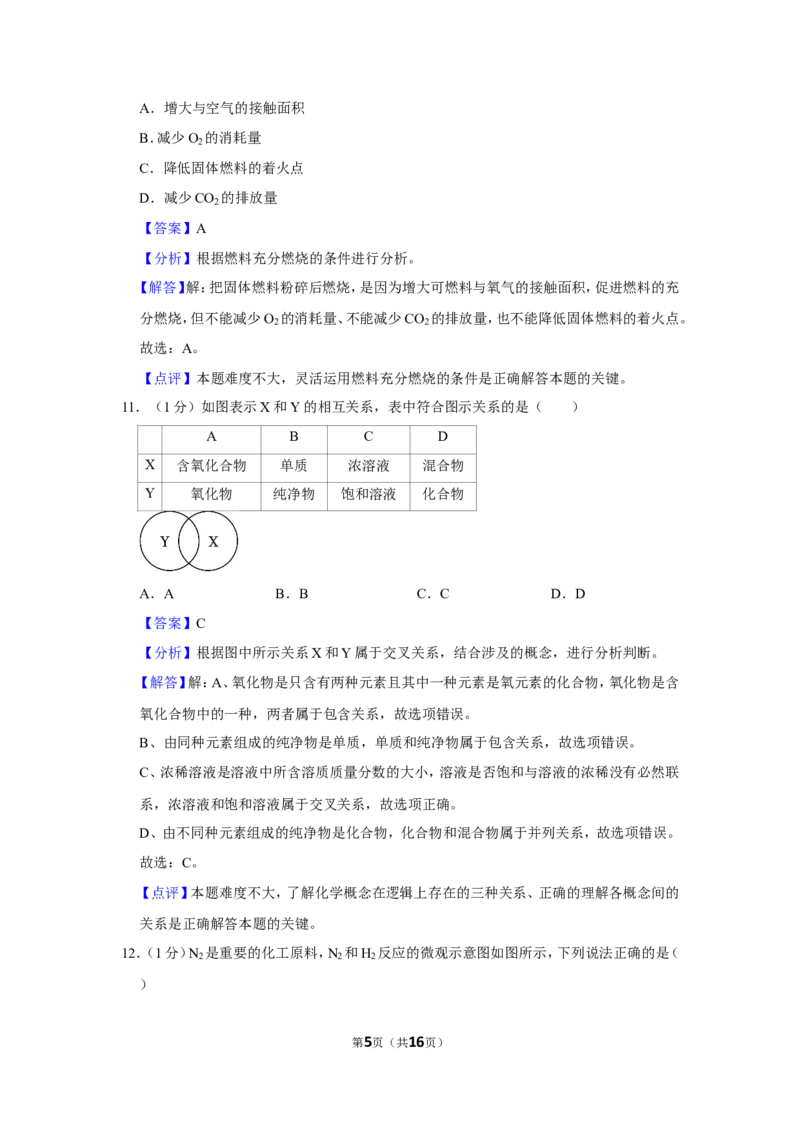
9.(1分)化学方程式书写正确的是( )
A.4Fe+3O 2Fe O
2 2 3
B.4Fe+3O 2Fe O
2 3 4
C.3Fe+2O Fe O
2 3 4
D.3Fe+2O ═Fe O
2 3 4
【答案】C
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否
正确;是否配平;反应条件是否正确;↑和↓的标注是否正确,进行分析判断。
【解答】解:铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O
2
Fe O 。
3 4
故选:C。
【点评】本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式
的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再
看反应条件,再看气体和沉淀,最后短线改成等号。
10.(1分)工业上常把固体燃料粉碎,目的是( )
第4页(共16页)A.增大与空气的接触面积
B.减少O 的消耗量
2
C.降低固体燃料的着火点
D.减少CO 的排放量
2
【答案】A
【分析】根据燃料充分燃烧的条件进行分析。
【解答】解:把固体燃料粉碎后燃烧,是因为增大可燃料与氧气的接触面积,促进燃料的充
分燃烧,但不能减少O 的消耗量、不能减少CO 的排放量,也不能降低固体燃料的着火点。
2 2
故选:A。
【点评】本题难度不大,灵活运用燃料充分燃烧的条件是正确解答本题的关键。
11.(1分)如图表示X和Y的相互关系,表中符合图示关系的是( )
A B C D
X 含氧化合物 单质 浓溶液 混合物
Y 氧化物 纯净物 饱和溶液 化合物
A.A B.B C.C D.D
【答案】C
【分析】根据图中所示关系X和Y属于交叉关系,结合涉及的概念,进行分析判断。
【解答】解:A、氧化物是只含有两种元素且其中一种元素是氧元素的化合物,氧化物是含
氧化合物中的一种,两者属于包含关系,故选项错误。
B、由同种元素组成的纯净物是单质,单质和纯净物属于包含关系,故选项错误。
C、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联
系,浓溶液和饱和溶液属于交叉关系,故选项正确。
D、由不同种元素组成的纯净物是化合物,化合物和混合物属于并列关系,故选项错误。
故选:C。
【点评】本题难度不大,了解化学概念在逻辑上存在的三种关系、正确的理解各概念间的
关系是正确解答本题的关键。
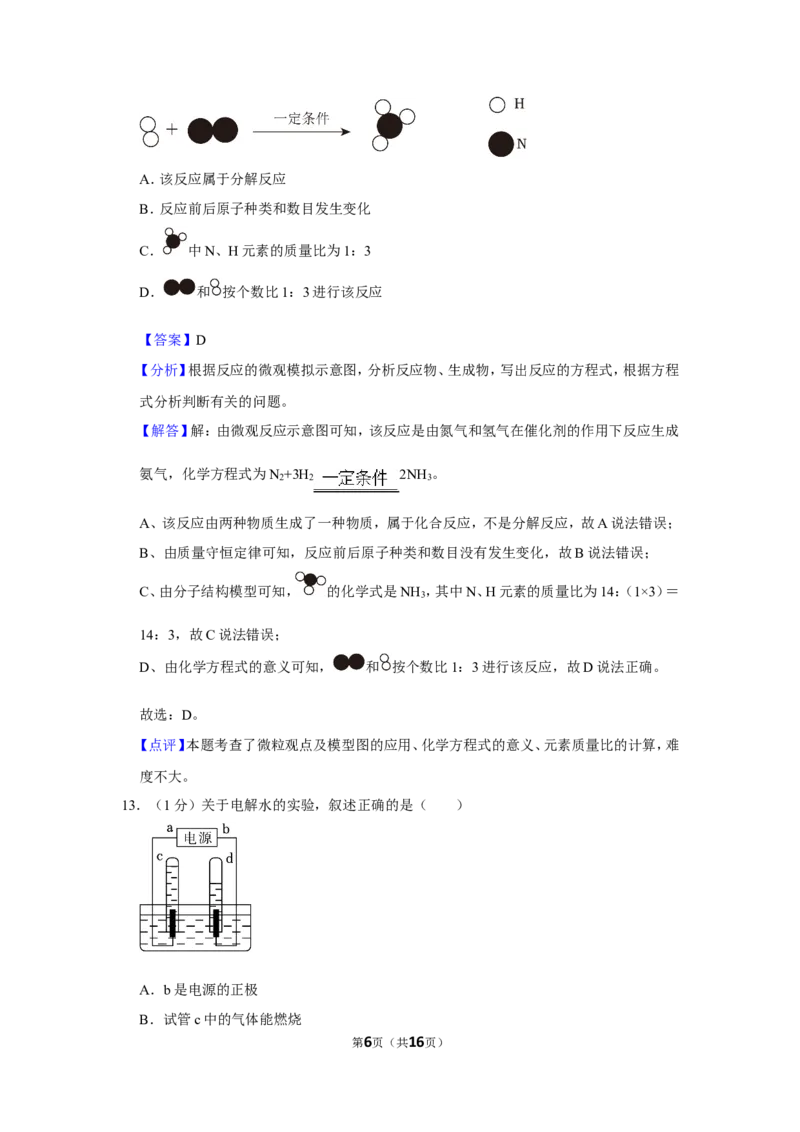
12.(1分)N 是重要的化工原料,N 和H 反应的微观示意图如图所示,下列说法正确的是(
2 2 2
)
第5页(共16页)A.该反应属于分解反应
B.反应前后原子种类和数目发生变化
C. 中N、H元素的质量比为1:3
D. 和 按个数比1:3进行该反应
【答案】D
【分析】根据反应的微观模拟示意图,分析反应物、生成物,写出反应的方程式,根据方程
式分析判断有关的问题。
【解答】解:由微观反应示意图可知,该反应是由氮气和氢气在催化剂的作用下反应生成
氨气,化学方程式为N +3H 2NH 。
2 2 3
A、该反应由两种物质生成了一种物质,属于化合反应,不是分解反应,故A说法错误;
B、由质量守恒定律可知,反应前后原子种类和数目没有发生变化,故B说法错误;
C、由分子结构模型可知, 的化学式是NH ,其中N、H元素的质量比为14:(1×3)=
3
14:3,故C说法错误;
D、由化学方程式的意义可知, 和 按个数比1:3进行该反应,故D说法正确。
故选:D。
【点评】本题考查了微粒观点及模型图的应用、化学方程式的意义、元素质量比的计算,难
度不大。
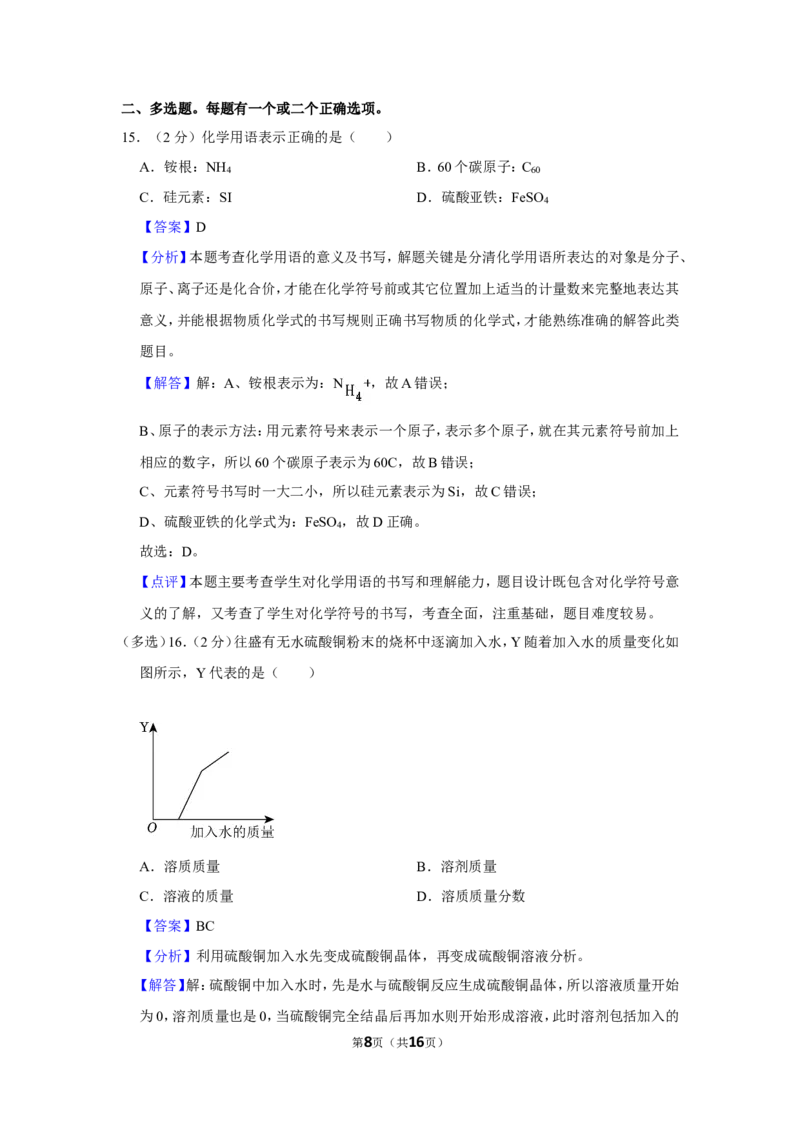
13.(1分)关于电解水的实验,叙述正确的是( )
A.b是电源的正极
B.试管c中的气体能燃烧
第6页(共16页)C.产生的H 和O 的体积比为1:2
2 2
D.该实验能证明水是由氢、氧元素组成的
【答案】D
【分析】根据电极水“正氧负氢、氢二氧一”的现象及结论进行分析。
【解答】解:A、电极水时,正极产生氧气,负极产生氢气,且生成的氧气和氢气的体积比为
1:2,由图可知,d试管收集的气体较多,则收集的气体为氢气,则b为电源的负极,故叙述
不正确;
B、试管c收集的气体为氧气,氧气具有助燃性,而不是可燃物,故叙述不正确;
C、电解水生成的氢气和氧气的体积比为2:1,故叙述不正确;
D、氢气是由氢元素组成,氧气是由氧元素组成,根据反应前后元素种类不变,则水是由氢、
氧元素组成,故叙述正确。
故选:D。
【点评】本题比较简单,主要考查电解水的实验,理解电解水的现象、结论、注意事项等为
解答该题的关键。
14.(1分)鉴别和除杂是重要的实验技能,实验方法正确的是( )
A.用燃着的木条鉴别二氧化碳和氮气
B.用灼热的铜丝除去氮气中的氧气
C.通过观察固体颜色鉴别木炭粉和氧化铜
D.用澄清石灰水除去二氧化碳中的一氧化碳
【答案】B
【分析】A、二氧化碳和氮气都不支持燃烧。
B、加热时铜和氧气反应生成氧化铜。
C、木炭粉和氧化铜都是黑色固体。
D、氢氧化钙能和二氧化碳反应生成碳酸钙沉淀和水。
【解答】解:A、二氧化碳和氮气都不支持燃烧,过程中木条都熄灭,该选项不正确。
B、加热时铜和氧气反应生成氧化铜,氮气不能反应,该选项正确。
C、木炭粉和氧化铜都是黑色固体,不能通过观察颜色区分两种物质,该选项不正确。
D、氢氧化钙能和二氧化碳反应生成碳酸钙沉淀和水,该选项不正确。
故选:B。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
第7页(共16页)二、多选题。每题有一个或二个正确选项。
15.(2分)化学用语表示正确的是( )
A.铵根:NH B.60个碳原子:C
4 60
C.硅元素:SI D.硫酸亚铁:FeSO
4
【答案】D
【分析】本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、
原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其
意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类
题目。
【解答】解:A、铵根表示为:N ,故A错误;
B、原子的表示方法:用元素符号来表示一个原子,表示多个原子,就在其元素符号前加上
相应的数字,所以60个碳原子表示为60C,故B错误;
C、元素符号书写时一大二小,所以硅元素表示为Si,故C错误;
D、硫酸亚铁的化学式为:FeSO ,故D正确。
4
故选:D。
【点评】本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意
义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易。
(多选)16.(2分)往盛有无水硫酸铜粉末的烧杯中逐滴加入水,Y随着加入水的质量变化如
图所示,Y代表的是( )
A.溶质质量 B.溶剂质量
C.溶液的质量 D.溶质质量分数
【答案】BC
【分析】利用硫酸铜加入水先变成硫酸铜晶体,再变成硫酸铜溶液分析。
【解答】解:硫酸铜中加入水时,先是水与硫酸铜反应生成硫酸铜晶体,所以溶液质量开始
为0,溶剂质量也是0,当硫酸铜完全结晶后再加水则开始形成溶液,此时溶剂包括加入的
第8页(共16页)水和原晶体中的水,当硫酸铜晶体完全溶解后,再加入不溶液增加的质量就是加入的水的
质量,溶剂再增加的就是加入的水。
故选:BC。
【点评】考查硫酸铜加水的溶液变化情况,难度中等。
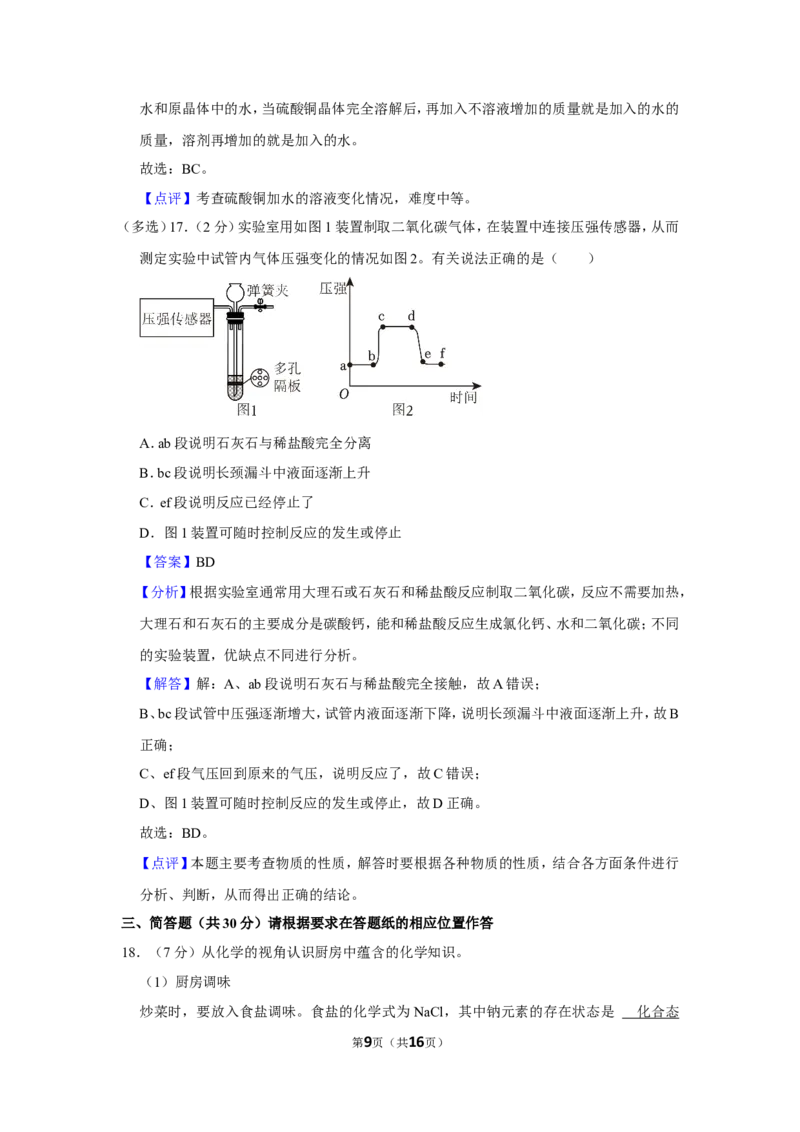
(多选)17.(2分)实验室用如图1装置制取二氧化碳气体,在装置中连接压强传感器,从而
测定实验中试管内气体压强变化的情况如图2。有关说法正确的是( )
A.ab段说明石灰石与稀盐酸完全分离
B.bc段说明长颈漏斗中液面逐渐上升
C.ef段说明反应已经停止了
D.图1装置可随时控制反应的发生或停止
【答案】BD
【分析】根据实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,
大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;不同
的实验装置,优缺点不同进行分析。
【解答】解:A、ab段说明石灰石与稀盐酸完全接触,故A错误;
B、bc段试管中压强逐渐增大,试管内液面逐渐下降,说明长颈漏斗中液面逐渐上升,故B
正确;
C、ef段气压回到原来的气压,说明反应了,故C错误;
D、图1装置可随时控制反应的发生或停止,故D正确。
故选:BD。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
三、简答题(共30分)请根据要求在答题纸的相应位置作答
18.(7分)从化学的视角认识厨房中蕴含的化学知识。
(1)厨房调味
炒菜时,要放入食盐调味。食盐的化学式为NaCl,其中钠元素的存在状态是 化合态
第9页(共16页)(选填“游离态”或“化合态”)。
(2)厨房用水
从净水器中可获取直饮水,净水器中活性炭的作用是 吸附作用 ,直饮水属于 混合
物 (选填“纯净物”或“混合物”)。
(3)厨房燃料
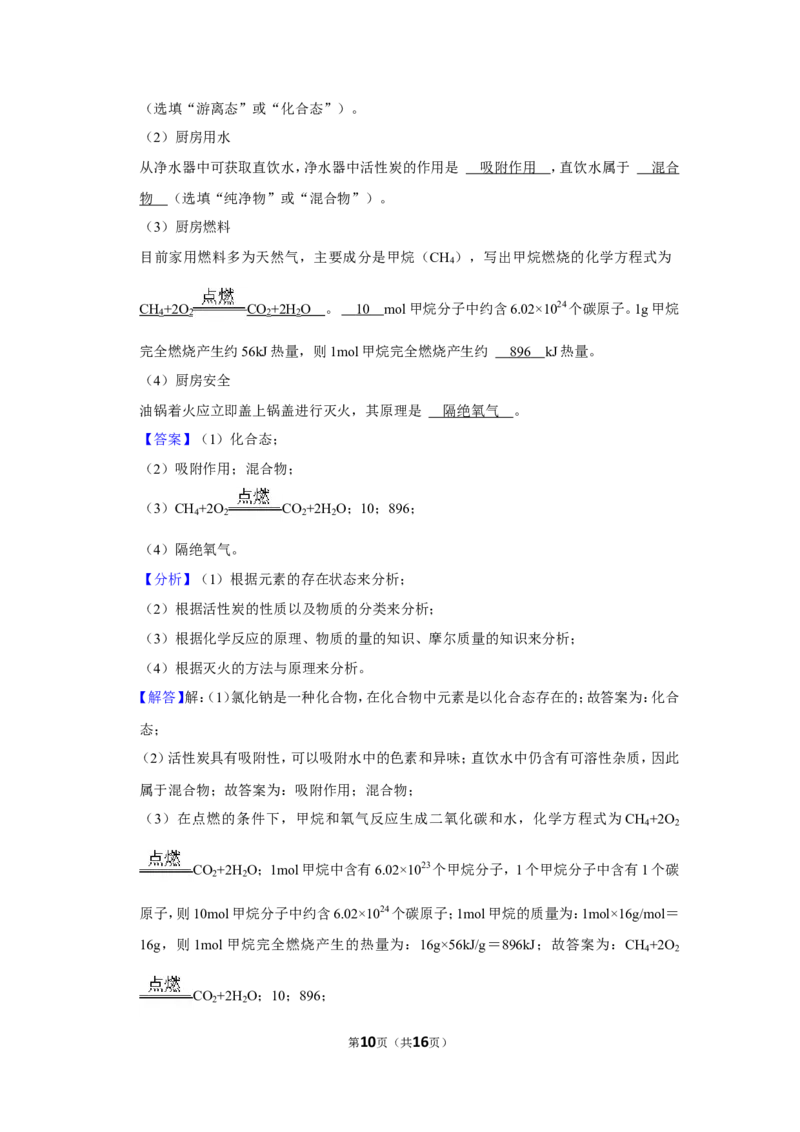
目前家用燃料多为天然气,主要成分是甲烷(CH ),写出甲烷燃烧的化学方程式为
4
CH +2O CO +2H O 。 1 0 mol甲烷分子中约含6.02×1024个碳原子。1g甲烷
4 2 2 2
完全燃烧产生约56kJ热量,则1mol甲烷完全燃烧产生约 89 6 kJ热量。
(4)厨房安全
油锅着火应立即盖上锅盖进行灭火,其原理是 隔绝氧气 。
【答案】(1)化合态;
(2)吸附作用;混合物;
(3)CH +2O CO +2H O;10;896;
4 2 2 2
(4)隔绝氧气。
【分析】(1)根据元素的存在状态来分析;
(2)根据活性炭的性质以及物质的分类来分析;
(3)根据化学反应的原理、物质的量的知识、摩尔质量的知识来分析;
(4)根据灭火的方法与原理来分析。
【解答】解:(1)氯化钠是一种化合物,在化合物中元素是以化合态存在的;故答案为:化合
态;
(2)活性炭具有吸附性,可以吸附水中的色素和异味;直饮水中仍含有可溶性杂质,因此
属于混合物;故答案为:吸附作用;混合物;
(3)在点燃的条件下,甲烷和氧气反应生成二氧化碳和水,化学方程式为CH +2O
4 2
CO +2H O;1mol甲烷中含有6.02×1023个甲烷分子,1个甲烷分子中含有1个碳
2 2
原子,则10mol甲烷分子中约含6.02×1024个碳原子;1mol甲烷的质量为:1mol×16g/mol=
16g,则1mol甲烷完全燃烧产生的热量为:16g×56kJ/g=896kJ;故答案为:CH +2O
4 2
CO +2H O;10;896;
2 2
第10页(共16页)(4)油锅着火应立即盖上锅盖进行灭火,其原理是隔绝氧气;故答案为:隔绝氧气。
【点评】本题考查的知识点较多,掌握元素的存在状态、物质的性质与用途、化学方程式的
写法、灭火的方法与原理等是解题的关键。
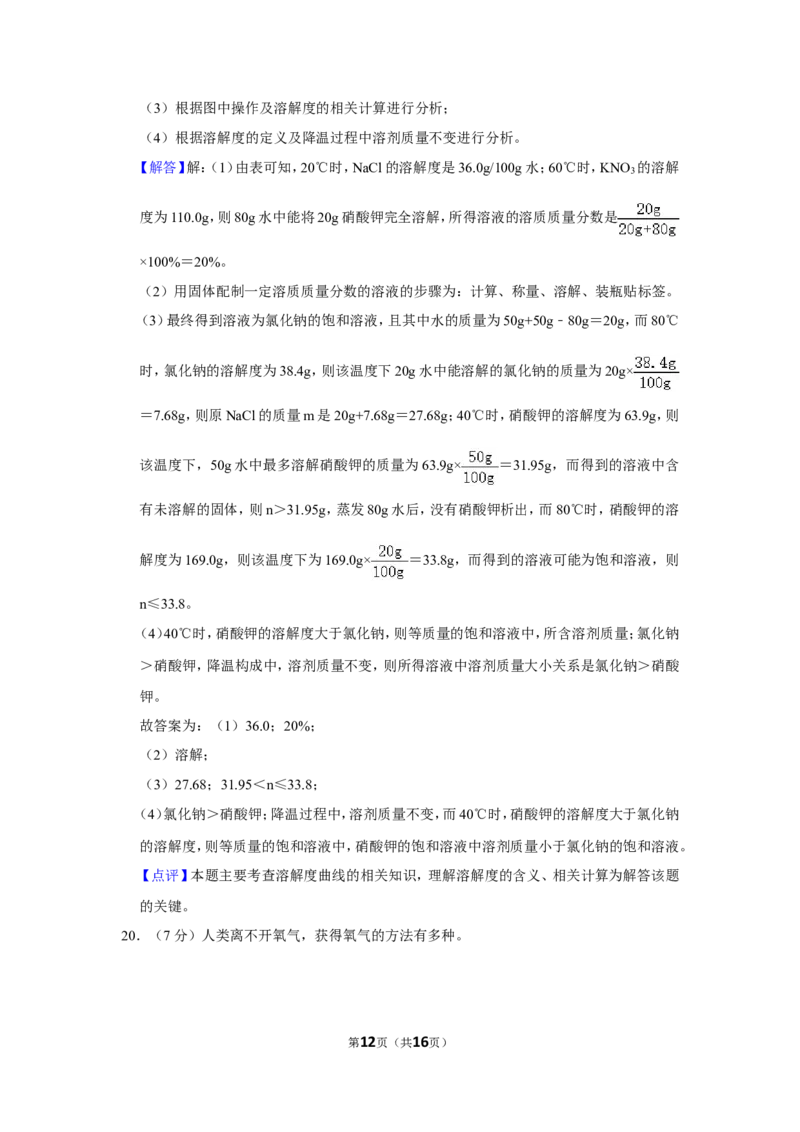
19.(9分)硝酸钾和氯化钠的部分溶解度数据如下表:
温度℃ 0 10 20 40 60 80
溶 解 度 ( g/100gNaCl 35.7 35.8 36.0 36.6 37.3 38.4
水)
KNO 13.3 20.9 31.6 63.9 110.0 169.0
3
(1)20℃时,NaCl的溶解度是 36. 0 g/100g水。60℃时,20gKNO 完全溶解在80g水中,
3
所得溶液的溶质质量分数是 20% 。
(2)配制5%的氯化钠溶液100g,其过程为:计算、称5g氯化钠和量取95mL水、 溶解 、
装瓶贴标签。
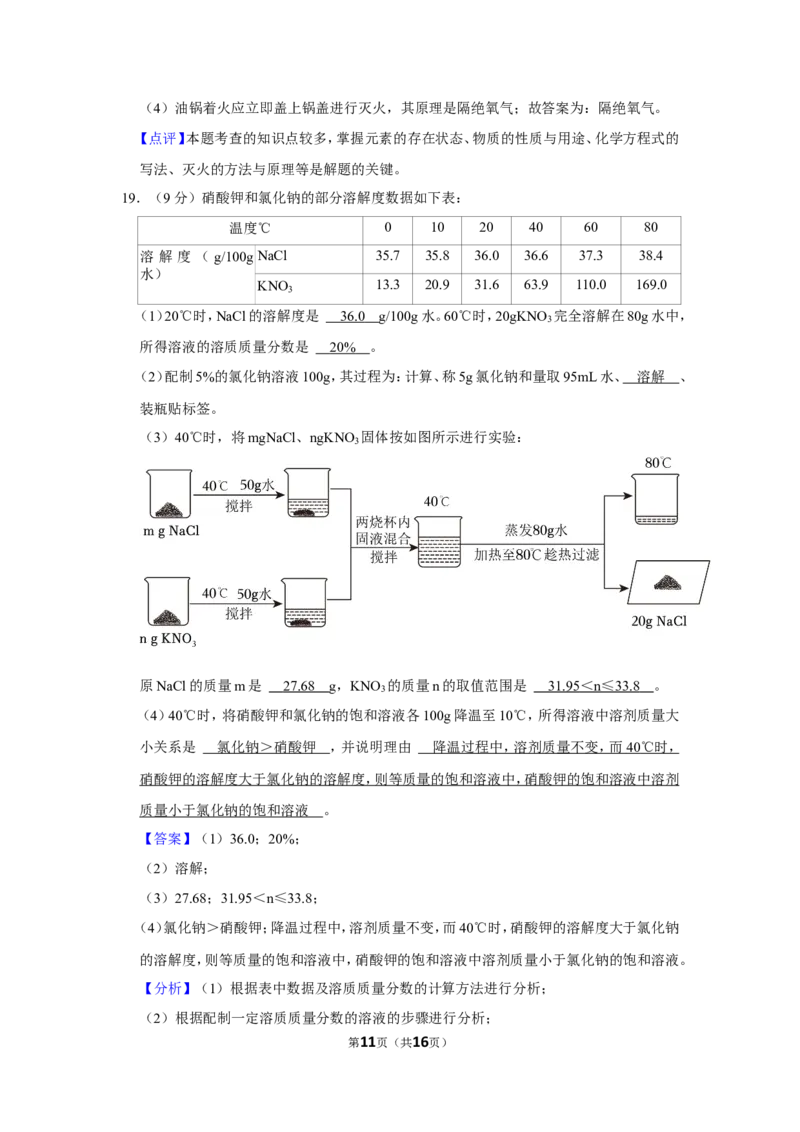
(3)40℃时,将mgNaCl、ngKNO 固体按如图所示进行实验:
3
原NaCl的质量m是 27.6 8 g,KNO 的质量n的取值范围是 31.9 5 < n ≤ 33. 8 。
3
(4)40℃时,将硝酸钾和氯化钠的饱和溶液各100g降温至10℃,所得溶液中溶剂质量大
小关系是 氯化钠>硝酸钾 ,并说明理由 降温过程中,溶剂质量不变,而 4 0 ℃时,
硝酸钾的溶解度大于氯化钠的溶解度,则等质量的饱和溶液中,硝酸钾的饱和溶液中溶剂
质量小于氯化钠的饱和溶液 。
【答案】(1)36.0;20%;
(2)溶解;
(3)27.68;31.95<n≤33.8;
(4)氯化钠>硝酸钾;降温过程中,溶剂质量不变,而40℃时,硝酸钾的溶解度大于氯化钠
的溶解度,则等质量的饱和溶液中,硝酸钾的饱和溶液中溶剂质量小于氯化钠的饱和溶液。
【分析】(1)根据表中数据及溶质质量分数的计算方法进行分析;
(2)根据配制一定溶质质量分数的溶液的步骤进行分析;
第11页(共16页)(3)根据图中操作及溶解度的相关计算进行分析;
(4)根据溶解度的定义及降温过程中溶剂质量不变进行分析。
【解答】解:(1)由表可知,20℃时,NaCl的溶解度是36.0g/100g水;60℃时,KNO 的溶解
3
度为110.0g,则80g水中能将20g硝酸钾完全溶解,所得溶液的溶质质量分数是
×100%=20%。
(2)用固体配制一定溶质质量分数的溶液的步骤为:计算、称量、溶解、装瓶贴标签。
(3)最终得到溶液为氯化钠的饱和溶液,且其中水的质量为50g+50g﹣80g=20g,而80℃
时,氯化钠的溶解度为38.4g,则该温度下20g水中能溶解的氯化钠的质量为20g×
=7.68g,则原NaCl的质量m是20g+7.68g=27.68g;40℃时,硝酸钾的溶解度为63.9g,则
该温度下,50g水中最多溶解硝酸钾的质量为63.9g× =31.95g,而得到的溶液中含
有未溶解的固体,则n>31.95g,蒸发80g水后,没有硝酸钾析出,而80℃时,硝酸钾的溶
解度为169.0g,则该温度下为169.0g× =33.8g,而得到的溶液可能为饱和溶液,则
n≤33.8。
(4)40℃时,硝酸钾的溶解度大于氯化钠,则等质量的饱和溶液中,所含溶剂质量;氯化钠
>硝酸钾,降温构成中,溶剂质量不变,则所得溶液中溶剂质量大小关系是氯化钠>硝酸
钾。
故答案为:(1)36.0;20%;
(2)溶解;
(3)27.68;31.95<n≤33.8;
(4)氯化钠>硝酸钾;降温过程中,溶剂质量不变,而40℃时,硝酸钾的溶解度大于氯化钠
的溶解度,则等质量的饱和溶液中,硝酸钾的饱和溶液中溶剂质量小于氯化钠的饱和溶液。
【点评】本题主要考查溶解度曲线的相关知识,理解溶解度的含义、相关计算为解答该题
的关键。
20.(7分)人类离不开氧气,获得氧气的方法有多种。
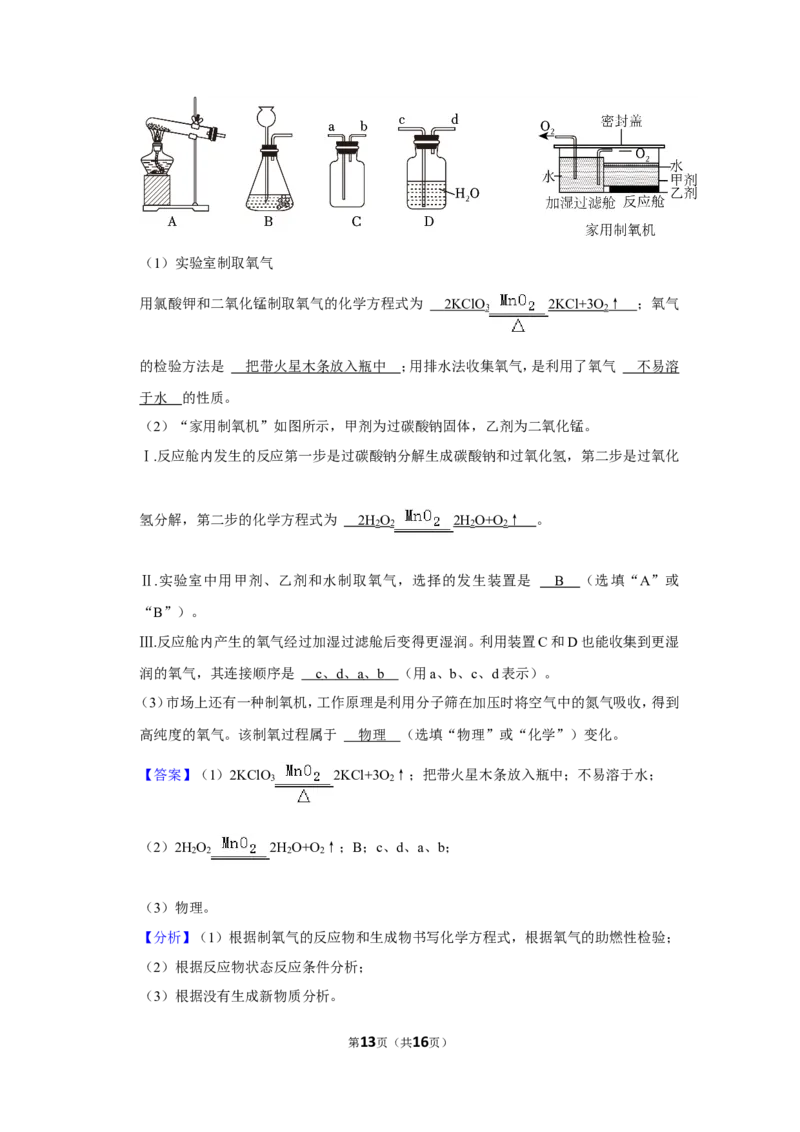
第12页(共16页)(1)实验室制取氧气
用氯酸钾和二氧化锰制取氧气的化学方程式为 2KClO 2KCl+3O ↑ ;氧气
3 2
的检验方法是 把带火星木条放入瓶中 ;用排水法收集氧气,是利用了氧气 不易溶
于水 的性质。
(2)“家用制氧机”如图所示,甲剂为过碳酸钠固体,乙剂为二氧化锰。
Ⅰ.反应舱内发生的反应第一步是过碳酸钠分解生成碳酸钠和过氧化氢,第二步是过氧化
氢分解,第二步的化学方程式为 2H O 2H O+O ↑ 。
2 2 2 2
Ⅱ.实验室中用甲剂、乙剂和水制取氧气,选择的发生装置是 B (选填“A”或
“B”)。
Ⅲ.反应舱内产生的氧气经过加湿过滤舱后变得更湿润。利用装置C和D也能收集到更湿
润的氧气,其连接顺序是 c 、 d 、 a 、 b (用a、b、c、d表示)。
(3)市场上还有一种制氧机,工作原理是利用分子筛在加压时将空气中的氮气吸收,得到
高纯度的氧气。该制氧过程属于 物理 (选填“物理”或“化学”)变化。
【答案】(1)2KClO 2KCl+3O ↑;把带火星木条放入瓶中;不易溶于水;
3 2
(2)2H O 2H O+O ↑;B;c、d、a、b;
2 2 2 2
(3)物理。
【分析】(1)根据制氧气的反应物和生成物书写化学方程式,根据氧气的助燃性检验;
(2)根据反应物状态反应条件分析;
(3)根据没有生成新物质分析。
第13页(共16页)【解答】解:(1)氯酸钾和二氧化锰加热生成氯化钾和氧气,由此书写化学方程式。氧气具
有助燃性,检验方法是把带火星木条放入瓶中,若复燃则是氧气。不易溶于水,可以用排
水法收集。故答案为:2KClO 2KCl+3O ↑;把带火星木条放入瓶中;不易溶于水;
3 2
(2)过氧化氢分解生成水和氧气,由此书写化学方程式。用甲剂、乙剂和水制取氧气,选择
固液常温型发生装置,所以选B,氧气不易溶于水,密度比空气大,所以连接顺序是c、d、
a、b。故答案为:2H O 2H O+O ↑;B;c、d、a、b;
2 2 2 2
(3)利用分子筛在加压时将空气中的氮气吸收,得到高纯度的氧气,只是把氮气和氧气分
离,没有生成新物质,因此是物理变化。故答案为:物理;
【点评】本题主要考查氧气制取方法,检验验满方法,制取操作中注意事项。
21.(7分)碳是形成化合物种类最多的元素,兴趣小组同学对含碳化合物进行研究。
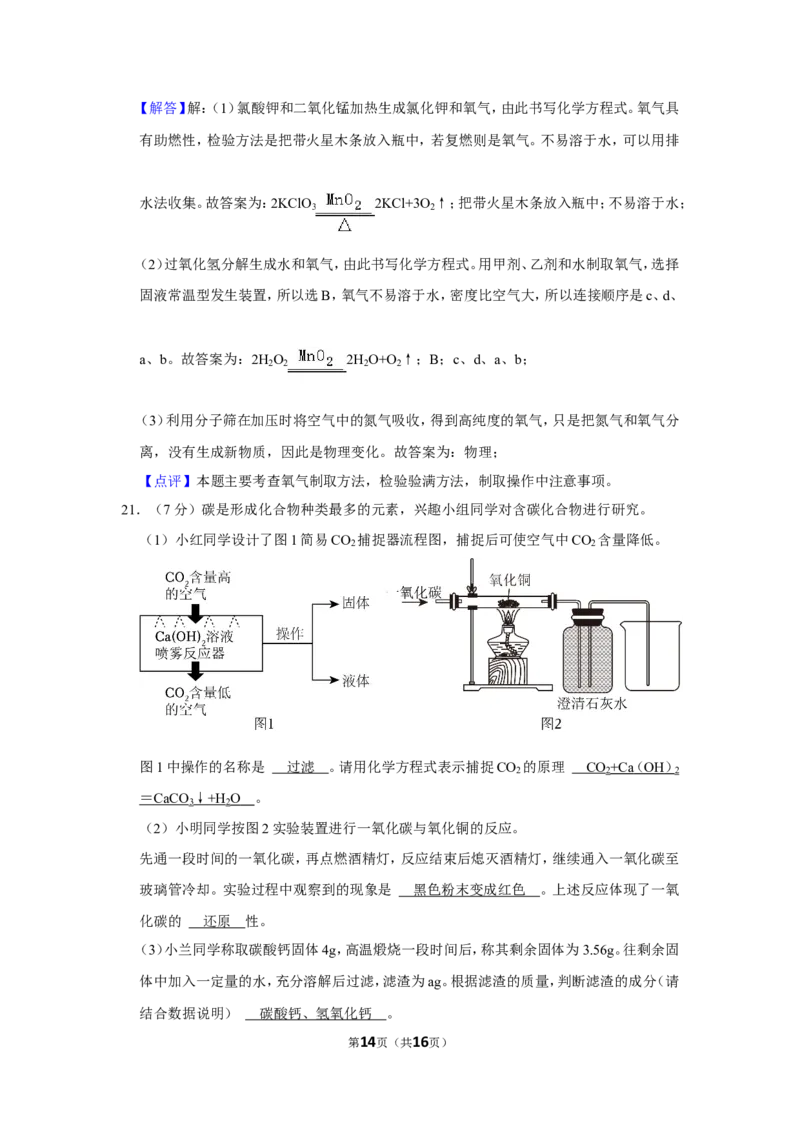
(1)小红同学设计了图1简易CO 捕捉器流程图,捕捉后可使空气中CO 含量降低。
2 2
图1中操作的名称是 过滤 。请用化学方程式表示捕捉CO 的原理 CO +Ca( OH )
2 2 2
= CaCO ↓ +H O 。
3 2
(2)小明同学按图2实验装置进行一氧化碳与氧化铜的反应。
先通一段时间的一氧化碳,再点燃酒精灯,反应结束后熄灭酒精灯,继续通入一氧化碳至
玻璃管冷却。实验过程中观察到的现象是 黑色粉末变成红色 。上述反应体现了一氧
化碳的 还原 性。
(3)小兰同学称取碳酸钙固体4g,高温煅烧一段时间后,称其剩余固体为3.56g。往剩余固
体中加入一定量的水,充分溶解后过滤,滤渣为ag。根据滤渣的质量,判断滤渣的成分(请
结合数据说明) 碳酸钙、氢氧化钙 。
第14页(共16页)【答案】(1)过滤;CO +Ca(OH) =CaCO ↓+H O;
2 2 3 2
(2)黑色粉末变成红色;还原;
(3)碳酸钙、氢氧化钙。
【分析】(1)根据分离混合物的方法、化学反应的原理、流程图信息来分析;
(2)根据在加热时氧化碳还原氧化铜的反应分析回答;
(3)根据碳酸钙高温分解的反应、氧化钙与水的反应分析计算。
【解答】解:(1)过滤是将固体与液体分离的一种操作方法。图中固体和液体分离的操作方
法是过滤;二氧化碳能与氢氧化钙反应生成了碳酸钙和水,流程中是用氢氧化钙溶液捕捉
CO ,反应的化学方程式为:CO +Ca(OH) =CaCO ↓+H O;
2 2 2 3 2
(2)在加热时一氧化碳与氧化铜反应生成了铜和二氧化碳,实验过程中观察到的现象是黑
色粉末变成红色。上述反应中一氧化碳夺取了氧化铜的氧,体现了一氧化碳的还原性。
(3)设4g碳酸钙高温分解生成氧化钙的质量为x。
CaCO CaO+CO ↑
3 2
100 56
4g x
解得:x=2.24g<3.56,说明了碳酸钙没有完全分解,
往剩余固体中加入水中时氧化钙与水反应生成了氢氧化钙,氢氧化钙微溶于水,所以滤渣
的成分有碳酸钙、氢氧化钙。
第15页(共16页)故答案为:(1)过滤;CO +Ca(OH) =CaCO ↓+H O;
2 2 3 2
(2)黑色粉末变成红色;还原;
(3)碳酸钙、氢氧化钙。
【点评】本题的难度不大,熟练掌握二氧化碳、一氧化碳的性质、方程式的书写方法是解答
本题的关键。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布日期:2024/1/17 16:34:14;用户:郭亚红;邮箱:18317538760;学号:45050889
第16页(共16页)