文档内容
专题07 气体制备实验
目录
【题型一】选择题
【题型二】 实验题
题型一 选择题
1.(2023·上海徐汇·统考二模).用启普发生器制备较纯净的氢气,应添加的试剂为
A.锌粒、稀硫酸 B.锌粉、稀硫酸
C.锌粒、浓盐酸 D.锌粉、稀盐酸
【答案】A
【详解】启普发生器应使用块状固体药品,以便于固液分离控制反应的发生和停止。常使用锌和稀硫酸制
取氢气,不是用浓盐酸或稀盐酸,因为盐酸具有挥发性,氢气中会混入氯化氢气体导致制取的气体不纯。
所以选择的药品是锌粒和稀硫酸。故选A。
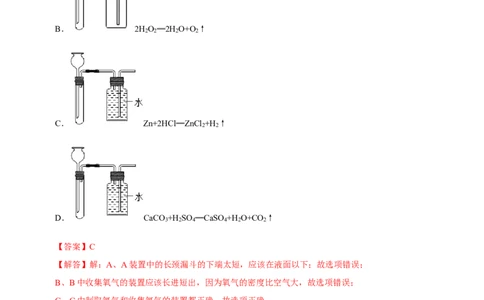
2(2023·上海虹口·统考二模).用如图所示的装置制取二氧化碳,相关分析正确的是( )
A.以碳酸钙粉末和稀盐酸为原料
B.用该方法收集二氧化碳是因为其能溶于水
C.用燃着的木条放入瓶内以检验气体是否收集满
D.关闭k,若固液不分离,可能是某种反应物已消耗完
【答案】D
【解答】解:A、应该用块状的碳酸钙和稀盐酸为原料,不能用碳酸钙粉末和稀盐酸,故A错误;
B、用该方法收集二氧化碳是由于二氧化碳密度比空气的大,故A错误;
C、应该把燃着的木条放在集气瓶口,若木条熄灭,说明收集已满,故C错误;
D、关闭K,若固液不分离,可能是某种反应物已消耗完,故D正确。
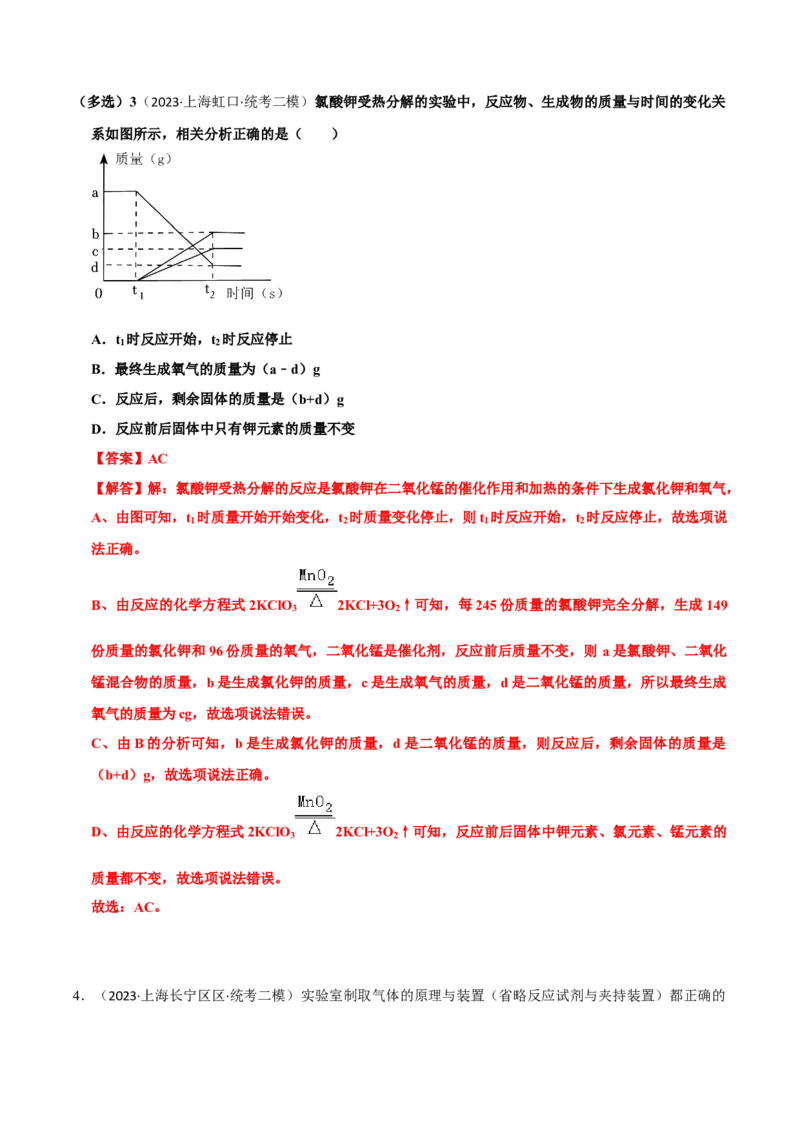
故选:D。(多选)3(2023·上海虹口·统考二模)氯酸钾受热分解的实验中,反应物、生成物的质量与时间的变化关
系如图所示,相关分析正确的是( )
A.t 时反应开始,t 时反应停止
1 2
B.最终生成氧气的质量为(a﹣d)g
C.反应后,剩余固体的质量是(b+d)g
D.反应前后固体中只有钾元素的质量不变
【答案】AC
【解答】解:氯酸钾受热分解的反应是氯酸钾在二氧化锰的催化作用和加热的条件下生成氯化钾和氧气,
A、由图可知,t 时质量开始开始变化,t 时质量变化停止,则t 时反应开始,t 时反应停止,故选项说
1 2 1 2
法正确。
B、由反应的化学方程式2KClO 2KCl+3O ↑可知,每245份质量的氯酸钾完全分解,生成149
3 2
份质量的氯化钾和96份质量的氧气,二氧化锰是催化剂,反应前后质量不变,则 a是氯酸钾、二氧化
锰混合物的质量,b是生成氯化钾的质量,c是生成氧气的质量,d是二氧化锰的质量,所以最终生成
氧气的质量为cg,故选项说法错误。
C、由B的分析可知,b是生成氯化钾的质量,d是二氧化锰的质量,则反应后,剩余固体的质量是
(b+d)g,故选项说法正确。
D、由反应的化学方程式2KClO 2KCl+3O ↑可知,反应前后固体中钾元素、氯元素、锰元素的
3 2
质量都不变,故选项说法错误。
故选:AC。
4.(2023·上海长宁区区·统考二模)实验室制取气体的原理与装置(省略反应试剂与夹持装置)都正确的是( )
A. Mg+2HCl═MgCl +H ↑
2 2
B. 2H O ═2H O+O ↑
2 2 2 2
C. Zn+2HCl═ZnCl +H ↑
2 2
D. CaCO +H SO ═CaSO +H O+CO ↑
3 2 4 4 2 2
【答案】C
【解答】解:A、A装置中的长颈漏斗的下端太短,应该在液面以下;故选项错误;
B、B中收集氧气的装置应该长进短出,因为氧气的密度比空气大,故选项错误;
C、C中制取氢气和收集氢气的装置都正确,故选项正确;
D、实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生
2
成氯化钙和水和二氧化碳,因此不需要加热;碳酸钙和硫酸反应生成的硫酸钙微溶于水,阻碍反应的进
行,因此不能用硫酸。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,不能
用排水法收集;故选项错误;
故选:C。题型二 实验题
1.(2023·上海宝山·统考二模).实验室利用下图装置及仪器制取氧气。
(1)实验室用双氧水和二氧化锰制取氧气,该反应属于___________(填基本反应类型),二氧化锰的作用是
___________,若要平稳收集到较纯的氧气,应选用B装置和仪器____________(填编号)组合成整套制气装
置;
(2)实验室若用氯酸钾和二氧化锰制取氧气,从上图选取合适的装置和仪器外,还需要补充铁架台和
___________(填仪器名称)才能进行实验,该反应的化学方程式为___________,若实验中消耗氯酸钾
0.02mol,理论上可制得氧气___________g;
(3)某同学用氯酸钾制氧气(未加二氧化锰),他用排水集气法收集了2瓶60mL氧气,集气中该同学发现第2
瓶氧气集满所用的时间明显少于第1瓶,除了温度对反应的影响外,你认为还可能的原因是___________。
【答案】(1) 分解反应 催化作用 DFGH
(2) 酒精灯
0.96
(3)可能是氯酸钾分解生成的氯化钾对反应有催化作用
【详解】(1)过氧化氢在二氧化锰的催化下分解为水和氧气,该反应符合“一变多”的特点,属于分解
反应;
在该反应中,二氧化锰是催化剂,起到催化作用;
该反应属于固液不加热反应,要想得到平稳的气流,发生装置应选BD,可通过分液漏斗控制液体的滴加速
率,从而控制反应速率,氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,排水法收集
的氧气比较纯净,故收集装置可选FGH,故填:DFGH;
(2)实验室若用氯酸钾和二氧化锰制取氧气,该反应属于固体加热反应,故还需要补充酒精灯作热源;
氯酸钾在二氧化锰的催化下受热分解生成氯化钾和氧气,该反应的化学方程式为:;
0.02mol氯酸钾的质量为:0.02mol×122.5g/mol=2.45g
解:设理论上可制得氧气的质量为x
x=0.96g
答:理论上可制得氧气的质量为0.96g
(3)氯酸钾受热分解生成氯化钾和氧气,第2瓶氧气集满所用的时间明显少于第1瓶,故除了温度对反应
的影响外,还可能是氯酸钾分解生成的氯化钾对反应有催化作用。
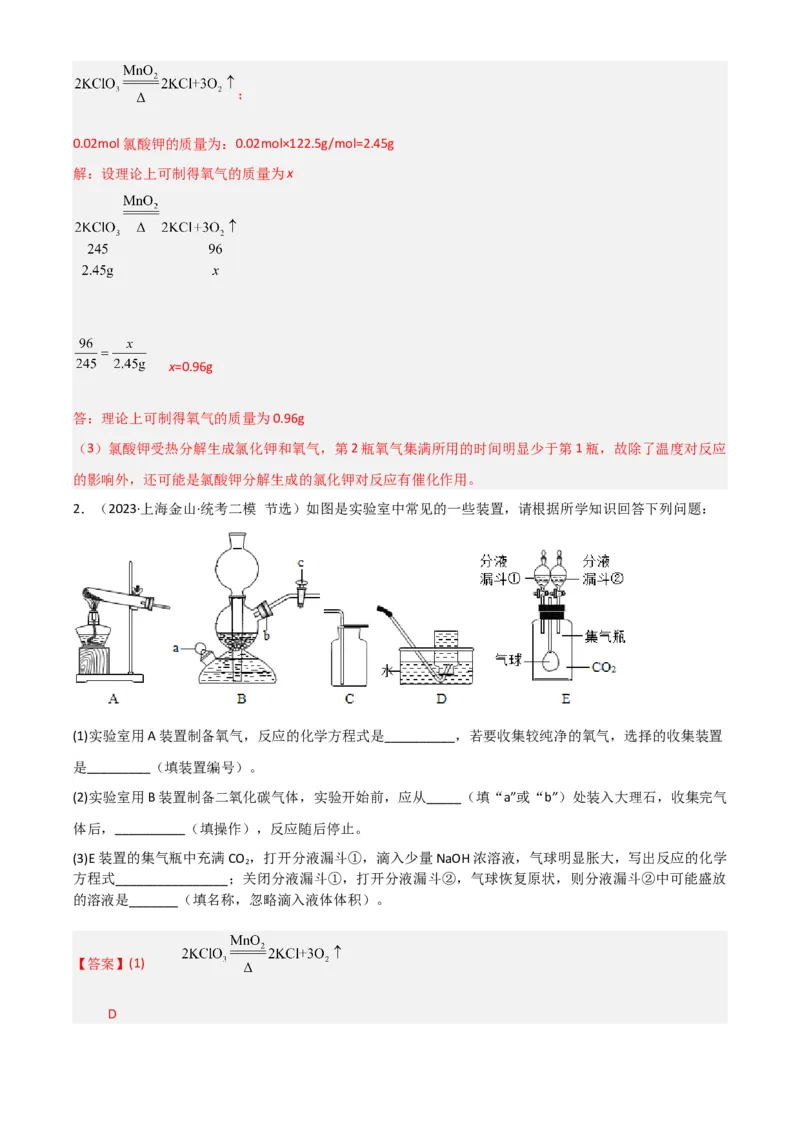
2.(2023·上海金山·统考二模 节选)如图是实验室中常见的一些装置,请根据所学知识回答下列问题:
(1)实验室用A装置制备氧气,反应的化学方程式是__________,若要收集较纯净的氧气,选择的收集装置
是_________(填装置编号)。
(2)实验室用B装置制备二氧化碳气体,实验开始前,应从_____(填“a”或“b”)处装入大理石,收集完气
体后,__________(填操作),反应随后停止。
(3)E装置的集气瓶中充满CO ,打开分液漏斗①,滴入少量NaOH浓溶液,气球明显胀大,写出反应的化学
2
方程式________________;关闭分液漏斗①,打开分液漏斗②,气球恢复原状,则分液漏斗②中可能盛放
的溶液是_______(填名称,忽略滴入液体体积)。
【答案】(1)
D(2) b 关闭活塞c
(3)
稀盐酸等(合理即可)
【详解】(1)实验室用装置A制备氧气,反应物应为固体且需要加热,又由于试管口未放置一团棉花,
选用的药品为氯酸钾和二氧化锰,氯酸钾在二氧化锰催化和加热的条件下反应生成氯化钾和氧气,反应的
化学方程式为: ;氧气密度比空气大,不易溶于水且不与水反应,可选用向上
排空气法和排水法收集,排水法收集的气体更纯净,因此收集装置选D;
(2)用装置B制备二氧化碳,实验开始前,应从b处装入大理石,从长颈漏斗上端加入稀盐酸,反应物一
接触立即产生气体,收集完气体后,关闭活塞c,装置B中压强增大,将稀盐酸“压”回长颈漏斗中,反
应物分离,反应随后停止;
3(2023·上海嘉定·统考二模).根据下图回答问题。
(1)A中现象是迅速涌出柱状的泡沫,可形象地称为“大象牙膏”,其原理主要是H O 在某些催化剂作用下
2 2
迅速分解产生水和氧气,反应的化学方程式为_______。
(2)实验室用B装置制取二氧化碳,从长颈漏斗中加入的药品为_______。可用装置C收集二氧化碳,该收
集气体方法的名称是_______。实验室若用装置D制二氧化碳,关闭弹簧夹后,容器内压强_______(选填
“>”、“=”或“<”表示)容器外压强。
(3)0.lmol碳酸钙和足量稀盐酸完全反应,生成二氧化碳的质量是_______克。
【答案】(1)(2) 稀盐酸 向上排空气法 >
(3)4.4
【详解】(1)H O 在催化剂作用下分解产生水和氧气,化学方程式为: ;
2 2
(2)实验室用稀盐酸和石灰石制取二氧化碳,用B装置作发生装置时,从长颈漏斗中加入的药品为稀盐
酸;二氧化碳密度比空气大,装置C的导气管伸入正放在桌面上的集气瓶底部,可用来收集二氧化碳气体,
该收集气体方法的名称是向上排空气法;实验室若用装置D制取二氧化碳,关闭弹簧夹后,反应仍然进行,
继续产生气体,容器内压强增大,把液体药品压回到长颈漏斗中,直到液体与固体不再接触,反应停止,
故容器内压强>容器外压强;
(3)设0.lmol碳酸钙和足量稀盐酸完全反应,生成二氧化碳的质量是x,0.lmol碳酸钙的质量为
, , ,生成二氧化碳的质量是
4.4g。
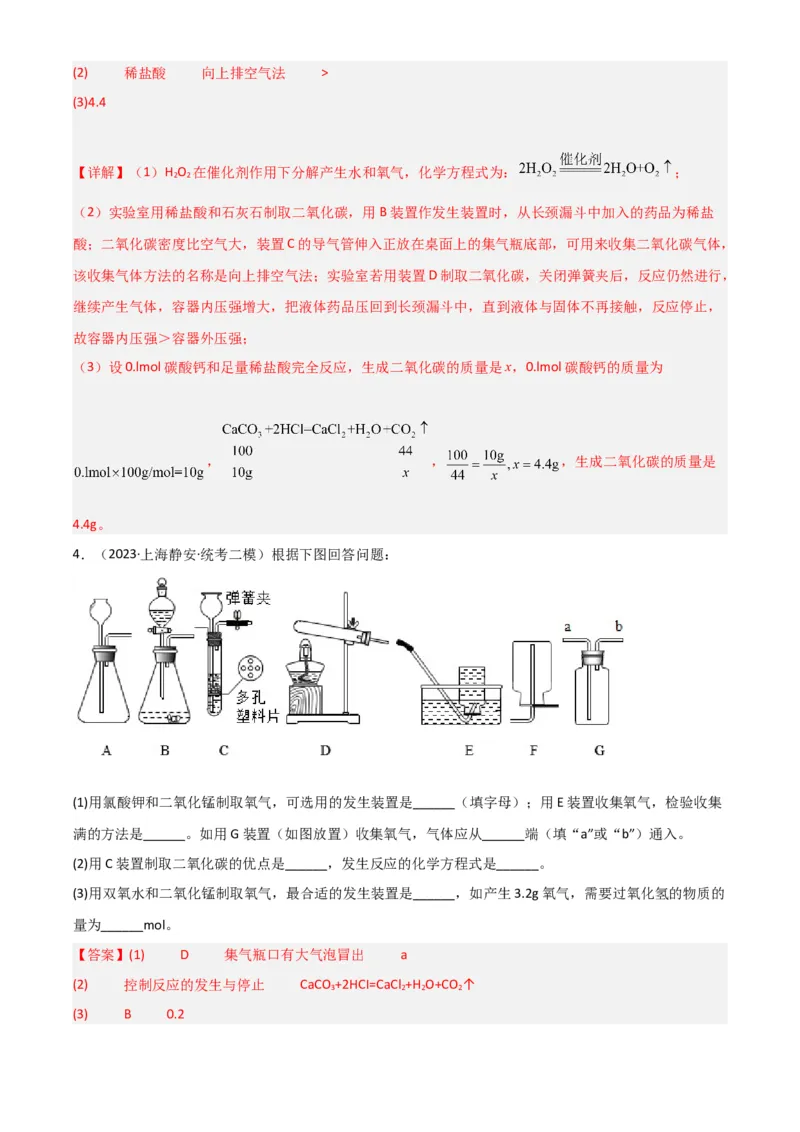
4.(2023·上海静安·统考二模)根据下图回答问题:
(1)用氯酸钾和二氧化锰制取氧气,可选用的发生装置是______(填字母);用E装置收集氧气,检验收集
满的方法是______。如用G装置(如图放置)收集氧气,气体应从______端(填“a”或“b”)通入。
(2)用C装置制取二氧化碳的优点是______,发生反应的化学方程式是______。
(3)用双氧水和二氧化锰制取氧气,最合适的发生装置是______,如产生3.2g氧气,需要过氧化氢的物质的
量为______mol。
【答案】(1) D 集气瓶口有大气泡冒出 a
(2) 控制反应的发生与停止 CaCO +2HCI=CaCl +H O+CO ↑
3 2 2 2
(3) B 0.2【详解】(1)氯酸钾制取氧气的反应为加热固体的反应,则发生装置选D;
E装置为排水法收集装置,当集气瓶口用大气泡冒出时,则说明已收集满;
氧气密度比空气大,若用装置G收集,则气体应从a端通入。
(2)C装置中,将固体放在多孔塑料板上,关闭弹簧夹,产生的气体无法排出,装置中的压强增大,液体
被压入长颈漏斗中,固液分离,反应停止,则该装置的优点为控制反应的发生与停止或者随开随用,随关
随停;
实验室制取二氧化碳的反应为碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为
。
(3)双氧水和二氧化锰的反应为固液常温装置,由于二氧化锰为粉末状,且B装置能通过分液漏斗控制
液体的滴加速度,从而控制反应速率,则最合适的发生装置是B;
设需要过氧化氢的质量为x,则
解得x=6.8g
则需要过氧化氢的物质的量为 。
5.(2023·上海浦东新区·统考二模)实验小组探究影响H O 溶液对化学反应速率的因素。
2 2
(1)用H O 溶液和MnO制取较纯氧气,为使反应平稳进行,可选择的发生装置如图中的______,采用的收
2 2
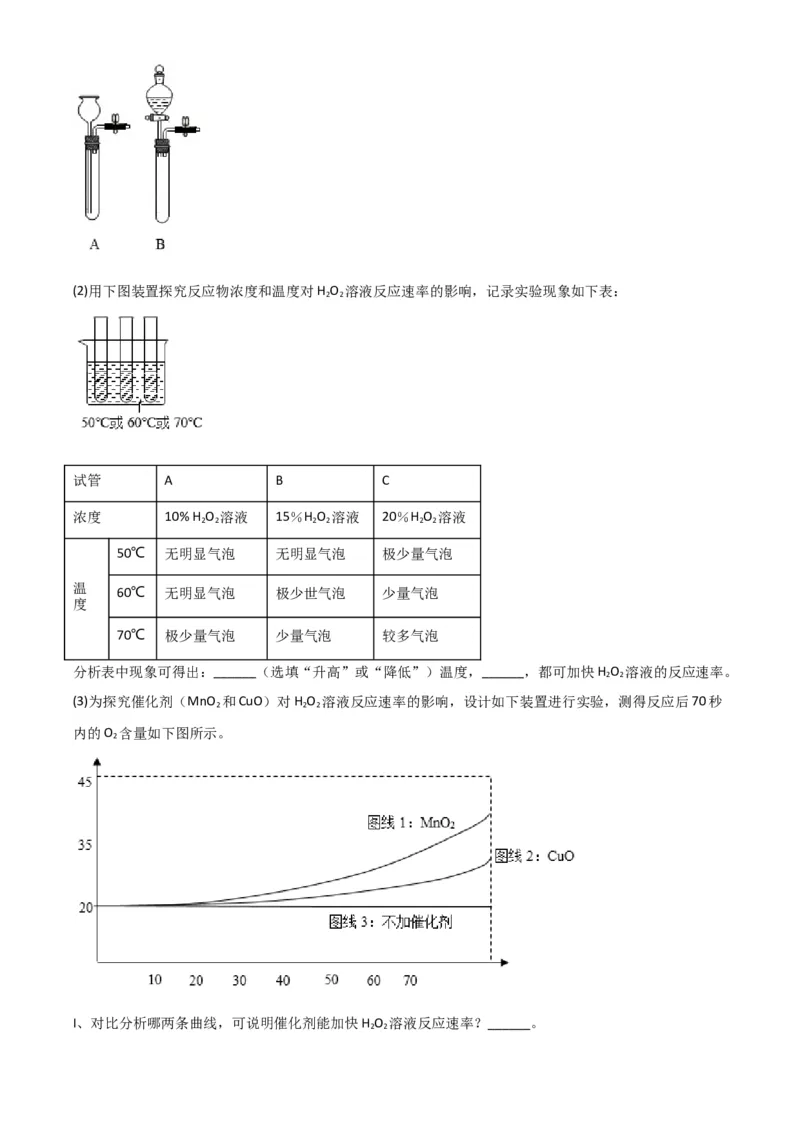
集方法是______,发生反应的化学方程式为______。(2)用下图装置探究反应物浓度和温度对H O 溶液反应速率的影响,记录实验现象如下表:
2 2
试管 A B C
浓度 10% H O 溶液 15%H O 溶液 20%H O 溶液
2 2 2 2 2 2
50℃ 无明显气泡 无明显气泡 极少量气泡
温
60℃ 无明显气泡 极少世气泡 少量气泡
度
70℃ 极少量气泡 少量气泡 较多气泡
分析表中现象可得出:______(选填“升高”或“降低”)温度,______,都可加快H O 溶液的反应速率。
2 2
(3)为探究催化剂(MnO 和CuO)对H O 溶液反应速率的影响,设计如下装置进行实验,测得反应后70秒
2 2 2
内的O 含量如下图所示。
2
I、对比分析哪两条曲线,可说明催化剂能加快H O 溶液反应速率?______。
2 2II、和CuO相比,MnO 能使H O 分解得更快,判断依据是______。
2 2 2
【答案】(1) B 排水法
(2) 升高 增大过氧化氢溶液浓度
(3) 图3和图1或图3和图2 相同的时间内,加入MnO 装置内的氧气浓度大于加入CuO装置内的
2
氧气浓度
【详解】(1)过氧化氢在二氧化锰催化作用下分解生成水和氧气,该反应的反应物是固体和液体,不需
加热,发生装置可用固、液混合不加热型,发生装置可用A或B,B装置中的分液漏斗能控制液体的滴加
速率,从而能控制反应速率,用H O 溶液和MnO制取较纯氧气,为使反应平稳进行,可选择的发生装置
2 2
如图中的B;氧气密度大于空气,不易溶于水,可用向上排空气法收集或排水法收集,排水法收集的气体
较纯,收集氧气的装置是排水法;反应的化学方程式是: ;
(2)分析表中现象可得出:升高温度(C管在不同温度的实验现象),增大过氧化氢溶液浓度(70℃时,
A、B、C三试管的实验现象),都可加快H O 溶液的反应速率。
2 2
(3)I、说明催化剂能加快H O 溶液反应速率需作对比实验,在相同条件下,一个实验不加催化剂,一个
2 2
实验加入催化剂比较两个实验的反应速率,因此对比分析图3和图1或图3和图2,可说明催化剂能加快
H O 溶液反应速率;
2 2
II、和CuO相比,MnO 能使H O 分解得更快,判断依据是相同的时间内,加入MnO 装置内的氧气浓度大
2 2 2 2
于加入CuO装置内的氧气浓度。
6.(2023·上海松江区·统考二模)结合下列装置回答问题。
(1)实验室用双氧水和二氧化锰制取氧气,反应的化学方程式是______,选择能控制反应速率的发生装置是
______(填装置序号),收集方法是______。(2)装置B中加入大理石和稀盐酸制取二氧化碳,导气管与装置D中______(选填“m”或“n”)端相连。
(3)图中装置B的活塞处于______(选填“开启”或“关闭”)状态。
(4)实验结束后,分别倒出B中的固体和溶液,测得固体质量比反应前的固体质量小,则减少的质量______
(选填“大于”、“小于”或“等于”)生成的二氧化碳质量;为确定倒出的溶液成分,往该溶液中滴加
碳酸钠溶液,观察到有气泡生成,可知溶液中溶质是______。
【答案】(1) C 向上排空气法/排水集气法
(2)m
(3)关闭
(4) 大于 CaCl 、HCl
2
【详解】(1)过氧化氢在催化剂二氧化锰催化作用下分解生成水和氧气,反应的化学方程式是
;装置A、B、C都属于固液常温型,装置A不能控制反应速率;装置B能控制反
应发生和停止,且药品为固体颗粒和液体,而实验室用双氧水和二氧化锰制氧气,二氧化锰为粉末;装置
C能通过分液漏斗的活塞控制液体药品的滴加速率,从而控制反应速率,故选择能控制反应速率的发生装
置是C;氧气的密度比空气略大,不易溶于水,故收集方法可用向上排空气法和排水法。
(2)因为二氧化碳的密度比空气大,用向上排空气法收集是,导气管与装置D中m端相连。
(3)装置B中液体和固体没有接触,说明活塞处于关闭状态。
(4)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,氯化钙溶于水,所以反应后固体减少的质量是碳酸
钙的质量,由化学方程式 可知,100>44,故减少的质量(反应的碳酸
钙质量)大于生成的二氧化碳质量;
向倒出的溶液中滴加碳酸钠溶液,有气泡生成,说明是碳酸钠和盐酸反应氯化钠、水和二氧化碳,故倒出
的溶液中溶质是反应生成的氯化钙和过量的氯化氢。7.(2023·上海徐汇区·统考二模)实验室中常用H O 溶液制各氧气,用下图所示的装置和下表所示的实验
2 2
探究获得平稳气流的方法。
实验编号 试剂 温度(℃) 收集一瓶气体的时间(秒)
① 50mL 5%H O 溶液 5g MnO 20 12
2 2 2
② XmL 3%H O 溶液 5g MnO 20 61
2 2 2
③ 50mL 5%H O 溶液 5g MnO 50 7
2 2 2
④ 50mL 5%H O 溶液 5g CuCl 20 31
2 2 2
⑤ 50mL 5%H O 溶液 5g FeCl 溶液 20 48
2 2 3
(1)写出实验①中制备氧气的化学方程式__________。
(2)用排水法收集氧气,是因为氧气__________(选填“易”或“不易”)溶于水。上图装置中导管a应与
导管__________(选填“b”或“c”)相连接。
(3)若用实验①和②比较H O 的浓度对生成气流快慢的影响,则实验②中应加入H O 溶液的体积为
2 2 2 2
__________mL。
(4)从实验_________(填实验编号)可比较温度对生成气流快慢的影响,得到结论:温度越高,生成气流
越_______(选填“快”或“慢”)。
(5)实验④和⑤能否用于比较不同盐酸盐对H O 分解的催化效果?理由是________。
2 2
【答案】(1)
(2) 不易 c
(3)50(4) / 快
(5)不能,①实③验④③用①的是氯化铜固体,而实验⑤加入氯化铁溶液会稀释H O 溶液,没有控制变量
2 2
【详解】(1)H O 溶液在MnO 的催化作用下生成水和氧气,化学方程式 。
2 2 2
(2)由于氧气不易溶于水,所以图中装置中导管a应与导管c相连接。
(3)根据实验①、②的目的是探究H O 浓度对反应速率的影响,除了双氧水的浓度不同外,其它条件完
2 2
全相同。则则实验②中应加入H O 溶液的体积为50mL。
2 2
(4)从实验①③可比较温度对生成气流快慢的影响,得到结论:温度越高,生成气流越快。
(5)由于实验④用的是氯化铜固体,而实验⑤加入氯化铁溶液会稀释H O 溶液,没有控制变量,所以实
2 2
验④和⑤不能用于比较不同盐酸盐对H O 分解的催化效果。
2 2
8.(2023·上海黄埔区·统考二模) 如图是实验室常用的气体发生装置。
(1)双氧水和二氧化锰混合制取氧气的化学方程式是______;反应的基本类型是______;收集氧气可以
用向上排气法,该方法所利用的氧气的物理性质是______。
的
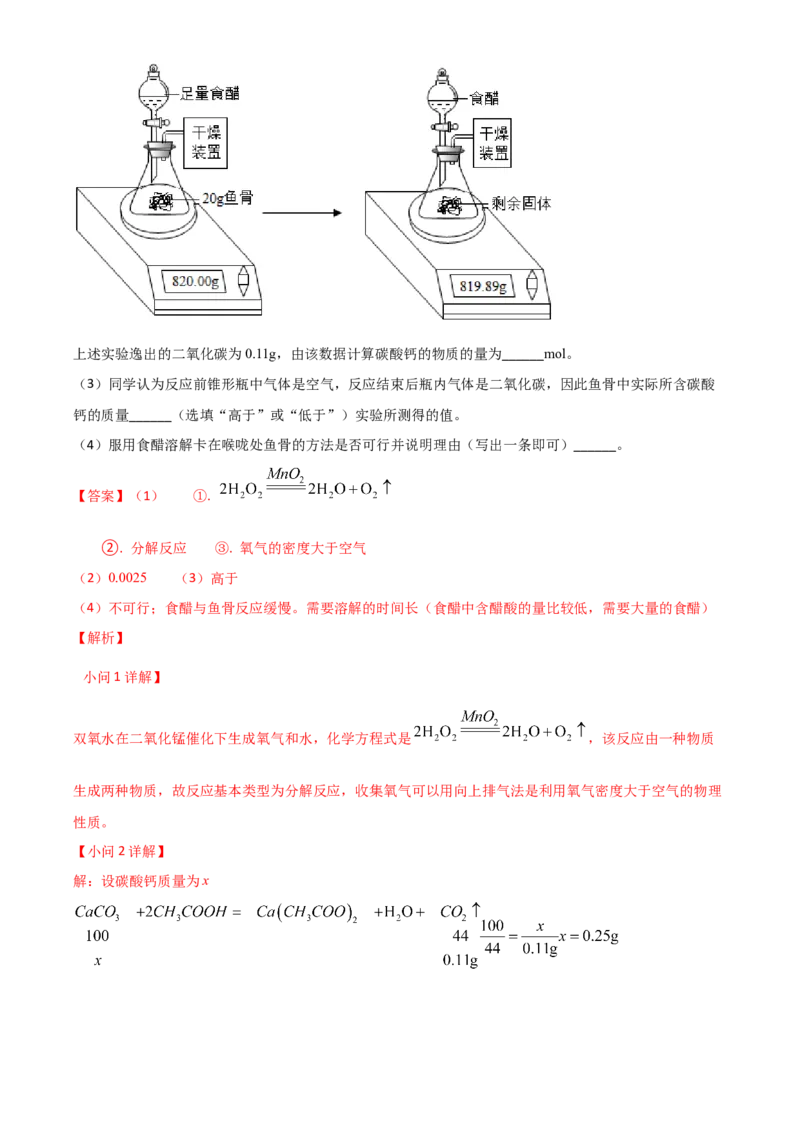
(2)下图是测定某鱼骨中碳酸钙质量 实验。取20g鱼骨加入锥形瓶中,放在电子天平上称量;加入足量
食醋,约20小时后至气泡不再产生,再次称量,记录数据。(食醋中主要成分醋酸与碳酸钙反应,生成可
溶性的醋酸钙、水和二氧化碳。干燥装置只吸收水)上述实验逸出的二氧化碳为0.11g,由该数据计算碳酸钙的物质的量为______mol。
(3)同学认为反应前锥形瓶中气体是空气,反应结束后瓶内气体是二氧化碳,因此鱼骨中实际所含碳酸
钙的质量______(选填“高于”或“低于”)实验所测得的值。
(4)服用食醋溶解卡在喉咙处鱼骨的方法是否可行并说明理由(写出一条即可)______。
【答案】(1) ①.
②. 分解反应 ③. 氧气的密度大于空气
(2)0.0025 (3)高于
(4)不可行;食醋与鱼骨反应缓慢。需要溶解的时间长(食醋中含醋酸的量比较低,需要大量的食醋)
【解析】
【
小问1详解】
双氧水在二氧化锰催化下生成氧气和水,化学方程式是 ,该反应由一种物质
生成两种物质,故反应基本类型为分解反应,收集氧气可以用向上排气法是利用氧气密度大于空气的物理
性质。
【小问2详解】
解:设碳酸钙质量为x已知碳酸钙相对分子质量为100,质量为0.25g,物质的量等于质量与相对分子质量的比值,故相对分子质
量为0.0025mol。
【小问3详解】
由于二氧化碳密度大于空气,因此第二次称量的剩余固体质量数值偏大 (反应生成的二氧化碳不能完全溢
出瓶外),计算溢出的二氧化碳质量比实际产生的偏小,所以鱼骨中实际所含碳酸钙的质量高于实验所测得
的值。
【小问4详解】
不可行;食醋与鱼骨反应缓慢。需要溶解的时间长,或者由实验可知,食醋不能完全溶解鱼骨头。(其他答
案合理亦可)