文档内容
专题10 物质的检验、除杂、鉴别
目录
【题型一】物质的检验与鉴别
【题型二】 物质的除杂
题型一 物质的检验与鉴别
1.(2023·上海宝山·统考二模)灼烧时火焰呈紫色的物质是
A.Na CO B.CuSO C.KNO D.CaCl
2 3 4 3 2
【答案】C
【分析】焰色反应是元素的性质;
【详解】A、钠元素焰色反应的颜色为黄色,故A错误;
B、铜元素焰色反应的颜色为绿色,故B错误;
C、钾元素焰色反应的颜色为紫色(透过蓝色钴玻璃观察),故C正确;
D、钙元素焰色反应的颜色为砖红色,故D错误。
故选C。
2.(不定向)(2023·上海宝山·统考二模 )不能用来鉴别盐酸和稀硫酸的试剂是( )
A.BaCl B.Zn C.AgNO D.Ba(NO )
2 3 3 2
【答案】BC
【详解】A.加入BaCl 溶液能够和硫酸反应生成白色沉淀,而盐酸不能反应,故A可以鉴别;
2
B.Zn和稀盐酸、稀硫酸都能反应有气泡产生,故B不能鉴别;
C.AgNO 溶液与二者反应分别生成氯化银和硫酸银都是白色沉淀,故C不能鉴别;
3
D. Ba (NO ) 溶液能够和硫酸反应生成白色沉淀,而盐酸不能反应,故D可以鉴别。
3 2
故选:BC
【点睛】区别同类物质时要从不同点出发,而不是找共性和利用共性.硫酸和盐酸同样都是酸,所以如果
利用共性,如果现象是相同的,就无法进行区别.所以要通过个性来进行实验和区别。
3.(2023·上海徐汇·统考二模).能鉴别Na CO 溶液和Na SO 溶液的试剂是
2 3 2 4
A.氯化钡溶液 B.硝酸钾溶液 C.氯化钠溶液 D.稀硫酸
【答案】D
【详解】A、氯化钡与碳酸钠反应生成白色碳酸钡沉淀和氯化钠,与硫酸钠反应生成白色硫酸钡沉淀和氯
化钠。将氯化钡分别加入到Na CO 溶液和Na SO 溶液中,都产生白色沉淀,现象相同,不能鉴别,不符合
2 3 2 4题意;
B、硝酸钾溶液不能Na CO 溶液、Na SO 溶液发生反应,将硝酸钾溶液分别加入到Na CO 溶液和Na SO 溶
2 3 2 4 2 3 2 4
液中,都没有明显实验现象,现象相同,不能鉴别,不符合题意;
C、氯化钠溶液不能Na CO 溶液、Na SO 溶液发生反应,将硝酸钾溶液分别加入到Na CO 溶液和Na SO 溶
2 3 2 4 2 3 2 4
液中,都没有明显实验现象,现象相同,不能鉴别,不符合题意;
D、稀硫酸与碳酸钠反应产生硫酸钠、水和二氧化碳,不能与硫酸钠反应,将稀硫酸分别加入到Na CO 溶
2 3
液和Na SO 溶液中,产生气泡的是碳酸钠,无明显变化的是硫酸钠溶液,符合题意。
2 4
故选D。
4.(2023·上海松江·统考二模).焰色反应火焰呈黄色的是
A.CaCl B.K CO C.NaNO D.BaCl
2 2 3 3 2
【答案】C
【详解】A、CaCl 含钙元素,焰色反应为砖红色,不符合题意;
2
B、K CO 含钾元素,焰色反应为紫色,不符合题意;
2 3
C、NaCl含钠元素,焰色反应为黄色,符合题意;
D、BaCl 含钡元素,焰色反应为黄绿色,不符合题意。
2
故选:C。
5.(2023·上海松江·统考二模).下列方法可达到实验目的的是
A.用燃着的木条鉴别N 和CO B.用水鉴别NaCl固体和CuSO 固体
2 2 4
C.用稀盐酸除去CaO中混有的CaCO 杂质 D.用酚酞试液鉴别Na CO 溶液和NaOH溶液
3 2 3
【答案】B
【详解】A、二氧化碳和氮气均不燃烧、不支持燃烧,均能使燃着的木条熄灭,现象相同,无法区分,故
选项A不符合题意;
B、氯化钠溶于水形成无色溶液,硫酸铜溶于水形成蓝色溶液,现象不同,可以区分,故选项B符合题意;
C、氧化钙和稀盐酸反应生成氯化钙和水,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,不但除去了
杂质,也除去了原物质,故选项C不符合题意;
D、碳酸钠溶液和氢氧化钠溶液都呈碱性,都能使无色酚酞试液变红,现象相同,无法区分,故选项D不
符合题意;
故选:B。
6.(2023·上海金山·统考二模)能鉴别氢氧化钠溶液和氢氧化钙溶液的试剂是
A.酚酞试液 B.稀盐酸 C.碳酸钠溶液 D.硫酸铜溶液【答案】C
【详解】试题分析:鉴别物质所加试剂后要出现不同的现象,A选项氢氧化钠和氢氧化钙溶液都能使酚酞
试液变红色;B选项稀盐酸与二者反应无明显现象;C选项碳酸钠与氢氧化钠不反应,与氢氧化钙反应生
成沉淀;C选项二 者都能生成蓝色沉淀;故答案选择C
7.(2023·上海长宁区区·统考二模))能鉴别稀硫酸和水的物质是( )
A.酚酞试液 B.氢氧化钠溶液
C.无水硫酸铜粉末 D.碳酸钠溶液
【答案】D
【解答】解:A、稀硫酸和水分别显酸性、中性,均不能使无色酚酞溶液变色,不能鉴别,故选项错误。
B、氢氧化钠溶液与稀硫酸反应生成硫酸钠和水,但无明显现象,溶于水无明显现象,不能鉴别,故选
项错误。
C、无水硫酸铜粉末遇水变蓝色,无水硫酸铜粉末遇稀硫酸、水均变蓝色,不能鉴别,故选项错误。
D、碳酸钠溶液与稀硫酸反应生成硫酸钠、水和二氧化碳,加入水中无明显现象,可以鉴别,故选项正
确。
故选:D。
题型二 物质的除杂
1.(2023·上海杨浦·统考二模)除去下列各组物质中的杂质,方法正确的是
选项 实验目的 实验方法
A 除去CO 中的H O 氢氧化钠固体
2 2
B 除去CaCl 溶液中少量HCl 加过量的碳酸钙后过滤
2
C 除去NaCl溶液中少量KNO 降温结晶后过滤
3
D 除去H 中的CO 通过灼热的CuO
2
A.A B.B C.C D.D
【答案】B
【详解】A.氢氧化钠固体不但能吸收水分,还能与二氧化碳反应,不但能把杂质除去,也会把主要物质除
去,不符合除杂原则,故说法错误;
B.HCl能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故说法正确;
C.氯化钠、硝酸钾的溶解度均随温度的升高而增加,硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受
温度影响较小,故除去氯化钠溶液中少量硝酸钾,可采取蒸发结晶的方法,故说法错误;
D.一氧化碳和氢气都能与灼热的氧化铜反应,不但能把杂质除去,也会把主要物质除去,不符合除杂原则,
故说法错误。
故选B。
2.(不定向)(2023·上海浦东新区·统考二模)能达到实验目的的是
选项 实验目的 实验操作
A 鉴别O 和CO 燃着的木条伸入瓶中
2 2
B 除去CO中的CO 通过灼热的氧化饲
2
C 鉴别稀硫酸和稀盐酸 加入氯化钡溶液
D 除去NaOH中的Na CO 加入足量的稀盐酸
2 3
A.A B.B C.C D.D
【答案】AC
【详解】A、氧气具有助燃性,能使燃着木条燃烧更旺,二氧化碳不能燃烧也不能支持燃烧,燃着的木条
伸入瓶中燃烧更旺的是氧气,熄灭的二氧化碳,正确;
B、一氧化碳与氧化铜在加热条件下生成铜和二氧化碳,混合气体通过灼热氧化铜后,消耗一氧化碳,得
到二氧化碳气体,不能达到实验目的,错误;
C、氯化钡与稀硫酸反应生成硫酸钡沉淀,与稀盐酸不能反应,将氯化钡溶液分别加入稀硫酸和稀盐酸中,
产生白色沉淀的是稀硫酸,无明显变化的是稀盐酸,现象不同可以鉴别,正确;
D、稀盐酸都能与NaOH、Na CO 反应,混合物加入足量的稀盐酸,不但将杂质消耗,也将混合物中的主要
2 3
物质消耗,不能达到实验目的,错误。
故选AC。
3.(2023·上海闵行·统考二模)对应的实验操作能达到实验目的的是
选
实验目的 实验操作
项
A 鉴别稀盐酸和稀硫酸 取样,分别滴加AgNO 溶液
3B 证明中和反应放出热量 将NaOH固体放入稀盐酸中
C 检验CO 中是否混有HCl 将气体通入紫色石蕊试液中
2
D 除去Cu粉中混有的少量CuO 加入过量的稀H SO ,过滤
2 4
A.A B.B C.C D.D
【答案】D
【详解】A、硝酸银和盐酸反应生成氯化银沉淀和硝酸,硝酸银和硫酸生成微溶于水的硫酸银沉淀和硝酸,
因此都会出现浑浊现象,无法鉴别,选项错误;;
B、氢氧化钠固体溶于水时也会放热,因此氢氧化钠固体放入盐酸中无法判断是否为中和反应放出的热,
选项错误;
C、二氧化碳与水反应生成碳酸,碳酸显酸性能使石蕊变红,而氯化氢溶于水形成盐酸显酸性能使石蕊变
红,因此无法检验二氧化碳中是否含有氯化氢,选项错误;
D、氧化铜可以和过量的稀硫酸反应生成硫酸铜和水,因此过滤后可以除去铜中的氧化铜,选项正确;
故选:D。
4(不定向)(2023·上海静安·统考二模)某溶液中含Cu(NO ) 、Ba(NO ) 、AgNO ,三种溶质,为使
3 2 3 2 3
上述三种物质分别转化为沉淀,并将沉淀逐一分离出来,现提供①Na SO 溶液②稀盐酸 ③NaOH溶液三
2 4
种试剂。那么所加试剂先后顺序是
OH C1 NO SO CO
3 4 3
微
Ag --- 不 溶 不
溶
A.①②③ B.②③① C.②①③ D.①③②
【答案】BC
【详解】由于氯化银为沉淀,而硫酸银微溶,则最好先将银离子转化为沉淀,即先加入稀盐酸,又由于硝
酸铜能与氢氧化钠生成氢氧化铜沉淀,硝酸钡能与硫酸钠反应生成硫酸钡沉淀,两种试剂能分别将硝酸铜
和硝酸钡转化为沉淀,则硫酸钠和氢氧化钠的顺序不要求,故选BC。
5.(2023·上海嘉定·统考二模)下列除杂或鉴别方法正确的是选
实验目的 实验方法
项
A 除去CaCl 溶液中少量的Ca(OH) 加入过量盐酸、充分反应后过滤
2 2
B 除去盐酸中的少量H SO 加入适量的硝酸钡,充分反应后过滤
2 4
分别点燃,在火焰上方罩一内壁涂有澄清石灰水的烧
C 鉴别CO和CH
4 杯
D 鉴别Ba(OH) 、NaOH、稀盐酸三种溶液 取样,分别加入碳酸钠溶液
2
A.A B.B C.C D.D
【答案】D
【详解】A、除去CaCl 溶液中少量的Ca(OH) ,加入过量盐酸,盐酸和氢氧化钙反应生成氯化钙和水,除去
2 2
了氢氧化钙,引入新杂质盐酸,方法错误;
B、除去盐酸中的少量H SO ,加入适量的硝酸钡,硫酸和硝酸钡反应生成硝酸和硫酸钡沉淀,除去了硫酸,
2 4
引入新杂质硝酸,方法错误;
C、鉴别CO和CH ,分别点燃,在火焰上方罩一内壁涂有澄清石灰水的烧杯,一氧化碳和甲烷点燃后都生
4
成二氧化碳,都可以使火焰上方烧杯内壁涂的澄清石灰水变浑浊,方法错误;
D、鉴别Ba(OH) 、NaOH、稀盐酸三种溶液,取样分别加入碳酸钠溶液,氢氧化钡和碳酸钠反应生成碳酸钡
2
沉淀和氢氧化钠;氢氧化钠和碳酸钠不反应;稀盐酸和碳酸钠反应生成氯化钠、二氧化碳和水,可以观察
到有气泡产生;方法正确;
故选:D。
6(2023·上海虹口·统考二模)能够达成实验目的的是( )
A.用生石灰干燥二氧化碳
B.用灼热的氧化铜除去氢气中的水蒸气
C.用氯化钡溶液鉴别稀盐酸和稀硫酸
D.用二氧化碳鉴别氯化钠溶液和氯化钾溶液
【答案】C
【解答】解:A、氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,不能
用氧化钙干燥二氧化碳,该选项不正确。
B、加热时氧化铜和氢气反应生成铜和水,除去了原物质氢气,该选项不正确。
C、氯化钡不能和稀盐酸反应,和稀硫酸反应生成硫酸钡沉淀和盐酸,该选项正确。D、二氧化碳不能和氯化钠、氯化钾反应,不能鉴别两种物质,该选项不正确。
故选:C。
二.实验题
1.(2023·上海松江区·统考二模).某化工厂的废水中可能含有硫酸、盐酸中的一种或两种。为确定其中的
酸,设计如下实验方案:
(1)
实验步骤 实验现象 实验结论
I、取少量废水于试管中,滴加紫色石蕊试液 ______
II、另取少量废水于试管中,滴加______溶液,静置 无明显现象 废水中只含有盐酸
III、在步骤II后的溶液中,滴加______溶液。 ______
(2)步骤III中发生反应的化学方程式为______。
(3)上述方案中,______实验步骤可以省略。
A.无 B.I C.II D.III
【答案】(1) 溶液变红 硝酸钡/Ba(NO ) 硝酸银/AgNO 生成白色沉淀
3 2 3
(2)
(3)B
【详解】(1)I、硫酸、盐酸都呈酸性,紫色石蕊试液遇酸性溶液变红,故可观察到试管中溶液变红;
II、根据实验结论及实验现象可知,步骤II的目的是检验废水中是否含有硫酸(硫酸根),为了不影响对氯
离子的检验,滴加的试剂中不能含有氯元素,故选用硝酸钡溶液;
III、该步骤的目的是检验氯离子,向溶液中滴加硝酸银溶液,有白色沉淀生成,说明含有盐酸;
(2)步骤III中发生的反应为,盐酸与硝酸银反应,生成氯化银沉淀、硝酸,反应的化学方程式为:
;
(3)实验的目的是确定废水中酸的种类,石蕊试液只能检验出废水中是否含有酸性物质,而实验开始前,
已经确定废水中含有酸性物质,故步骤I是多余的,可省略,故选B。2. (2023·上海黄埔区·统考二模). 某溶液M中可能含氢氧化钠、碳酸钠、硫酸钠。为验证其成分,进
行如下实验。
(1)实验1:取样于试管中,滴入酚酞溶液,观察到溶液变红。请分析说明,用该方法证明溶液M中含
有氢氧化钠的可行性。______
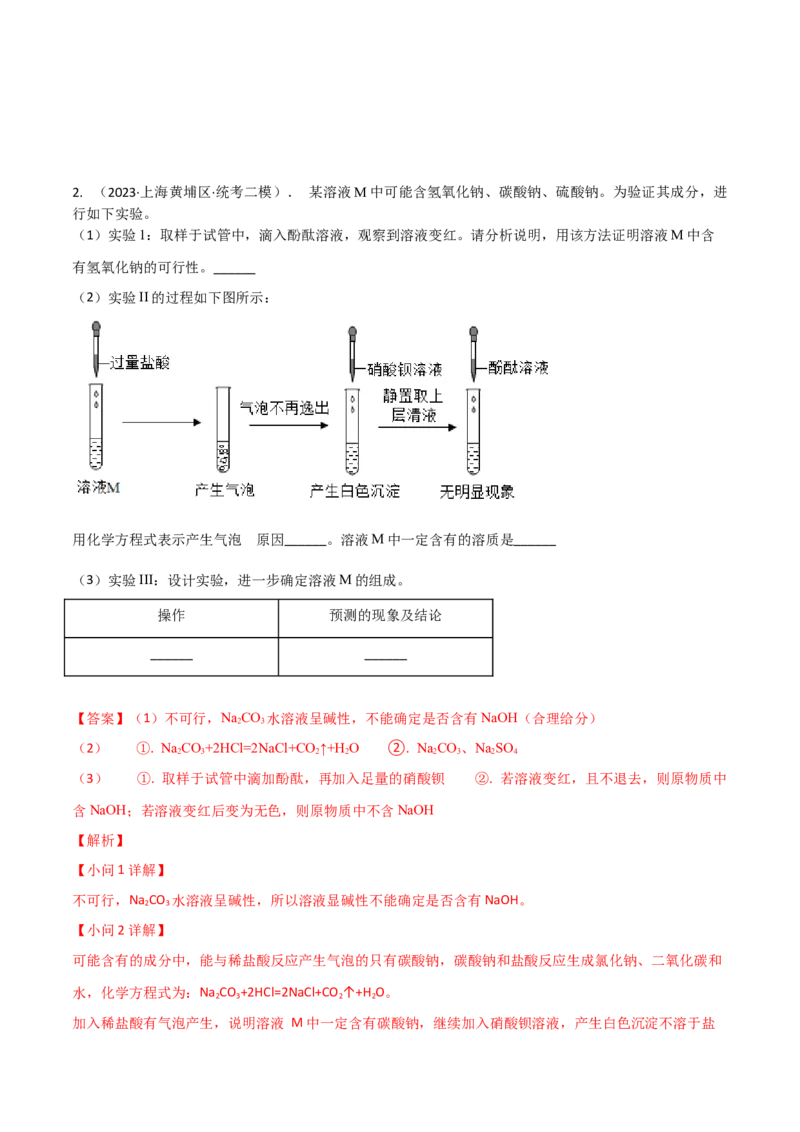
(2)实验II的过程如下图所示:
的
用化学方程式表示产生气泡 原因______。溶液M中一定含有的溶质是______
(3)实验III:设计实验,进一步确定溶液M的组成。
操作 预测的现象及结论
______ ______
【答案】(1)不可行,NaCO 水溶液呈碱性,不能确定是否含有NaOH(合理给分)
2 3
(2) ①. NaCO+2HCl=2NaCl+CO ↑+H O ②. NaCO、NaSO
2 3 2 2 2 3 2 4
(3) ①. 取样于试管中滴加酚酞,再加入足量的硝酸钡 ②. 若溶液变红,且不退去,则原物质中
含NaOH;若溶液变红后变为无色,则原物质中不含NaOH
【解析】
【小问1详解】
不可行,Na CO 水溶液呈碱性,所以溶液显碱性不能确定是否含有NaOH。
2 3
【小问2详解】
可能含有的成分中,能与稀盐酸反应产生气泡的只有碳酸钠,碳酸钠和盐酸反应生成氯化钠、二氧化碳和
水,化学方程式为:Na CO +2HCl=2NaCl+CO ↑+H O。
2 3 2 2
加入稀盐酸有气泡产生,说明溶液 M中一定含有碳酸钠,继续加入硝酸钡溶液,产生白色沉淀不溶于盐酸,说明生成的是硫酸钡沉淀,则说明溶液 M中一定含有硫酸钠,再加入酚酞,无明显现象,但由于实
验时加入了过量的稀盐酸,所以无法证明溶液 M 中是否含有氢氧化钠。即溶液 M中一定含有的溶质是碳
酸钠和硫酸钠。
【小问3详解】
可以另取适量溶液M于试管中,滴加酚酞,再加入足量的硝酸钡,硝酸钡溶液会与与M中的碳酸钠充分
反应后过滤,若溶液变红,且不退去,则原物质中含NaOH;若溶液变红后变为无色,则原物质中不含
NaOH