文档内容
宝山区 2022 学年第二学期初三质量调研(2023.04)
(满分50分,考试时间40分钟)
相对原子质量:相对原子质量:H-1 C-12 N-14 O-16 Cl-35.5 K-39 Fe-56 Cu-64
Zn-65 Ag-108
一、选择题(1~14每题只有1个正确选项,每题1分,共14分)
1. 空气中体积分数最大的气体是
A. 氮气 B. 氧气 C. 二氧化碳 D. 氦气
2. 灼烧时火焰呈紫色的物质是
A. NaCO B. CuSO C. KNO D. CaCl
2 3 4 3 2
3. 下列饮品属于溶液的是( )
A. 可乐 B. 牛奶 C. 果粒橙 D. 豆浆
4. 溴化银 (AgBr))见光色变深,广泛应用于变色镜片、照相底片,其中Br的化合价为
A. +1 B. +2 C. -1 D. -2
5. 互为同素异形体的是
A. 氧气和液氧 B. 石墨和碳-60 C. 冰和干冰 D. 水和双氧水
的
6. 生活中物质 pH大于7的是
A. 苏打水 B. 食盐水 C. 雪碧 D. 食醋
7. 属于混合物的是
A. 酒精 B. 盐酸 C. 烧碱 D. 冰水共存物
8. 煤气是一种常见家用燃料,其主要成分是
A. CH B. CO C. H D. CO
4 2 2
9. 有关铁丝燃烧现象描述不正确的是
A. 火星四射 B. 发出耀眼白光 C. 放出热量 D. 生成黑色固体
10. “ ”和“ ”表示两种原子,表示单质的微粒模型是
A. B. C.
第1页/共6页
学科网(北京)股份有限公司D.
的
11. 化学方程式书写正确 是
A. 2HO 2H↑+O ↑ B. 2Fe+6HCl=2FeCl +3H
2 2 2 3 2
C. 2NaOH+SO =Na SO +H O D. C+CuO Cu+CO ↑
2 2 3 2 2
12. 有关分子、原子的说法正确的是
A. 分子可以直接构成物质,而原子不可以
B. 分子由原子构成,分子可以分成原子
C. 分子可以再分,而原子不可以再分
的
D. 分子是保持物质性质 一种微粒
13. 属于物质的化学性质且描述正确的是
A. 稀有气体不活泼 B. 氧气能燃烧 C. 氢氧化钠易潮解 D. 石墨能导电
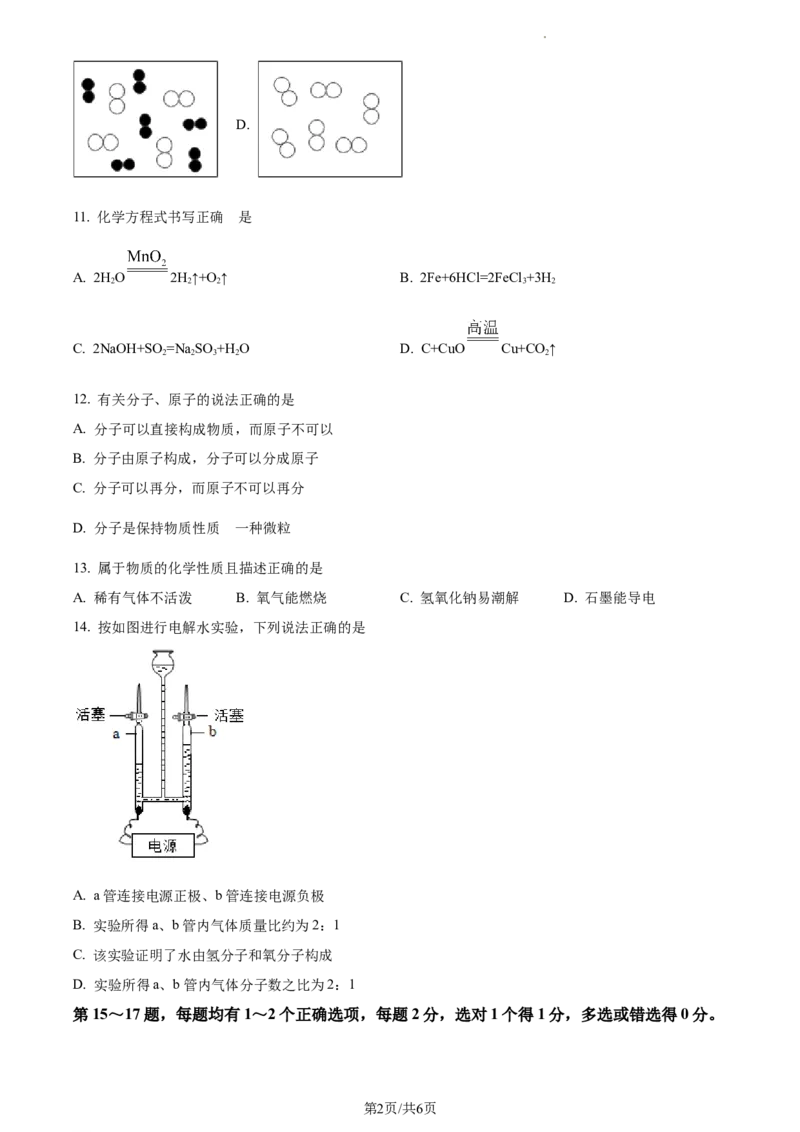
14. 按如图进行电解水实验,下列说法正确的是
A. a管连接电源正极、b管连接电源负极
B. 实验所得a、b管内气体质量比约为2:1
C. 该实验证明了水由氢分子和氧分子构成
D. 实验所得a、b管内气体分子数之比为2:1
第15~17题,每题均有1~2个正确选项,每题2分,选对1个得1分,多选或错选得0分。
第2页/共6页
学科网(北京)股份有限公司15. 不能用来鉴别盐酸和稀硫酸的试剂是
A. BaCl B. Zn C. AgNO D. Ba(NO )
2 3 3 2
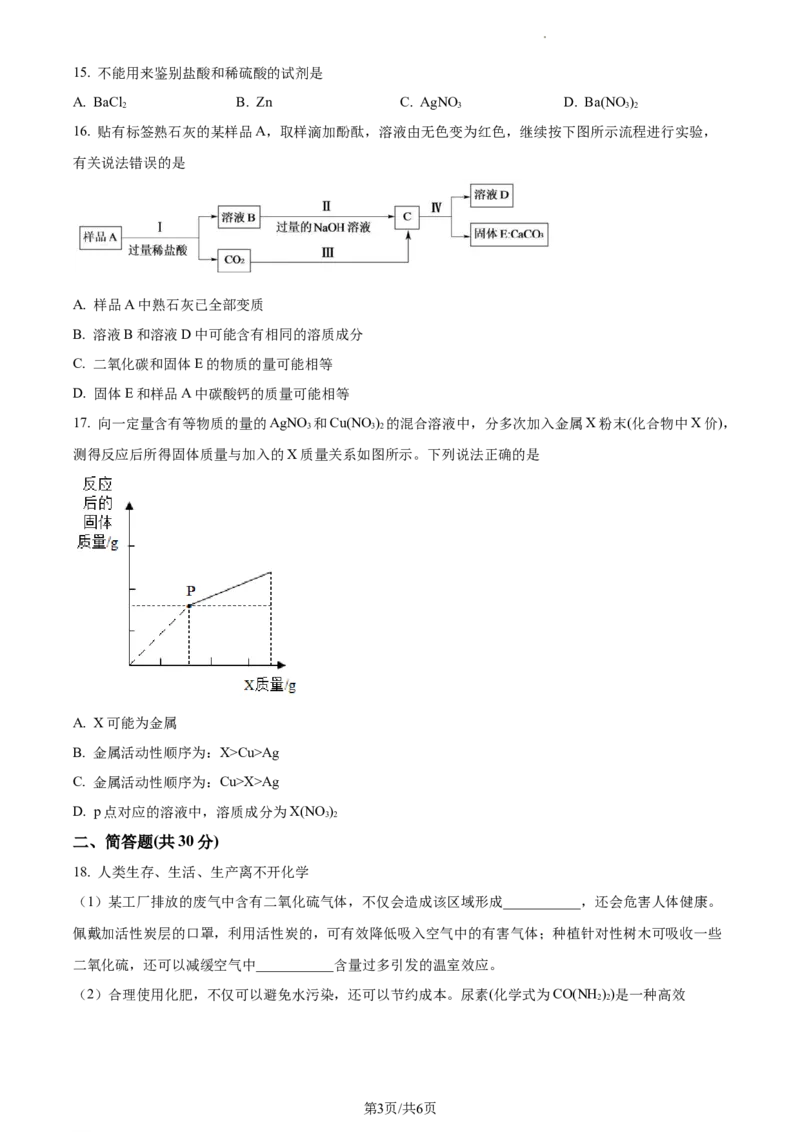
16. 贴有标签熟石灰的某样品A,取样滴加酚酞,溶液由无色变为红色,继续按下图所示流程进行实验,
有关说法错误的是
A. 样品A中熟石灰已全部变质
B. 溶液B和溶液D中可能含有相同的溶质成分
C. 二氧化碳和固体E的物质的量可能相等
D. 固体E和样品A中碳酸钙的质量可能相等
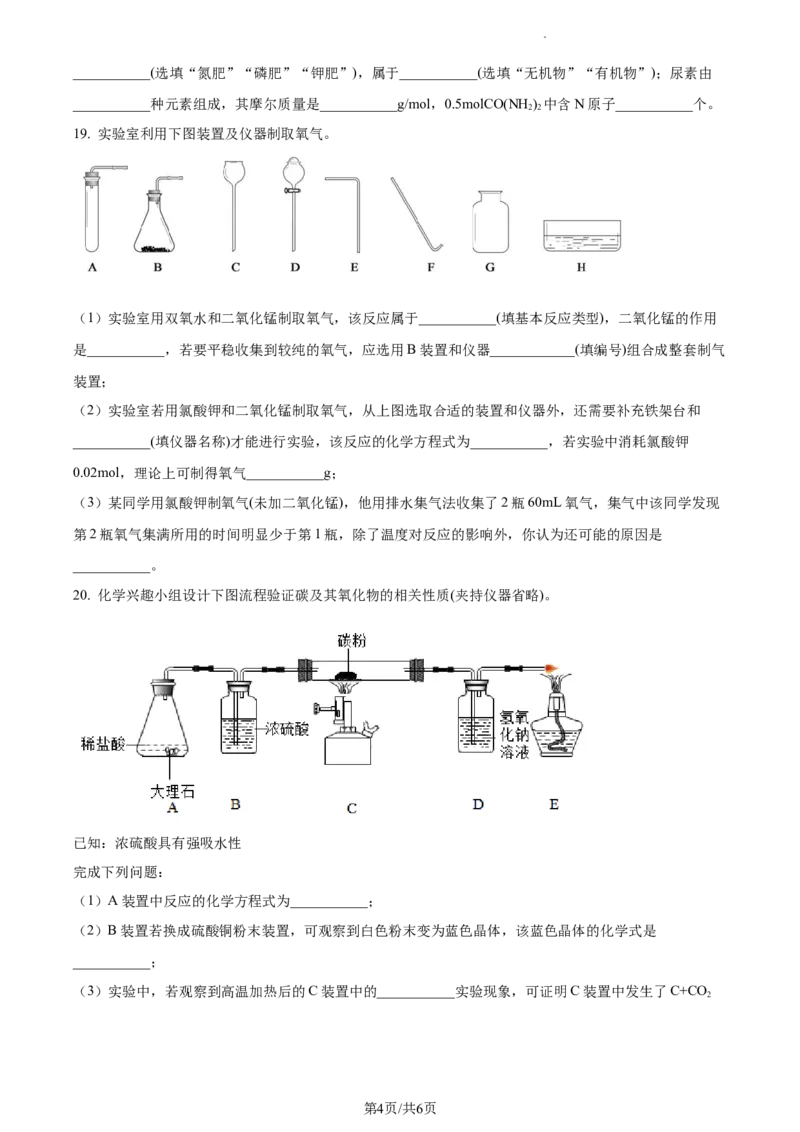
17. 向一定量含有等物质的量的AgNO 和Cu(NO ) 的混合溶液中,分多次加入金属X粉末(化合物中X价),
3 3 2
测得反应后所得固体质量与加入的X质量关系如图所示。下列说法正确的是
A. X可能为金属
B. 金属活动性顺序为:X>Cu>Ag
C. 金属活动性顺序为:Cu>X>Ag
D. p点对应的溶液中,溶质成分为X(NO)
3 2
二、简答题(共30分)
18. 人类生存、生活、生产离不开化学 。
(1)某工厂排放的废气中含有二氧化硫气体,不仅会造成该区域形成___________,还会危害人体健康。
佩戴加活性炭层的口罩,利用活性炭的,可有效降低吸入空气中的有害气体;种植针对性树木可吸收一些
二氧化硫,还可以减缓空气中___________含量过多引发的温室效应。
(2)合理使用化肥,不仅可以避免水污染,还可以节约成本。尿素(化学式为CO(NH))是一种高效
2 2
第3页/共6页
学科网(北京)股份有限公司___________(选填“氮肥”“磷肥”“钾肥”),属于___________(选填“无机物”“有机物”);尿素由
___________种元素组成,其摩尔质量是___________g/mol,0.5molCO(NH ) 中含N原子___________个。
2 2
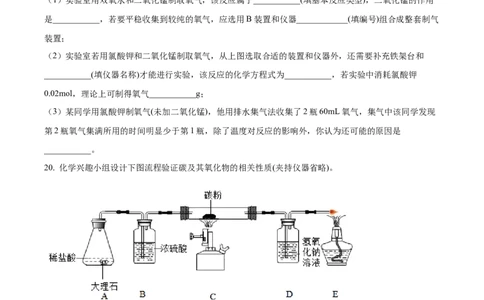
19. 实验室利用下图装置及仪器制取氧气。
(1)实验室用双氧水和二氧化锰制取氧气,该反应属于___________(填基本反应类型),二氧化锰的作用
是___________,若要平稳收集到较纯的氧气,应选用B装置和仪器____________(填编号)组合成整套制气
装置;
(2)实验室若用氯酸钾和二氧化锰制取氧气,从上图选取合适的装置和仪器外,还需要补充铁架台和
___________(填仪器名称)才能进行实验,该反应的化学方程式为___________,若实验中消耗氯酸钾
0.02mol,理论上可制得氧气___________g;
(3)某同学用氯酸钾制氧气(未加二氧化锰),他用排水集气法收集了2瓶60mL氧气,集气中该同学发现
第2瓶氧气集满所用的时间明显少于第1瓶,除了温度对反应的影响外,你认为还可能的原因是
___________。
20. 化学兴趣小组设计下图流程验证碳及其氧化物的相关性质(夹持仪器省略)。
已知:浓硫酸具有强吸水性
完成下列问题:
(1)A装置中反应的化学方程式为___________;
(2)B装置若换成硫酸铜粉末装置,可观察到白色粉末变为蓝色晶体,该蓝色晶体的化学式是
___________;
(3)实验中,若观察到高温加热后的C装置中的___________实验现象,可证明C装置中发生了C+CO
2
第4页/共6页
学科网(北京)股份有限公司2CO反应;该实验流程能否证明:CO 可以与碱反应,而CO不可以,请简单阐述。___________
2
21. 实验室现有一瓶敞口放置一段时间的20%的氢氧化钠溶液(室温),需知道其是否变质,再进行处理及
回收利用。甲乙两组探究性学习小组同学为此开展以下活动。
【理论分析】该氢氧化钠溶液可能已经变质
(1)氢氧化钠可能变质的原因的化学方程式是___________。
【甲组实验】
(2)利用物质的化学性质探究氢氧化钠溶液是否变质及变质程度
实验步骤及现象 实验结论
步骤1:取少许样品,滴加BaCl 溶液,观察到___________; 证明氢氧化钠已变质
2
步骤2:继续步骤1,滴加BaCl 溶液至过量,再___________(填实验操作及现 证明氢氧化钠部分变
2
象)。 质
【乙组实验】利用物质的溶解性探究氢氧化钠溶液是否变质及变质程度
资料:下表为氢氧化钠和碳酸钠在水中和酒精中的部分溶解度。
温度 水中S(g/100g) 酒精中S(g/100g)
氢氧化钠 碳酸钠 氢氧化钠 碳酸钠
20℃ 109 21.5 17.3 不溶
40℃ 129 49 40 不溶
的
(3)40℃时,碳酸钠在水中 溶解度为___________;
(4)原20%的氢氧化钠溶液是室温下的___________溶液(选填“饱和”“不饱和”);
取样品溶液10g蒸发,将所得固体全部放入温度为___________℃的10g酒精中,充分振荡,固体部分溶解,
证明氢氧化钠已变质且部分变质。
【处理与回收】将该瓶部分变质的氢氧化钠溶液回收再利用
(5)请你和学习小组一起完成回收氢氧化钠的实验方案:
实验目的 实验操作 实验结论
回收氢氧化
___________ 回收得到氢氧化钠溶液
钠
第5页/共6页
学科网(北京)股份有限公司第6页/共6页
学科网(北京)股份有限公司