文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海交通大学附属中学 2022—2023 学年度第二学期
高二化学摸底试卷
(满分 100分,60分钟完成。答案一律写在答题纸上)
可能用到的相对原子质量:N-14 O-16 Na-23 Cl-35.5 Cu-64
一、选择题(只有一个正确答案)
1. 化学与科技、生产、生活密切相关。下列有关说法错误的是
A B C D
在铁质水龙头镀
人工合成的结晶牛胰岛素属 大米酿制米酒过程中, 轮船外壳镶嵌锌块防腐,属
铜时,纯铜作阳
于高分子化合物 葡萄糖发生水解反应 于牺牲阳极的阴极保护法
极
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.结晶牛胰岛素是蛋白质,属于高分子化合物,A正确;
B.在铁制品镀铜时,镀件做阴极,纯铜做阳极,B正确;
C.大米发酵制取米酒过程中,淀粉水解生成葡萄糖,然后发酵生成乙醇,该过程不属于水解反应,C错
误;
D.在轮船外壳镶嵌锌块防腐,属于牺牲阳极的阴极保护法, D正确;
故选C。
2. 下列事实不能用勒夏特列原理解释的是
A. 实验室中用排饱和食盐水法收集氯气
B. 石蕊试液遇酸变红,遇碱变蓝
C. 压缩NO 与N O 混合气,气体颜色变深
2 2 4
第 1 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D. 工业上生产硫酸过程中,通入过量空气以提高SO 的转化率
2
【答案】C
【解析】
【详解】A.Cl
2
和水反应为Cl
2
+H
2
OHCl+HClO,饱和食盐水中Cl-浓度大,Cl
2
和水反应平衡逆向移
动,Cl 溶解度减小,能用勒夏特列原理解释,A不符合题意;
2
B.溶液中氢离子、氢氧根离子浓度的改变,导致石蕊向不同颜色的物质转化,能用勒夏特列原理解释,
B不符合题意;
C.NO
2
与N
2
O
4
混合气中存在2NO 2N
2
O
4
,压缩体积,平衡正向移动,NO
2
物质的量减小,但容器体
积减小,NO 浓度增大,颜色加深,不能用勒夏特列原理解释,C符合题意;
2
D.工业上生产硫酸过程中,通入过量空气,平衡正向移动,O 的转化率提高,能用勒夏特列原理解释,
2
D不符合题意;
故选C。
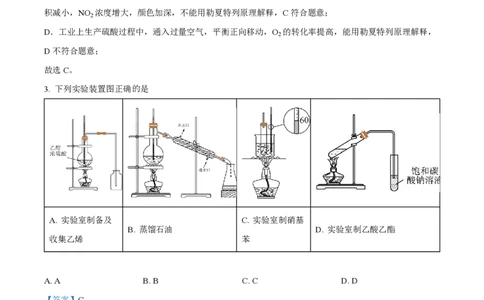
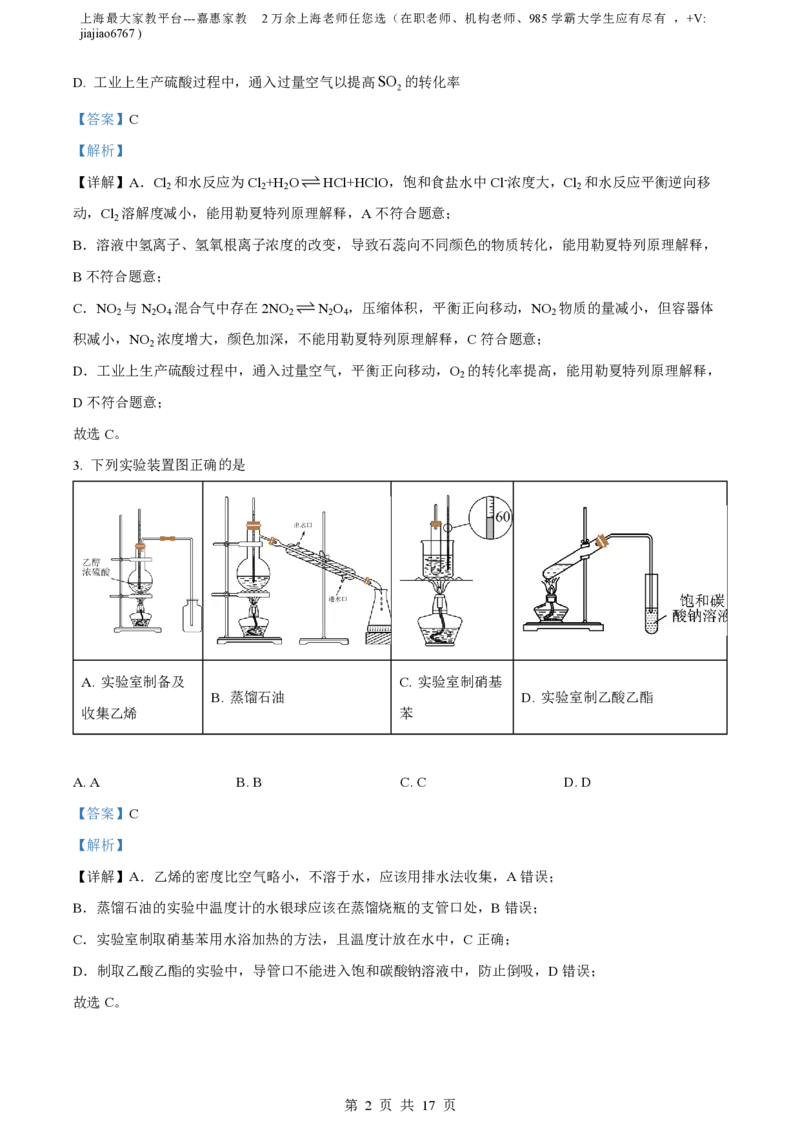
3. 下列实验装置图正确的是
A. 实验室制备及 C. 实验室制硝基
B. 蒸馏石油 D. 实验室制乙酸乙酯
收集乙烯 苯
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.乙烯的密度比空气略小,不溶于水,应该用排水法收集,A错误;
B.蒸馏石油的实验中温度计的水银球应该在蒸馏烧瓶的支管口处,B错误;
C.实验室制取硝基苯用水浴加热的方法,且温度计放在水中,C正确;
D.制取乙酸乙酯的实验中,导管口不能进入饱和碳酸钠溶液中,防止倒吸,D错误;
故选C。
第 2 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
4. 关于H 2 O H OH K w = H+ OH- ,下列说法正确的是
A. 向纯水中通入HClg ,水的电离被抑制,K 减小
w
B. 纯水中c
H+
为107 mol⋅L1
C. 若某溶液中,c
H+
= K ,则该溶液一定是中性的
w
D. 100℃时,0.1 mol/L的NaOH溶液的pH13
【答案】C
【解析】
【详解】A.向纯水中通入HClg ,溶液在氢离子浓度变大,水的电离被抑制,但是K 不变,故A错
w
误;
B.没有确定的温度,不能确定纯水中氢离子浓度,故B错误;
C.若某溶液中,c
H+
= K ,则该溶液氢离子浓度等于氢氧根离子浓度,溶液一定是中性的,故C正
w
确;
D.100℃时,0.1 mol/L的NaOH溶液中氢氧根离子浓度为0.1 mol/L,由于K 不是10-14,故氢离子浓度
w
不是10-13mol/L,pH不是13,故D错误;
故选C。
5. 世界某著名学术刊物近期介绍了一种新型中温全瓷铁-空气电池,其结构如图所示。下列有关该电池放电
时的说法正确的是
A. O2由b极移向a极
B. 正极的电极反应式为FeO 2xe FexO2
x
C. 若有22.4 L(标准状况)空气参与反应,则电路中有0.14 mol电子转移
第 3 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D. 铁表面发生的反应为xH OgFeFeO xH
2 x 2
【答案】D
【解析】
【分析】由新型中温全瓷铁--空气电池的装置图可知,a极通入空气,空气中氧气得电子发生还原反应为正
极,铁与水反应生成氢气,氢气在b极失电子发生氧化反应为负极,结合原电池原理分析解答。
【详解】A.原电池中,阴离子向负极移动,O2-由正极移向负极,即a极移向b极,故A错误;
B.a极空气中氧气得电子发生还原反应为正极,电极反应式为:O +4e-═2O2-,故B错误;
2
C.标准状况下,22.4L空气的物质的量为1mol,则参与反应的氧气为0.2mol,则电路中转移0.8mol电
子,故C错误;
D.由新型中温全瓷铁--空气电池的装置图可知,铁表面发生的反应为xH O(g)+Fe═FeO +xH ,故D正
2 x 2
确;
故选D。
二、综合分析题
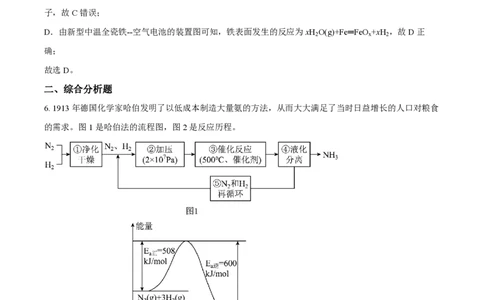
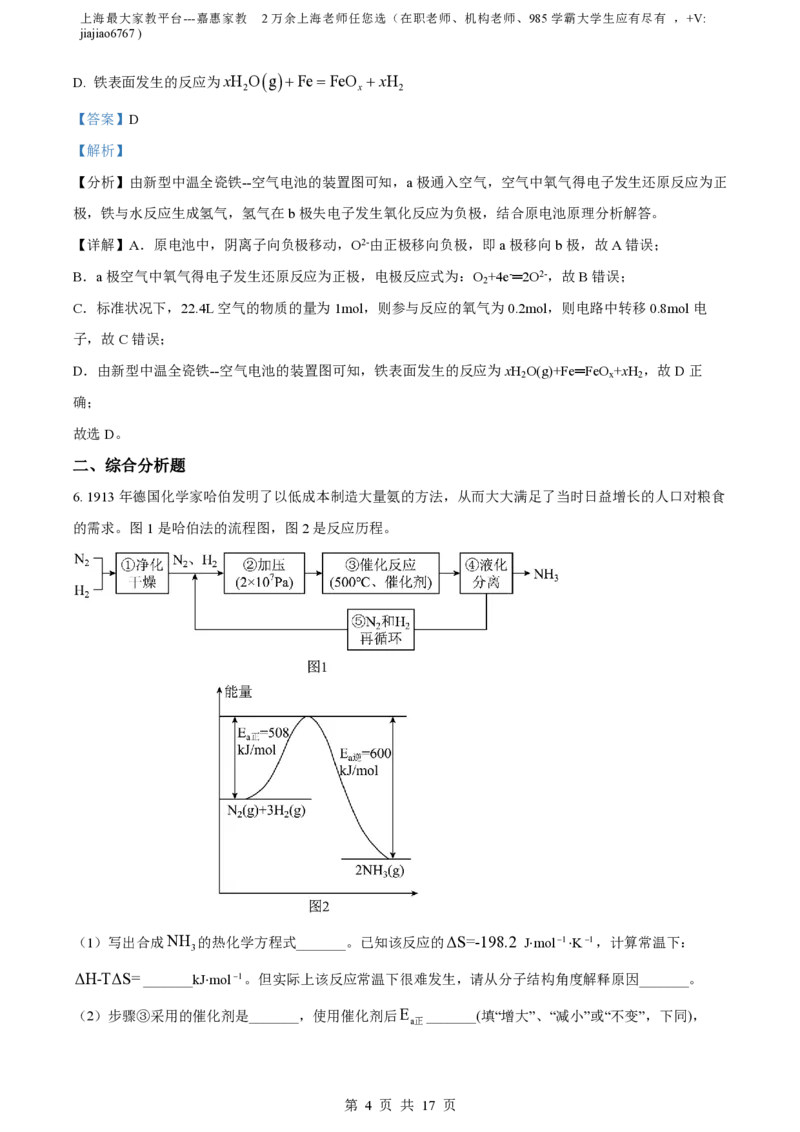
6. 1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食
的需求。图1是哈伯法的流程图,图2是反应历程。
(1)写出合成NH 的热化学方程式_______。已知该反应的ΔS=-198.2 J⋅mol1⋅K1,计算常温下:
3
ΔH-TΔS=_______kJ⋅mol1。但实际上该反应常温下很难发生,请从分子结构角度解释原因_______。
(2)步骤③采用的催化剂是_______,使用催化剂后E _______(填“增大”、“减小”或“不变”,下同),
a正
第 4 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
E _______。
a逆
(3)图1中为提高原料转化率而采取的措施是_______(选填编号)。
A. ①②③ B. ②④⑤ C. ①③⑤ D. ②③④
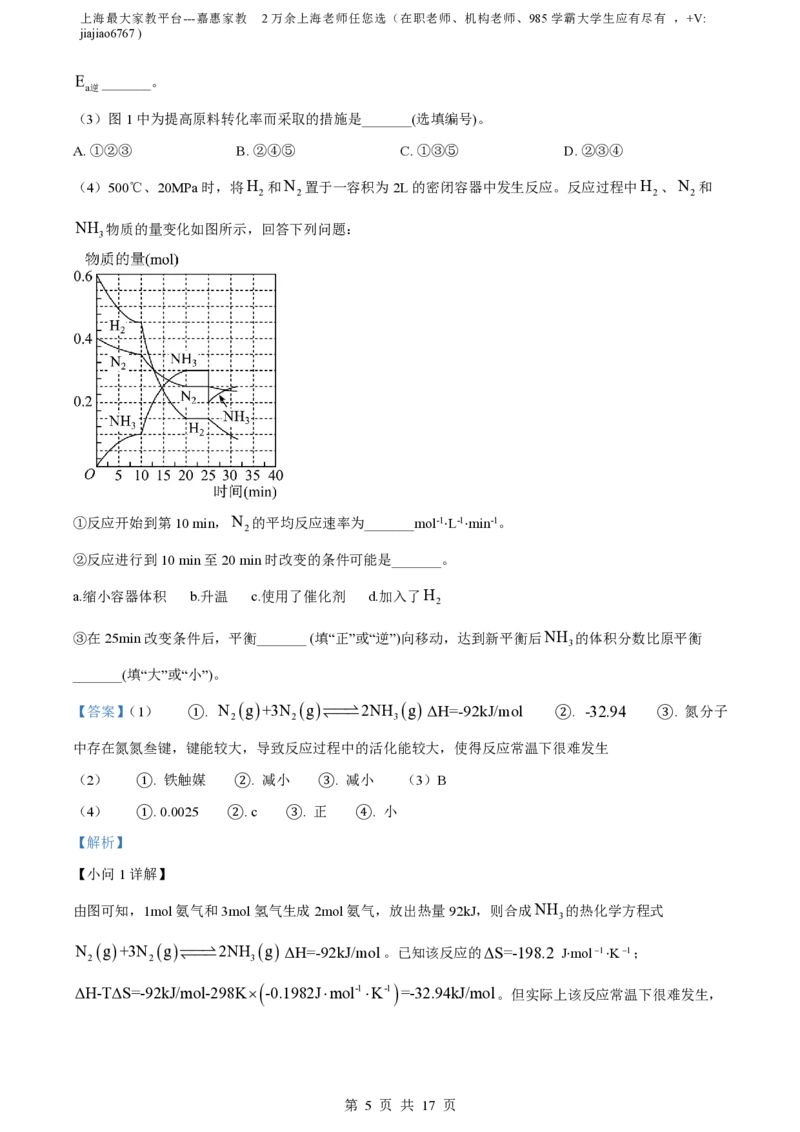
(4)500℃、20MPa时,将H 和N 置于一容积为2L的密闭容器中发生反应。反应过程中H 、N 和
2 2 2 2
NH 物质的量变化如图所示,回答下列问题:
3
①反应开始到第10 min,N 的平均反应速率为_______mol-1⋅L-1⋅min-1。
2
②反应进行到10 min至20 min时改变的条件可能是_______。
a.缩小容器体积 b.升温 c.使用了催化剂 d.加入了H
2
③在25min改变条件后,平衡_______ (填“正”或“逆”)向移动,达到新平衡后NH 的体积分数比原平衡
3
_______(填“大”或“小”)。
【答案】(1) ①. N g+3N g 2NH g ΔH=-92kJ/mol ②. -32.94 ③. 氮分子
2 2 3
中存在氮氮叁键,键能较大,导致反应过程中的活化能较大,使得反应常温下很难发生
(2) ①. 铁触媒 ②. 减小 ③. 减小 (3)B
(4) ①. 0.0025 ②. c ③. 正 ④. 小
【解析】
【小问1详解】
由图可知,1mol氨气和3mol氢气生成2mol氨气,放出热量92kJ,则合成NH 的热化学方程式
3
N g+3N g 2NH g ΔH=-92kJ/mol。已知该反应的ΔS=-198.2 J⋅mol1⋅K1;
2 2 3
ΔH-TΔS=-92kJ/mol-298K
-0.1982Jmol-1K-1
=-32.94kJ/mol。但实际上该反应常温下很难发生,
第 5 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
原因是氮分子中存在氮氮叁键,键能较大,导致反应过程中的活化能较大,使得反应常温下很难发生;
【小问2详解】
步骤③采用的催化剂是铁触媒催化剂,使用催化剂可以改变反应历程,降低反应的活化能,故E 减小,
a正
反应的焓变不变,则E 也减小;
a逆
【小问3详解】
①为净化原料气,不是提高原料转化率;②加压可以促使反应正向进行,利于提高原料转化率;③催化剂
可以加快反应速率,但是不改变平衡移动,不是提高原料转化率;④分离与产品氨气,利于平衡正向移
动,利于提高原料转化率;⑤氮气、氢气循环利用,利于提高原料转化率;
故选B;
【小问4详解】
0.4-0.35
①反应开始到第10 min,N 的平均反应速率为 mol-1L-1min-1=0.0025mol-1L-1min-1mol-
2 210
1⋅L-1⋅min-1。
②由图可知,反应进行到10 min至20 min时,各物质的量在原有基础上改变,反应速率加快,故改变的
条件可能是使用了催化剂,故选c;
③在25min时氨气量突然减小,故在25min改变条件为移走生成物氨气,导致平衡正向移动,达到新平衡
后NH 的体积分数比原平衡小。
3
7. 努力实现碳达峰、碳中和展现了我国积极参与和引领全球气候治理的大国担当。CO 的综合利用是实
2
现碳中和的保证。
I.回收利用CO 解决空间站供氧问题物质转化如图所示:
2
(1)反应A为CO 2 g4H 2 g CH 4 g2H 2 Og ,是回收利用CO 2 的关键步骤。
已知:2H gO g2H Og ΔH=-483.6 kJ⋅mol-1
2 2 2
CH g2O gCO g2H Og ΔH=-802.3 kJ⋅mol-1
4 2 2 2
反应A的ΔH=_______kJ⋅mol-1
第 6 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
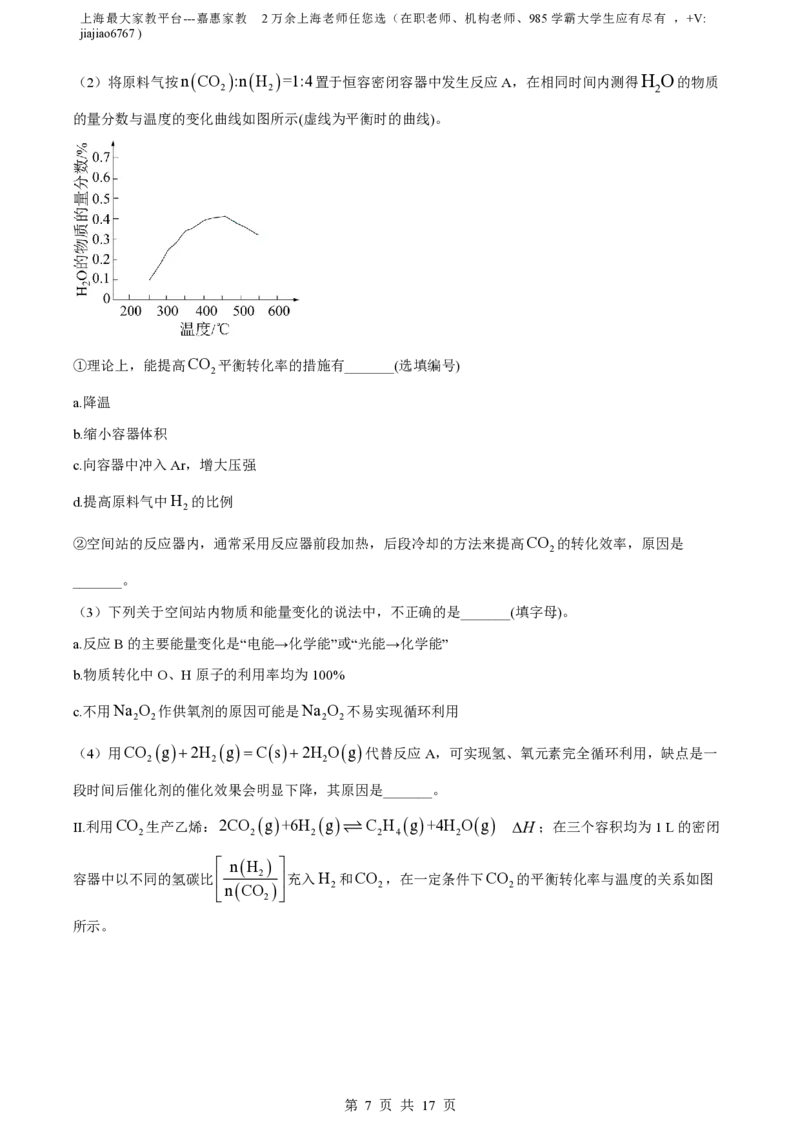
(2)将原料气按nCO :nH =1:4置于恒容密闭容器中发生反应A,在相同时间内测得H O的物质
2 2 2
的量分数与温度的变化曲线如图所示(虚线为平衡时的曲线)。
①理论上,能提高CO 平衡转化率的措施有_______(选填编号)
2
a.降温
b.缩小容器体积
c.向容器中冲入Ar,增大压强
d.提高原料气中H 的比例
2
②空间站的反应器内,通常采用反应器前段加热,后段冷却的方法来提高CO 的转化效率,原因是
2
_______。
(3)下列关于空间站内物质和能量变化的说法中,不正确的是_______(填字母)。
a.反应B的主要能量变化是“电能→化学能”或“光能→化学能”
b.物质转化中O、H原子的利用率均为100%
c.不用Na O 作供氧剂的原因可能是Na O 不易实现循环利用
2 2 2 2
(4)用CO g2H gCs2H Og 代替反应A,可实现氢、氧元素完全循环利用,缺点是一
2 2 2
段时间后催化剂的催化效果会明显下降,其原因是_______。
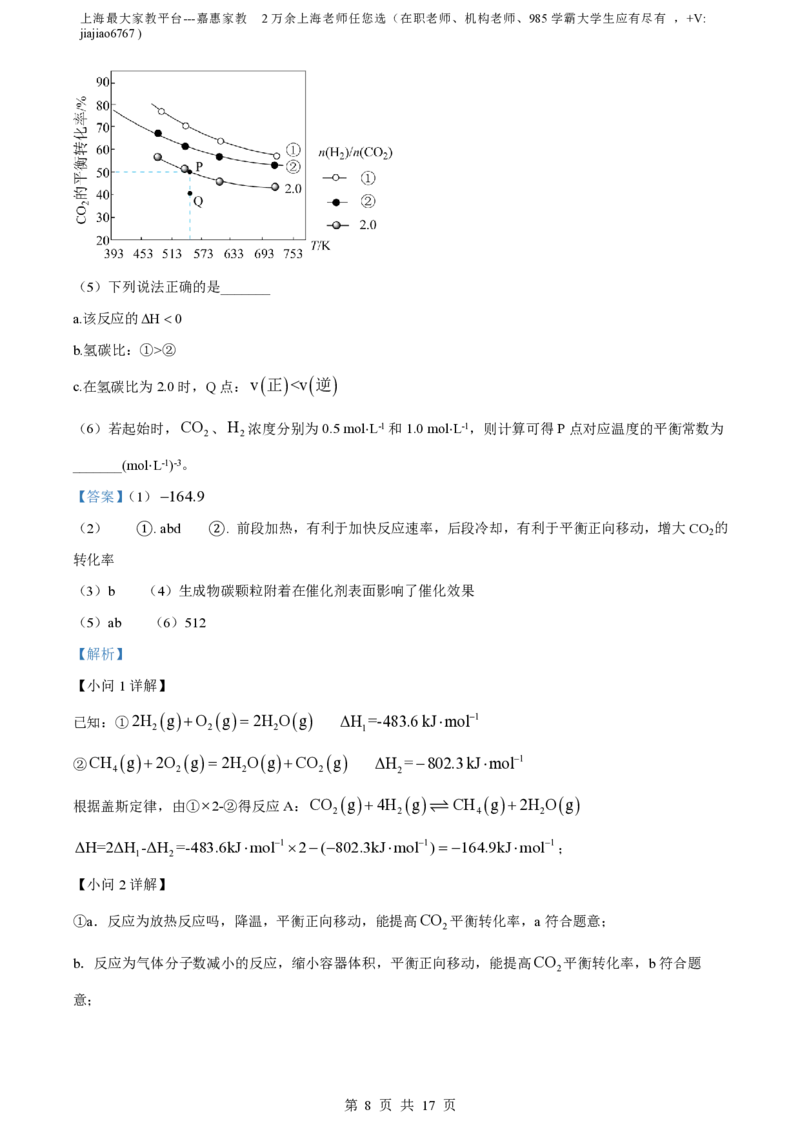
II.利用CO 2 生产乙烯:2CO 2 g+6H 2 g C 2 H 4 g+4H 2 Og H ;在三个容积均为1 L的密闭
nH
容器中以不同的氢碳比 2 充入H 和CO ,在一定条件下CO 的平衡转化率与温度的关系如图
nCO 2 2 2
2
所示。
第 7 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(5)下列说法正确的是_______
a.该反应的H0
b.氢碳比:①>②
c.在氢碳比为2.0时,Q点:v正②,选项b正确;
c.相同温度下,在氢碳比为2.0时,Q点二氧化碳转化率小于平衡时的转化率,说明Q点未到达平衡,反
应向正反应进行,故Q点v(正)>v(逆),选项c错误;
故选ab;
【小问6详解】
2CO (g)+6H (g)C H (g)+4H (g)
2 2 2 4 2
起始mol/L 0.5 1.0 0 0
转化mol/L 2a 6a a 4a
平衡mol/L 0.5-2a 1.0-6a a 4a
2a
依据图像得出此时二氧化碳的平衡转化率为50%,即 100%50%,解得a=0.125,
0.5
第 9 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
cC H c4H O
2 4 2
c(CO )=0.25mol/L,c(H )=0.25mol/L,c(C H )=0.125mol/L,c(H O)=0.5mol/L,故K= =
2 2 2 4 2 c2CO c6H
2 2
0.1250.54
=512(mol⋅L-1)-3。
0.2520.256
8. 某研究小组用微生物电池模拟淡化海水,同时做电解实验,实验装置如下图所示,C、D是铂电极。
(1)若A、B是惰性电极
①写出D极的电极反应式_______。
②写出甲中总反应的离子方程式_______。
(2)若甲是铁片镀铜装置,A、B质量相同。当B和A的质量差为12.8g时,C极产生的气体在标准状况
下的体积是_______L。
(3)苯酚的分子式为C H O。
6 6
①离子交换膜A为_______离子交换膜(填“阴”或“阳”)。
②a极的电极反应式为_______。
③理论上每消除1mol苯酚,同时消除_______mol NO;当电路中转移1mol电子时,模拟海水理论上除
3
盐_______g。
通电
【答案】(1) ①. 2H O+2e-=H +2OH- ②. 2Cu2 2H O 2CuO 4H
2 2 2 2
(2)1.12L (3) ①. 阴 ②. C H O28e 11H O6CO 28H ③. 5.6 ④.
6 6 2 2
58.5
【解析】
【分析】根据装置图可以知道,左侧为原电池,右侧为电解池。原电池中电极a苯酚失电子转化为CO ,
2
所以电极a为负极,则电极b为正极;在电解池中,根据电源正对阳极,负极对阴极,可知电极A、C为阳
极,电极B、D为阴极。
【小问1详解】
第 10 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
①电极D为阴极,阳离子H+和SO2移向电极D,H+优先得电子,故电极反应为
4
2H O+2e-=H +2OH-;②甲装置为电解池,且A、B为惰性电极,电解质为CuSO ;阳离子Cu2+和H+
2 2 4
移向阴极B反应,Cu2+优先得电子被还原为Cu,阴离子OH-和SO2移向阳极,OH-优先失电子被还原为
4
通电
O ,故甲中总反应的离子方程式为2Cu2 2H O 2CuO 4H。
2 2 2
【小问2详解】
若甲是铁片镀铜装置,则阳极A为单质Cu,电极反应为Cu2e Cu2,阴极B为镀件铁片,电极反
应为Cu2++2e-=Cu, 当B和A的质量差为17.8g时,电极A质量减小6.4g,电极B质量增加6.4g,通过电极
6.4g
反应可知,转移电子数为 ×2=0.2mol,根据电荷守恒,电极C(阳极)将失去0.2mol电子,根据
64g/mol
电极C的电极反应2H O4e O 4H,生成氧气为0.05mol,体积为0.05mol×22.4L/mol=1.12L。
2 2
【小问3详解】
①左侧原电池中NaCl溶液转化为淡水,可知Na+移向正极b,Cl-移向负极a,所以离子交换膜A为阴离子
2
交换膜;②电极a中反应物苯酚转化为CO ,其中苯酚中C的化合价为- 价,CO 中的C的化合价为+4
2 2
3
价,转移电子数目为28,故a电极反应为C H O28e 11H O6CO 28H;③根据a电极反应
6 6 2 2
可知,每消除1mol苯酚转移电子28mol,b电极反应为2NO+10e-+12H+=N ↑+6H O,转移28mol电子
3 2 2
28mol
时,消除NO 2=5.6mol;当电路中转移1mol电子时,有1mol的Na+移向正极,1molde Cl-移向
3 10mol
负极,模拟海水理论上除去1mol,即58.5gNaCl。
【点睛】在书写电极反应式时,要根据电解质的酸碱性分析电极反应的产物是否能稳定存在,如果产物能
与电解质的离子继续反应,就要合在一起写出总式,才是正确的电极反应式。有时燃料电池的负极反应会
较复杂,我们可以先写出总反应,再写正极反应,最后根据总反应和正极反应写出负极反应。
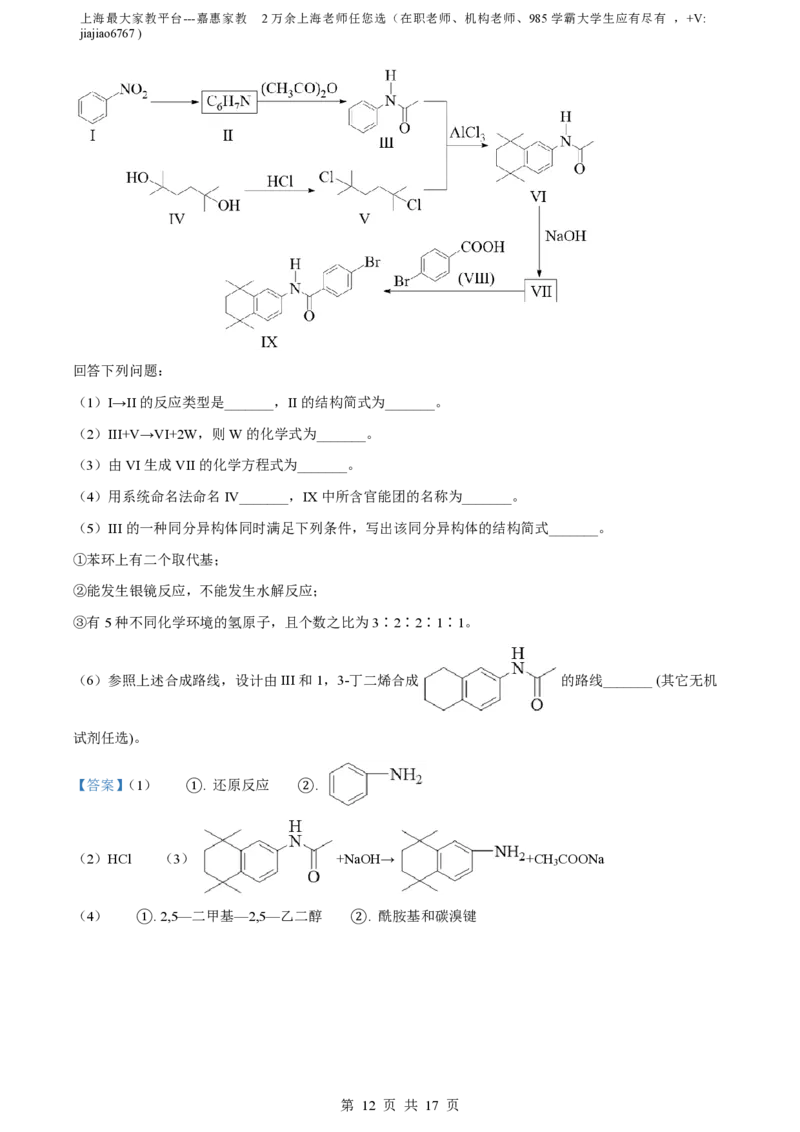
9. 有机物X是合成一种治疗细胞白血病药物的前体,其合成路线如图所示:
第 11 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
回答下列问题:
(1)I→II的反应类型是_______,II的结构简式为_______。
(2)III+V→VI+2W,则W的化学式为_______。
(3)由VI生成VII的化学方程式为_______。
(4)用系统命名法命名IV_______,IX中所含官能团的名称为_______。
(5)III的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式_______。
①苯环上有二个取代基;
②能发生银镜反应,不能发生水解反应;
③有5种不同化学环境的氢原子,且个数之比为3∶2∶2∶1∶1。
(6)参照上述合成路线,设计由III和1,3-丁二烯合成 的路线_______ (其它无机
试剂任选)。
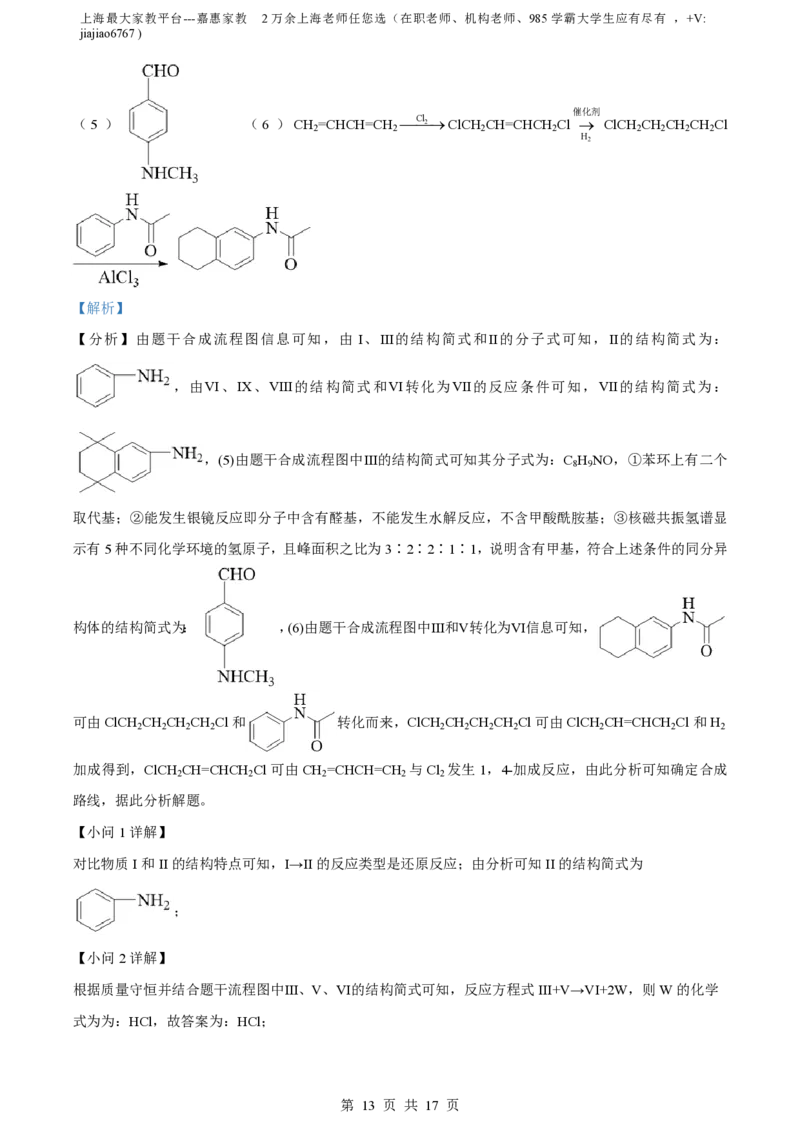
【答案】(1) ①. 还原反应 ②.
(2)HCl (3) +NaOH→ +CH COONa
3
(4) ①. 2,5—二甲基—2,5—乙二醇 ②. 酰胺基和碳溴键
第 12 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
催化剂
(5 ) (6 )CH =CHCH=CH Cl 2ClCH CH=CHCH Cl ClCH CH CH CH Cl
2 2 2 2 2 2 2 2
H
2
【解析】
【分析】由题干合成流程图信息可知,由 I、Ⅲ的结构简式和Ⅱ的分子式可知,Ⅱ的结构简式为:
,由Ⅵ、Ⅸ、Ⅷ的结构简式和Ⅵ转化为Ⅶ的反应条件可知,Ⅶ的结构简式为:
,(5)由题干合成流程图中Ⅲ的结构简式可知其分子式为:C H NO,①苯环上有二个
8 9
取代基;②能发生银镜反应即分子中含有醛基,不能发生水解反应,不含甲酸酰胺基;③核磁共振氢谱显
示有5种不同化学环境的氢原子,且峰面积之比为3∶2∶2∶1∶1,说明含有甲基,符合上述条件的同分异
构体的结构简式为: ,(6)由题干合成流程图中Ⅲ和Ⅴ转化为Ⅵ信息可知,
可由ClCH CH CH CH Cl和 转化而来,ClCH CH CH CH Cl可由ClCH CH=CHCH Cl和H
2 2 2 2 2 2 2 2 2 2 2
加成得到,ClCH CH=CHCH Cl可由CH =CHCH=CH 与Cl 发生1,4-加成反应,由此分析可知确定合成
2 2 2 2 2
路线,据此分析解题。
【小问1详解】
对比物质I和II的结构特点可知,I→II的反应类型是还原反应;由分析可知II的结构简式为
;
【小问2详解】
根据质量守恒并结合题干流程图中Ⅲ、Ⅴ、Ⅵ的结构简式可知,反应方程式III+V→VI+2W,则W的化学
式为为:HCl,故答案为:HCl;
第 13 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
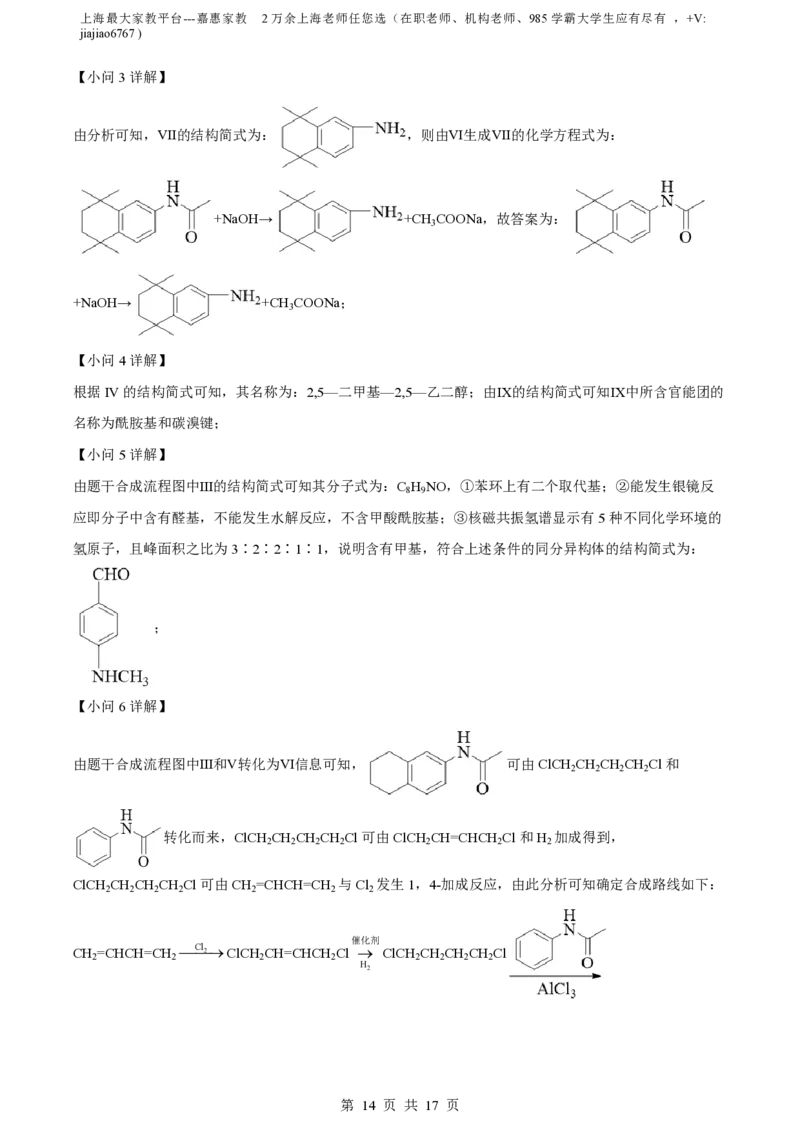
【小问3详解】
由分析可知,Ⅶ的结构简式为: ,则由Ⅵ生成Ⅶ的化学方程式为:
+NaOH→ +CH COONa,故答案为:
3
+NaOH→ +CH COONa;
3
【小问4详解】
根据IV的结构简式可知,其名称为:2,5—二甲基—2,5—乙二醇;由Ⅸ的结构简式可知Ⅸ中所含官能团的
名称为酰胺基和碳溴键;
【小问5详解】
由题干合成流程图中Ⅲ的结构简式可知其分子式为:C H NO,①苯环上有二个取代基;②能发生银镜反
8 9
应即分子中含有醛基,不能发生水解反应,不含甲酸酰胺基;③核磁共振氢谱显示有5种不同化学环境的
氢原子,且峰面积之比为3∶2∶2∶1∶1,说明含有甲基,符合上述条件的同分异构体的结构简式为:
;
【小问6详解】
由题干合成流程图中Ⅲ和Ⅴ转化为Ⅵ信息可知, 可由ClCH CH CH CH Cl和
2 2 2 2
转化而来,ClCH CH CH CH Cl可由ClCH CH=CHCH Cl和H 加成得到,
2 2 2 2 2 2 2
ClCH CH CH CH Cl可由CH =CHCH=CH 与Cl 发生1,4-加成反应,由此分析可知确定合成路线如下:
2 2 2 2 2 2 2
催化剂
CH =CHCH=CH Cl 2ClCH CH=CHCH Cl ClCH CH CH CH Cl
2 2 2 2 2 2 2 2
H
2
第 14 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
催化剂
,故答案为:CH =CHCH=CH Cl 2ClCH CH=CHCH Cl
2 2 2 2
H
2
ClCH CH CH CH Cl 。
2 2 2 2
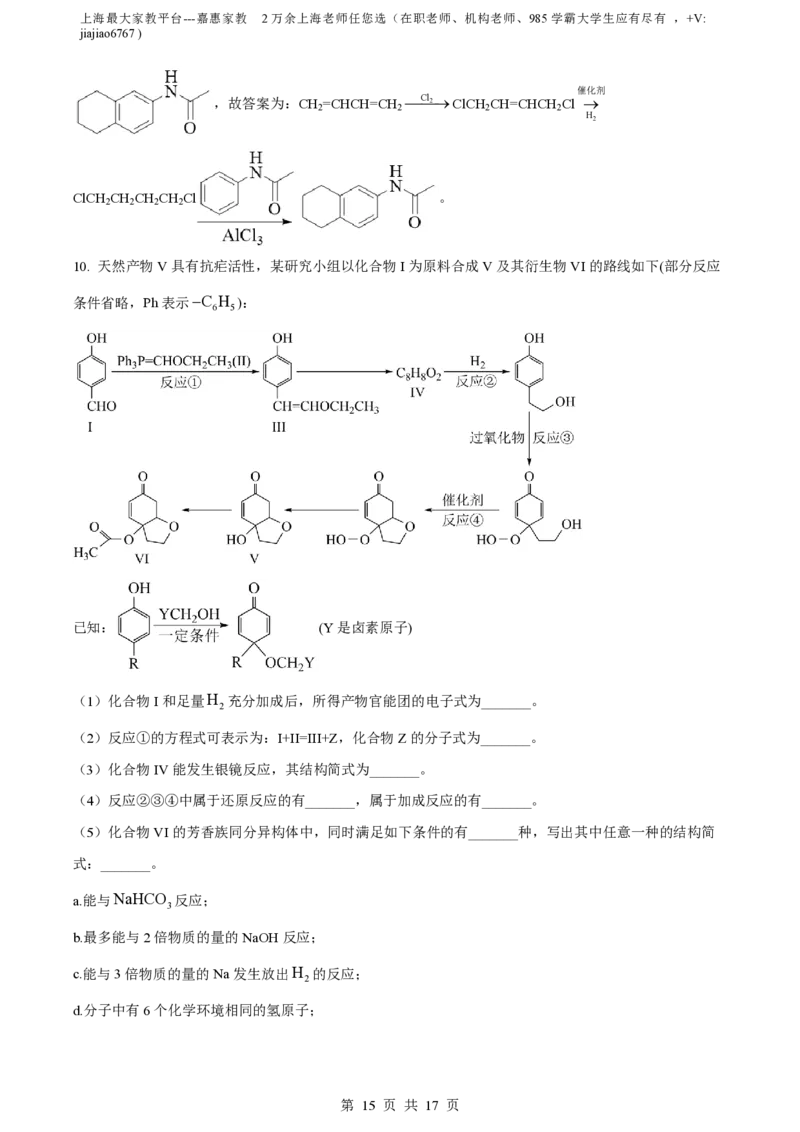
10. 天然产物V具有抗疟活性,某研究小组以化合物I为原料合成V及其衍生物VI的路线如下(部分反应
条件省略,Ph表示C H ):
6 5
已知: (Y是卤素原子)
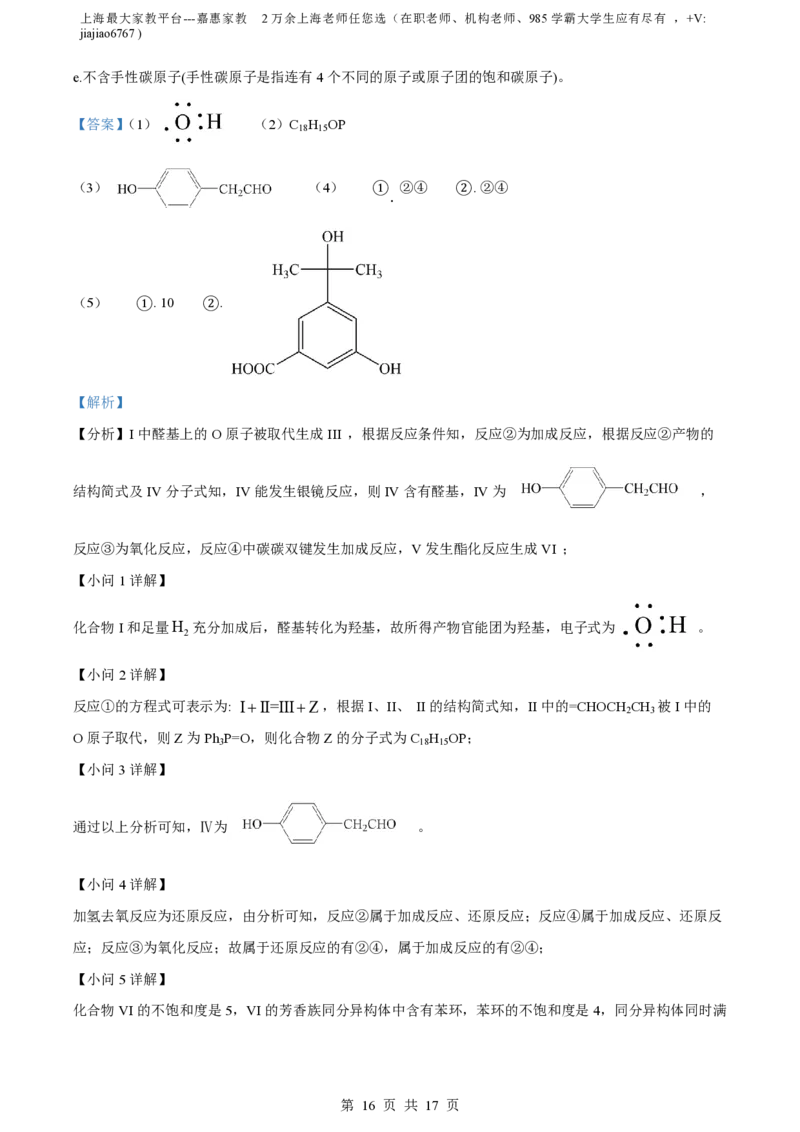
(1)化合物I和足量H 充分加成后,所得产物官能团的电子式为_______。
2
(2)反应①的方程式可表示为:I+II=III+Z,化合物Z的分子式为_______。
(3)化合物IV能发生银镜反应,其结构简式为_______。
(4)反应②③④中属于还原反应的有_______,属于加成反应的有_______。
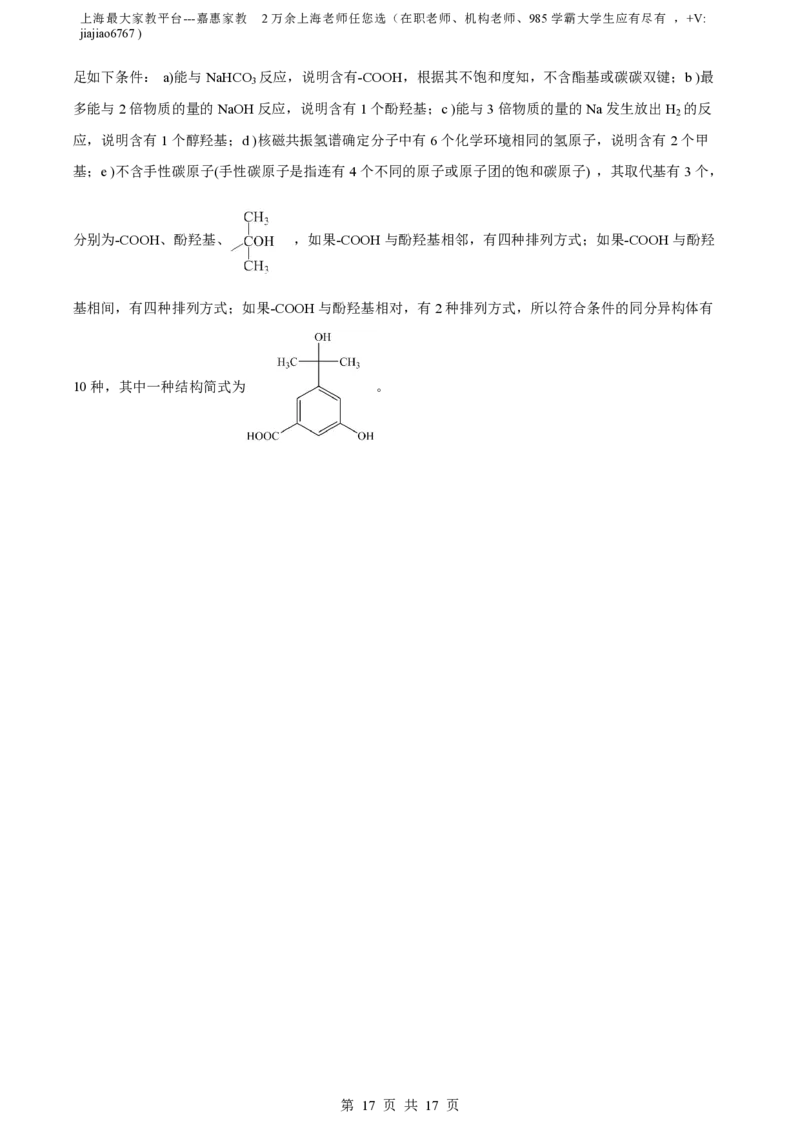
(5)化合物VI的芳香族同分异构体中,同时满足如下条件的有_______种,写出其中任意一种的结构简
式:_______。
a.能与NaHCO 反应;
3
b.最多能与2倍物质的量的NaOH反应;
c.能与3倍物质的量的Na发生放出H 的反应;
2
d.分子中有6个化学环境相同的氢原子;
第 15 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
e.不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)。
【答案】(1) (2)C H OP
18 15
(3) (4) ① ②④ ②. ②④
.
(5) ①. 10 ②.
【解析】
【分析】I中醛基上的O原子被取代生成III ,根据反应条件知,反应②为加成反应,根据反应②产物的
结构简式及IV分子式知,IV能发生银镜反应,则IV含有醛基,IV为 ,
反应③为氧化反应,反应④中碳碳双键发生加成反应,V发生酯化反应生成VI ;
【小问1详解】
化合物I和足量H 充分加成后,醛基转化为羟基,故所得产物官能团为羟基,电子式为 。
2
【小问2详解】
反应①的方程式可表示为: III=IIIZ,根据I、II、 II的结构简式知,II中的=CHOCH CH 被I中的
2 3
O原子取代,则Z为Ph P=O,则化合物Z的分子式为C H OP;
3 18 15
【小问3详解】
通过以上分析可知,Ⅳ为 。
【小问4详解】
加氢去氧反应为还原反应,由分析可知,反应②属于加成反应、还原反应;反应④属于加成反应、还原反
应;反应③为氧化反应;故属于还原反应的有②④,属于加成反应的有②④;
【小问5详解】
化合物VI的不饱和度是5,VI的芳香族同分异构体中含有苯环,苯环的不饱和度是4,同分异构体同时满
第 16 页 共 17 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
足如下条件: a)能与NaHCO 反应,说明含有-COOH,根据其不饱和度知,不含酯基或碳碳双键;b )最
3
多能与2倍物质的量的NaOH反应,说明含有1个酚羟基;c )能与3倍物质的量的Na发生放出H 的反
2
应,说明含有1个醇羟基;d )核磁共振氢谱确定分子中有6个化学环境相同的氢原子,说明含有2个甲
基;e )不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子) ,其取代基有3个,
分别为-COOH、酚羟基、 ,如果-COOH与酚羟基相邻,有四种排列方式;如果-COOH与酚羟
基相间,有四种排列方式;如果-COOH与酚羟基相对,有2种排列方式,所以符合条件的同分异构体有
10种,其中一种结构简式为 。
第 17 页 共 17 页