文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海交通大学附属中学 2022—2023 学年高一下学期(等级考)期中考试
化学试题
(满分 100分,60分钟完成,答案请写在答题纸上)
说明:1.本试题卷包含五个主题的内容,即五道大题,别看而错漏做了。
2.“双选”题的给分原则是:全对得“3分”,只答对一得“1分”,一对一错得“0”分。
3.相对原子量:H-1,N-14,O-16,Na-23,Si-28,S-32,Cl-35.5,Fe-56,Cu-64
一、84消毒液的制备及科学使用
1. 新冠病毒曾经伤害人类,也是曾经让你最为惧怕的病毒,但它却只不过是蛋白质包裹着的DNA而已,
使用适当浓度的84消毒液、双氧水等消毒剂即可将其杀死。但是两者混合使用,消毒效果几乎降为零。
此外,84消毒液呈碱性,可以通过氯气与氢氧化钠溶液的反应来制得,这是你知道的。
(1)写出上述两种消毒剂中有效成分的电子式。___________、___________
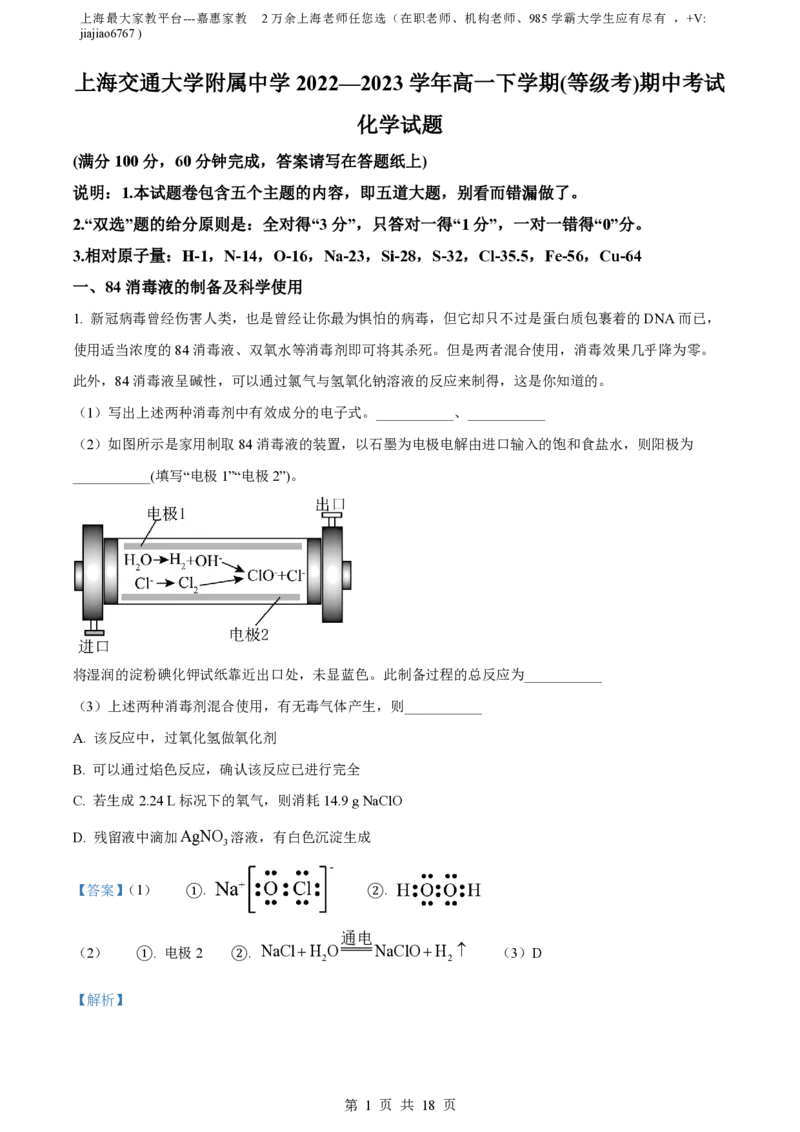
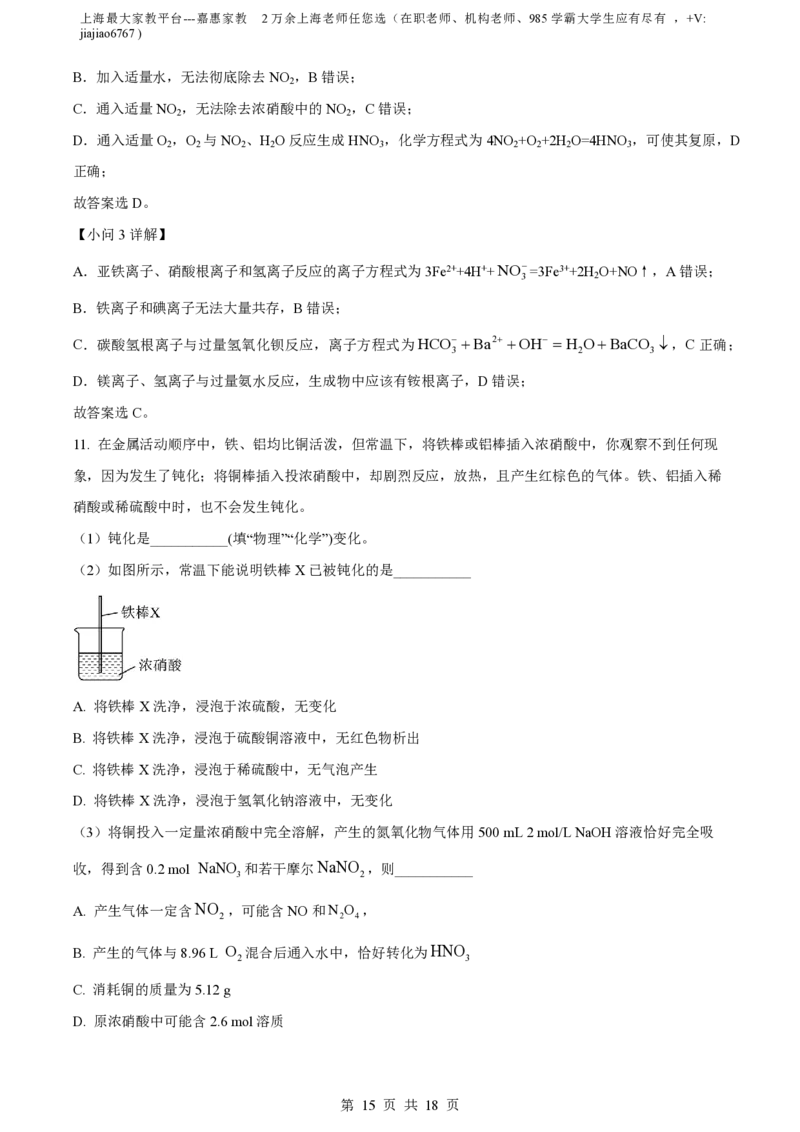
(2)如图所示是家用制取84消毒液的装置,以石墨为电极电解由进口输入的饱和食盐水,则阳极为
___________(填写“电极1”“电极2”)。
将湿润的淀粉碘化钾试纸靠近出口处,未显蓝色。此制备过程的总反应为___________
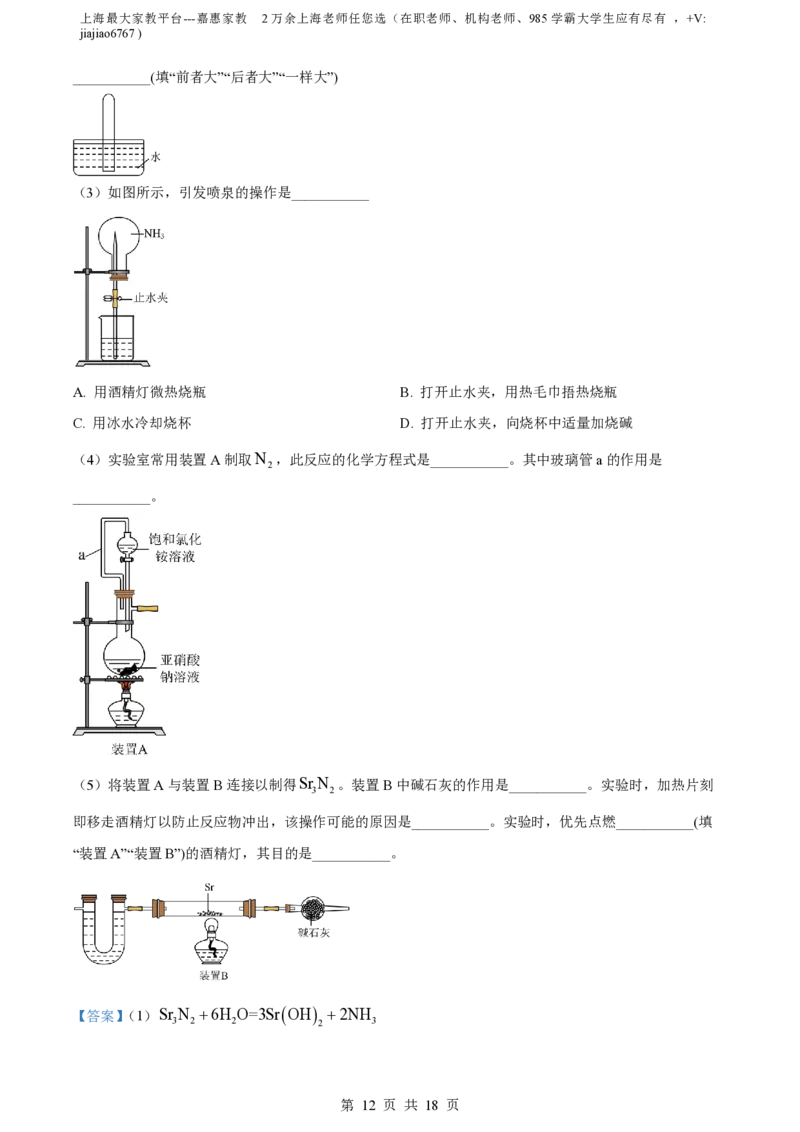
(3)上述两种消毒剂混合使用,有无毒气体产生,则___________
A. 该反应中,过氧化氢做氧化剂
B. 可以通过焰色反应,确认该反应已进行完全
C. 若生成2.24 L标况下的氧气,则消耗14.9 g NaClO
D. 残留液中滴加AgNO 溶液,有白色沉淀生成
3
【答案】(1) ①. ②.
通电
(2) ①. 电极2 ②. NaClH O NaClOH (3)D
2 2
【解析】
第 1 页 共 18 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【小问1详解】
84消毒液中有效成分为次氯酸钠,双氧水中有效成分为H O ,两者的电子式分别为 、
2 2
。
【小问2详解】
从图中可知,在电极2上氯离子失电子转化为氯气,则阳极为电极2。将湿润的淀粉碘化钾试纸靠近出口
处,未显蓝色,原因为氯气与氢氧根离子反应生成了氯离子和次氯酸根离子,制备过程的总反应为
通电
NaClH O NaClOH 。
2 2
【小问3详解】
双氧水和次氯酸钠反应的离子方程式为ClO-+H O =O ↑+H O+Cl-。
2 2 2 2
A.该反应中H O 中O失电子生成氧气,过氧化氢为还原剂,A错误;
2 2
B.钠离子不参与反应,无论反应是否进行完全,溶液中始终存在钠离子,焰色反应现象相同,B错误;
C.若生成标况下2.24L氧气即0.1mol,则消耗次氯酸钠0.1mol为7.45g,C错误;
D.该反应有氯离子生成,则残留液中滴加硝酸银,可生成AgCl白色沉淀,D正确;
故答案选D。
2. Ⅰ.利用75%酒精(分子式为C H O)也可以消杀新冠病毒。如果将84消毒液与之混用以提高消杀效果,那
2 6
你有可能会中毒。因为此时会产生氯仿(分子式为CHCl ,分子呈四面体型),进而继续被氧化为光气,光
3
气却是具有烂苹果气味的毒气,其分子结构如如图所示:
(1)由此推断的结论正确的是___________
A.氯仿分子含非极性键,是极性分子
B.光气分子含极性键,是非极性分子
C.上述变化过程中,-2价碳元素最终被氧化为+4价
D.氯仿和光气两种分子中,所有原子均达到稳定结构
E.酒精与84消毒液混用,一定放出氯气
(2)光气的分子中,C—Cl的键长大于C=O。请你用相关结构知识说明其理由___________。
Ⅱ.如果你把氯酸的浓度提高到40%以上,那将会发生分解反应:
第 2 页 共 18 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
aHClO =bO +cCl +dHClO +eH O,将湿润的淀粉碘化钾试纸较长时间地靠近产生的气体,则你
3 2 2 4 2
会看到试纸先变蓝后又变无色。
(3)根据以上信息做出的推断错误的是___________
A. 由反应可确定:氧化性HClO HClO
4 3
B. 若化学计量数a=8、b=3,则该反应转移电子数为20e
C. 变蓝的淀粉碘化钾试纸又褪色,是因为发生了:4Cl +I +6H O=12H++8Cl-+2IO
2 2 2 3
D. 若氯酸分解得1 mol混合气体的质量为47.6 g,则反应方程式可表示为:
26HClO =15O 8Cl 10HClO 8H O
3 2 2 4 2
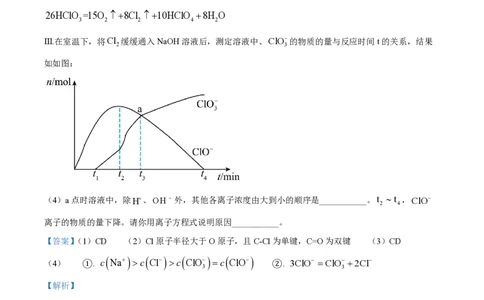
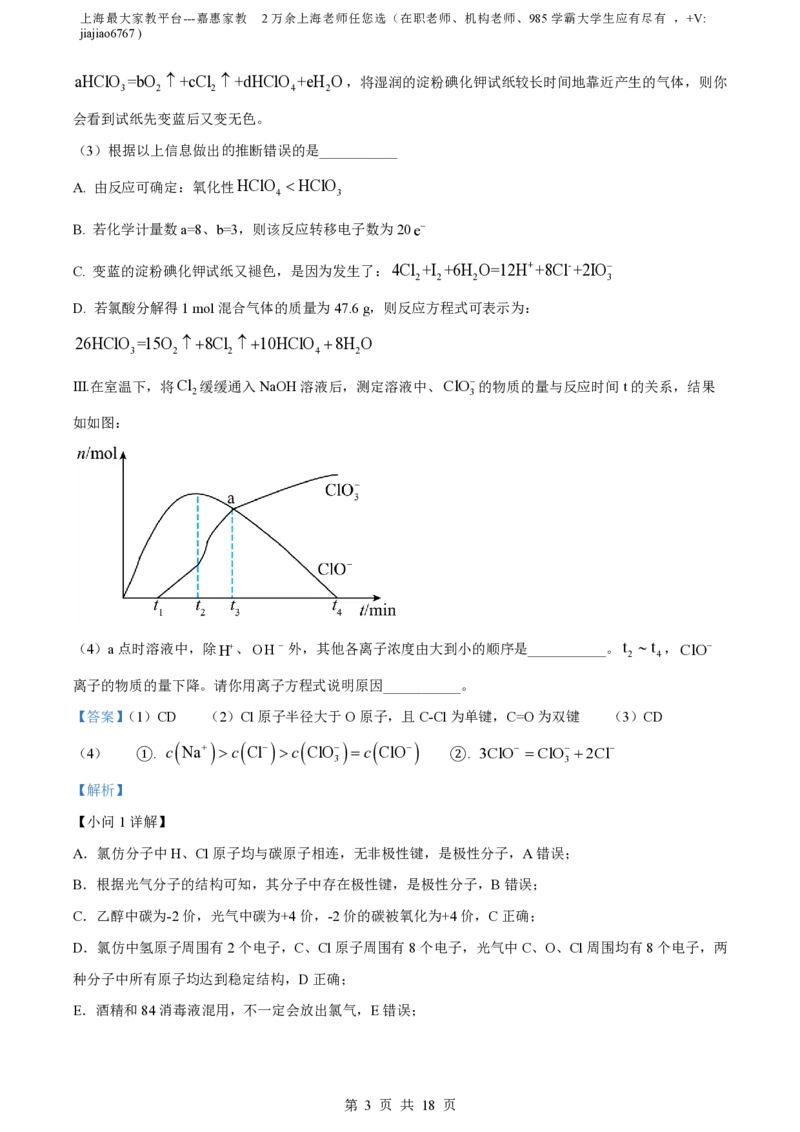
Ⅲ.在室温下,将Cl 缓缓通入NaOH溶液后,测定溶液中、ClO的物质的量与反应时间t的关系,结果
2 3
如如图:
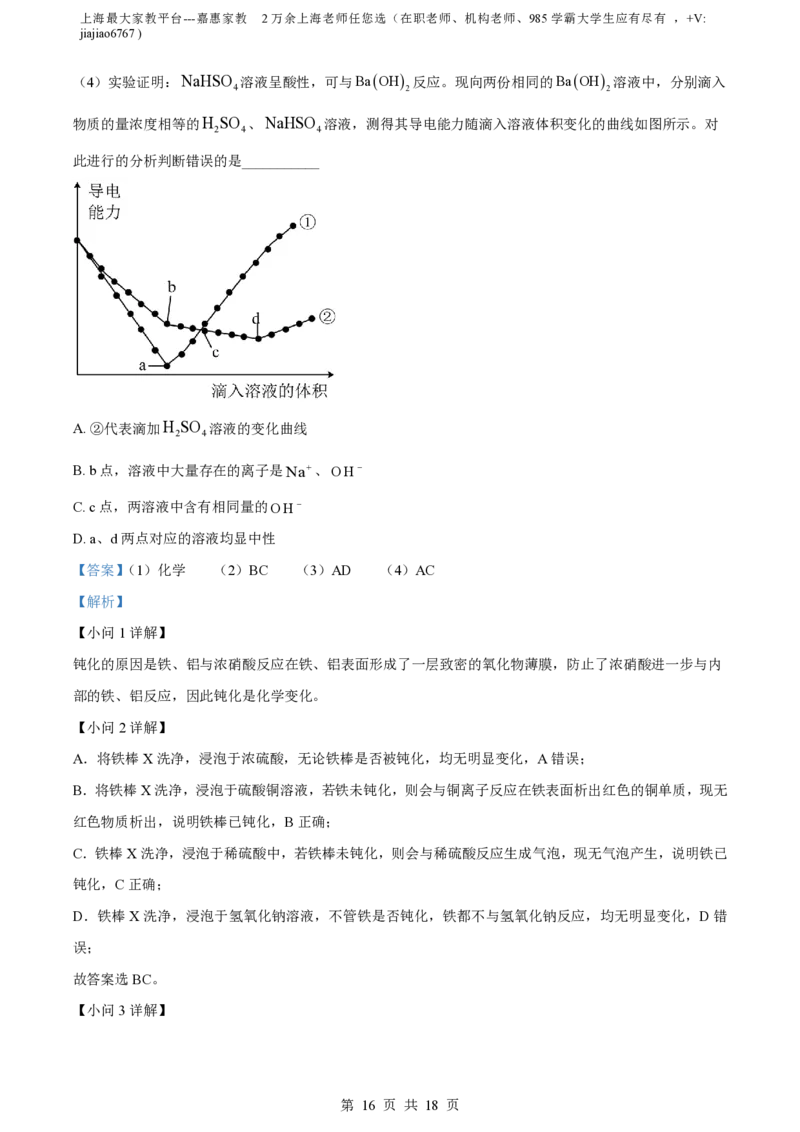
(4)a点时溶液中,除H、OH 外,其他各离子浓度由大到小的顺序是___________。t t ,ClO
2 4
离子的物质的量下降。请你用离子方程式说明原因___________。
【答案】(1)CD (2)Cl原子半径大于O原子,且C-Cl为单键,C=O为双键 (3)CD
(4) ①. c Na c Cl c ClO c ClO ②. 3ClO ClO 2Cl
3 3
【解析】
【小问1详解】
A.氯仿分子中H、Cl原子均与碳原子相连,无非极性键,是极性分子,A错误;
B.根据光气分子的结构可知,其分子中存在极性键,是极性分子,B错误;
C.乙醇中碳为-2价,光气中碳为+4价,-2价的碳被氧化为+4价,C正确;
D.氯仿中氢原子周围有2个电子,C、Cl原子周围有8个电子,光气中C、O、Cl周围均有8个电子,两
种分子中所有原子均达到稳定结构,D正确;
E.酒精和84消毒液混用,不一定会放出氯气,E错误;
第 3 页 共 18 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
故答案选CD。
【小问2详解】
氯原子的半径大于氧原子的半径,且C-Cl键为单键,C=O为双键,双键的键能更大,键长更短,因此C-
Cl的键长大于C=O。
【小问3详解】
A.该反应中HClO 既是氧化剂也是还原剂,HClO 为氧化产物,故氧化性HClO I ,同理I 能与SO 反应
2 2 2 2
且I 作氧化剂,则氧化性I >SO ,C正确;
2 2 2
D.Cu2+与碘离子反应的离子方程式为2Cu2++4I-=2CuI↓+I ,转移2mol电子,生成2molCuI,D正确;
2
故答案选CD。
三、物质结构与化学反应中的能量
5. 科研人员曾发明了一种水电池,这种电池能利用淡水和海水之间的含盐量差进行供电,该电池的化学反
应为:5MnO 2Ag2NaCl Na Mn O 2AgCl
2 2 5 10
(1)该反应中,发生的还原过程是___________。溶液中减小1 mol Cl时,转移电子数是___________。
(2)简述NaCl晶体的熔点比Na O低原因___________。
2
(3)晶体Na O晶胞结构如图,其中黑球代表Na,推断正确的是___________
2
第 7 页 共 18 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. Na半径大于O2半径
B. 其熔点高于冰,是因为Na O分子间作用力较大
2
C. 晶胞中,与Na距离最近O2有6个
248
2
D. 晶胞中,若最近的O2之间的距离为 a cm,则其密度为 (g·cm-3)
2
a3N
A
【答案】(1) ①.
M
4
nM
3.
n
6 (或MnO
2
Mn
5
O
1
2
0
) ②. N
A
(2)NaCl和Na O均为离子晶体,熔点由离子键强弱决定,Cl电荷数小于O2,且离子半径大于O2,
2
NaCl中离子键较Na O弱,故NaCl晶体的熔点比Na O低 (3)D
2 2
【解析】
【小问1详解】
5MnO 2Ag2NaCl Na Mn O 2AgCl反应中,发生的还原过程是元素化合价降低的过程,即
2 2 5 10
M
4
nM
3.
n
6 (或MnO
2
Mn
5
O
1
2
0
);溶液中减小1mol Cl时,生成1mol AgCl,有1mol Ag参加反应,
转移电子数是N 。
A
【小问2详解】
NaCl晶体的熔点比Na O低原因:NaCl和Na O均为离子晶体,熔点由离子键强弱决定,Cl电荷数小
2 2
于O2,且离子半径大于O2,NaCl中离子键较Na O弱,故NaCl晶体的熔点比Na O低。
2 2
【小问3详解】
A.电子层数越多,原子或离子的半径越大,电子层数相同时,核电荷数越大,对核外电子的吸引能力越
强,离子半径越小,Na半径小于O2半径,故A错误;
B.其熔点高于冰,是因为Na O是离子晶体,冰是分子晶体,离子晶体的熔点高于分子晶体,故B错
2
误;
C.晶胞中,与Na距离最近O2有4个,故C错误;
第 8 页 共 18 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2
D.晶胞中,若最近的O2之间的距离为 a cm,面对角线为 2 a cm,晶胞的边长为a cm,阴离子位
2
1
1
于晶胞的顶点和面心,阳离子位于晶胞的体心,则Na+的个数为8,O2-的个数为8× +6× =4,每个晶胞
8 2
416232 248 248
的质量为 g,晶胞的体积为a3 cm3,则晶体的密度为ρ= (g·cm-3),故D正
N N a3N
A A A
确;
故答案为D。
6. 高纯硅具有良好的硬度和耐磨性以及良好的光、电性能,广泛用于芯片、集成电路、光伏电池板等领
域。工业上制备高纯硅反应的化学方程式:SiCl
4
g2H
2
g
Sis4HClg
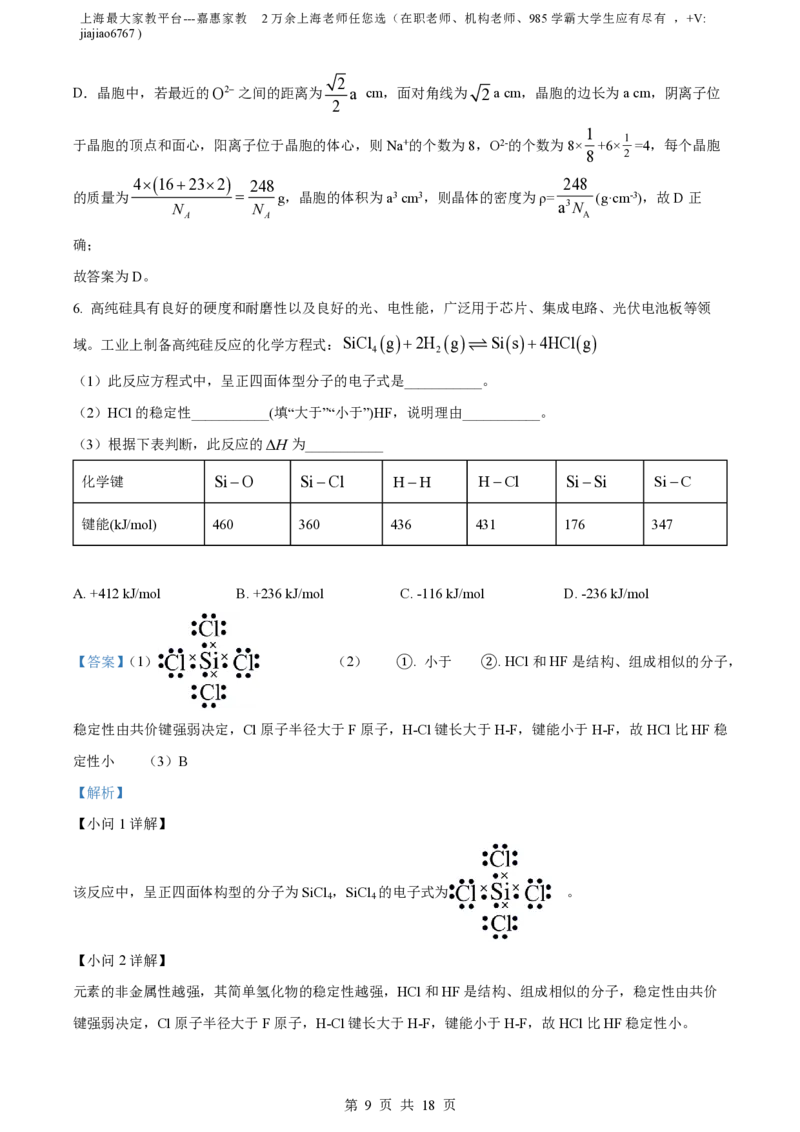
(1)此反应方程式中,呈正四面体型分子的电子式是___________。
(2)HCl的稳定性___________(填“大于”“小于”)HF,说明理由___________。
(3)根据下表判断,此反应的H 为___________
化学键 SiO SiCl HH HCl SiSi SiC
键能(kJ/mol) 460 360 436 431 176 347
A. +412 kJ/mol B. +236 kJ/mol C. -116 kJ/mol D. -236 kJ/mol
【答案】(1) (2) ①. 小于 ②. HCl和HF是结构、组成相似的分子,
稳定性由共价键强弱决定,Cl原子半径大于F原子,H-Cl键长大于H-F,键能小于H-F,故HCl比HF稳
定性小 (3)B
【解析】
【小问1详解】
该反应中,呈正四面体构型的分子为SiCl ,SiCl 的电子式为 。
4 4
【小问2详解】
元素的非金属性越强,其简单氢化物的稳定性越强,HCl和HF是结构、组成相似的分子,稳定性由共价
键强弱决定,Cl原子半径大于F原子,H-Cl键长大于H-F,键能小于H-F,故HCl比HF稳定性小。
第 9 页 共 18 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【小问3详解】
ΔH=反应物键能总和-生成物键能总和=(4×360+2×436-431×4-2×176)kJ/mol=+236kJ/mol,故答案选B。
7. 由于人类的活动向大气排放NO对环境造成了一定的污染,我国严格控制其排放总量,标志着国家已经
x
从单纯控制SO 向全面控制酸性气体排放的方向走出了新的一步。
2
用CH 催化还原NO可以消除氮氧化合物的污染。例如:
4 x
①CH g4NO g4NOgCO g2H Og ;ΔH 574 kJ/mol
4 2 2 2
②CH g4NOg2N gCO g2H Og ;ΔH 1160 kJ/mol
4 2 2 2
(1)根据上述信息推断正确的是___________
A. 等物质的量的CH 在反应①、②中转移电子数相同
4
B. 由反应②可推知:CH g4NOg2N gCO g2H Ol ;ΔH 1160 kJ/mol
4 2 2 2
C. 4NO g2N g8NOg ;ΔH 586 kJ/mol
2 2
D. 若用标准状况下4.48 L CH 把NO 还原为N ,整个过程中转移的电子总数为1.6N
4 2 2 A
(2)正确的选项是___________
A. 化学反应中,吸热反应需不断从外界获得能量,放热反应不需从外界获得能量
B. 甲烷的燃烧热ΔH 890 kJ/mol,则甲烷燃烧的热化学方程式为:
CH g2O gCO g2H Og ΔH 890 kJ/mol
4 2 2 2
C.
常温常压下:HClaqNaOHaq NaClaqH Ol
ΔH 57.3 kJ/mol,则:
2
H SO aqBaOH aqBaSO s2H Ol ΔH 114.6 kJ/mol
2 4 2 4 2
D. 已知SsO gSO g ΔH Q kJ·mol1,SgO gSO g ΔH Q kJ/mol,
2 2 1 2 2 2
则Q Q
1 2
【答案】(1)AD (2)D
【解析】
【小问1详解】
A.两个反应中CH 均转化为CO ,则等物质的量的CH 在反应①、②中转移电子数相同,A正确;
4 2 4
B.由气态水转化为液态水,ΔH<0,则由反应②可知,ΔH<-1160kJ/mol,B错误;
C.选项中的反应可由反应①-反应②得到,ΔH=(-574+1160)kJ/mol=+586kJ/mol,C错误;
第 10 页 共 18 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D.标况下4.48LCH 为0.2mol,0.2molCH 转化为CO 转移电子数为0.2×8=1.6mol,D正确;
4 4 2
故答案选AD。
【小问2详解】
A.有些放热反应也需要从外界获得能量,如铝热反应,A错误;
B.燃烧热的热化学方程式中生成的水需为液态水,选项中为气态水,B错误;
C.硫酸和氢氧化钡反应中除了生成水还有硫酸钡生成,会放出热量,ΔH<-114.6kJ/mol,C错误;
D.固态硫转化为气态硫吸热,则-Q >-Q ,即Q