文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海交通大学附属中学 2023—2024 学年度第一学期
高二化学摸底测试
可能用到的相对原子质量:H:1 C:12 O:16 Na:23 S:32 Cl:35.5 Fe:56
Cu:64 I:127
1. 下列物质中的硫元素不能表现出氧化性的是
A. S B. Na S C. SO D. H SO
2 2 2 4
2. 下列有关浓硫酸的说法中,不正确的是
A. 浓硫酸能与锌粒反应制备氢气
B. 浓硫酸能与灼热的木炭反应,产生二氧化碳和二氧化硫气体
C. 浓硫酸具有吸水性,在实验中常用作干燥剂
D. 冷的浓硫酸可以用铁质或铝质容器储存
3. 将4g铁粉与2.5g硫粉在研钵中充分混合后装入试管中,在试管口塞上带长导管的橡皮塞,并在导管末
端放入一小团蘸有NaOH溶液的棉花,加热试管。
(1)写出铁与硫反应的化学方程式___________。
(2)已知硫的熔点为106.8℃、沸点为444.7℃,解释试管口为什么向上倾斜___________。
(3)棉花中的NaOH用于吸收反应过程中产生的二氧化硫,写出该反应的离子方程式___________。
(4)工业上通常用接触法制硫酸。在制硫酸的生产中,若有32吨硫黄最终全部转化为硫酸,则可以制得
质量分数为98%的浓硫酸为___________吨。已知98%的硫酸密度为1.84g/cm3,计算此溶液的物质的量浓
度为___________mol/L。
4. 氮循环是大气中的氮气经微生物等作用进入土壤与海洋,为动植物所利用,最终又在微生物的参与下返
回大气,如此反复循环,建立起的平衡。
(1)土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要
化学原理如下:___K S+____KNO ___H O___N ___K SO ___KOH,配平上述反应方程
2 3 2 2 2 4
第 1 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
式,并标出电子转移的方向和数目__________________________。
(2)氨态氮(NH )与亚硝态氮(NO )可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol
3 2
氮气时,转移电子的物质的量为___________mol。
5. 下列关于化学键与化合物的叙述正确的是
A. 含有正离子的物质一定是离子化合物
B. 离子化合物中一定含有离子键,可能含有共价键
C. 分子晶体中一定含有共价键,不含离子键
D. 只由共价键形成的物质一定是共价化合物
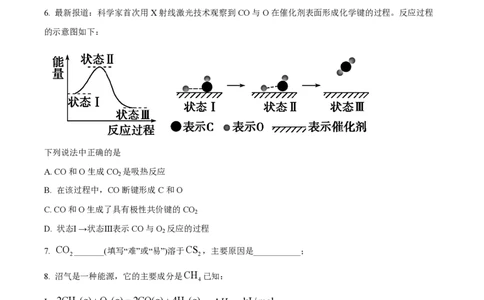
6. 最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程
的示意图如下:
下列说法中正确的是
A. CO和O生成CO 是吸热反应
2
B. 在该过程中,CO断键形成C和O
C. CO和O生成了具有极性共价键的CO
2
D. 状态Ⅰ →状态Ⅲ表示CO与O 反应的过程
2
7. CO _______(填写“难”或“易”)溶于CS ,主要原因是___________;
2 2
8. 沼气是一种能源,它的主要成分是CH 已知:
4
Ⅰ:2CH (g)O (g)2CO(g)4H (g) H akJ/mol
4 2 2
Ⅱ:CO(g)2H (g)CH OH(g) H bkJ/mol
2 3
则由CH 和O 制取气态甲醇的热化学方程式:2CH (g)O (g)2CH OH ΔH 中ΔH =
4 2 4 2 3 3 3
___________。
9. 实现下列变化,需克服相同类型作用力的是
A. 硫酸氢钠和氯化钠分别受热熔化 B. 冰的融化和水的分解
第 2 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. 乙醇和HCl溶于水 D. 干冰和碘的升华
10. 常温下,0.5molCH 完全燃烧生成CO (g)和液态水时,放出445kJ热量,则该反应的热化学方程式
4 2
为___________。
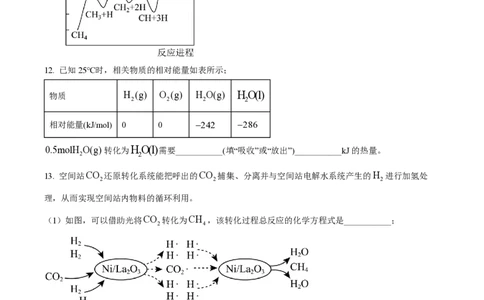
11. 一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第_______步的
4
正反应活化能最大。
12. 已知25℃时,相关物质的相对能量如表所示;
物质 H (g) O (g) H O(g) HO(l)
2 2 2 2
相对能量(kJ/mol) 0 0 242 286
0.5molH O(g)转化为HO(l)需要___________(填“吸收”或“放出”)___________kJ的热量。
2 2
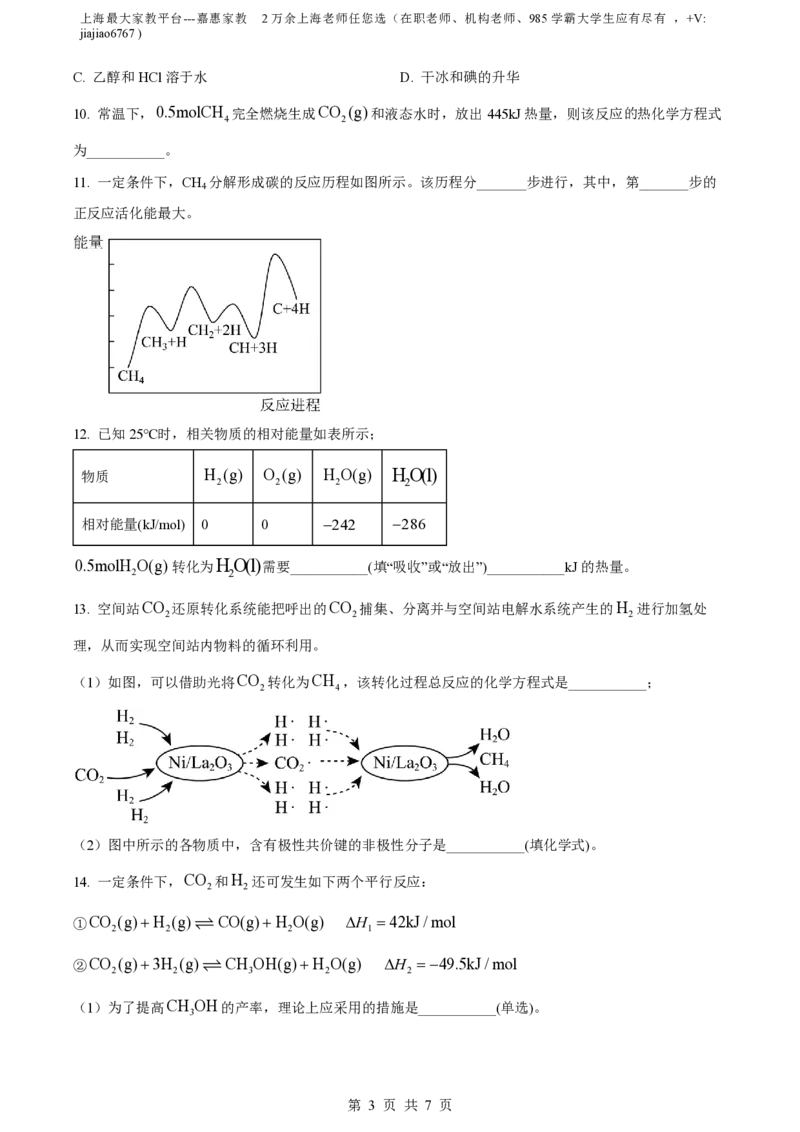
13. 空间站CO 还原转化系统能把呼出的CO 捕集、分离并与空间站电解水系统产生的H 进行加氢处
2 2 2
理,从而实现空间站内物料的循环利用。
(1)如图,可以借助光将CO 转化为CH ,该转化过程总反应的化学方程式是___________;
2 4
(2)图中所示的各物质中,含有极性共价键的非极性分子是___________(填化学式)。
14. 一定条件下,CO 和H 还可发生如下两个平行反应:
2 2
①CO
2
(g)H
2
(g)
CO(g)H
2
O(g) H
1
42kJ/mol
②CO
2
(g)3H
2
(g)
CH
3
OH(g)H
2
O(g) H
2
49.5kJ/mol
(1)为了提高CH OH的产率,理论上应采用的措施是___________(单选)。
3
第 3 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 低温低压 B. 高温低压 C. 高温高压 D. 低温高压
nCO 1
(2)保持温度533K、压强3MPa,按投料比 2 向容器中充入CO 和H ,反应相同时间测得
nH 3 2 2
2
不同催化剂下CO 转化率和CH OH选择性的相关实验数据如下表所示(已知CH OH选择性:转化的
2 3 3
CO 中生成CH OH的百分比)。
2 3
催化剂 CO 转化率 CH OH选择性
2 3
催化剂A 21.9% 67.3%
催化剂B 36.1% 100.0%
上述条件下,使用催化剂B作催化剂,下列说法能判断反应②达到平衡状态的是___________(单选)。
A. 气体压强不再变化 B. 气体平均相对分子质量不再变化
C. CH OH和H O的物质的量之比为1:1 D. CO 和H 的物质的量之比不再变化
3 2 2 2
(3)一定条件下,向0.5L恒容密闭容器中充入1molCO 和3molH ,只发生上述反应②,达平衡时,
2 2
H 的转化率为80%,则该温度下的平衡常数K ___________(保留两位小数。)
2
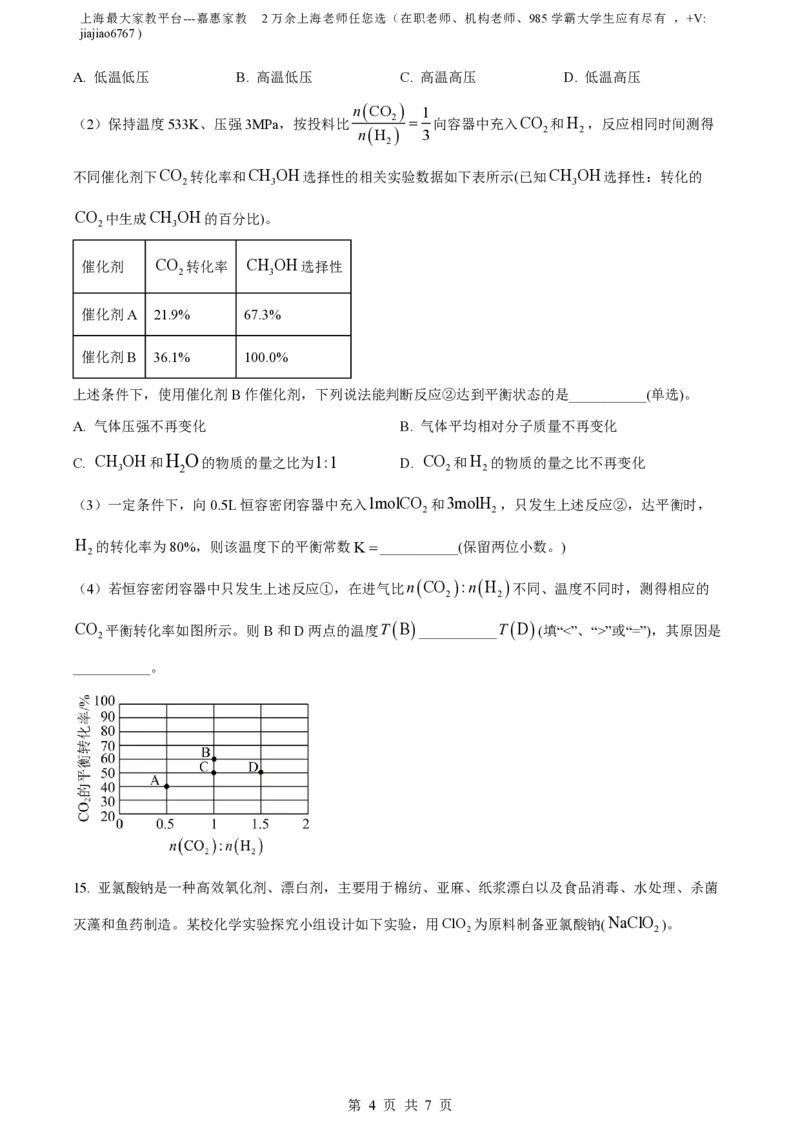
(4)若恒容密闭容器中只发生上述反应①,在进气比nCO :nH
不同、温度不同时,测得相应的
2 2
CO 平衡转化率如图所示。则B和D两点的温度TB ___________TD (填“<”、“>”或“=”),其原因是
2
___________。
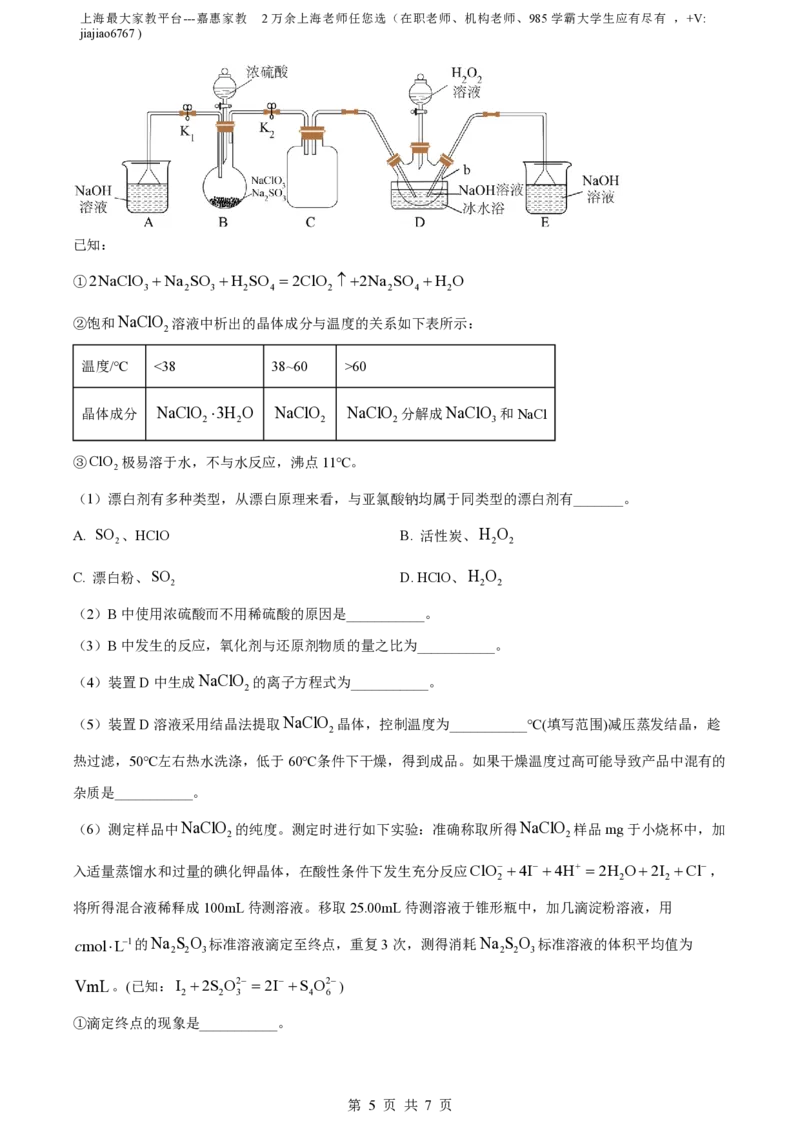
15. 亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、亚麻、纸浆漂白以及食品消毒、水处理、杀菌
灭藻和鱼药制造。某校化学实验探究小组设计如下实验,用ClO 为原料制备亚氯酸钠(NaClO )。
2 2
第 4 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知:
①2NaClO Na SO H SO 2ClO 2Na SO H O
3 2 3 2 4 2 2 4 2
②饱和NaClO 溶液中析出的晶体成分与温度的关系如下表所示:
2
温度/℃ <38 38~60 >60
晶体成分 NaClO 3H O NaClO NaClO 分解成NaClO 和NaCl
2 2 2 2 3
③ClO 极易溶于水,不与水反应,沸点11℃。
2
(1)漂白剂有多种类型,从漂白原理来看,与亚氯酸钠均属于同类型的漂白剂有_______。
A. SO 、HClO B. 活性炭、H O
2 2 2
C. 漂白粉、SO D. HClO、H O
2 2 2
(2)B中使用浓硫酸而不用稀硫酸的原因是___________。
(3)B中发生的反应,氧化剂与还原剂物质的量之比为___________。
(4)装置D中生成NaClO 的离子方程式为___________。
2
(5)装置D溶液采用结晶法提取NaClO 晶体,控制温度为___________℃(填写范围)减压蒸发结晶,趁
2
热过滤,50℃左右热水洗涤,低于60℃条件下干燥,得到成品。如果干燥温度过高可能导致产品中混有的
杂质是___________。
(6)测定样品中NaClO 的纯度。测定时进行如下实验:准确称取所得NaClO 样品mg于小烧杯中,加
2 2
入适量蒸馏水和过量的碘化钾晶体,在酸性条件下发生充分反应ClO 4I 4H 2H O2I Cl,
2 2 2
将所得混合液稀释成100mL待测溶液。移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用
cmolL1的Na S O 标准溶液滴定至终点,重复3次,测得消耗Na S O 标准溶液的体积平均值为
2 2 3 2 2 3
VmL。(已知:I 2S O2 2I S O2)
2 2 3 4 6
①滴定终点的现象是___________。
第 5 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
②该样品中NaClO 质量分数为___________(用含c、V、m的代数式表示)。
2
16. 水是一种很好的溶剂,也是物质发生化学反应的主要介质。水中世界千千万,它与我们的生活、生产
密切相关,请用所学知识,解决下列问题。
(1)某温度下纯水中的c(H)2107mol/L,则此时溶液中的c(OH)___________;在该温度下,
0.04molL的NaOH溶液的pH=___________;
(2)该温度下,某溶液中由水电离产生的c(OH)和c(H)的乘积为1.61017,则该溶液的
pH=___________。
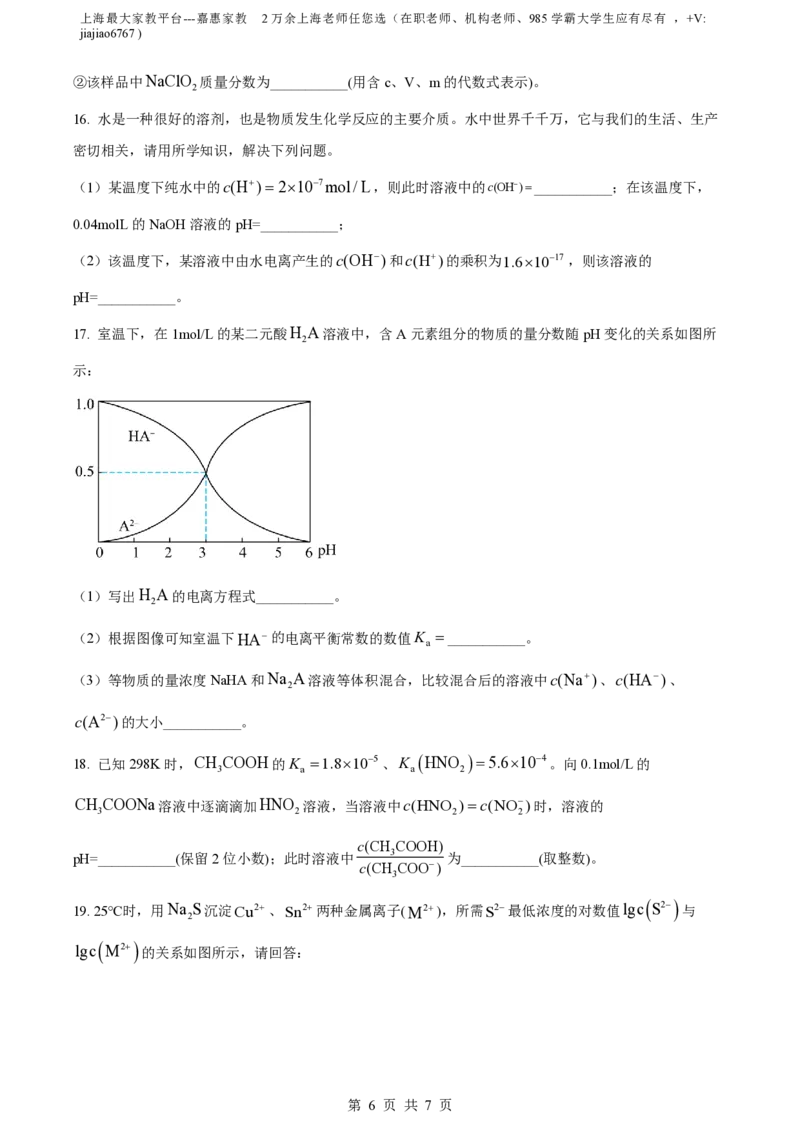
17. 室温下,在1mol/L的某二元酸H A溶液中,含A元素组分的物质的量分数随pH变化的关系如图所
2
示:
(1)写出H A的电离方程式___________。
2
(2)根据图像可知室温下HA 的电离平衡常数的数值K ___________。
a
(3)等物质的量浓度NaHA和Na A溶液等体积混合,比较混合后的溶液中c(Na)、c(HA)、
2
c(A2)的大小___________。
18. 已知298K时,CH COOH的K 1.8105、K HNO 5.6104。向0.1mol/L的
3 a a 2
CH COONa溶液中逐滴滴加HNO 溶液,当溶液中c(HNO )c(NO)时,溶液的
3 2 2 2
c(CH COOH)
pH=___________(保留2位小数);此时溶液中 3 为___________(取整数)。
c(CH COO)
3
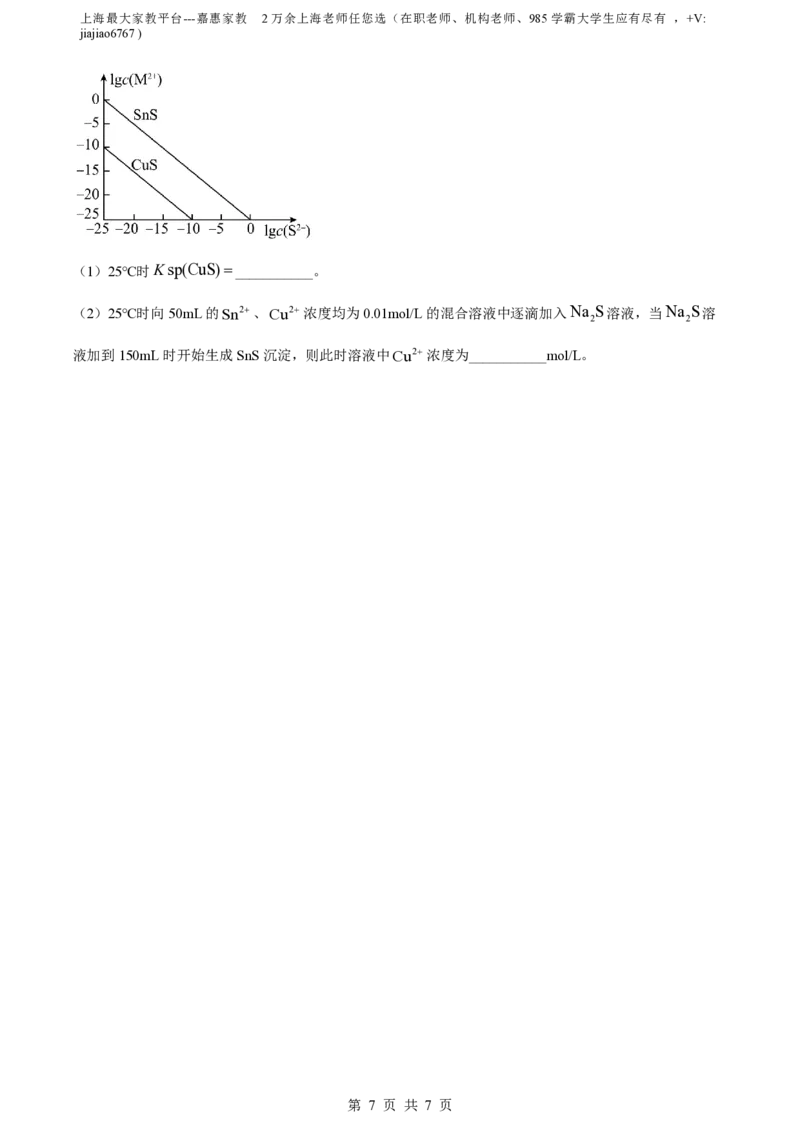
19. 25℃时,用Na S沉淀Cu2、Sn2两种金属离子(M2),所需S2最低浓度的对数值lgc
S2
与
2
lgc
M2
的关系如图所示,请回答:
第 6 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(1)25℃时Ksp(CuS)___________。
(2)25℃时向50mL的Sn2、Cu2浓度均为0.01mol/L的混合溶液中逐滴加入Na S溶液,当Na S溶
2 2
液加到150mL时开始生成SnS沉淀,则此时溶液中Cu2浓度为___________mol/L。
第 7 页 共 7 页