文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海交通大学附属中学 2022—2023 学年度
第二学期高二化学期中试卷
可能用到的相对原子质量:Cu-64
1. 通过电解法精炼铜不仅仅是一种炼铜的方法,也是一种回收提纯铜的方法。已知粗铜中含有的主要杂质
有Zn、Fe、Ni、Ag、Pt、Au等金属。
(1)在电解精炼铜中,纯铜作为该装置的______极,而粗铜与外接电源的______极相连。
(2)该电化学装置中,电解质溶液的主要溶质是一种硫酸正盐,则该溶质为______(填入化学式),精炼结
束后,该溶质的浓度______(填字母)。
A.变大 B.变小 C.不变 D.无法判断
(3)纯铜每增加3.2g,则外电路中转移了______mol电子。
(4)电解质溶液中还会加入少许稀硫酸,其主要作用为______(填字母)。
A. 增加硫酸根的浓度 B. 让粗铜中部分杂质与稀硫酸反应
C. 利用其氧化性促进Cu溶解 D. 抑制Cu2+水解
(5)电解一段时间后,阳极附近产生沉淀,称为“阳极泥”,其成分为______(填字母)。
A. Ag B. Pt C. Au D. Fe
金属铜的纯度可以通过滴定的方式测定。某精炼后的铜样品质量为0.2539g,经处理后完全转化为含Cu2+
的溶液,向其中加入过量的KI溶液,发生反应2Cu2++4I-=2CuI+I 。经再次处理后,用0.1099mol•L-1的
2
Na S O 溶液滴定生成的I ,发生反应I +2Na S O =Na S O +2NaI,消耗Na S O 溶液36.05mL。
2 2 3 2 2 2 2 3 2 4 6 2 2 3
(6)本实验使用______试剂作为指示剂。滴定达到终点时,溶液颜色由______色变为_____色,且
______。
(7)基于本实验得数据,可以算出该精炼铜样品中铜的质量分数为______(以小数表示,保留4位有效
数)。
(8)下列操作中,哪些会使得最终测定结果偏大______(填字母)。
A. 滴定前滴定管尖嘴处有气泡,滴定后气泡消失
B. 滴定管用蒸馏水润洗后未用标准液润洗
C. 在滴定过程中,有少许待测液溅出
D. 用于装待测液的锥形瓶未用待测液润洗
2. 工业废水中常含有一定量的Cr O2和CrO2,它们会对人类及生态系统产生很大的伤害,必须进行处
2 7 4
理。该法的工艺流程为:
第 1 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
CrO2 H+ Cr O2 Fe2 Cr3+OH Cr(OH) ↓
4 ①转化 2 7 ②还原 ③沉淀 3
其中第①步存在平衡:2CrO2
4
(黄色)+2H+‡ˆ ˆˆ†ˆ Cr
2
O
7
2(橙色)+H
2
O
(1) Cr的价层电子轨道表示式为______。
24
(2)Cr元素在自然界有4种同位素,其丰度如表所示:
质量数 50 52 53 54
丰度 4.31% 83.76% 9.55% 2.38%
则Cr元素的近似相对原子质量为______(结果保留2位小数)。
(3)若第①步中平衡体系的pH=2,则该溶液显_____色;向该溶液中加入Ba(NO ) 溶液(已知BaCrO 为
3 2 4
黄色沉淀)则平衡_____移动(填“向左”或“向右”或“不变”)。
(4)能说明第①步反应达平衡状态的是_____(填字母)。
A.Cr O2和CrO2的浓度相同 B.2v(Cr O2)=v(CrO2) C.溶液的颜色不变
2 7 4 2 7 4
(5)第②步中,还原1molCr O2离子,需要_____mol的FeSO •7H O。
2 7 4 2
(6)第③步生成Cr(OH) 沉淀前,先向[Cr3+]=0.1mol•L-1的溶液中加碱,调节pH至_____~___________分
3
离回收Fe(OH) 。
3
(已知:常温下,Fe(OH) 的溶度积K =1×10-39,Cr(OH) 的溶度积K =1×10-32;某种离子的浓度小于10-
3 sp 3 sp
5mol•L-1时,认为其完全沉淀)
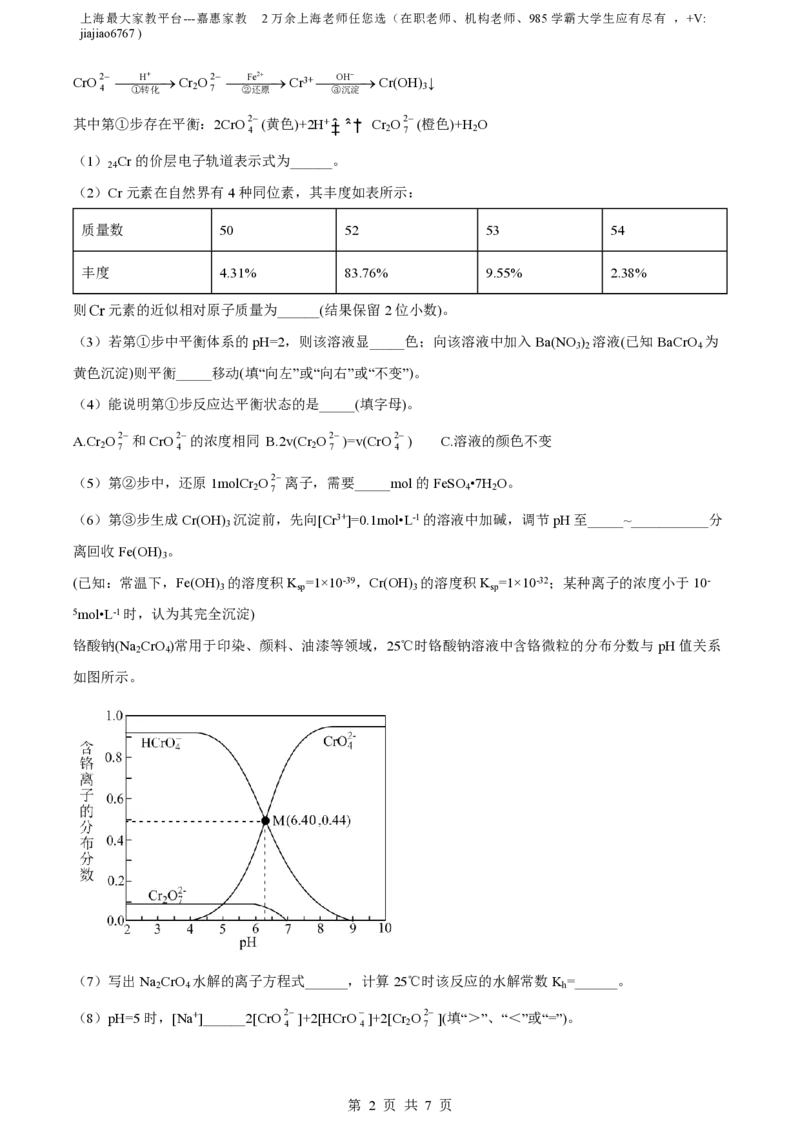
铬酸钠(Na CrO )常用于印染、颜料、油漆等领域,25℃时铬酸钠溶液中含铬微粒的分布分数与pH值关系
2 4
如图所示。
(7)写出Na CrO 水解的离子方程式______,计算25℃时该反应的水解常数K =______。
2 4 h
(8)pH=5时,[Na+]______2[CrO2]+2[HCrO]+2[Cr O2](填“>”、“<”或“=”)。
4 4 2 7
第 2 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
3. 研究NO 、SO 、CO等气体的无害化处理对治理大气污染、建设生态文明具有重要意义。
x 2
(1)已知:2SO
2
(g)+O
2
(g)‡ˆ ˆˆ†ˆ 2SO
3
(g) △H
1
=-196.6kJ•mol-1
2NO(g)+O
2
(g)‡ˆ ˆˆ†ˆ 2NO
2
(g) △H
2
=-113.0kJ•mol-1
计算:NO
2
(g)+SO
2
(g)‡ˆ ˆˆ†ˆ SO
3
(g)+NO(g)的△H=______kJ•mol-1。
(2)对于上述反应,下列说法错误的是______(填字母)。
A. 该反应在理论上可设计为原电池
B. 反应气体分子数不变,因此反应熵变较小
C. 若反应是基元反应,每一次分子间的碰撞均为有效碰撞
D. 若将NO 中的氧原子用18O标记,一段时间后会出现18O标记的SO 分子
2 2
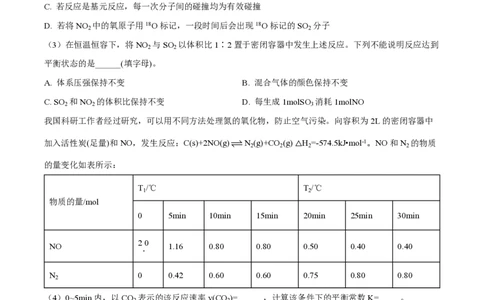
(3)在恒温恒容下,将NO 与SO 以体积比1∶2置于密闭容器中发生上述反应。下列不能说明反应达到
2 2
平衡状态的是______(填字母)。
A. 体系压强保持不变 B. 混合气体的颜色保持不变
C. SO 和NO 的体积比保持不变 D. 每生成1molSO 消耗1molNO
2 2 3
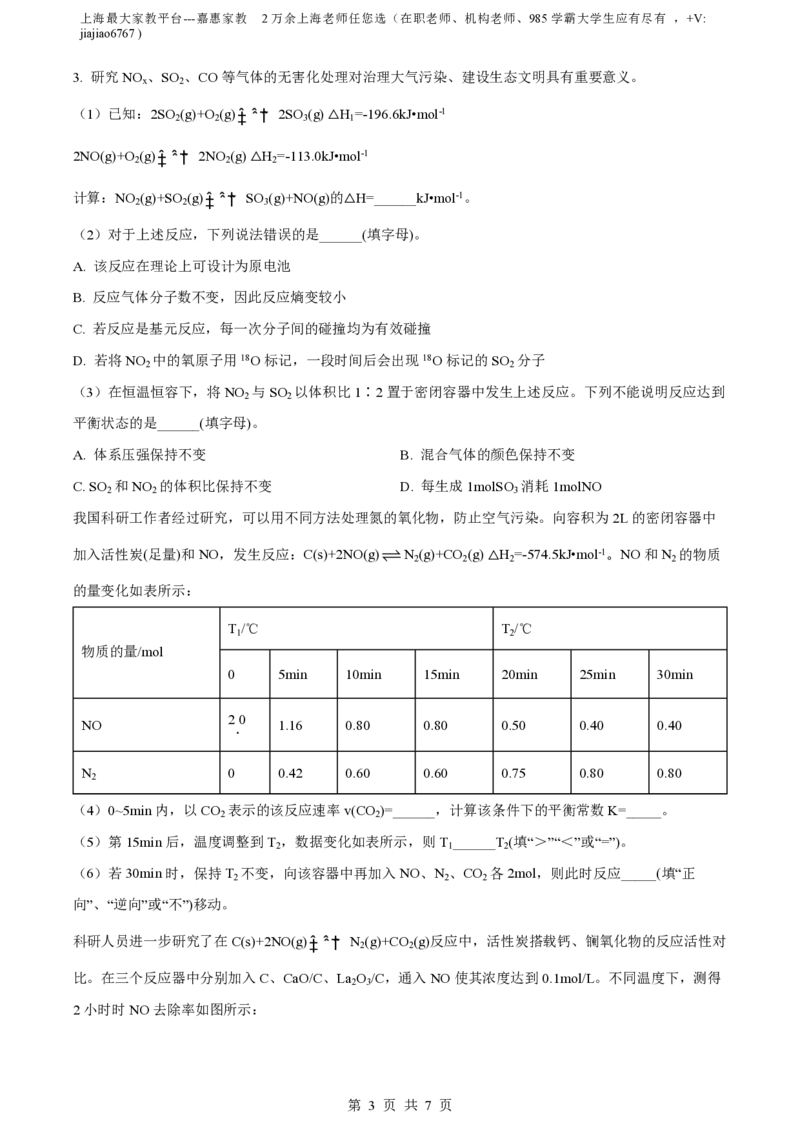
我国科研工作者经过研究,可以用不同方法处理氮的氧化物,防止空气污染。向容积为2L的密闭容器中
加入活性炭(足量)和NO,发生反应:C(s)+2NO(g) N (g)+CO (g) △H =-574.5kJ•mol-1。NO和N 的物质
2 2 2 2
的量变化如表所示:
T /℃ T /℃
1 2
物质的量/mol
0 5min 10min 15min 20min 25min 30min
20
NO . 1.16 0.80 0.80 0.50 0.40 0.40
N 0 0.42 0.60 0.60 0.75 0.80 0.80
2
(4)0~5min内,以CO 表示的该反应速率v(CO )=______,计算该条件下的平衡常数K=_____。
2 2
(5)第15min后,温度调整到T ,数据变化如表所示,则T ______T (填“>”“<”或“=”)。
2 1 2
(6)若30min时,保持T 不变,向该容器中再加入NO、N 、CO 各2mol,则此时反应_____(填“正
2 2 2
向”、“逆向”或“不”)移动。
科研人员进一步研究了在C(s)+2NO(g)‡ˆ ˆˆ†ˆ N
2
(g)+CO
2
(g)反应中,活性炭搭载钙、镧氧化物的反应活性对
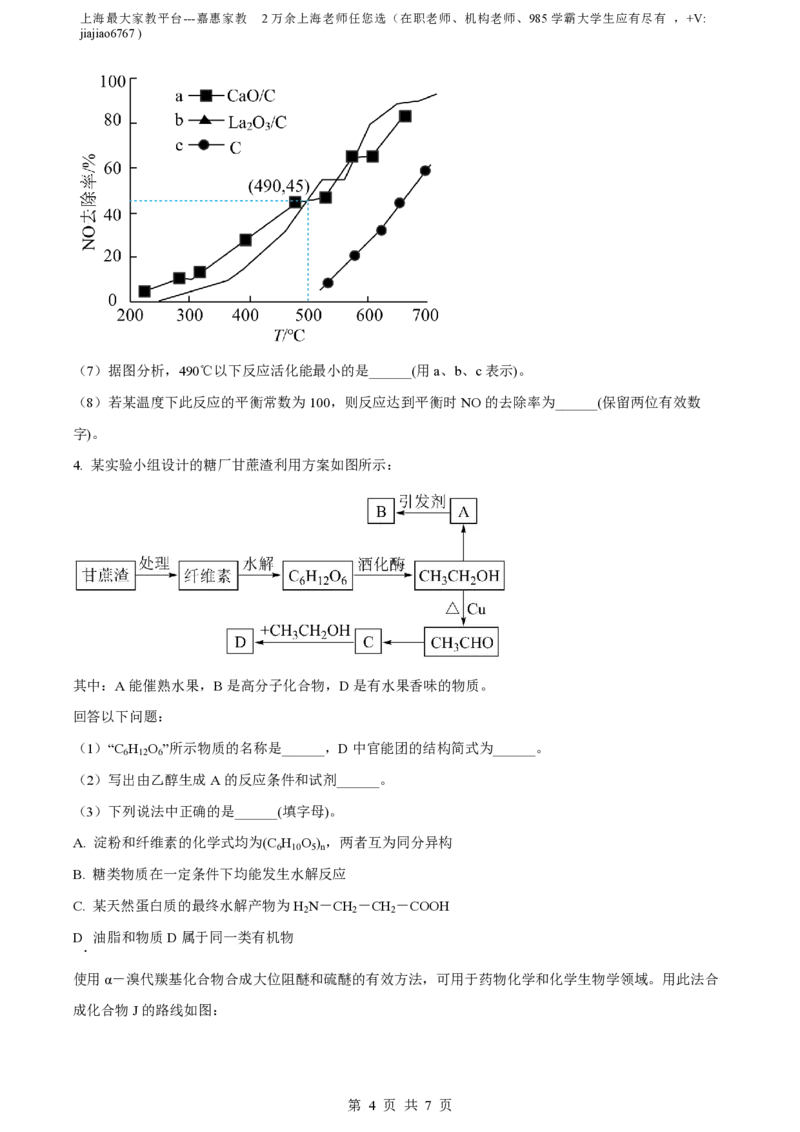
比。在三个反应器中分别加入C、CaO/C、La O /C,通入NO使其浓度达到0.1mol/L。不同温度下,测得
2 3
2小时时NO去除率如图所示:
第 3 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
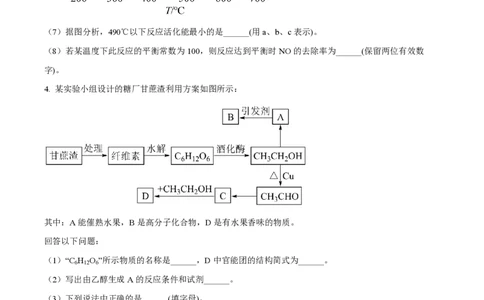
(7)据图分析,490℃以下反应活化能最小的是______(用a、b、c表示)。
(8)若某温度下此反应的平衡常数为100,则反应达到平衡时NO的去除率为______(保留两位有效数
字)。
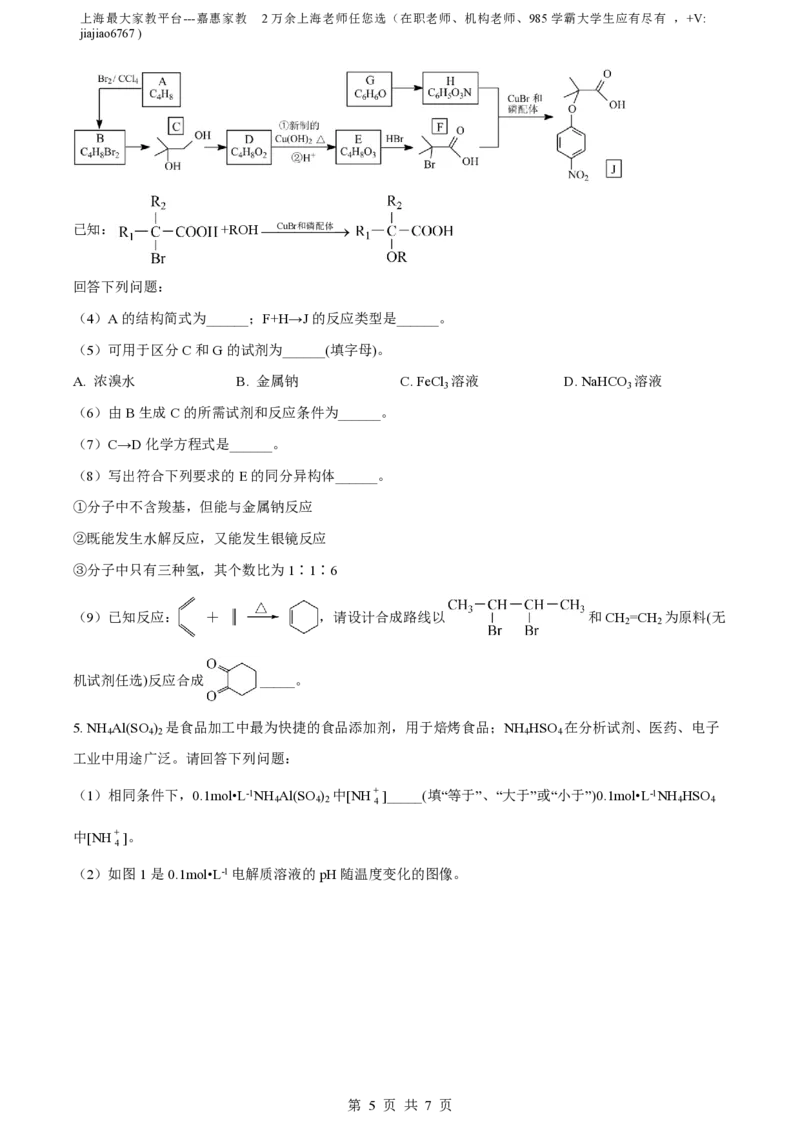
4. 某实验小组设计的糖厂甘蔗渣利用方案如图所示:
其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质。
回答以下问题:
(1)“C H O ”所示物质的名称是______,D中官能团的结构简式为______。
6 12 6
(2)写出由乙醇生成A的反应条件和试剂______。
(3)下列说法中正确的是______(填字母)。
A. 淀粉和纤维素的化学式均为(C H O ) ,两者互为同分异构
6 10 5 n
B. 糖类物质在一定条件下均能发生水解反应
C. 某天然蛋白质的最终水解产物为H N-CH -CH -COOH
2 2 2
D 油脂和物质D属于同一类有机物
.
使用α-溴代羰基化合物合成大位阻醚和硫醚的有效方法,可用于药物化学和化学生物学领域。用此法合
成化合物J的路线如图:
第 4 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知: +ROHCuBr和磷配体
回答下列问题:
(4)A的结构简式为______;F+H→J的反应类型是______。
(5)可用于区分C和G的试剂为______(填字母)。
A. 浓溴水 B. 金属钠 C. FeCl 溶液 D. NaHCO 溶液
3 3
(6)由B生成C的所需试剂和反应条件为______。
(7)C→D化学方程式是______。
(8)写出符合下列要求的E的同分异构体______。
①分子中不含羧基,但能与金属钠反应
②既能发生水解反应,又能发生银镜反应
③分子中只有三种氢,其个数比为1∶1∶6
(9)已知反应: ,请设计合成路线以 和CH =CH 为原料(无
2 2
机试剂任选)反应合成 _____。
5. NH Al(SO ) 是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH HSO 在分析试剂、医药、电子
4 4 2 4 4
工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1mol•L-1NH Al(SO ) 中[NH]_____(填“等于”、“大于”或“小于”)0.1mol•L-1NH HSO
4 4 2 4 4 4
中[NH]。
4
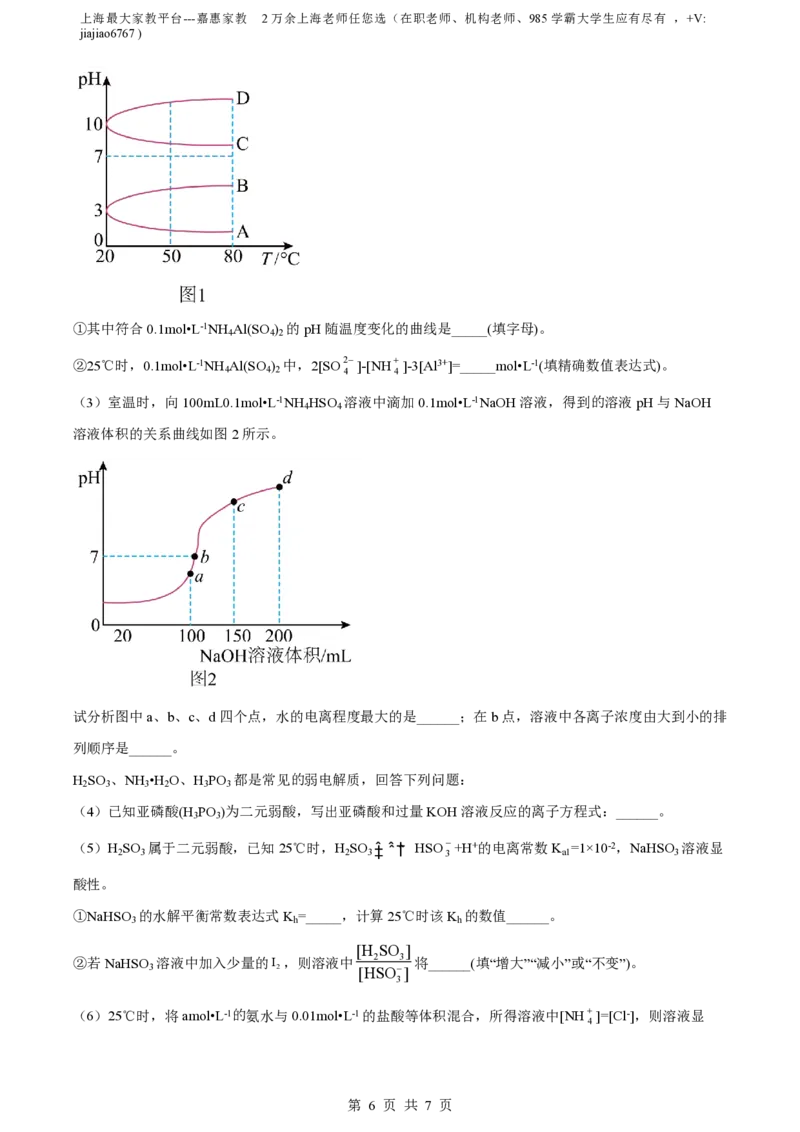
(2)如图1是0.1mol•L-1电解质溶液的pH随温度变化的图像。
第 5 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
①其中符合0.1mol•L-1NH Al(SO ) 的pH随温度变化的曲线是_____(填字母)。
4 4 2
②25℃时,0.1mol•L-1NH Al(SO ) 中,2[SO2]-[NH]-3[Al3+]=_____mol•L-1(填精确数值表达式)。
4 4 2 4 4
(3)室温时,向100mL0.1mol•L-1NH HSO 溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH
4 4
溶液体积的关系曲线如图2所示。
试分析图中a、b、c、d四个点,水的电离程度最大的是______;在b点,溶液中各离子浓度由大到小的排
列顺序是______。
H SO 、NH •H O、H PO 都是常见的弱电解质,回答下列问题:
2 3 3 2 3 3
(4)已知亚磷酸(H PO )为二元弱酸,写出亚磷酸和过量KOH溶液反应的离子方程式:______。
3 3
(5)H
2
SO
3
属于二元弱酸,已知25℃时,H
2
SO 3‡ˆ ˆˆ†ˆ HSO
3
+H+的电离常数K
a1
=1×10-2,NaHSO
3
溶液显
酸性。
①NaHSO 的水解平衡常数表达式K =_____,计算25℃时该K 的数值______。
3 h h
[H SO ]
②若NaHSO 溶液中加入少量的I ,则溶液中 2 3 将______(填“增大”“减小”或“不变”)。
3 2 [HSO]
3
(6)25℃时,将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,所得溶液中[NH]=[Cl-],则溶液显
4
第 6 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
______(填“酸”“碱”或“中”)性;用含a的代数式表示NH •H O的电离平衡常数K =_____。
3 2 b
第 7 页 共 7 页