文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2022 学年第一学期南模中学
高二年级化学学科线上期末考试
(本次考试时间 60 分钟,满分 100 分)
一、选择题(每小题只有一个正确选项)
的
1. M N+Q这是一放热 可逆基元反应,正反应的活化能为E ,逆反应的活化能为E ′, 则下列关系表述正
a a
确的是
A. E <E ′ B. E =E ′ C. Ea-1=E ′ D. E >E ′
a a a a a a a
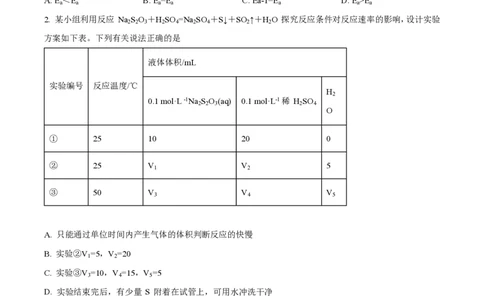
2. 某小组利用反应 Na S O +H SO =Na SO +S↓+SO ↑+H O 探究反应条件对反应速率的影响,设计实验
2 2 3 2 4 2 4 2 2
方案如下表。下列有关说法正确的是
液体体积/mL
实验编号 反应温度/℃
H
2
0.1 mol·L -1Na S O (aq) 0.1 mol·L-1稀 H SO
2 2 3 2 4
O
① 25 10 20 0
② 25 V V 5
1 2
③ 50 V V V
3 4 5
A. 只能通过单位时间内产生气体的体积判断反应的快慢
B. 实验②V =5,V =20
1 2
C. 实验③V =10,V =15,V =5
3 4 5
D. 实验结束完后,有少量 S 附着在试管上,可用水冲洗干净
3. “孔蚀”是一种集中于金属表面极小范围并能深入到金属内部的电化学腐蚀。某铁合金表面钝化膜破损后,
发生“孔蚀”的电化学腐蚀过程如图所示。下列有关说法正确的是
第 1 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 正极反应:Fe-2e-=Fe2+
B. 氧化 0.2 mol Fe,需消耗 3.36 LO
2
C. 铁合金腐蚀的最终产物为 Fe(OH)
2
D. 为防止孔蚀发生可以将外接电源负极与金属相连
4. 研究发现,在牙膏中添加氟化物能起到预防龋齿的作用,这是因为氟离子能与牙齿表面的釉质层{主要
成分是羟基磷灰石
Ca
5
PO
4
3
OH }发生反应生成氟磷灰石:
Ca PO OH(s)+F-(aq)Ca PO F(s)+OH-(aq)。下列说法错误的是
5 4 3 5 4 3
c(OH)-
A.
该反应的平衡常数表达式为K=
c
F-
B. 常温下,氟磷灰石的K 比羟基磷灰石的大
sp
C. 相比羟基磷灰石,氟磷灰石能够抵抗有机酸对牙齿的侵蚀
D. 反应达到平衡时,羟基磷灰石的溶解速率等于氟磷灰石的溶解速率
5. 正常血液pH范围是7.35~7.45,小于7.2引起酸中毒。H CO /HCO缓冲体系可稳定血液的pH,其
2 3 3
缓冲作用可表示为H+(aq)+HCO(aq)H CO (aq)CO (aq)+H O(l),H CO 的
3 2 3 2 2 2 3
K =4.5107。下列说法错误的是
a1
nH CO
2 3
A. 缓冲体系中增加少量强酸时,
n
HCO 变大
3
B. 缓冲体系中加入少量强碱时,主要反应为:HCO+OH-=CO2+H O
3 3 2
c
HCO
3
C. 血浆中 =4.5时,会引起酸中毒
cH CO
2 3
D. 酸中毒时,可以注射少量NaHCO 溶液缓解症状
3
第 2 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
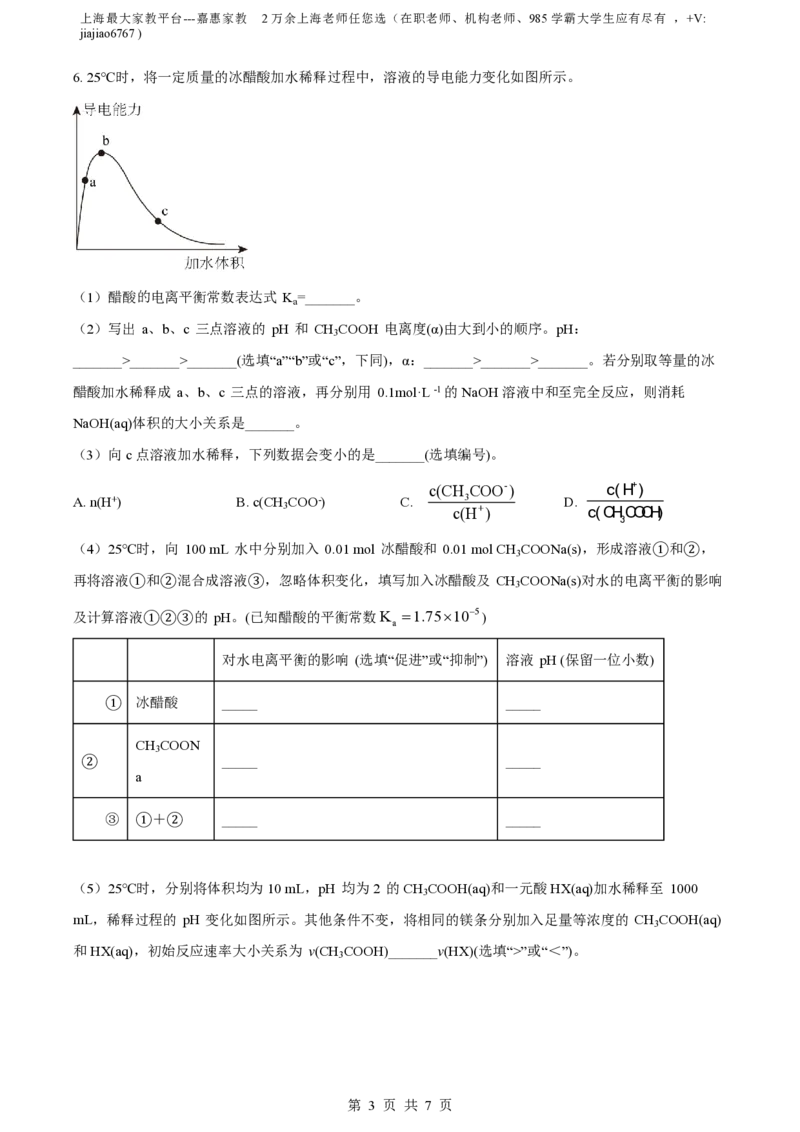
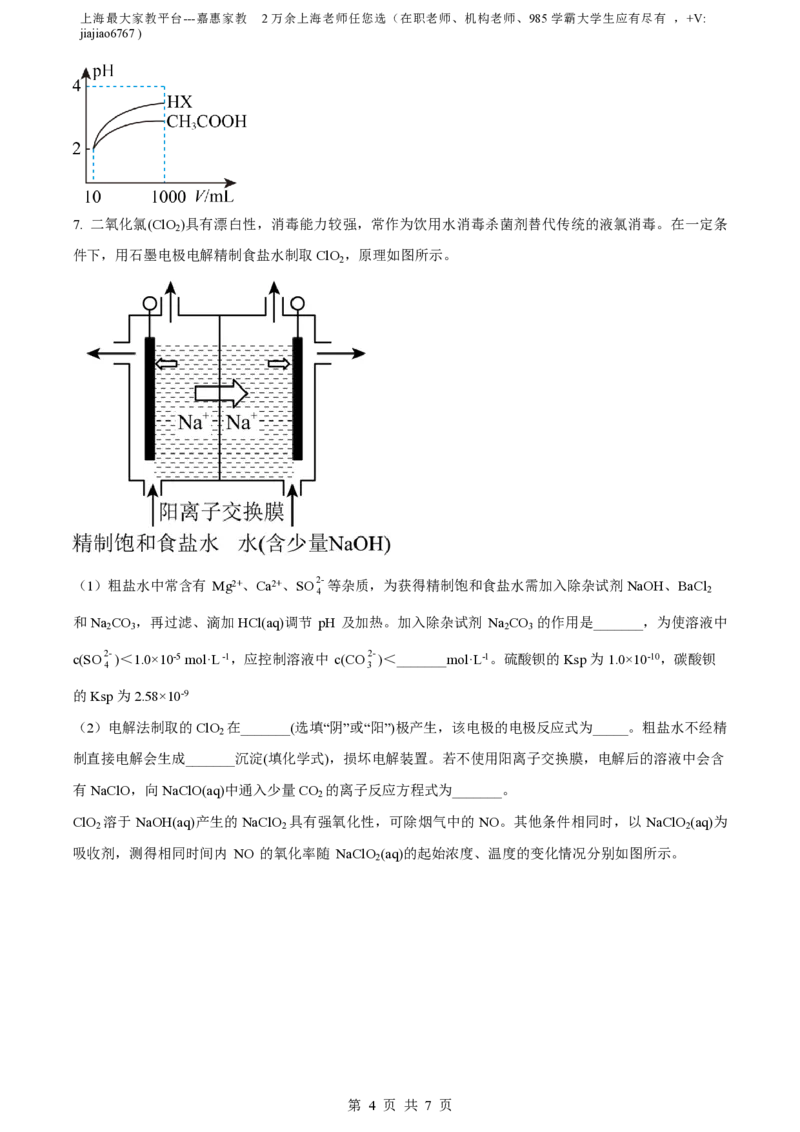
6. 25℃时,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。
(1)醋酸的电离平衡常数表达式 K =_______。
a
(2)写出 a、b、c 三点溶液的 pH 和 CH COOH 电离度(α)由大到小的顺序。pH:
3
_______>_______>_______(选填“a”“b”或“c”,下同),α:_______>_______>_______。若分别取等量的冰
醋酸加水稀释成 a、b、c 三点的溶液,再分别用 0.1mol·L -1的NaOH溶液中和至完全反应,则消耗
NaOH(aq)体积的大小关系是_______。
(3)向c点溶液加水稀释,下列数据会变小的是_______(选填编号)。
c(CH COO-) c(H+)
A. n(H+) B. c(CH COO-) C. 3 D.
3 c(H+) c(CHCOOH)
3
(4)25℃时,向 100 mL 水中分别加入 0.01 mol 冰醋酸和 0.01 mol CH COONa(s),形成溶液①和②,
3
再将溶液①和②混合成溶液③,忽略体积变化,填写加入冰醋酸及 CH COONa(s)对水的电离平衡的影响
3
及计算溶液①②③的 pH。(已知醋酸的平衡常数K 1.75105)
a
对水电离平衡的影响 (选填“促进”或“抑制”) 溶液 pH (保留一位小数)
① 冰醋酸 _____ _____
CH COON
3
② _____ _____
a
③ ①+② _____ _____
(5)25℃时,分别将体积均为10 mL,pH 均为2 的CH COOH(aq)和一元酸HX(aq)加水稀释至 1000
3
mL,稀释过程的 pH 变化如图所示。其他条件不变,将相同的镁条分别加入足量等浓度的 CH COOH(aq)
3
和HX(aq),初始反应速率大小关系为 v(CH COOH)_______v(HX)(选填“>”或“<”)。
3
第 3 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
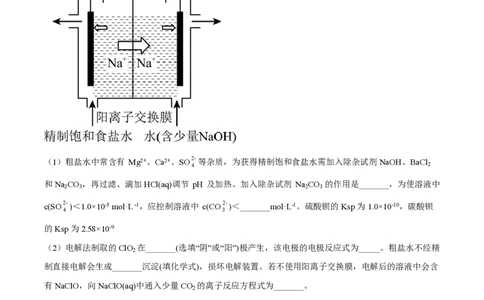
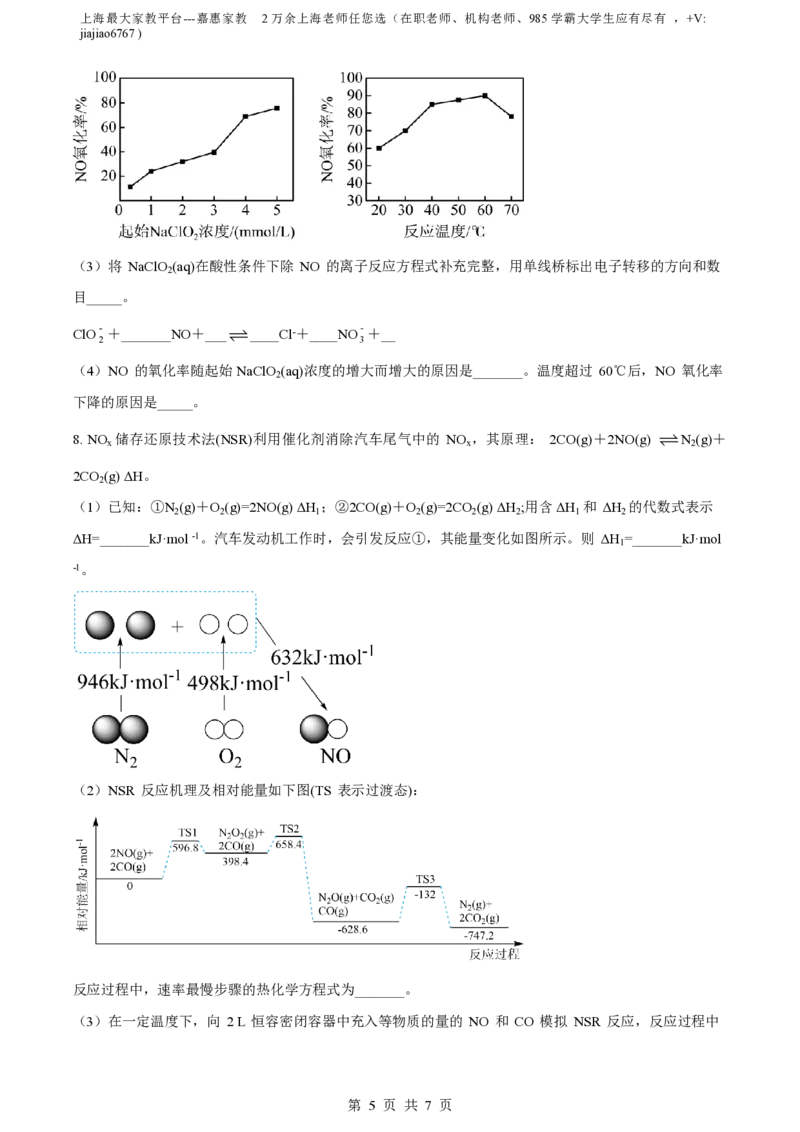
7. 二氧化氯(ClO )具有漂白性,消毒能力较强,常作为饮用水消毒杀菌剂替代传统的液氯消毒。在一定条
2
件下,用石墨电极电解精制食盐水制取ClO ,原理如图所示。
2
(1)粗盐水中常含有 Mg2+、Ca2+、SO2-等杂质,为获得精制饱和食盐水需加入除杂试剂NaOH、BaCl
4 2
和Na CO ,再过滤、滴加HCl(aq)调节 pH 及加热。加入除杂试剂 Na CO 的作用是_______,为使溶液中
2 3 2 3
c(SO2-)<1.0×10-5 mol·L -1,应控制溶液中 c(CO2-)<_______mol·L-1。硫酸钡的Ksp为1.0×10-10,碳酸钡
4 3
的Ksp为2.58×10-9
(2)电解法制取的ClO 在_______(选填“阴”或“阳”)极产生,该电极的电极反应式为_____。粗盐水不经精
2
制直接电解会生成_______沉淀(填化学式),损坏电解装置。若不使用阳离子交换膜,电解后的溶液中会含
有NaClO,向NaClO(aq)中通入少量CO 的离子反应方程式为_______。
2
ClO 溶于NaOH(aq)产生的NaClO 具有强氧化性,可除烟气中的NO。其他条件相同时,以NaClO (aq)为
2 2 2
吸收剂,测得相同时间内 NO 的氧化率随 NaClO (aq)的起始浓度、温度的变化情况分别如图所示。
2
第 4 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(3)将 NaClO (aq)在酸性条件下除 NO 的离子反应方程式补充完整,用单线桥标出电子转移的方向和数
2
目_____。
ClO- +_______NO+___ ____Cl-+____NO-+__
2 3
(4)NO 的氧化率随起始NaClO (aq)浓度的增大而增大的原因是_______。温度超过 60℃后,NO 氧化率
2
下降的原因是_____。
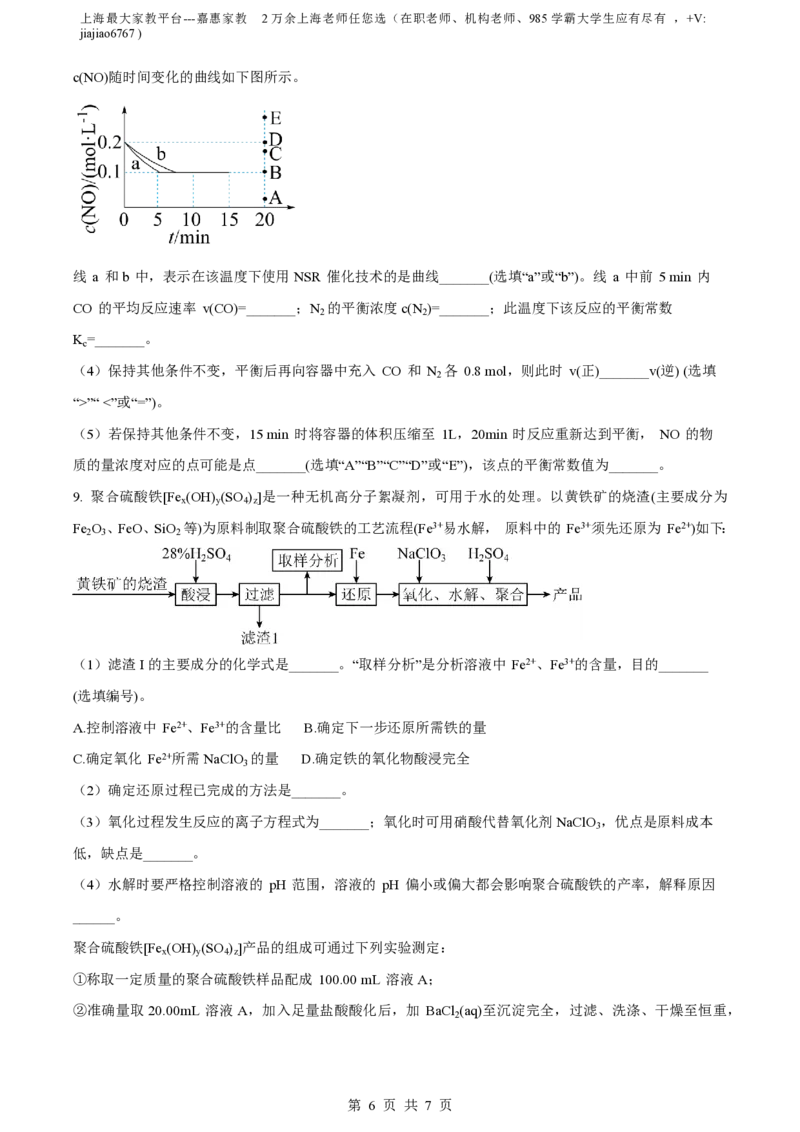
8. NO 储存还原技术法(NSR)利用催化剂消除汽车尾气中的 NO ,其原理: 2CO(g)+2NO(g) N (g)+
x x 2
2CO (g) ΔH。
2
(1)已知:①N (g)+O (g)=2NO(g) ΔH ;②2CO(g)+O (g)=2CO (g) ΔH ;用含ΔH 和 ΔH 的代数式表示
2 2 1 2 2 2 1 2
ΔH=_______kJ·mol -1。汽车发动机工作时,会引发反应①,其能量变化如图所示。则 ΔH =_______kJ·mol
1
-1。
(2)NSR 反应机理及相对能量如下图(TS 表示过渡态):
反应过程中,速率最慢步骤的热化学方程式为_______。
(3)在一定温度下,向 2 L 恒容密闭容器中充入等物质的量的 NO 和 CO 模拟 NSR 反应,反应过程中
第 5 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
c(NO)随时间变化的曲线如下图所示。
线 a 和b 中,表示在该温度下使用NSR 催化技术的是曲线_______(选填“a”或“b”)。线 a 中前 5 min 内
CO 的平均反应速率 v(CO)=_______;N 的平衡浓度c(N )=_______;此温度下该反应的平衡常数
2 2
K =_______。
c
(4)保持其他条件不变,平衡后再向容器中充入 CO 和 N 各 0.8 mol,则此时 v(正)_______v(逆) (选填
2
“>”“ <”或“=”)。
(5)若保持其他条件不变,15 min 时将容器的体积压缩至 1L,20min 时反应重新达到平衡, NO 的物
质的量浓度对应的点可能是点_______(选填“A”“B”“C”“D”或“E”),该点的平衡常数值为_______。
9. 聚合硫酸铁[Fe (OH) (SO ) ]是一种无机高分子絮凝剂,可用于水的处理。以黄铁矿的烧渣(主要成分为
x y 4 z
Fe O 、FeO、SiO 等)为原料制取聚合硫酸铁的工艺流程(Fe3+易水解, 原料中的 Fe3+须先还原为 Fe2+)如下:
2 3 2
(1)滤渣I的主要成分的化学式是_______。“取样分析”是分析溶液中 Fe2+、Fe3+的含量,目的_______
(选填编号)。
A.控制溶液中 Fe2+、Fe3+的含量比 B.确定下一步还原所需铁的量
C.确定氧化 Fe2+所需NaClO 的量 D.确定铁的氧化物酸浸完全
3
(2)确定还原过程已完成的方法是_______。
(3)氧化过程发生反应的离子方程式为_______;氧化时可用硝酸代替氧化剂NaClO ,优点是原料成本
3
低,缺点是_______。
(4)水解时要严格控制溶液的 pH 范围,溶液的 pH 偏小或偏大都会影响聚合硫酸铁的产率,解释原因
______。
聚合硫酸铁[Fe (OH) (SO ) ]产品的组成可通过下列实验测定:
x y 4 z
①称取一定质量的聚合硫酸铁样品配成 100.00 mL 溶液A;
②准确量取20.00mL 溶液A,加入足量盐酸酸化后,加 BaCl (aq)至沉淀完全,过滤、洗涤、干燥至恒重,
2
第 6 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
得到白色固体11.65g;
③准确量取20.00 mL 溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL
溶液B;
④准确量取25.00 mL 溶液B,用0.1000 mol·L-1的KMnO (H+)滴定至终点,消耗 KMnO (aq) 8.00 mL。
4 4
(5)如何确定步骤②中已沉淀完全____?
(6)步骤④滴定终点的现象是_______;该聚合硫酸铁的化学式为_______。若步骤③配制溶液B操作时
间过长,则 y 会_____ (选填“偏大”“偏小”或“不变”)
第 7 页 共 7 页