文档内容
一、选择题
1. 化学与生活密切相关。下列叙述正确的是
A. 漂白粉与盐酸可混合使用以提高消毒效果 B. 温室气体是形成酸雨的主要物质
C. 棉花、麻和蚕丝均为碳水化合物 D. 干冰可用在舞台上制造“云雾”
【答案】D
【解析】
【详解】A.漂白粉的有效成分次氯酸钙与盐酸混合,会发生氧化还原反应生成有毒的氯气,两者不能混
合使用,A错误;
B.温室气体主要是指二氧化碳,二氧化碳不是形成酸雨的主要物质,形成酸雨的主要物质是硫氧化物、
氮氧化物等,B错误;
C.棉花、麻来源于植物,主要成分均是纤维素,为碳水化合物,但蚕丝来源于动物,主要成分是蛋白
质,蛋白质不是碳水化合物,C错误;
D.干冰是固态的二氧化碳,干冰升华时,吸收大量的热,使周围温度降低,大量的水蒸气凝结成了小液
滴,形成 “云雾”效果,D正确;
答案选D。
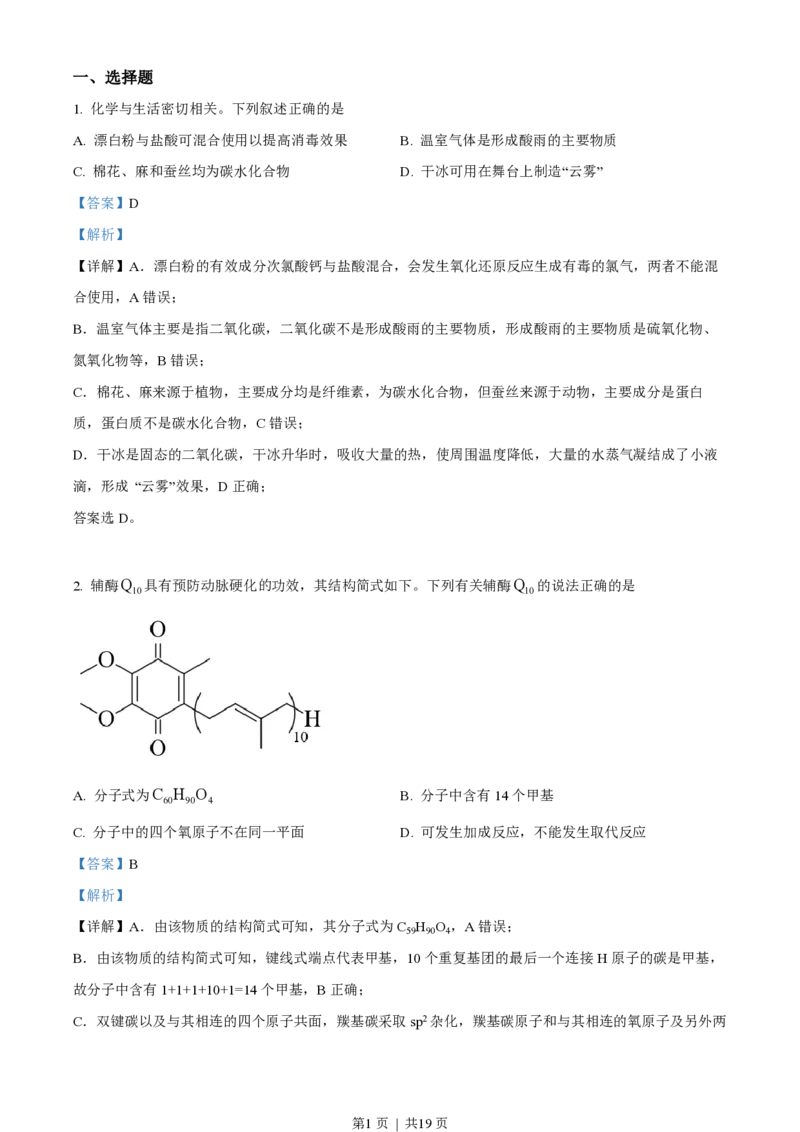
2. 辅酶Q 具有预防动脉硬化的功效,其结构简式如下。下列有关辅酶Q 的说法正确的是
10 10
A. 分子式为C H O B. 分子中含有14个甲基
60 90 4
C. 分子中的四个氧原子不在同一平面 D. 可发生加成反应,不能发生取代反应
【答案】B
【解析】
【详解】A.由该物质的结构简式可知,其分子式为C H O ,A错误;
59 90 4
B.由该物质的结构简式可知,键线式端点代表甲基,10个重复基团的最后一个连接H原子的碳是甲基,
故分子中含有1+1+1+10+1=14个甲基,B正确;
C.双键碳以及与其相连的四个原子共面,羰基碳采取sp2杂化,羰基碳原子和与其相连的氧原子及另外两
第1页 | 共19页个原子共面,因此分子中的四个氧原子在同一平面上,C错误;
D.分子中有碳碳双键,能发生加成反应,分子中含有甲基,能发生取代反应,D错误;
答案选B。
3. 能正确表示下列反应的离子方程式为
A. 硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B. 明矾溶液与过量氨水湿合:Al3++4NH +2H O=AlO-+4NH+
3 2 2 4
C. 硅酸钠溶液中通入二氧化碳:SiO2-+CO +H O=HSiO-+HCO-
3 2 2 3 3
D. 将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO2-
2 4 4 4
=BaSO ↓+2H O
4 2
【答案】D
【解析】
【详解】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或NO ,反应
2
的离子方程式为4H++2NO-+S2-=S↓+2NO ↑+2H O(浓)或8H++2NO-+3S2-=3S↓+2NO↑+4H O(稀),A错误;
3 2 2 3 2
B.明矾在水中可以电离出Al3+,可以与氨水中电离出的OH-发生反应生成Al(OH) ,但由于氨水的碱性较
3
弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为
3
Al3++3NH ·H O=Al(OH) ↓+3NH+,B错误;
3 2 3 4
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据其通入的量
的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO2-+H O+CO =H SiO ↓+CO2-(CO 少量)或SiO
3 2 2 2 3 3 2
2-+2H O+2CO =H SiO ↓+2HCO-(CO 过量),C错误;
3 2 2 2 3 3 2
D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的OH-与
2 4 4 2
NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO2-反应生成BaSO 沉
4 4 2 4 4 4 4
淀,反应的离子方程为为Ba2++2OH-+2H++SO2-=BaSO ↓+2H O,D正确;
4 4 2
故答案选D。
4. 一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)2-存在)。电池放
2 4
电时,下列叙述错误的是
第2页 | 共19页A. Ⅱ区的K+通过隔膜向Ⅲ区迁移
B. Ⅰ区的SO2-通过隔膜向Ⅱ区迁移
4
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D. 电池总反应:Zn+4OH-+MnO +4H+=Zn(OH)2-+Mn2++2H O
2 4 2
【答案】A
【解析】
【分析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH)2-,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于
4 2 2 2
两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此
可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO2-向Ⅱ区移动,Ⅲ区消耗OH-,生成
4
Zn(OH)2-,Ⅱ区的SO2-向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
4 4
【详解】A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO2-向Ⅱ区移动,B正确;
4
C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D.电池的总反应为Zn+4OH-+MnO +4H+=Zn(OH)2-+Mn2++2H O,D正确;
2 4 2
故答案选A。
5. N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 25℃,101kPa下,28L氢气中质子的数目为2.5N
A
B. 2.0L 1.0mol×L-1 AlCl 溶液中,Al3+的数目为2.0N
3 A
第3页 | 共19页C. 0.20mol苯甲酸完全燃烧,生成CO 的数目为1.4N
2 A
D. 电解熔融CuCl ,阴极增重6.4g,外电路中通过电子的数目为0.10N
2 A
【答案】C
【解析】
【详解】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故A错
误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于2.0N ,故B
3 3 A
错误;
点燃
15
C.苯甲酸燃烧的化学方程式为C H COOH+ O 7CO +3H O,1mol苯甲酸燃烧生成
6 5 2 2 2 2
7molCO ,则0.2mol苯甲酸完全燃烧生成1.4molCO ,数目为1.4N ,故C正确;
2 2 A
D.电解熔融CuCl 时,阳极反应为2Cl--2e-=Cl ,阴极反应为Cu2++2e-=Cu,阴极增加的重量为Cu
2 2
的质量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目
为0.2N ,故D错误;
A
答案选C。
6. Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。Q与X、Y、Z位于
不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下列说法正确的是
A. 非金属性:X>Q B. 单质的熔点:X>Y
C. 简单氢化物的沸点:Z>Q D. 最高价含氧酸的酸性:Z>Y
【答案】D
【解析】
【分析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,Y原子最
外层电子数为Q元原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于第三周期,Y的最外
层电子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则X为Al元素,Q、X、Y、Z的
最外层电子数之和为19,则Q、Z的最外层电子数之和为19-3-4=12,主族元素的最外层电子数最多为7,
若Q的最外层电子数为7,为F元素,Z的最外层电子数为5,为P元素,若Q的最外层电子数为6,为
O元素,则Z的最外层电子数为6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数
为7,为Cl元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P,据此分析解题。
第4页 | 共19页【详解】A.X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一主族从上往下依
次减弱,故非金属性:Q>X,A错误;
B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,即Y>X,
B错误;
C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为H O或NH 或HF,Z为Cl
2 3
或S或P,其简单氢化物为HCl或H S或PH ,由于前者物质中存在分子间氢键,而后者物质中不存在,
2 3
故沸点Q>Z,C错误;
D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最高价含氧
酸酸性:Z>Y,D正确;
故答案为:D。
7. 根据实验目的,下列实验及现象、结论都正确的是
选
实验目的 实验及现象 结论
项
分别测浓度均为0.1mol×L-1的
比较CH COO-和
3
A CH COONH 和NaHCO 溶液 K
CH
COO-