文档内容
2025 届初中毕业班学生学业水平综合测试
化学
注意事项:
1.答题前,考生务必在答题卡第1面和第3面用黑色字迹的钢笔或签字笔填写学校、班级、
姓名、试室号和座位号,将自己的条形码粘贴在答题卡的“条形码粘贴处”。
2.选择题每小题选出答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号;不能答在卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相
应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不能超出指
定的区域;不准使用铅笔、圆珠笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,答题结束时,将本卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Ca-40 Zn-65
一、选择题:本题包括14小题,每小题3分,共42分。每小题给出的四个选项中,只有一
项最符合题意。错选、不选、多选或涂改不清的,均不给分。
1. 下列物品的主要成分属于合成材料的是
A.塑料饮料瓶 B.大理石栏杆 C.羊绒毛衣 D.青铜大面具
A. A B. B C. C D. D
2. 下列说法不正确的是
A. 利用活性炭脱色生产白糖
B. 淀粉虽然没有甜味,但属于糖类
的
C. 食物中 蛋白质能被人体直接用于生长发育
D. 将固体试剂配制成溶液进行化学反应,可以增大反应速率
3. 对下列事实的微观解释合理的是
选项 事实 解释
第1页/共10页
学科网(北京)股份有限公司A 蒸馏水不能导电 水分子中没有带电粒子
B 硫在氧气中燃烧遵守质量守恒定律 化学反应前后分子种类不变
C 金刚石和石墨的物理性质不同 碳原子的结构不同
KMnO 溶液呈紫红色,KCl溶液呈无
4
D
MnO4在水溶液中呈紫红色
色
A. A B. B C. C D. D
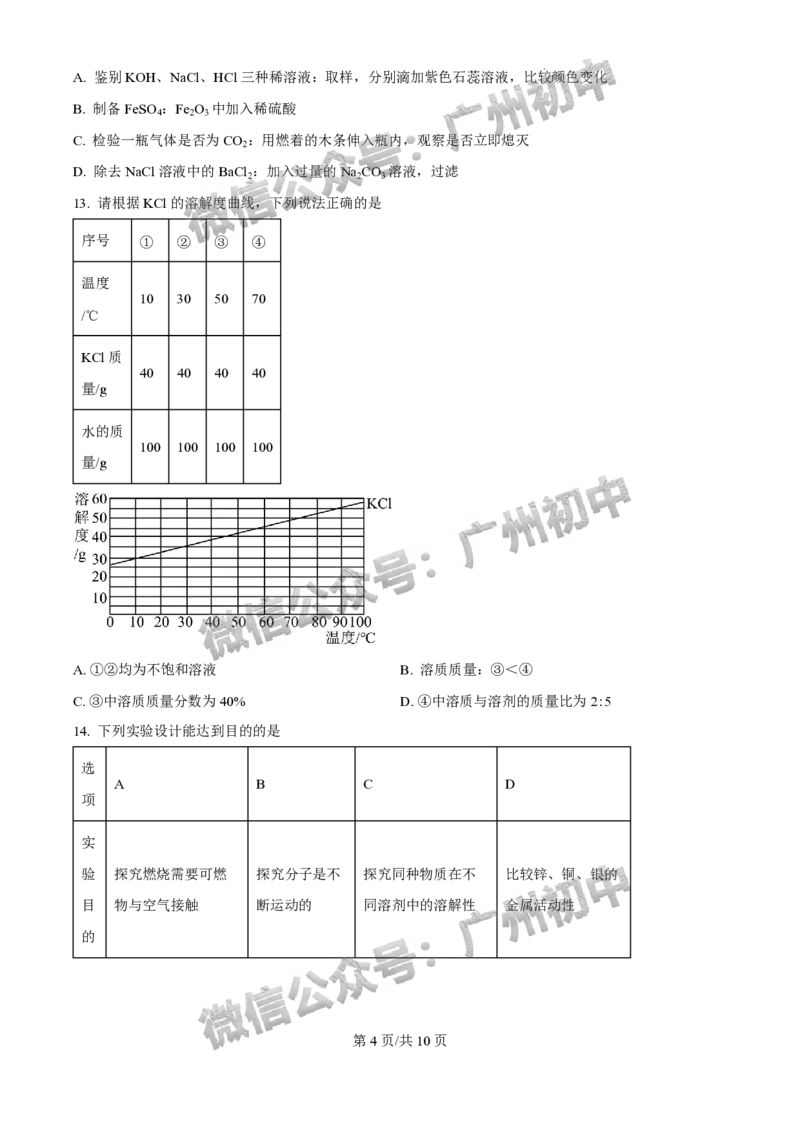
4. 钛合金在航天、医学等方面应用广泛。下列关于钛的说法正确的是
A 钛合金属于化合物 B. x=8
.
C. 一个钛原子的质量为47.87 D. Ti2+的核外电子数为20
5. 缺锌者可在医生指导下服用葡萄糖酸锌(C H O Zn)口服液来补锌。下列说法正确的是
12 22 14
A. 葡萄糖酸锌中含有单质锌 B. 葡萄糖酸锌由四种元素组成
C. 葡萄糖酸锌由49个原子构成 D. 葡萄糖酸锌中氢元素质量分数最大
6. 下列说法不正确的是
A. 人体呼出气体中含量最高的是二氧化碳
B. 液态氦用于制造低温环境
C. 净水过程中明矾能使水中悬浮杂质沉降
D. 电解水实验中,与正极相连玻璃管内产生的气体是氧气
7. 如图是CO 转化为甲酸(HCOOH)的微观示意图,以下说法正确的是
2
A. 的化学式为H
2
第2页/共10页
学科网(北京)股份有限公司B. 该反应属于置换反应
C. 整个转化过程共涉及3种氧化物
D. 反应中消耗 和生成 的物个数比为2:1
8. 以下劳动项目与化学知识不相符的是
选项 劳动项目 化学知识
A 用硝酸钠给植物施肥巴 硝酸钠属于氮肥
B 用天然气作燃料炒菜 天然气主要成分是CO
C 用锡铅合金焊接金属而不用锡 锡铅合金的熔点比锡的熔点低
D 用6B铅笔芯制作电极 石墨具有导电性能
A. A B. B C. C D. D
9. 下列做法不正确的是
A. 图书馆着火时,使用二氧化碳灭火器
B. 稀释浓硫酸时,将水倒入浓硫酸中,并不断搅拌
C. 蒸发操作中,用玻璃棒不断搅拌蒸发皿中的溶液,避免液滴飞溅
D. 氢氧化钠溶液沾到皮肤上,先用大量水冲洗,再涂1%的硼酸溶液
10. 古籍记载了丰富的化学知识,下列说法不正确的是
A. 《三国志》中记载“实以薪草,膏油灌其中”,涉及燃然烧条件中的提供可燃物
B. 《吕氏春秋》中记载“金(铜单质)柔锡(锡单质)柔,合两柔则刚”,说明合金的硬度一般比组成金属的大
C. 《抱朴子》中记载“丹砂(HgS)烧之成水银”,该过程发生的是物理变化
D. 《开宝本草》中记载了KNO 的制取过程,“所在山泽,冬月地上有霜”,涉及的实验过程是结晶
3
11. 钇(Y)在新能源和医疗中发挥关键作用,钇的金属活动性介于铝和锌之间,下列预测合理的是
物质 Y O Y(OH) YCl Y (CO )
2 3 3 3 2 3 3
在水中的溶解性 难溶 难溶 易溶 难溶
A. Y能从MgCl 溶液中置换出Mg B. Y(OH) 与盐酸反应无明显现象
2 3
C. YCl 能与NaOH溶液反应制备Y(OH) D. Y (CO ) 能与稀硫酸反应生成YCl
3 3 2 3 3 3
12. 下列实验方案中,正确的是
第3页/共10页
学科网(北京)股份有限公司A. 鉴别KOH、NaCl、HCl三种稀溶液:取样,分别滴加紫色石蕊溶液,比较颜色变化
B. 制备FeSO :Fe O 中加入稀硫酸
4 2 3
C. 检验一瓶气体是否为CO :用燃着的木条伸入瓶内,观察是否立即熄灭
2
D. 除去NaCl溶液中的BaCl :加入过量的Na CO 溶液,过滤
2 2 3
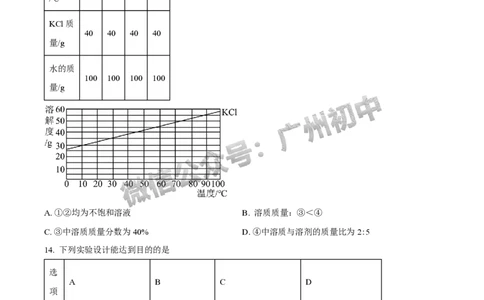
13. 请根据KCl的溶解度曲线,下列说法正确的是
序号 ① ② ③ ④
温度
10 30 50 70
/℃
KCl质
40 40 40 40
量/g
水的质
100 100 100 100
量/g
A. ①②均为不饱和溶液 B. 溶质质量:③<④
C. ③中溶质质量分数为40% D. ④中溶质与溶剂的质量比为2:5
14. 下列实验设计能达到目的的是
选
A B C D
项
实
验 探究燃烧需要可燃 探究分子是不 探究同种物质在不 比较锌、铜、银的
目 物与空气接触 断运动的 同溶剂中的溶解性 金属活动性
的
第4页/共10页
学科网(北京)股份有限公司实
验
设
计
A. A B. B C. C D. D
二、非选择题:本题包括6小题,共48分。
15. 土壤的酸碱性对植物生长非常重要,造成土壤酸化的因素有多种。
(1)酸雨是土壤酸化的主要原因,现检测到某地区雨水的pH为5.3,该雨水______(填“是”或“不是”)
酸雨,酸雨的成因之一是大气中的氮氧化合物NO 与水反应形成硝酸。硝酸的化学式为______,NO 中氮
x x
元素的化合价为______(用x表示)。
(2)微生物分解有机质产生有机酸(含乙酸)也会导致土壤酸化,已知乙酸(CH COOH)溶液具有与盐酸相似
3
的化学性质,依据是乙酸能在水溶液中解离出______(写离子符号),验证乙酸溶液有该相似化学性质的方
法是:取少量乙酸溶液于试管中,加______(不能用指示剂),可观察到______。
(3)“绿色化学”提倡从源头避免有害物质的使用与排放。下列预防土壤酸化的措施中,符合“绿色化学”
理念的是______。
A. 烧煤工厂烟囱建高 B. 控制工业废气(SO 、NO )排放
2 x
C. 用熟石灰中和土壤酸性 D. 在酸性土壤中施用草木灰(含K CO )
2 3
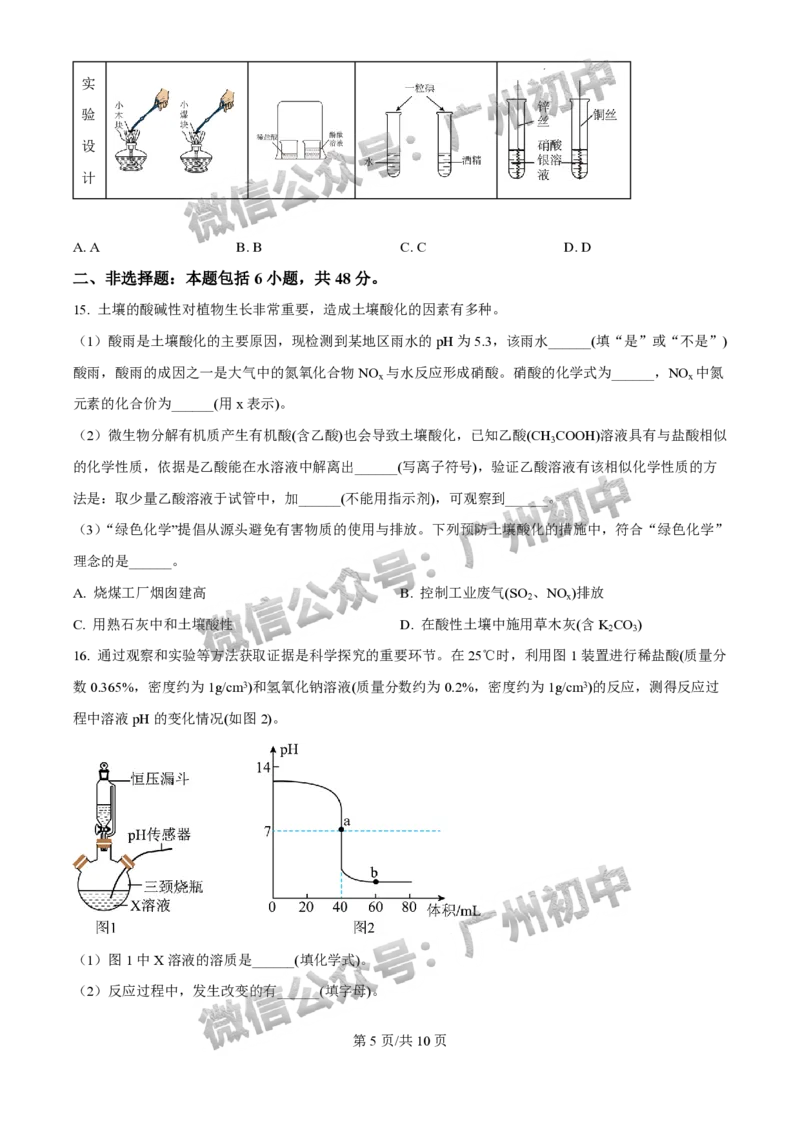
16. 通过观察和实验等方法获取证据是科学探究的重要环节。在25℃时,利用图1装置进行稀盐酸(质量分
数0.365%,密度约为1g/cm3)和氢氧化钠溶液(质量分数约为0.2%,密度约为1g/cm3)的反应,测得反应过
程中溶液pH的变化情况(如图2)。
(1)图1中X溶液的溶质是______(填化学式)。
(2)反应过程中,发生改变的有______(填字母)。
第5页/共10页
学科网(北京)股份有限公司A. 钠离子的数目 B. 三颈烧瓶中溶液的溶质种类
C. 溶剂的质量 D. 图1装置的总质量
(3)图2中a点的溶质质量为______g。在图中画出b点溶液中存在的微观粒子______。
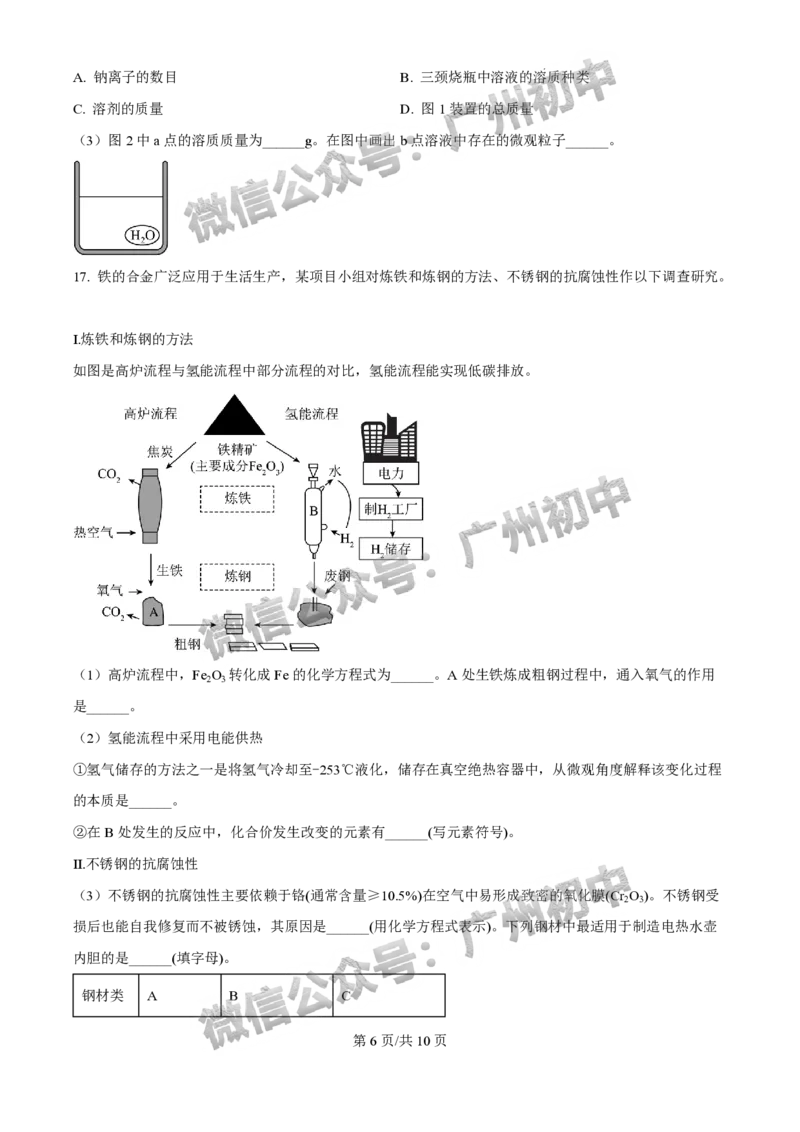
17. 铁的合金广泛应用于生活生产,某项目小组对炼铁和炼钢的方法、不锈钢的抗腐蚀性作以下调查研究。
I.炼铁和炼钢的方法
如图是高炉流程与氢能流程中部分流程的对比,氢能流程能实现低碳排放。
(1)高炉流程中,Fe O 转化成Fe的化学方程式为______。A处生铁炼成粗钢过程中,通入氧气的作用
2 3
是______。
(2)氢能流程中采用电能供热
①氢气储存的方法之一是将氢气冷却至-253℃液化,储存在真空绝热容器中,从微观角度解释该变化过程
的本质是______。
②在B处发生的反应中,化合价发生改变的元素有______(写元素符号)。
II.不锈钢的抗腐蚀性
(3)不锈钢的抗腐蚀性主要依赖于铬(通常含量≥10.5%)在空气中易形成致密的氧化膜(Cr O )。不锈钢受
2 3
损后也能自我修复而不被锈蚀,其原因是______(用化学方程式表示)。下列钢材中最适用于制造电热水壶
内胆的是______(填字母)。
钢材类 A B C
第6页/共10页
学科网(北京)股份有限公司型
碳
碳<0.08% 碳 0.38%~0.37%
铬 0.75%~0.84% 铬
成分
16~26% 锰≤0.40% 0.90%~1.20%
镍6~22% 硅≤0.35 钼
0.15%~0.30%
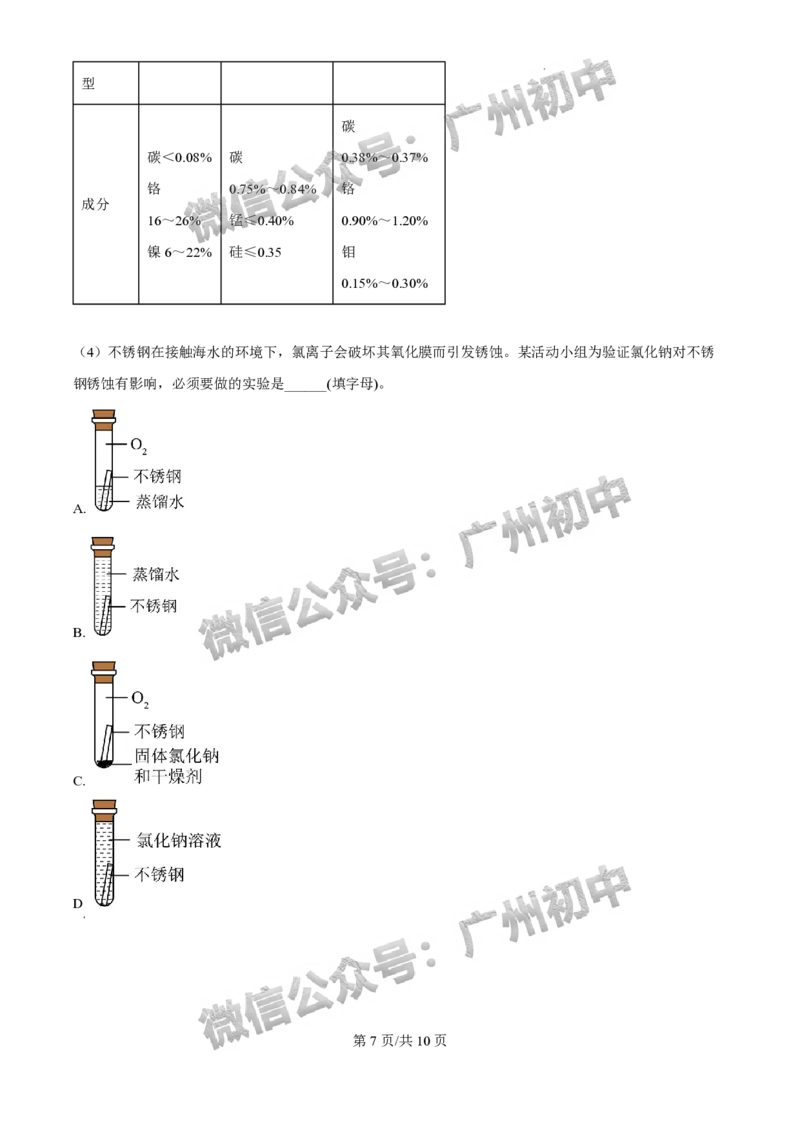
(4)不锈钢在接触海水的环境下,氯离子会破坏其氧化膜而引发锈蚀。某活动小组为验证氯化钠对不锈
钢锈蚀有影响,必须要做的实验是______(填字母)。
A.
B.
C.
D
.
第7页/共10页
学科网(北京)股份有限公司E.
18. 实验小组对生石灰干燥剂的变质情况及其制备原理进行探究
I.探究干燥剂变质情况
(1)生石灰会与空气中的______反应变质,可能生成氢氧化钙、碳酸钙。
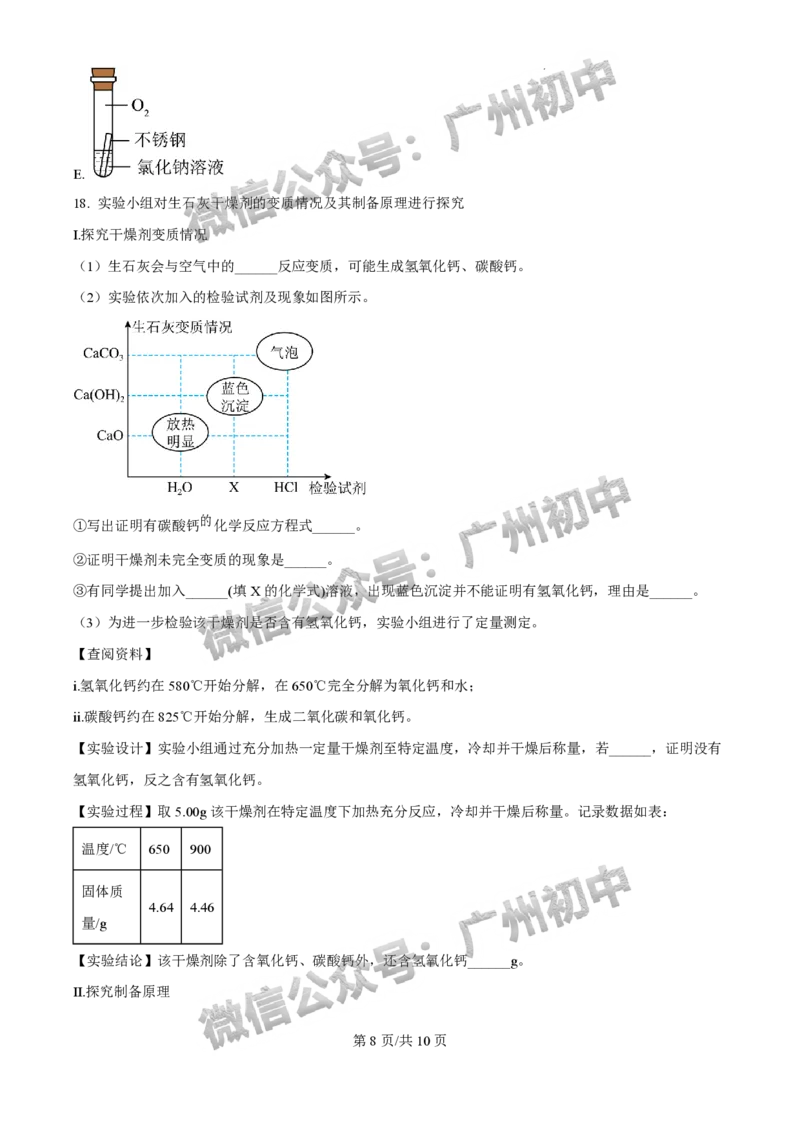
(2)实验依次加入的检验试剂及现象如图所示。
的
①写出证明有碳酸钙 化学反应方程式______。
②证明干燥剂未完全变质的现象是______。
③有同学提出加入______(填X的化学式)溶液,出现蓝色沉淀并不能证明有氢氧化钙,理由是______。
(3)为进一步检验该干燥剂是否含有氢氧化钙,实验小组进行了定量测定。
【查阅资料】
i.氢氧化钙约在580℃开始分解,在650℃完全分解为氧化钙和水;
ii.碳酸钙约在825℃开始分解,生成二氧化碳和氧化钙。
【实验设计】实验小组通过充分加热一定量干燥剂至特定温度,冷却并干燥后称量,若______,证明没有
氢氧化钙,反之含有氢氧化钙。
【实验过程】取5.00g该干燥剂在特定温度下加热充分反应,冷却并干燥后称量。记录数据如表:
温度/℃ 650 900
固体质
4.64 4.46
量/g
【实验结论】该干燥剂除了含氧化钙、碳酸钙外,还含氢氧化钙______g。
II.探究制备原理
第8页/共10页
学科网(北京)股份有限公司(4)活动小组设想利用石灰石制备纯净的生石灰干燥剂,需要进行的转化路径有(以钙元素为转化主线,
其余杂质、所需试剂和条件忽略不写):
①石灰石→生石灰→氢氧化钙→碳酸钙→生石灰;
②石灰石→______→生石灰。
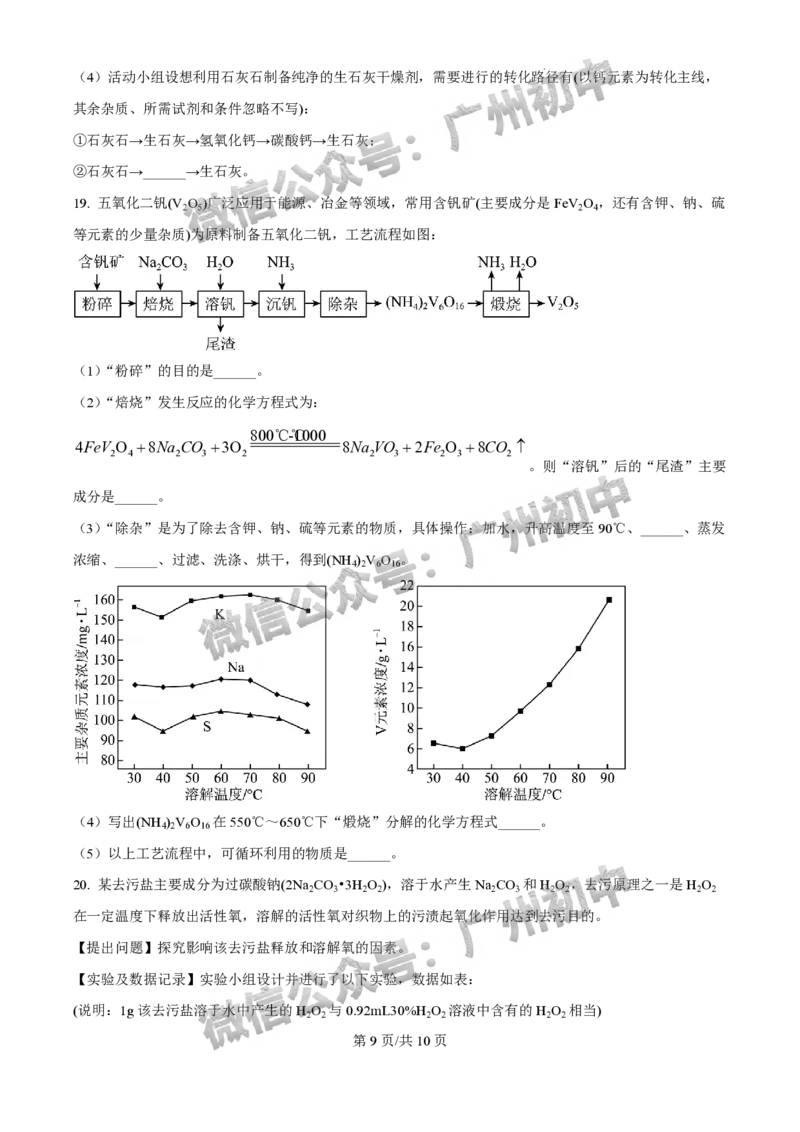
19. 五氧化二钒(V O )广泛应用于能源、冶金等领域,常用含钒矿(主要成分是FeV O ,还有含钾、钠、硫
2 5 2 4
等元素的少量杂质)为原料制备五氧化二钒,工艺流程如图:
(1)“粉碎”的目的是______。
(2)“焙烧”发生反应的化学方程式为:
800℃-℃1000
4FeV O 8Na CO 3O 8NaVO 2Fe O 8CO
2 4 2 3 2 2 3 2 3 2
。则“溶钒”后的“尾渣”主要
成分是______。
(3)“除杂”是为了除去含钾、钠、硫等元素的物质,具体操作:加水,升高温度至90℃、______、蒸发
浓缩、______、过滤、洗涤、烘干,得到(NH ) V O 。
4 2 6 16
(4)写出(NH ) V O 在550℃~650℃下“煅烧”分解的化学方程式______。
4 2 6 16
(5)以上工艺流程中,可循环利用的物质是______。
20. 某去污盐主要成分为过碳酸钠(2Na CO •3H O ),溶于水产生Na CO 和H O ,去污原理之一是H O
2 3 2 2 2 3 2 2 2 2
在一定温度下释放出活性氧,溶解的活性氧对织物上的污渍起氧化作用达到去污目的。
【提出问题】探究影响该去污盐释放和溶解氧的因素。
【实验及数据记录】实验小组设计并进行了以下实验,数据如表:
(说明:1g该去污盐溶于水中产生的H O 与0.92mL30%H O 溶液中含有的H O 相当)
2 2 2 2 2 2
第9页/共10页
学科网(北京)股份有限公司实验 物质 水/mL 温度/℃ 释放氧持续时间/s 最大溶解氧/(mg/L)
I 1g去污盐 100 60 100 0.8
II 5g去污盐 100 40 110 1.3
III 5g去污盐 100 60 140 2.2
IV 5g去污盐 100 80 60 0.6
V 10g去污盐 100 60 360 4.4
0.92mL30%H O 溶
2 2 05
VI 100 60 78 .
液
VII 1g纯Na CO 100 60 0 0
2 3
【实验分析】
(1)写出 H O 在一定温度下释放出氧气的化学方程式______。
2 2
(2)分析数据可知,去污盐释放和溶解氧的最佳温度是______℃。分析80℃时,5g去污盐在100mL水中,
最大溶解氧量少的原因是______。
(3)对比实验I、VI和VII,可推测去污盐溶于水后Na CO 的作用是______。
2 3
【实验结论】
(4)影响该去污盐释放和溶解氧的因素有______、______。
【实验拓展】实验小组要测定1g去污盐能释放氧气的最大体积,取1g该去污盐完全溶解在100mL水中,
充分加热并测定气体体积。
(5)可选用以下装置______(填字母)连接进行实验,如图仪器a的名称是______。
(6)有组员提出该方法测定的氧气体积有误差,原因是______。
第10页/共10页
学科网(北京)股份有限公司