文档内容
专练 31 化学反应中的能量变化及反应历程分析
授课提示:对应学生用书61页
1.[2024·湖北部分重点中学考试]一种生产和利用氢能的途径如图所示。下列说法错误
的是( )
A.氢能属于二次能源
B.图中能量转化的方式至少有6种
C.太阳能电池的供电原理与燃料电池相同
D.太阳能、风能、氢能都属于新能源
答案:C
解析:氢能是一种高效且没有污染的二次能源,A项正确;图中能量转化方式有太阳
能转化为电能、风能转化为机械能、水能转化为机械能、机械能转化为电能、电能转化为
化学能、化学能转化为电能、电能转化为光能等,B项正确;太阳能电池是用半导体将光
能转化为电能,燃料电池是将化学能转化为电能,二者供电原理不同,C项错误;太阳能、
风能、氢能都是人类开发利用的新型能源,D项正确。
2.
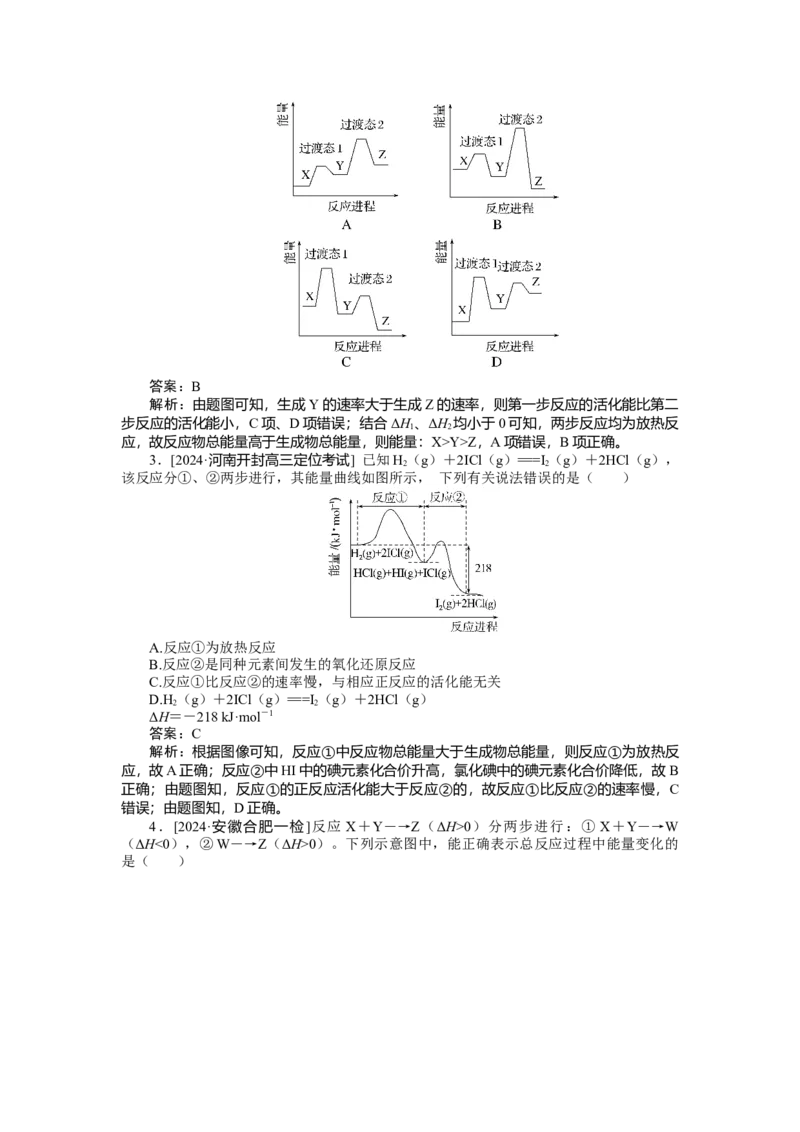
[2024·安徽卷]某温度下,在密闭容器中充入一定量的 X(g),发生下列反应:X
(g) ⇌Y(g)(ΔH
1
<0),Y(g) ⇌Z(g)(ΔH
2
<0),测得各气体浓度与反应时间的关
系如图所示。下列反应进程示意图符合题意的是( )答案:B
解析:由题图可知,生成Y的速率大于生成Z的速率,则第一步反应的活化能比第二
步反应的活化能小,C项、D项错误;结合ΔH 、ΔH 均小于0可知,两步反应均为放热反
1 2
应,故反应物总能量高于生成物总能量,则能量:X>Y>Z,A项错误,B项正确。
3.[2024·河南开封高三定位考试] 已知H (g)+2ICl(g)===I (g)+2HCl(g),
2 2
该反应分①、②两步进行,其能量曲线如图所示, 下列有关说法错误的是( )
A.反应①为放热反应
B.反应②是同种元素间发生的氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.H(g)+2ICl(g)===I (g)+2HCl(g)
2 2
ΔH=-218 kJ·mol-1
答案:C
解析:根据图像可知,反应①中反应物总能量大于生成物总能量,则反应①为放热反
应,故A正确;反应②中HI中的碘元素化合价升高,氯化碘中的碘元素化合价降低,故B
正确;由题图知,反应①的正反应活化能大于反应②的,故反应①比反应②的速率慢,C
错误;由题图知,D正确。
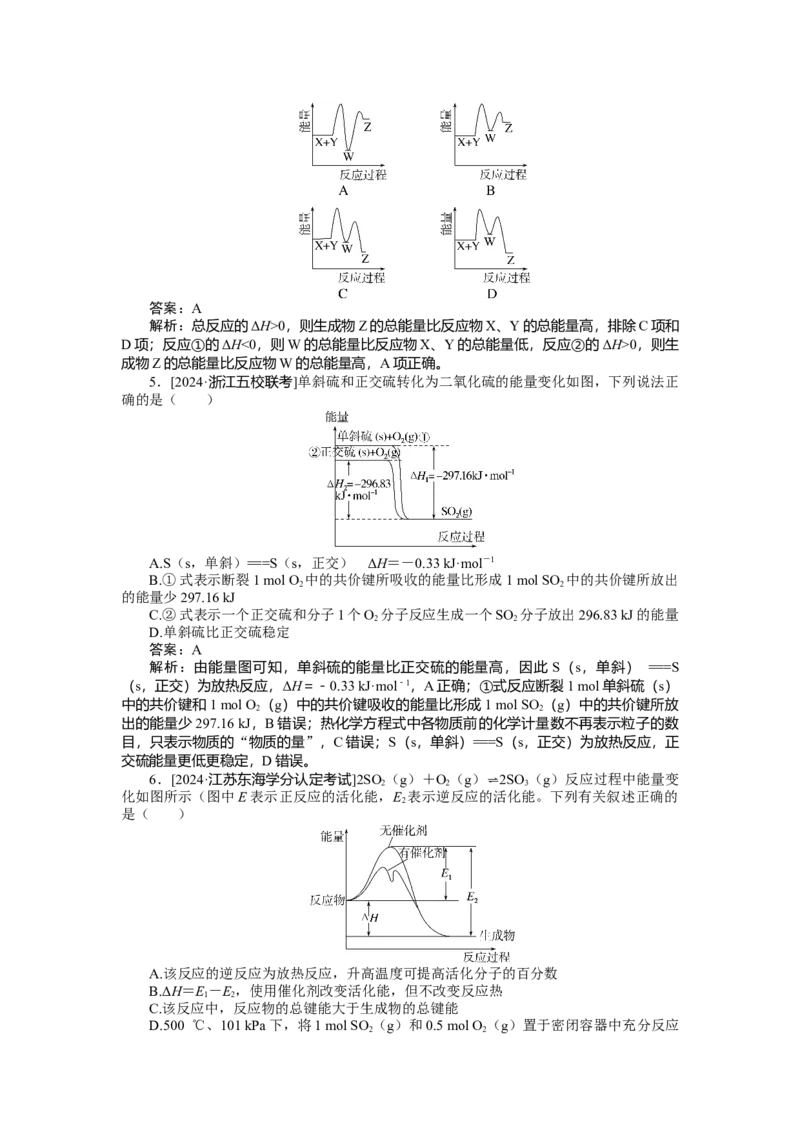
4.[2024·安徽合肥一检]反应 X+Y―→Z(ΔH>0)分两步进行:① X+Y―→W
(ΔH<0),②W―→Z(ΔH>0)。下列示意图中,能正确表示总反应过程中能量变化的
是( )答案:A
解析:总反应的ΔH>0,则生成物Z的总能量比反应物X、Y的总能量高,排除C项和
D项;反应①的ΔH<0,则W的总能量比反应物X、Y的总能量低,反应②的ΔH>0,则生
成物Z的总能量比反应物W的总能量高,A项正确。
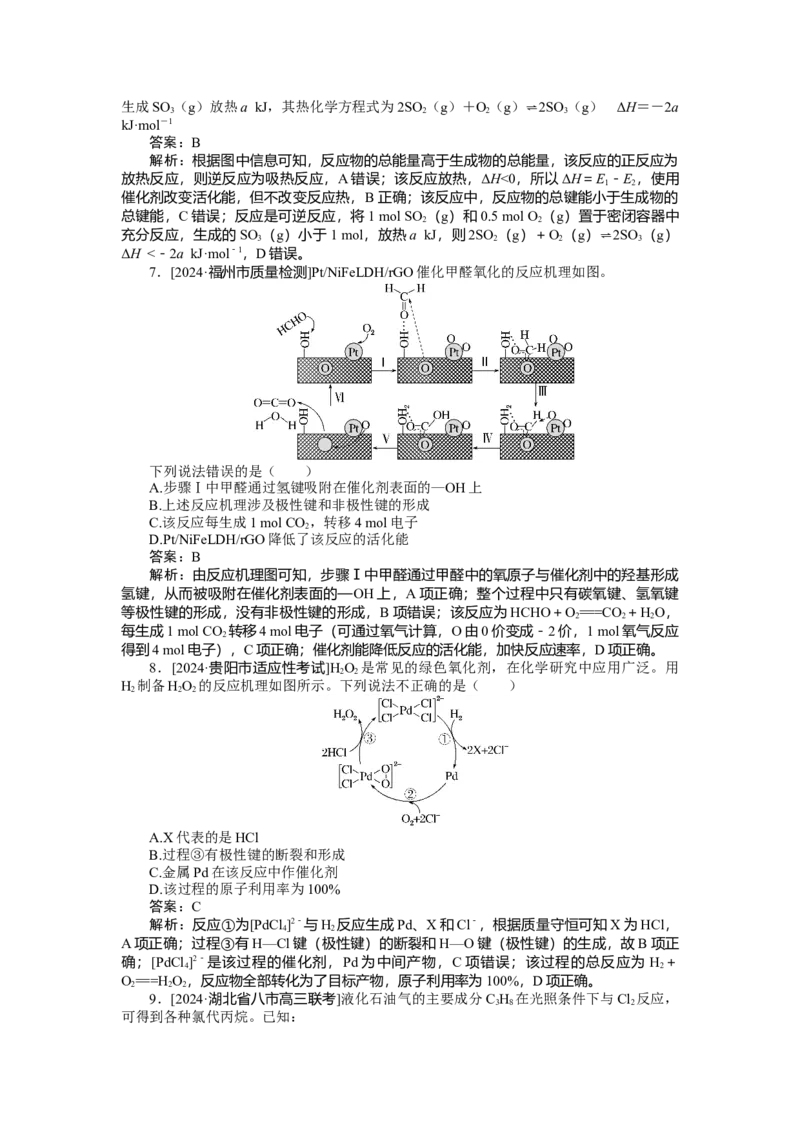
5.[2024·浙江五校联考]单斜硫和正交硫转化为二氧化硫的能量变化如图,下列说法正
确的是( )
A.S(s,单斜)===S(s,正交) ΔH=-0.33 kJ·mol-1
B.①式表示断裂1 mol O 中的共价键所吸收的能量比形成1 mol SO 中的共价键所放出
2 2
的能量少297.16 kJ
C.②式表示一个正交硫和分子1个O 分子反应生成一个SO 分子放出296.83 kJ的能量
2 2
D.单斜硫比正交硫稳定
答案:A
解析:由能量图可知,单斜硫的能量比正交硫的能量高,因此 S(s,单斜) ===S
(s,正交)为放热反应,ΔH=-0.33 kJ·mol-1,A正确;①式反应断裂1 mol单斜硫(s)
中的共价键和1 mol O (g)中的共价键吸收的能量比形成1 mol SO (g)中的共价键所放
2 2
出的能量少297.16 kJ,B错误;热化学方程式中各物质前的化学计量数不再表示粒子的数
目,只表示物质的“物质的量”,C错误;S(s,单斜)===S(s,正交)为放热反应,正
交硫能量更低更稳定,D错误。
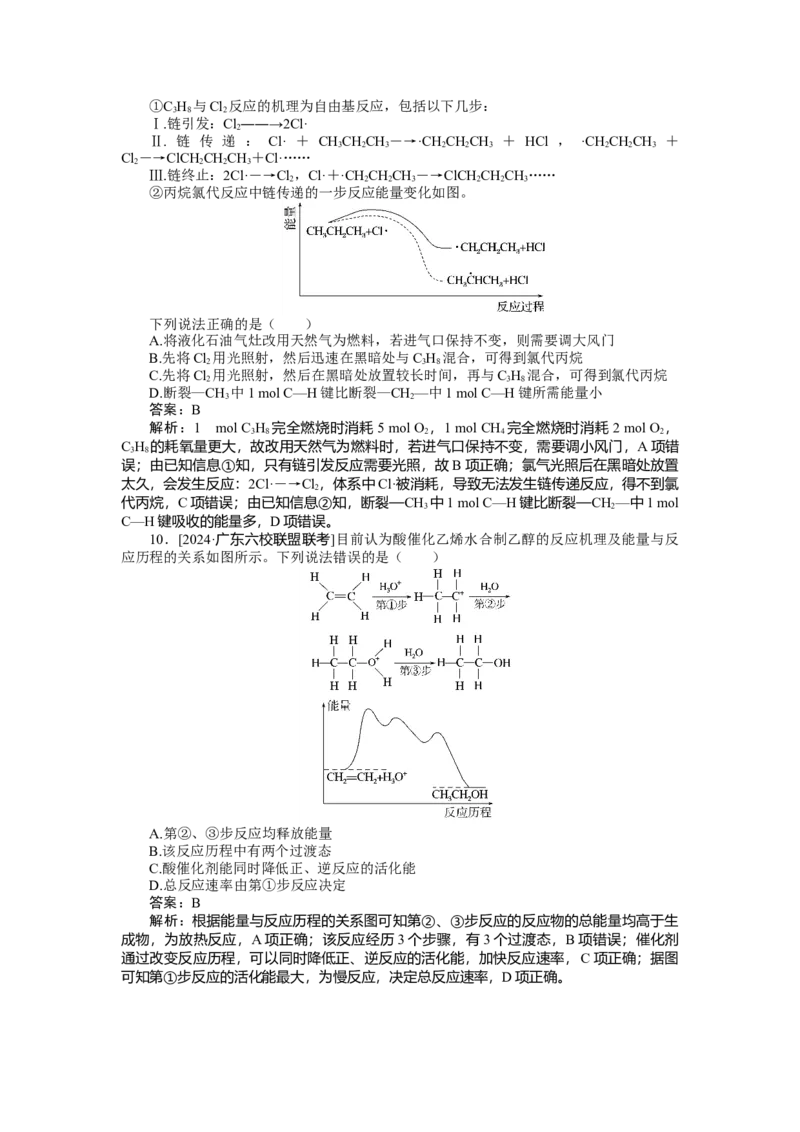
6.[2024·江苏东海学分认定考试]2SO
2
(g)+O
2
(g) ⇌2SO
3
(g)反应过程中能量变
化如图所示(图中E表示正反应的活化能,E 表示逆反应的活化能。下列有关叙述正确的
2
是( )
A.该反应的逆反应为放热反应,升高温度可提高活化分子的百分数
B.ΔH=E-E,使用催化剂改变活化能,但不改变反应热
1 2
C.该反应中,反应物的总键能大于生成物的总键能
D.500 ℃、101 kPa下,将1 mol SO (g)和0.5 mol O (g)置于密闭容器中充分反应
2 2生成SO
3
(g)放热a kJ,其热化学方程式为2SO
2
(g)+O
2
(g) ⇌2SO
3
(g) ΔH=-2a
kJ·mol-1
答案:B
解析:根据图中信息可知,反应物的总能量高于生成物的总能量,该反应的正反应为
放热反应,则逆反应为吸热反应,A错误;该反应放热,ΔH<0,所以ΔH=E -E ,使用
1 2
催化剂改变活化能,但不改变反应热,B正确;该反应中,反应物的总键能小于生成物的
总键能,C错误;反应是可逆反应,将1 mol SO (g)和0.5 mol O (g)置于密闭容器中
2 2
充分反应,生成的SO
3
(g)小于1 mol,放热a kJ,则2SO
2
(g)+O
2
(g)⇌2SO
3
(g)
ΔH <-2a kJ·mol-1,D错误。
7.[2024·福州市质量检测]Pt/NiFeLDH/rGO催化甲醛氧化的反应机理如图。
下列说法错误的是( )
A.步骤Ⅰ中甲醛通过氢键吸附在催化剂表面的—OH上
B.上述反应机理涉及极性键和非极性键的形成
C.该反应每生成1 mol CO ,转移4 mol电子
2
D.Pt/NiFeLDH/rGO降低了该反应的活化能
答案:B
解析:由反应机理图可知,步骤Ⅰ中甲醛通过甲醛中的氧原子与催化剂中的羟基形成
氢键,从而被吸附在催化剂表面的—OH上,A项正确;整个过程中只有碳氧键、氢氧键
等极性键的形成,没有非极性键的形成,B项错误;该反应为HCHO+O===CO +HO,
2 2 2
每生成1 mol CO 转移4 mol电子(可通过氧气计算,O由0价变成-2价,1 mol氧气反应
2
得到4 mol电子),C项正确;催化剂能降低反应的活化能,加快反应速率,D项正确。
8.[2024·贵阳市适应性考试]HO 是常见的绿色氧化剂,在化学研究中应用广泛。用
2 2
H 制备HO 的反应机理如图所示。下列说法不正确的是( )
2 2 2
A.X代表的是HCl
B.过程③有极性键的断裂和形成
C.金属Pd在该反应中作催化剂
D.该过程的原子利用率为100%
答案:C
解析:反应①为[PdCl ]2-与H 反应生成Pd、X和Cl-,根据质量守恒可知X为HCl,
4 2
A项正确;过程③有H—Cl键(极性键)的断裂和H—O键(极性键)的生成,故B项正
确;[PdCl ]2-是该过程的催化剂,Pd为中间产物,C项错误;该过程的总反应为 H +
4 2
O===H O,反应物全部转化为了目标产物,原子利用率为100%,D项正确。
2 2 2
9.[2024·湖北省八市高三联考]液化石油气的主要成分C H 在光照条件下与Cl 反应,
3 8 2
可得到各种氯代丙烷。已知:①C H 与Cl 反应的机理为自由基反应,包括以下几步:
3 8 2
Ⅰ.链引发:Cl――→2Cl·
2
Ⅱ. 链 传 递 : Cl· + CHCHCH―→·CHCHCH + HCl , ·CHCHCH +
3 2 3 2 2 3 2 2 3
Cl―→ClCH CHCH+Cl·……
2 2 2 3
Ⅲ.链终止:2Cl·―→Cl,Cl·+·CHCHCH―→ClCH CHCH……
2 2 2 3 2 2 3
②丙烷氯代反应中链传递的一步反应能量变化如图。
下列说法正确的是( )
A.将液化石油气灶改用天然气为燃料,若进气口保持不变,则需要调大风门
B.先将Cl 用光照射,然后迅速在黑暗处与C H 混合,可得到氯代丙烷
2 3 8
C.先将Cl 用光照射,然后在黑暗处放置较长时间,再与C H 混合,可得到氯代丙烷
2 3 8
D.断裂—CH 中1 mol C—H键比断裂—CH—中1 mol C—H键所需能量小
3 2
答案:B
解析:1 mol C H 完全燃烧时消耗5 mol O ,1 mol CH 完全燃烧时消耗2 mol O ,
3 8 2 4 2
C H 的耗氧量更大,故改用天然气为燃料时,若进气口保持不变,需要调小风门,A项错
3 8
误;由已知信息①知,只有链引发反应需要光照,故B项正确;氯气光照后在黑暗处放置
太久,会发生反应:2Cl·―→Cl,体系中Cl·被消耗,导致无法发生链传递反应,得不到氯
2
代丙烷,C项错误;由已知信息②知,断裂—CH 中1 mol C—H键比断裂—CH—中1 mol
3 2
C—H键吸收的能量多,D项错误。
10.[2024·广东六校联盟联考]目前认为酸催化乙烯水合制乙醇的反应机理及能量与反
应历程的关系如图所示。下列说法错误的是( )
A.第②、③步反应均释放能量
B.该反应历程中有两个过渡态
C.酸催化剂能同时降低正、逆反应的活化能
D.总反应速率由第①步反应决定
答案:B
解析:根据能量与反应历程的关系图可知第②、③步反应的反应物的总能量均高于生
成物,为放热反应,A项正确;该反应经历3个步骤,有3个过渡态,B项错误;催化剂
通过改变反应历程,可以同时降低正、逆反应的活化能,加快反应速率,C项正确;据图
可知第①步反应的活化能最大,为慢反应,决定总反应速率,D项正确。