文档内容
专练 38 金属的腐蚀与防护
授课提示:对应学生用书75页
1.[2024·湖北卷]2024年5月8日,我国第三艘航空母舰福建舰顺利完成首次海试。舰
体表面需要采取有效的防锈措施,下列防锈措施中不形成表面钝化膜的是( )
A.发蓝处理 B.阳极氧化
C.表面渗镀 D.喷涂油漆
答案:D
解析:发蓝处理是将钢在空气中加热或直接浸在浓氧化性溶液中,使其表面产生极薄
的氧化物膜的材料保护技术,故A不符合题意;阳极氧化是使阳极材料表面形成一层氧化
膜的过程,B不符合题意;表面渗镀是向金属中渗入一种或几种元素以在表面形成一层扩
散合金层,C不符合题意;喷涂油漆是利用油漆隔绝空气中的水蒸气和氧气,不形成表面
钝化膜,D符合题意。
2.[2024·浙江1月]破损的镀锌铁皮在氨水中发生电化学腐蚀,生成[Zn(NH ) ]2+和
3 4
H,下列说法不正确的是( )
2
A.氨水浓度越大,腐蚀趋势越大
B.随着腐蚀的进行,溶液的pH变大
C.铁电极上发生的电极反应式为:2NH +2e-===H ↑+2NH
3 2
D.每生成标准状况下224 mL H ,消耗0.010 mol Zn
2
答案:C
解析:Zn比Fe活泼,在氨水中二者可形成原电池,电化学腐蚀的总反应方程式为Zn
+4NH ·H O===[Zn(NH ) ]2++H↑+2HO+2OH-,氨水浓度越大,生成[Zn(NH ) ]2
3 2 3 4 2 2 3 4
+的速率越快,腐蚀趋势越大,A项正确;总反应方程式中有OH-生成,故溶液pH变大,
B项正确;Zn生成[Zn(NH ) ]2+,发生氧化反应,作负极,则Fe作正极,正极上水解离
3 4
出来的H+得电子生成氢气,结合电解液为氨水知,Fe电极上发生的电极反应式为2HO+
2
2e-===H ↑+2OH-,C项错误;根据总反应方程式,可得关系式:H ~Zn,故每生成标
2 2
准状况下224 mL(0.010 mol) H,消耗0.010 mol Zn,D项正确。
2
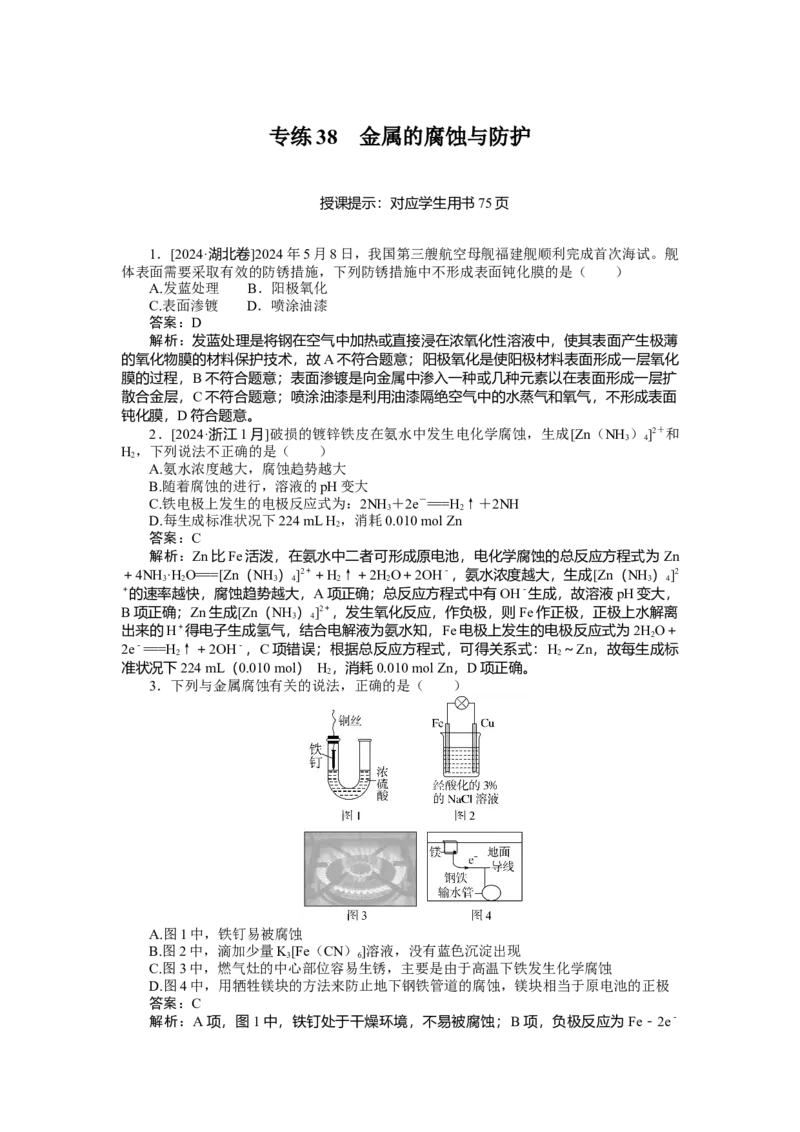
3.下列与金属腐蚀有关的说法,正确的是( )
A.图1中,铁钉易被腐蚀
B.图2中,滴加少量K[Fe(CN)]溶液,没有蓝色沉淀出现
3 6
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极
答案:C
解析:A项,图1中,铁钉处于干燥环境,不易被腐蚀;B项,负极反应为Fe-2e-===Fe2+,Fe2+与[Fe(CN) ]3-反应生成Fe [Fe(CN) ] 蓝色沉淀;D项,为牺牲阳极的
6 3 6 2
阴极保护法,镁块相当于原电池的负极。
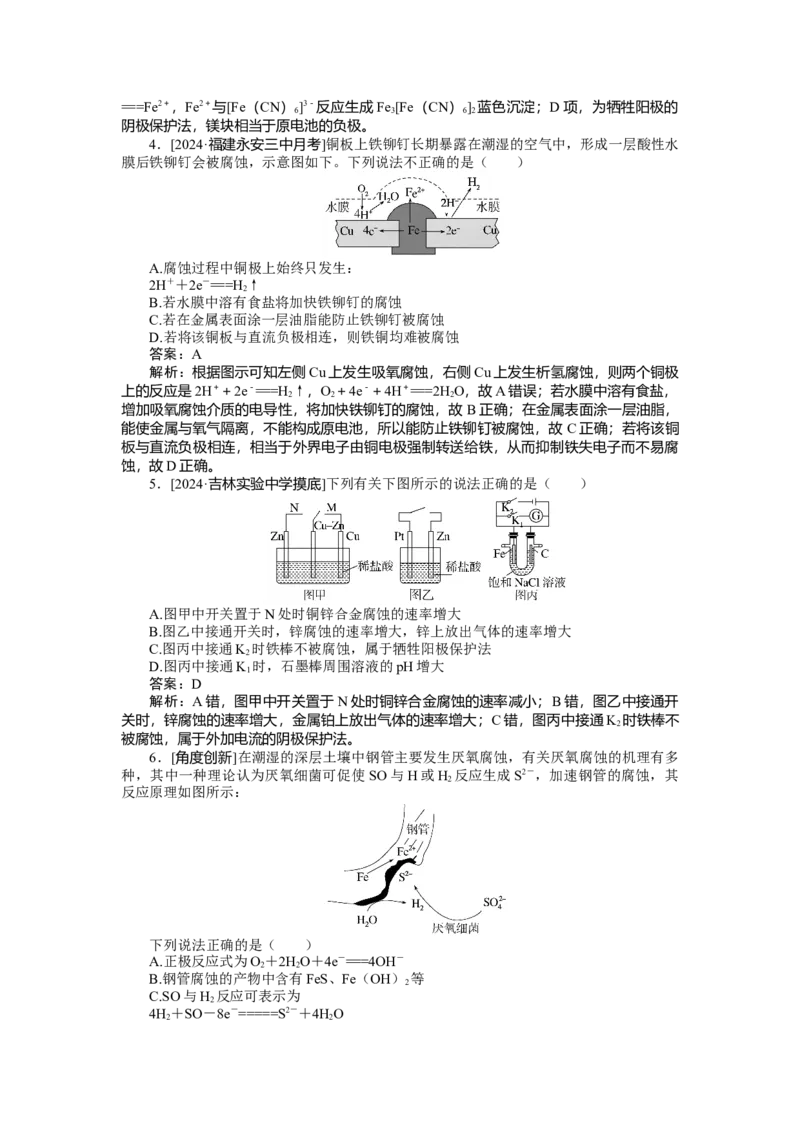
4.[2024·福建永安三中月考]铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水
膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是( )
A.腐蚀过程中铜极上始终只发生:
2H++2e-===H ↑
2
B.若水膜中溶有食盐将加快铁铆钉的腐蚀
C.若在金属表面涂一层油脂能防止铁铆钉被腐蚀
D.若将该铜板与直流负极相连,则铁铜均难被腐蚀
答案:A
解析:根据图示可知左侧Cu上发生吸氧腐蚀,右侧Cu上发生析氢腐蚀,则两个铜极
上的反应是2H++2e-===H ↑,O+4e-+4H+===2H O,故A错误;若水膜中溶有食盐,
2 2 2
增加吸氧腐蚀介质的电导性,将加快铁铆钉的腐蚀,故 B正确;在金属表面涂一层油脂,
能使金属与氧气隔离,不能构成原电池,所以能防止铁铆钉被腐蚀,故 C正确;若将该铜
板与直流负极相连,相当于外界电子由铜电极强制转送给铁,从而抑制铁失电子而不易腐
蚀,故D正确。
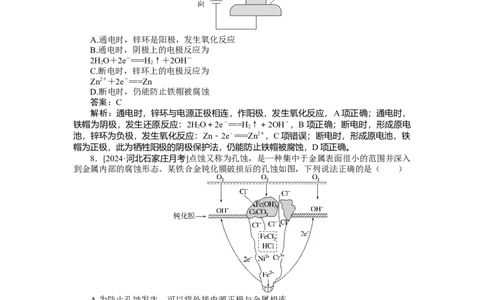
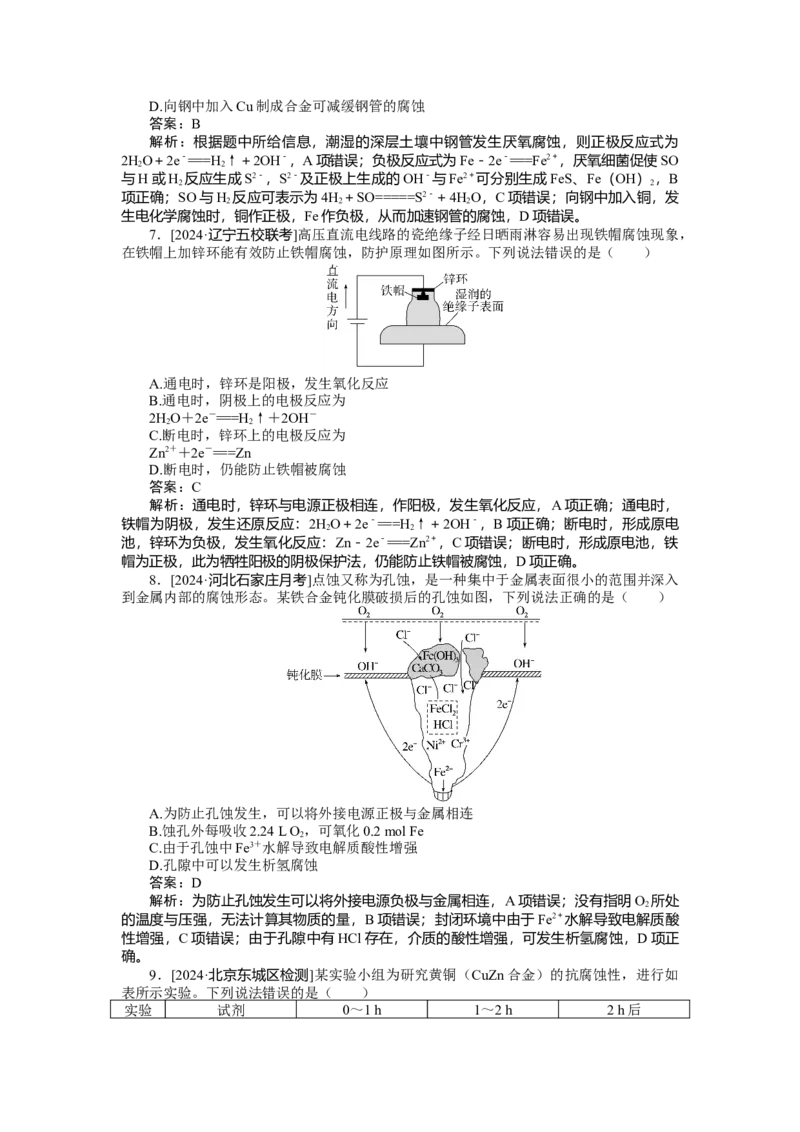
5.[2024·吉林实验中学摸底]下列有关下图所示的说法正确的是( )
A.图甲中开关置于N处时铜锌合金腐蚀的速率增大
B.图乙中接通开关时,锌腐蚀的速率增大,锌上放出气体的速率增大
C.图丙中接通K 时铁棒不被腐蚀,属于牺牲阳极保护法
2
D.图丙中接通K 时,石墨棒周围溶液的pH增大
1
答案:D
解析:A错,图甲中开关置于N处时铜锌合金腐蚀的速率减小;B错,图乙中接通开
关时,锌腐蚀的速率增大,金属铂上放出气体的速率增大;C错,图丙中接通K 时铁棒不
2
被腐蚀,属于外加电流的阴极保护法。
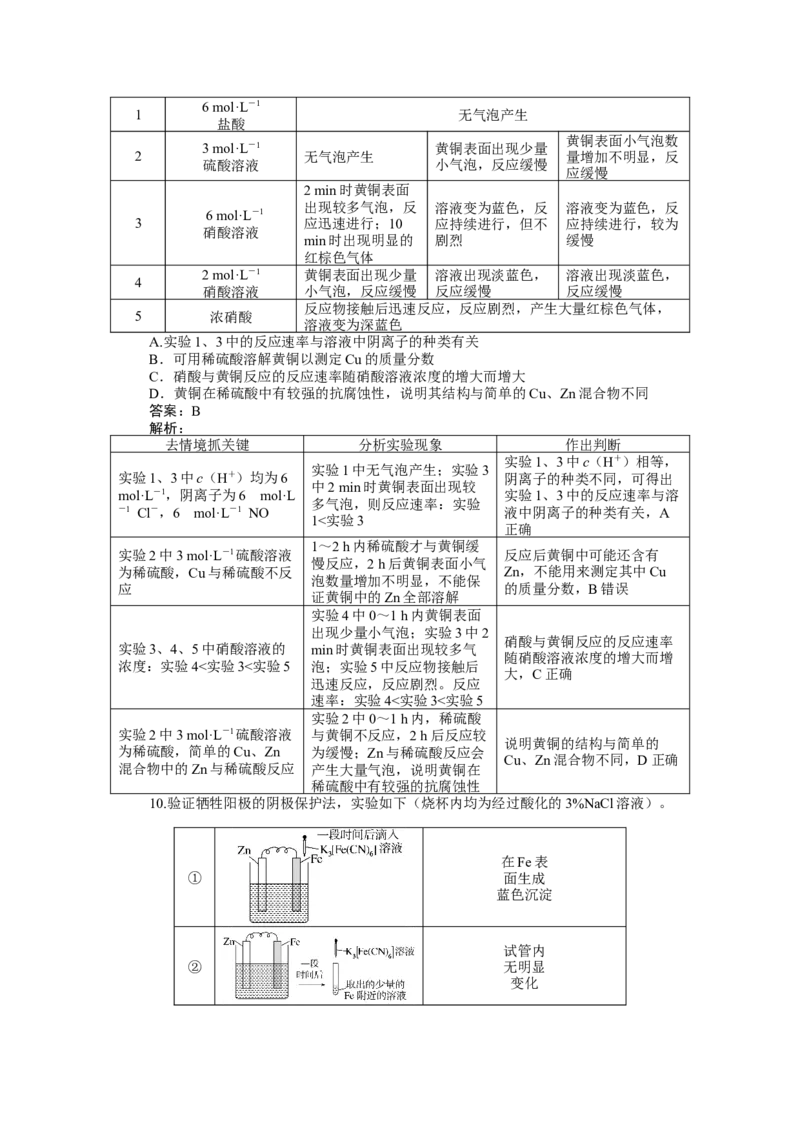
6.[角度创新]在潮湿的深层土壤中钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多
种,其中一种理论认为厌氧细菌可促使 SO与H或H 反应生成S2-,加速钢管的腐蚀,其
2
反应原理如图所示:
下列说法正确的是( )
A.正极反应式为O+2HO+4e-===4OH-
2 2
B.钢管腐蚀的产物中含有FeS、Fe(OH) 等
2
C.SO与H 反应可表示为
2
4H+SO-8e-=====S2-+4HO
2 2D.向钢中加入Cu制成合金可减缓钢管的腐蚀
答案:B
解析:根据题中所给信息,潮湿的深层土壤中钢管发生厌氧腐蚀,则正极反应式为
2HO+2e-===H ↑+2OH-,A项错误;负极反应式为Fe-2e-===Fe2+,厌氧细菌促使SO
2 2
与H或H 反应生成S2-,S2-及正极上生成的OH-与Fe2+可分别生成FeS、Fe(OH) ,B
2 2
项正确;SO与H 反应可表示为4H +SO=====S2-+4HO,C项错误;向钢中加入铜,发
2 2 2
生电化学腐蚀时,铜作正极,Fe作负极,从而加速钢管的腐蚀,D项错误。
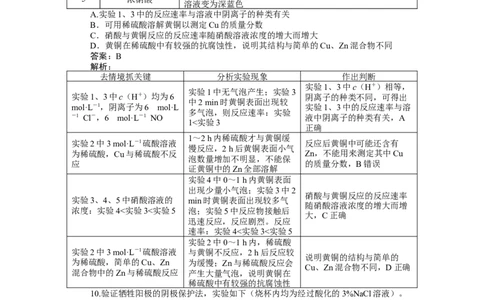
7.[2024·辽宁五校联考]高压直流电线路的瓷绝缘子经日晒雨淋容易出现铁帽腐蚀现象,
在铁帽上加锌环能有效防止铁帽腐蚀,防护原理如图所示。下列说法错误的是( )
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为
2HO+2e-===H ↑+2OH-
2 2
C.断电时,锌环上的电极反应为
Zn2++2e-===Zn
D.断电时,仍能防止铁帽被腐蚀
答案:C
解析:通电时,锌环与电源正极相连,作阳极,发生氧化反应,A项正确;通电时,
铁帽为阴极,发生还原反应:2HO+2e-===H ↑+2OH-,B项正确;断电时,形成原电
2 2
池,锌环为负极,发生氧化反应:Zn-2e-===Zn2+,C项错误;断电时,形成原电池,铁
帽为正极,此为牺牲阳极的阴极保护法,仍能防止铁帽被腐蚀,D项正确。
8.[2024·河北石家庄月考]点蚀又称为孔蚀,是一种集中于金属表面很小的范围并深入
到金属内部的腐蚀形态。某铁合金钝化膜破损后的孔蚀如图,下列说法正确的是( )
A.为防止孔蚀发生,可以将外接电源正极与金属相连
B.蚀孔外每吸收2.24 L O ,可氧化0.2 mol Fe
2
C.由于孔蚀中Fe3+水解导致电解质酸性增强
D.孔隙中可以发生析氢腐蚀
答案:D
解析:为防止孔蚀发生可以将外接电源负极与金属相连,A项错误;没有指明O 所处
2
的温度与压强,无法计算其物质的量,B项错误;封闭环境中由于Fe2+水解导致电解质酸
性增强,C项错误;由于孔隙中有HCl存在,介质的酸性增强,可发生析氢腐蚀,D项正
确。
9.[2024·北京东城区检测]某实验小组为研究黄铜(CuZn合金)的抗腐蚀性,进行如
表所示实验。下列说法错误的是( )
实验 试剂 0~1 h 1~2 h 2 h后6 mol·L-1
1 无气泡产生
盐酸
黄铜表面小气泡数
3 mol·L-1 黄铜表面出现少量
2 无气泡产生 量增加不明显,反
硫酸溶液 小气泡,反应缓慢
应缓慢
2 min时黄铜表面
出现较多气泡,反 溶液变为蓝色,反 溶液变为蓝色,反
6 mol·L-1
3 应迅速进行;10 应持续进行,但不 应持续进行,较为
硝酸溶液
min时出现明显的 剧烈 缓慢
红棕色气体
2 mol·L-1 黄铜表面出现少量 溶液出现淡蓝色, 溶液出现淡蓝色,
4
硝酸溶液 小气泡,反应缓慢 反应缓慢 反应缓慢
反应物接触后迅速反应,反应剧烈,产生大量红棕色气体,
5 浓硝酸
溶液变为深蓝色
A.实验1、3中的反应速率与溶液中阴离子的种类有关
B.可用稀硫酸溶解黄铜以测定Cu的质量分数
C.硝酸与黄铜反应的反应速率随硝酸溶液浓度的增大而增大
D.黄铜在稀硫酸中有较强的抗腐蚀性,说明其结构与简单的Cu、Zn混合物不同
答案:B
解析:
去情境抓关键 分析实验现象 作出判断
实验1、3中c(H+)相等,
实验1中无气泡产生;实验3
实验1、3中c(H+)均为6 阴离子的种类不同,可得出
中2 min时黄铜表面出现较
mol·L-1,阴离子为6 mol·L 实验1、3中的反应速率与溶
多气泡,则反应速率:实验
-1 Cl-,6 mol·L-1 NO 液中阴离子的种类有关,A
1<实验3
正确
1~2 h内稀硫酸才与黄铜缓
实验2中3 mol·L-1硫酸溶液 反应后黄铜中可能还含有
慢反应,2 h后黄铜表面小气
为稀硫酸,Cu与稀硫酸不反 Zn,不能用来测定其中Cu
泡数量增加不明显,不能保
应 的质量分数,B错误
证黄铜中的Zn全部溶解
实验4中0~1 h内黄铜表面
出现少量小气泡;实验3中2
硝酸与黄铜反应的反应速率
实验3、4、5中硝酸溶液的 min时黄铜表面出现较多气
随硝酸溶液浓度的增大而增
浓度:实验4<实验3<实验5 泡;实验5中反应物接触后
大,C正确
迅速反应,反应剧烈。反应
速率:实验4<实验3<实验5
实验2中0~1 h内,稀硫酸
实验2中3 mol·L-1硫酸溶液 与黄铜不反应,2 h后反应较
说明黄铜的结构与简单的
为稀硫酸,简单的Cu、Zn 为缓慢;Zn与稀硫酸反应会
Cu、Zn混合物不同,D正确
混合物中的Zn与稀硫酸反应 产生大量气泡,说明黄铜在
稀硫酸中有较强的抗腐蚀性
10.验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
在Fe表
① 面生成
蓝色沉淀
试管内
② 无明显
变化试管内
③ 生成蓝
色沉淀
下列说法不正确的是( )
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K[Fe(CN)]可能将Fe氧化
3 6
C.验证Zn保护Fe时可用②的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
答案:D
解析:②中试管内无明显变化,说明Fe附近溶液中无Fe2+,③中生成蓝色沉淀,说明
存在Fe2+,对比可说明Zn的存在保护了Fe,A正确;①中加入K[Fe(CN) ]在Fe表面
3 6
产生蓝色沉淀,说明Fe表面产生了Fe2+,对比①②的异同,①中可能是K[Fe(CN) ]将
3 6
Fe氧化成Fe2+,B正确;②中无变化说明无Fe2+生成,Zn保护Fe,C正确;将Zn换成
Cu,若产生蓝色沉淀,则可能是因为Fe比Cu活泼,形成原电池产生Fe2+,也可能是因为
K[Fe(CN)]氧化Fe生成Fe2+,因此不能作为判断Fe比Cu活泼的依据,D错误。
3 6