文档内容
镇江市 2008 年初中毕业、升学统一考试化学试卷
题 号 一、二 三 四 五 六 总 分 结分人 核分人
得 分
说明:1.本试卷共6页,满分100分。考试时间100分钟。
2.可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 Ca-40 Fe-56 Ba-137
得分 评卷人 一 、选择题(本题包括16小题,每小题2分,共32分。 每小题只有一个选
项符合题意)
1.“节能降耗、保护环境”是当今社会发展的主题。下列做法符合这一要求的是 ( )
A.大型超市提倡顾客使用塑料袋
B.利用太阳能、风能和氢能等替代化石能源
C.鼓励私人购买家用轿车代替公交车
D.含磷洗衣粉去污效果好,应提倡广泛使用
2.下列日常生活中的物质属于纯净物的是 ( )
3.用化学的观点解释下列成语,错误的是 ( )
A.十年树木:树木生长,无化学变化 B.花香四溢:分子在不断运动
C.釜底抽薪:将可燃物撤出燃烧区 D.百炼成钢:逐渐降低生铁中碳、硅等含量
4.生活中的下列物品,用合成材料制作的是 ( )
A.铝合金门窗 B.玻璃钢桌椅 C.塑料洗衣盆 D.景德镇瓷器
5.现对①碳酸氢铵;②生石灰;③甲烷;④烧碱;⑤酒精;⑥镁;⑦干冰;⑧棉花;⑨维生素C;
⑩红磷等物质进行分类,下列分类正确的是 ( )
A.单质:⑥⑦ B.有机物:③⑤⑧⑨
C.氧化物:②⑩ D.盐:①④
6.下列有关人体生理活动的叙述,错误的是 ( )
A.代谢产生的CO,如不能及时排出,会使血液的pH增大
2
B.无机盐和水虽不能提供能量,却是人体必需的
C.胃液中少量的盐酸可以帮助消化
D.香烟烟气中的CO会使血红蛋白携氧能力降低
7.“绿色化学”要求从根本上减少或杜绝污染。下列做法中符合绿色化学理念的是 ( )
A.实验中未说明药品用量时,取用较多量药品进行实验
B.实验室将废液直接倒入下水道
C.对废旧电池作深埋处理,消除其污染
D.化工生产中使原料尽可能地转化为产品
8.下列主题知识的归纳中,正确的一组是 ( )
A. 生活常识 B. 安全常识
用铁锅烹调食物→防止贫血 煤气泄漏→先打开排气扇
蛋白质摄入过少→使人生长发育迟缓等 海鲜防腐→甲醛溶液浸泡
C.物质鉴别 D.环保知识
蚕丝布料和化纤布料→点燃 臭氧层空洞→温室效应
加碘食盐和无碘食盐→淀粉溶液 过度施用农药、化肥→水污染和土壤板结
9.今年春节前,我省发生了特大冰雪灾害,为确保道路畅通,交通部门使用了大量的氯化钠融雪剂。下列关于该融雪剂的说法中,
错误的是 ( )
A.氯化钠能融雪是因为其溶液的凝固点比水低
B.氯化钠的大量使用会造成地下水污染
C.使用氯化钠融雪,会加快钢铁桥梁的锈蚀
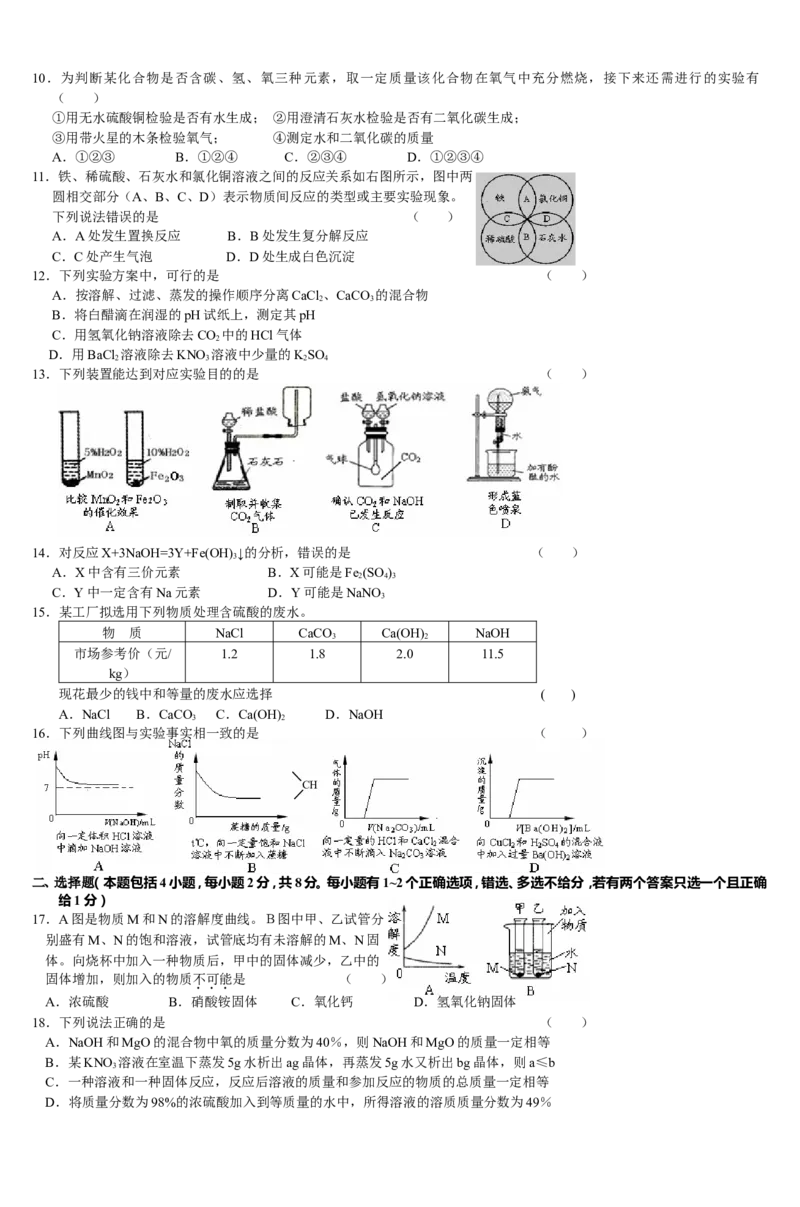
D.使用大量氯化钠融雪,对公路周围农作物的生长无影响10.为判断某化合物是否含碳、氢、氧三种元素,取一定质量该化合物在氧气中充分燃烧,接下来还需进行的实验有
( )
①用无水硫酸铜检验是否有水生成; ②用澄清石灰水检验是否有二氧化碳生成;
③用带火星的木条检验氧气; ④测定水和二氧化碳的质量
A.①②③ B.①②④ C.②③④ D.①②③④
11.铁、稀硫酸、石灰水和氯化铜溶液之间的反应关系如右图所示,图中两
圆相交部分(A、B、C、D)表示物质间反应的类型或主要实验现象。
下列说法错误的是 ( )
A.A处发生置换反应 B.B处发生复分解反应
C.C处产生气泡 D.D处生成白色沉淀
12.下列实验方案中,可行的是 ( )
A.按溶解、过滤、蒸发的操作顺序分离CaCl 、CaCO 的混合物
2 3
B.将白醋滴在润湿的pH试纸上,测定其pH
C.用氢氧化钠溶液除去CO 中的HCl气体
2
D.用BaCl 溶液除去KNO 溶液中少量的KSO
2 3 2 4
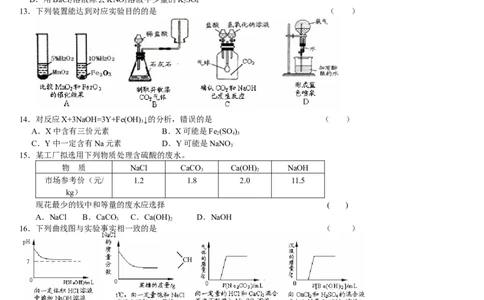
13.下列装置能达到对应实验目的的是 ( )
14.对反应X+3NaOH=3Y+Fe(OH) ↓的分析,错误的是 ( )
3
A.X中含有三价元素 B.X可能是Fe (SO )
2 4 3
C.Y中一定含有Na元素 D.Y可能是NaNO
3
15.某工厂拟选用下列物质处理含硫酸的废水。
物 质 NaCl CaCO Ca(OH) NaOH
3 2
市场参考价(元/ 1.2 1.8 2.0 11.5
kg)
现花最少的钱中和等量的废水应选择 ( )
A.NaCl B.CaCO C.Ca(OH) D.NaOH
3 2
16.下列曲线图与实验事实相一致的是 ( )
CH
二、选择题(本题包括4小题,每小题2分,共8分。每小题有1~2个正确选项,错选、多选不给分,若有两个答案只选一个且正确
给1分)
17.A图是物质M和N的溶解度曲线。B图中甲、乙试管分
别盛有M、N的饱和溶液,试管底均有未溶解的M、N固
体。向烧杯中加入一种物质后,甲中的固体减少,乙中的
固体增加,则加入的物质不可能是 ( )
A.浓硫酸 B.硝酸铵固体 C.氧化钙 D.氢氧化钠固体
18.下列说法正确的是 ( )
A.NaOH和MgO的混合物中氧的质量分数为40%,则NaOH和MgO的质量一定相等
B.某KNO 溶液在室温下蒸发5g水析出ag晶体,再蒸发5g水又析出bg晶体,则a≤b
3
C.一种溶液和一种固体反应,反应后溶液的质量和参加反应的物质的总质量一定相等
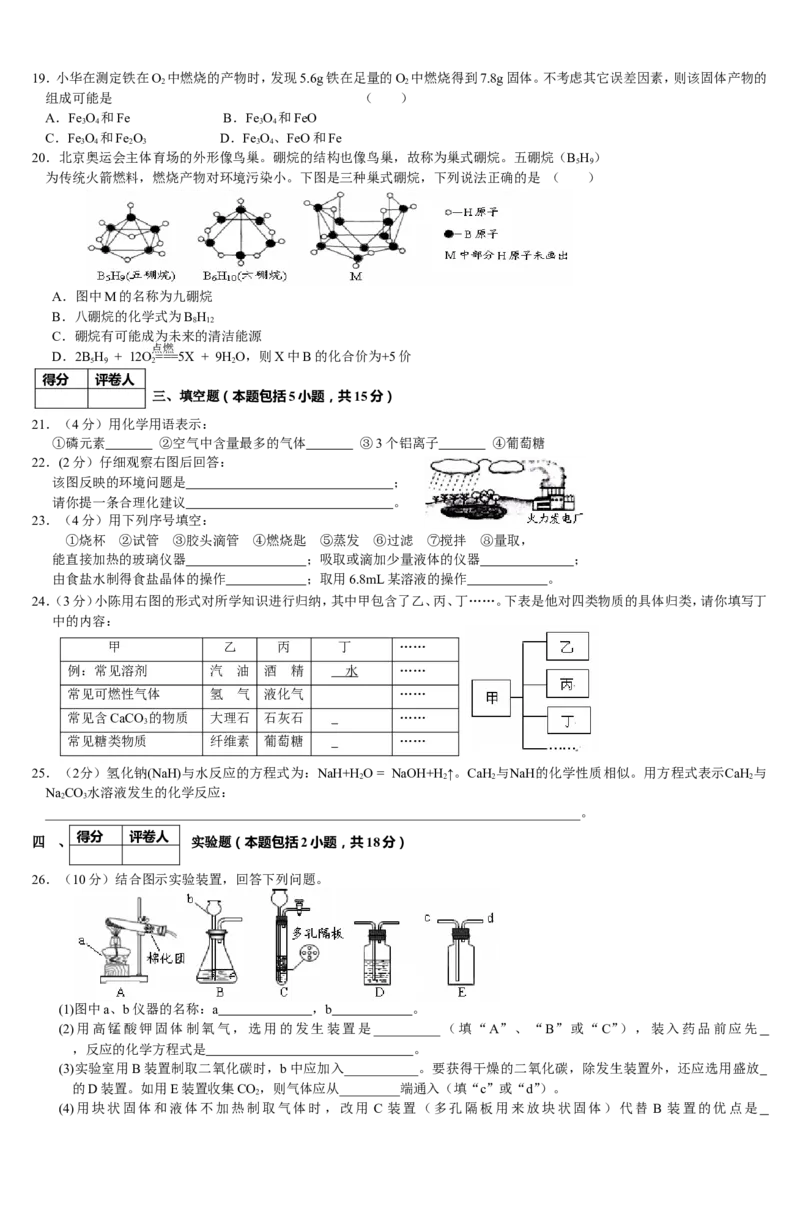
D.将质量分数为98%的浓硫酸加入到等质量的水中,所得溶液的溶质质量分数为49%19.小华在测定铁在O 中燃烧的产物时,发现5.6g铁在足量的O 中燃烧得到7.8g固体。不考虑其它误差因素,则该固体产物的
2 2
组成可能是 ( )
A.Fe O 和Fe B.Fe O 和FeO
3 4 3 4
C.Fe O 和Fe O D.Fe O、FeO和Fe
3 4 2 3 3 4
20.北京奥运会主体育场的外形像鸟巢。硼烷的结构也像鸟巢,故称为巢式硼烷。五硼烷(B H)
5 9
为传统火箭燃料,燃烧产物对环境污染小。下图是三种巢式硼烷,下列说法正确的是 ( )
A.图中M的名称为九硼烷
B.八硼烷的化学式为B H
8 12
C.硼烷有可能成为未来的清洁能源
点燃
D.2B H + 12O===5X + 9HO,则X中B的化合价为+5价
5 9 2 2
得分 评卷人
三、填空题(本题包括5小题,共15分)
21.(4分)用化学用语表示:
①磷元素 ②空气中含量最多的气体 ③3个铝离子 ④葡萄糖
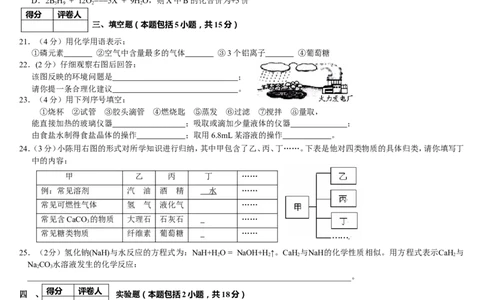
22.(2分)仔细观察右图后回答:
该图反映的环境问题是 ;
请你提一条合理化建议 。
23.(4分)用下列序号填空:
①烧杯 ②试管 ③胶头滴管 ④燃烧匙 ⑤蒸发 ⑥过滤 ⑦搅拌 ⑧量取,
能直接加热的玻璃仪器 ;吸取或滴加少量液体的仪器 ;
由食盐水制得食盐晶体的操作 ;取用6.8mL某溶液的操作 。
24.(3分)小陈用右图的形式对所学知识进行归纳,其中甲包含了乙、丙、丁……。下表是他对四类物质的具体归类,请你填写丁
中的内容:
甲 乙 丙 丁 ……
例:常见溶剂 汽 油 酒 精 水 ……
常见可燃性气体 氢 气 液化气 ……
常见含CaCO
3
的物质 大理石 石灰石 ……
常见糖类物质 纤维素 葡萄糖 ……
25.(2分)氢化钠(NaH)与水反应的方程式为:NaH+H O = NaOH+H ↑。CaH 与NaH的化学性质相似。用方程式表示CaH 与
2 2 2 2
NaCO水溶液发生的化学反应:
2 3
________________________________________________________________________________。
得分 评卷人
四 、 实验题(本题包括2小题,共18分)
26.(10分)结合图示实验装置,回答下列问题。
(1)图中a、b仪器的名称:a ,b 。
(2)用高锰酸钾固体制氧气,选用的发生装置是__________(填“A”、“B”或“C”),装入药品前应先
,反应的化学方程式是 。
(3)实验室用B装置制取二氧化碳时,b中应加入___________。要获得干燥的二氧化碳,除发生装置外,还应选用盛放
的D装置。如用E装置收集CO,则气体应从_________端通入(填“c”或“d”)。
2
(4)用块状固体和液体不加热制取气体时,改用 C 装置(多孔隔板用来放块状固体)代替 B 装置的优点是(答出一点即可)。
27.(8分)草酸晶体(HC O•2HO)熔点较低,加热会熔化、气化和分解。草酸(HC O)受热会分解,它与氢氧化钙的反应为:
2 2 4 2 2 2 4
HC O + Ca(OH) = CaC O↓(白色)+ 2HO。
2 2 4 2 2 4 2
甲、乙两同学对草酸受热分解的产物作如下探究:
(1)猜想与假设:
第一种:草酸分解生成CO 和 H; 第二种:草酸分解生成CO 、CO和 HO;
2 2 2 2
第三种:草酸分解:HC O CO↑+ HO(未配平);
2 2 4 2 2
有同学从理论上就可判断第三种假设不成立,老师也认为这一判断是正确的,该同学判断的理论依据是
。
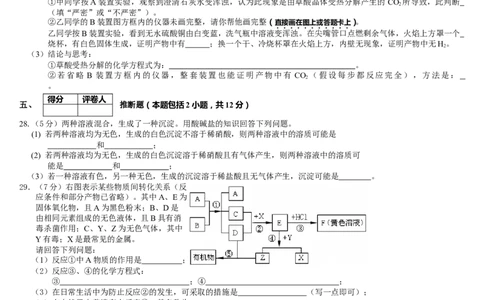
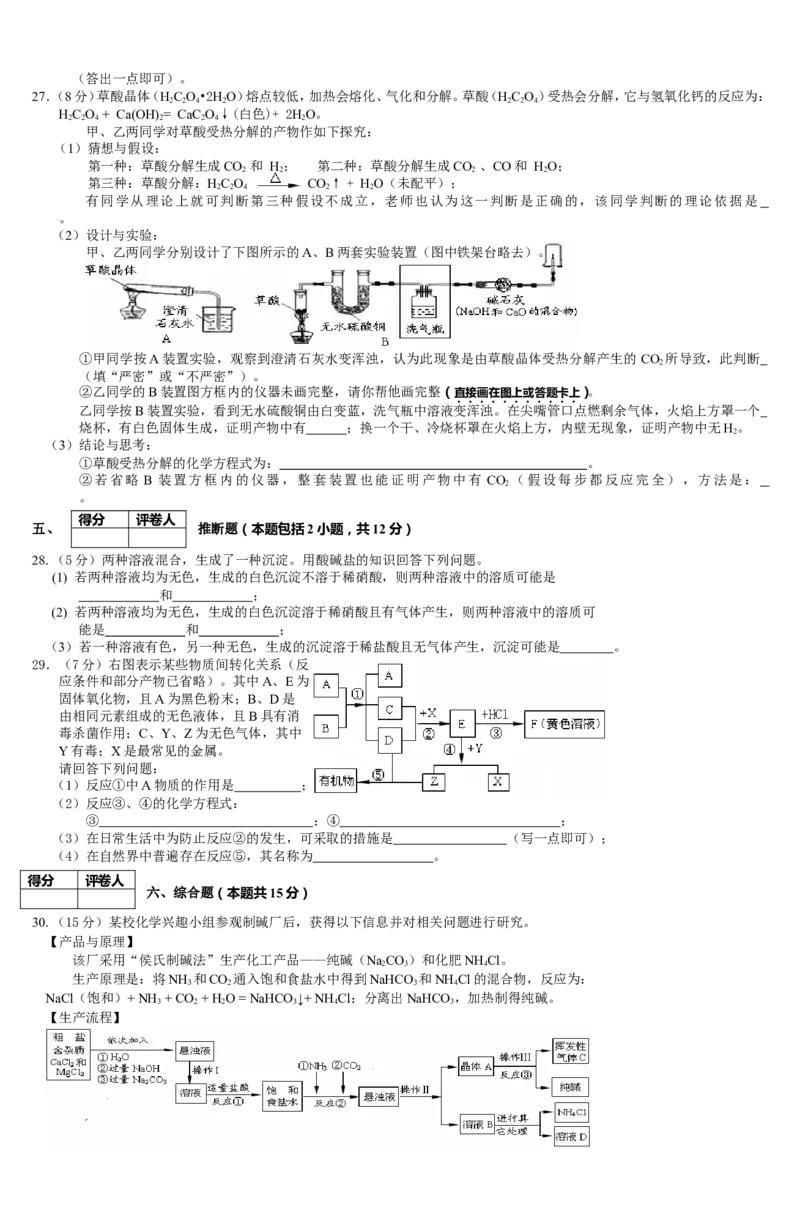
(2)设计与实验:
甲、乙两同学分别设计了下图所示的A、B两套实验装置(图中铁架台略去)。
①甲同学按A装置实验,观察到澄清石灰水变浑浊,认为此现象是由草酸晶体受热分解产生的 CO 所导致,此判断
2
(填“严密”或“不严密”)。
②乙同学的B装置图方框内的仪器未画完整,请你帮他画完整(直接画在图上或答题卡上)。
乙同学按B装置实验,看到无水硫酸铜由白变蓝,洗气瓶中溶液变浑浊。在尖嘴管口点燃剩余气体,火焰上方罩一个
烧杯,有白色固体生成,证明产物中有 ;换一个干、冷烧杯罩在火焰上方,内壁无现象,证明产物中无H。
2
(3)结论与思考:
①草酸受热分解的化学方程式为: 。
②若省略 B 装置方框内的仪器,整套装置也能证明产物中有 CO (假设每步都反应完全),方法是:
2
。
得分 评卷人
五、 推断题(本题包括2小题,共12分)
28.(5分)两种溶液混合,生成了一种沉淀。用酸碱盐的知识回答下列问题。
(1) 若两种溶液均为无色,生成的白色沉淀不溶于稀硝酸,则两种溶液中的溶质可能是
和 ;
(2) 若两种溶液均为无色,生成的白色沉淀溶于稀硝酸且有气体产生,则两种溶液中的溶质可
能是 和 ;
(3)若一种溶液有色,另一种无色,生成的沉淀溶于稀盐酸且无气体产生,沉淀可能是 。
29.(7分)右图表示某些物质间转化关系(反
应条件和部分产物已省略)。其中A、E为
固体氧化物,且A为黑色粉末;B、D是
由相同元素组成的无色液体,且B具有消
毒杀菌作用;C、Y、Z为无色气体,其中
Y有毒;X是最常见的金属。
请回答下列问题:
(1)反应①中A物质的作用是 ;
(2)反应③、④的化学方程式:
③ ;④ ;
(3)在日常生活中为防止反应②的发生,可采取的措施是 (写一点即可);
(4)在自然界中普遍存在反应⑤,其名称为 。
得分 评卷人
六、综合题(本题共15分)
30.(15分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。
【产品与原理】
该厂采用“侯氏制碱法”生产化工产品——纯碱(NaCO)和化肥NH Cl。
2 3 4
生产原理是:将NH 和CO 通入饱和食盐水中得到NaHCO 和NH Cl的混合物,反应为:
3 2 3 4
NaCl(饱和)+ NH + CO + H O = NaHCO ↓+ NH Cl;分离出NaHCO ,加热制得纯碱。
3 2 2 3 4 3
【生产流程】【相关资料】
△
⑴ NH Cl == NH ↑+HCl↑
4 3
⑵ 已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
物质 NaCl NaHCO NH Cl NH CO
3 4 3 2
溶解度 36.0g 9.6g 37.2g 710 0.9
【问题讨论】:
⑴ 操作Ⅰ、Ⅱ、Ⅲ中,相同操作的名称为 。
⑵ 反应①中发生了两个反应,写出其中的一个化学方程式:
。
⑶ 反应③中得到纯碱的化学方程式为: 。
⑷ 溶液B中的溶质有 (至少写出两种)。
⑸ 上述生产流程中可循环使用的是 (填序号)。
A.挥发性气体C B.溶液D C.氢氧化镁 D.化肥NH Cl
4
【组成确定】
⑴ 称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
⑵ 另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO,再滴加AgNO 溶液,有白色沉淀。
3 3
由上述实验可确定纯碱样品含有杂质 (写化学式)。
【含量测定】
称取纯碱样品10.8g加入适量水,再加入过量CaCl 溶 工业纯碱标准:(NaCO%
2 2 3
液,搅拌、过滤、洗涤、干燥后称得固体质量为10.0g, ≥)
请通过计算并结合右表判断此纯碱样品等级为 品。 优等品 一等品 合格品
计算过程: 99.2 98.8 98.0
【总结反思】
某同学认为,在上述纯碱含量测定中,将CaCl 溶液改为BaCl 溶液,测定误差会减小,其理由是
2 2
。
镇江市 2008 年初中毕业、升学统一考试化学试卷
参考答案及评分标准
说明:1.化学专用名词或仪器名称写错不给分;
2.化学方程式中化学式写错不给分;若化学方程式不配平、未注明反应条件、未标出产物状态(↑或↓)或出现差错,全卷
共扣1分;
3.与参考答案不同的合理答案均给分。
一、选择题(本题包括16小题,每小题2分,共32分)
1.B 2.C 3.A 4.C 5.B 6.A 7.D 8.A
9.D 10.B 11.D 12.A 13.C 14.B 15.C 16.B
二、选择题(本题包括4小题,每小题2分,共8分。每小题有1~2个正确选项,错选、多选不给分,若有两个答案只选一个且正确
给1分)
17.B 18.BD 19.C 20.BC
三、填空题(本题包括5小题,共15分)
21.(共4分,每空1分)
①P ②N
2
③3Al3+ ④C
6
H
12
O
6
22.(共2分,每空1分)
酸雨问题、酸雨现象或酸雨(只要提及到“酸雨”均给分)(或大气污染、空气污染等)
减少化石燃料的使用(或工业废气净化后再排放等,其它合理答案均给分)
23.(共4分,每空1分)
② ③ ⑤ ⑧
24.(共3分,每空1分)
煤气[或天然气(CH)、一氧化碳(CO)等]
4
汉白玉(或鸡蛋壳、贝壳、方解石、白垩、珍珠、水垢等)(填CaCO 或碳酸钙不给分)
3
淀粉(或蔗糖、冰糖、麦芽糖等)
注:写名称、符号均给分
25.(共2分)
CaH+2HO + Na CO==CaCO ↓+2NaOH +2H↑(2分)
2 2 2 3 3 2
(或CaH+2HO =Ca(OH)+2H↑ ,Ca(OH)+ Na CO==CaCO ↓+2NaOH )(各1分)
2 2 2 2 2 2 3 3
四、实验题(本题包括2小题,共18分)26.(共10分)
(1) 酒精灯,(1分) 长颈漏斗(1分)。
(2) A,(1分) 检查装置气密性(意思相近的表述均给分),(1分)
△
2KMnO === KMnO +MnO+O 。(2分)
4 2 4 2 2
(3) 稀盐酸或稀硝酸(1分,写化学式也可) 浓硫酸或浓HSO (1分) c(1分)
2 4
(4) 随开随用、随关随停,容易控制(其它合理答案均给分,如节约药品等)(1分)
27.(共8分)
(1)无法进行配平、配不平或不符合质量守恒定律或只有化合价的升高,无化合价的降低 (1分)
(2)①不严密(1分)
②如右图 (长管不伸入液面下不给分,不作美观要求) (1分)
内壁附有澄清石灰水(其它合理答案均给分)(1分) CO(1分)
△
(3)① HC O CO↑+CO↑+HO(2分);
2 2 4 2 2
② 称量实验前后盛有碱石灰的干燥管的质量(意思相近的表述均给分)(1分)
五、推断题(本题包括2小题,共12分)
28、(共5分,每空1分)
(1)AgNO 和NaCl(或Ba(NO ) 和NaSO 等)
3 3 2 2 4
(2)BaCl 和NaCO(Ca(OH) 和NaCO 等)
2 2 3 2 2 3
(3)Cu(OH) 或Fe(OH) 或Fe(OH)
2 2 3
注:其它合理答案均给分,写名称或名称符号混写也可。
29.(共7分)
(1)催化作用(写“催化剂”、“催化”、“催化性”也给分); (1分)
高温
(2)③Fe O+6HCl===2FeCl +3H O (2分) ④3CO + Fe O===2Fe+3CO (2分)
2 3 3 2 2 3 2
(3)涂油(或刷漆、电镀等,其它合理答案均给分) (1分)
(4)光合作用(1分)
六、综合题(本题共15分)
30.(共15分)
【问题讨论】:
⑴ 过滤(1分)
⑵ NaOH+HCl===NaCl+H O 或 NaCO + 2HCl=2NaCl+H O+CO↑(2分)
2 2 3 2 2
△
⑶ 2NaHCO =NaCO+H O+CO↑ (2分)
3 2 3 2 2
⑷ NaHCO 、NaCl、NH Cl、NH HCO 四种中的任意两种(2分),(写名称或名称符号混写也可。只写1个且正确给1分,
3 4 4 3
只要写错1个就不给分)
⑸ A、B(2分),(选对1个给1分,只要选错1个不给分)
【组成确定】:
NaCl(1分)
【含量测定】(除计算过程3分外,其余每空1分。)
合格(1分)
解:设NaCO 的质量为x
2 3
NaCO+ CaCl =CaCO ↓+2NaCl……………………………………… (1分)
2 3 2 3
106 100
x 10.0g
106∶ 100 = x∶10.0g
解得: x= 10.6g ……………………………………………………… (1分)
10.6g/10.8g ×100%=98.1%(或98.14%或98.15%或98.2%)………(1分)
若用关系式解答:
NaCO ∽ CaCO ……………………………………………………… (1分)
2 3 3
106 100
x 10.0g
106∶ 100 = x∶10.0g
解得: x= 10.6g ……………………………………………………… (1分)
10.6g/10.8g ×100%=98.1%(或98.14%或98.15%或98.2%)………(1分)
(解、设不写不扣分。)
【总结反思】
等质量的碳酸钠与BaCl 反应产生的沉淀质量大,称量时的(相对)误差小(1分,其他意思相近的表
2
述,也可得分)。