文档内容
2014 年贵州省黔东南州中考化学试题及答案
一、选择题(共8小题,每小题2分,满分16分)
1.(2分)(2014•黔东南州)化学与我们的生活息息相关,下列有关说法中正确的是( )
A 人类需求的不断增加以及对自然资源的过度开发和不恰当使用,造成了温室效应、酸雨、
.赤潮、白色污染、潮汐等环境问题
B 绿色化学是指绿色植物为原料的化学新工艺
.
C 北京等城市雾霾天气是由液态水变成水蒸气导致的结果
.
D 氯氟烃(一种用于冰箱的制冷剂)是破坏臭氧层,导致臭氧层空洞的祸首
.
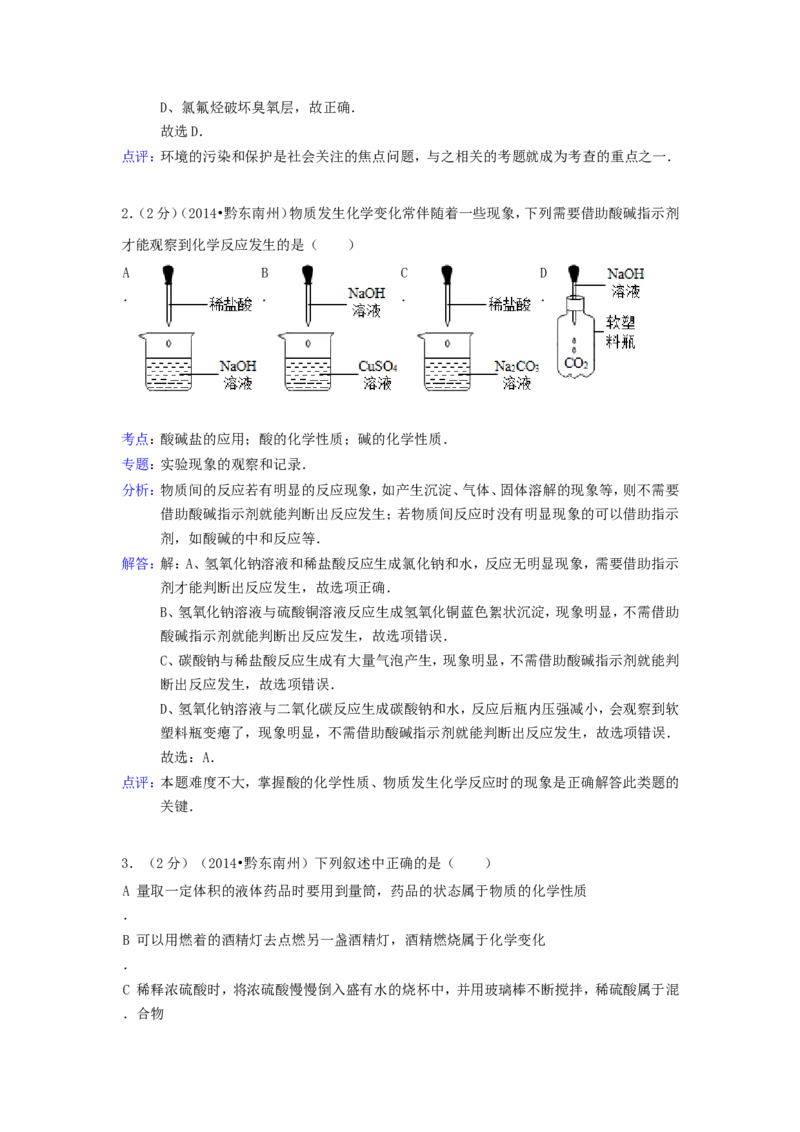
2.(2分)(2014•黔东南州)物质发生化学变化常伴随着一些现象,下列需要借助酸碱指示剂
才能观察到化学反应发生的是( )
A B C D
. . . .
3.(2分)(2014•黔东南州)下列叙述中正确的是( )
A 量取一定体积的液体药品时要用到量筒,药品的状态属于物质的化学性质
.
B 可以用燃着的酒精灯去点燃另一盏酒精灯,酒精燃烧属于化学变化
.
C 稀释浓硫酸时,将浓硫酸慢慢倒入盛有水的烧杯中,并用玻璃棒不断搅拌,稀硫酸属于混
.合物
D 实验室制取CO 需要用酒精灯、锥形瓶、分液漏斗、导管、集气瓶等仪器,该反应属于复分
2
.解反应
4.(2分)(2014•黔东南州)青少年过多摄入蛋糕里的人造奶油会产生一种影响身体发育的
反式脂肪酸,其化学式为C H O,下列反式脂肪酸的说法中正确的是( )
18 34 2
A 该物质中C、H、O三种元素的质量比为9:17:1.
B 该物质是由18个碳原子、34个氢原子、2个氧原子构成的
.
C 该物质的相对分子质量为282g
.
D 该物质在空气中完全燃烧的产物只有CO 和HO
2 2
.
5.(2分)(2014•黔东南州)下列有关溶液的说法中正确的是( )
A 常温下将100mL饱和Ca(OH) 溶液加热到50℃,会使溶液由饱和溶液变为不饱和溶液
2
.
B 从浓度为25%的HSO 溶液中取出10mL,则取出的10mL HSO 溶液浓度仍为25%
2 4 2 4
.
C 20℃时,50克水中溶解了18克NaCl,则20℃时NaCl的溶解度为36克
.
D 将95克KCl溶液蒸干得到5克KCl固体,则原溶液中KCl的浓度为5%
.
6.(2分)(2014•黔东南州)将一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定
条件下发生化学反应,一段时间后,测得各物质的质量数据如下
物质 甲 乙 丙 丁
反应前各物质的质 3 2 9 4
量/g
反应后各物质的质 5 2 未知数 6
量/g
下列选项中正确的是( )
A 该反应中甲和丙两物质变化的质量比为1:1
.
B 乙一定是该反应的催化剂
.
C 丙一定是化合物
.
D 该反应一定是化合反应
.
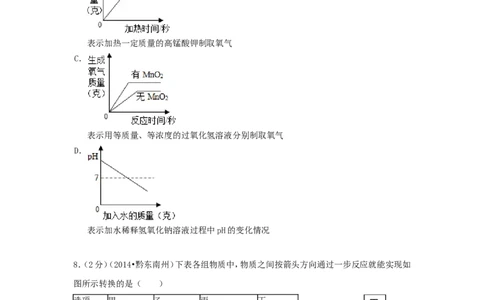
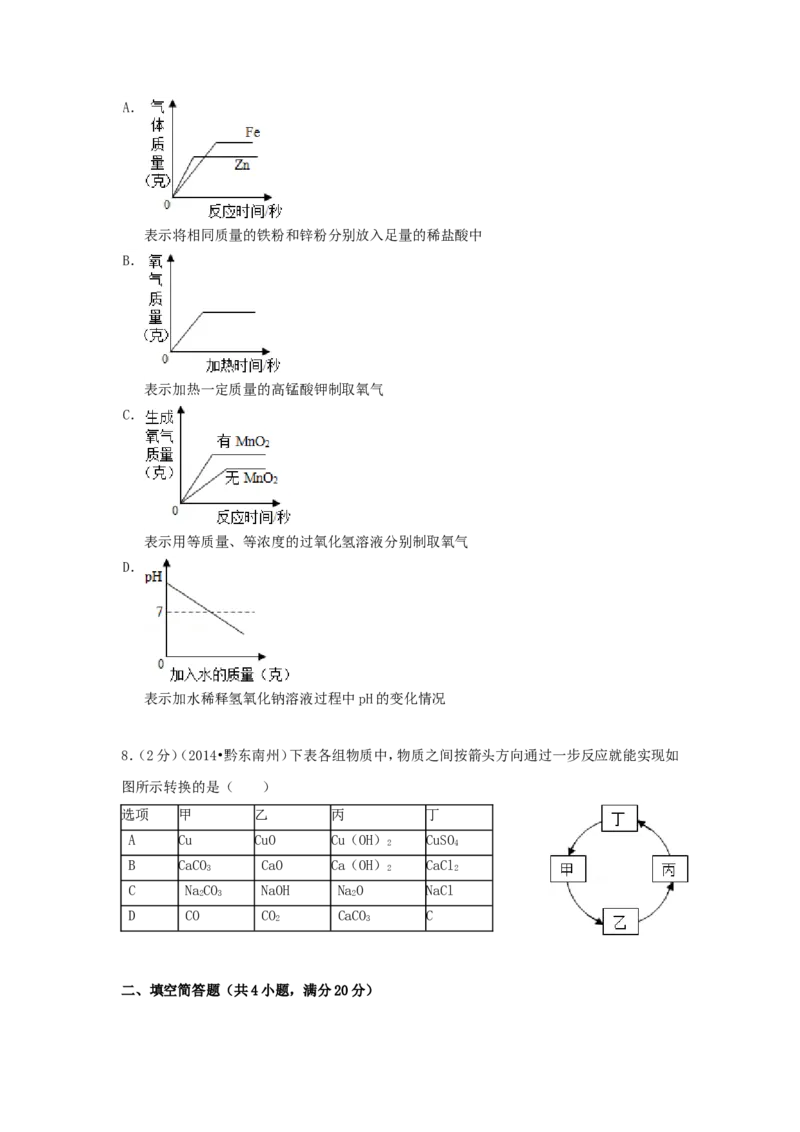
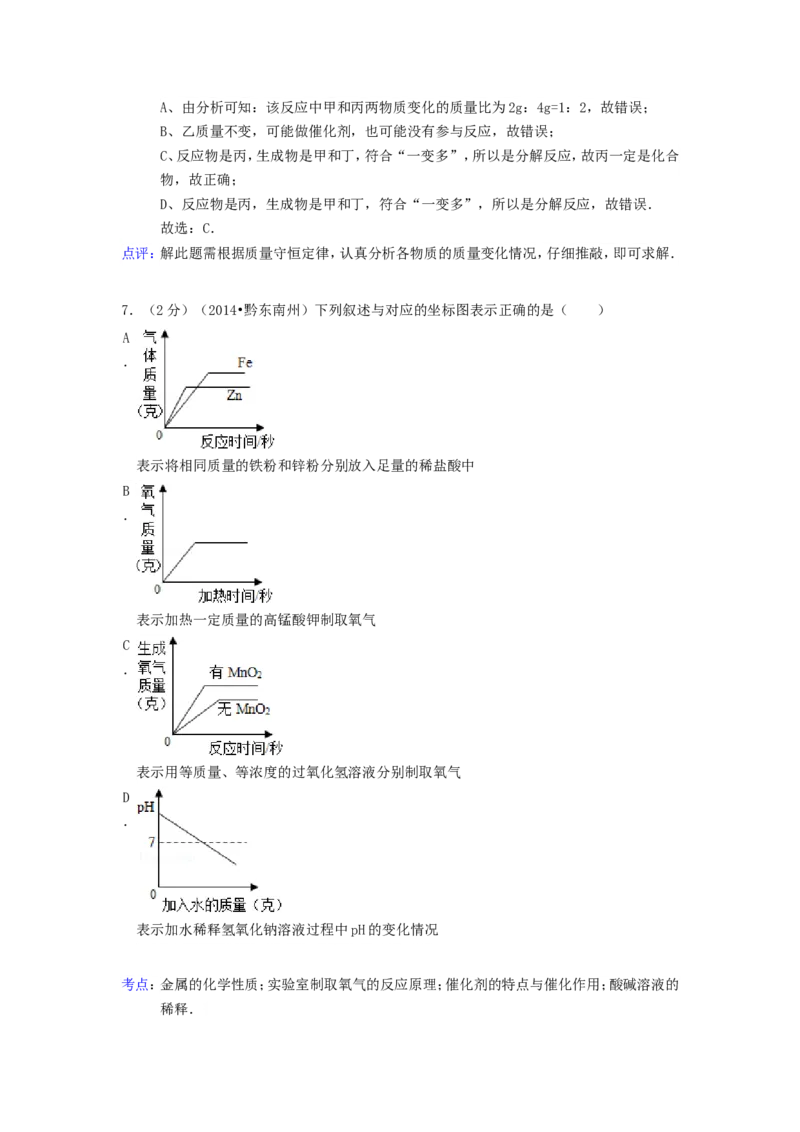
7.(2分)(2014•黔东南州)下列叙述与对应的坐标图表示正确的是( )A.
表示将相同质量的铁粉和锌粉分别放入足量的稀盐酸中
B.
表示加热一定质量的高锰酸钾制取氧气
C.
表示用等质量、等浓度的过氧化氢溶液分别制取氧气
D.
表示加水稀释氢氧化钠溶液过程中pH的变化情况
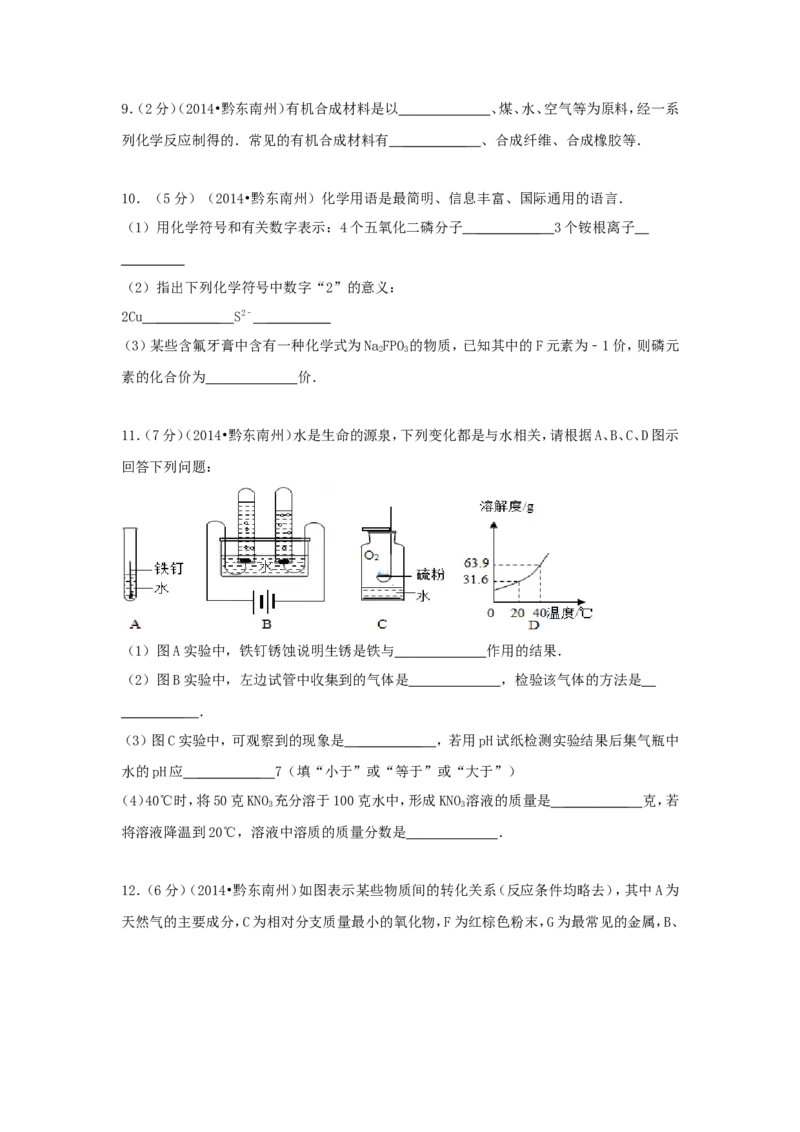
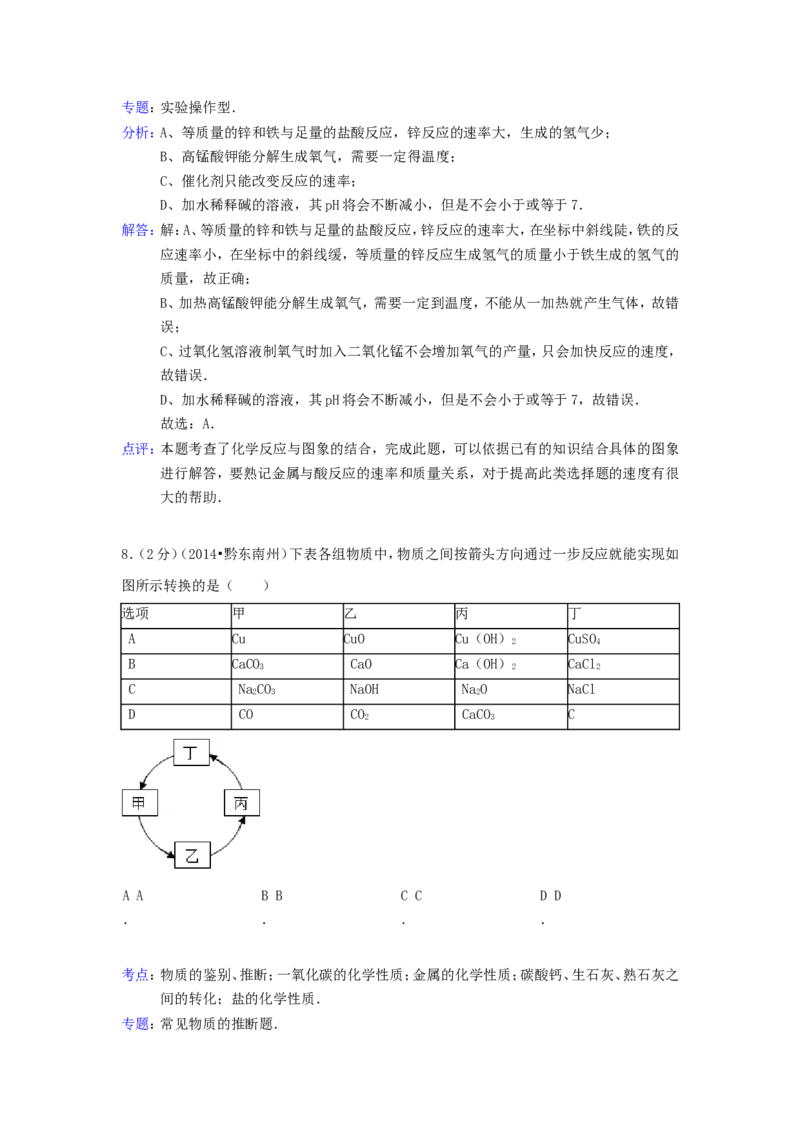
8.(2分)(2014•黔东南州)下表各组物质中,物质之间按箭头方向通过一步反应就能实现如
图所示转换的是( )
选项 甲 乙 丙 丁
A Cu CuO Cu(OH) CuSO
2 4
B CaCO CaO Ca(OH) CaCl
3 2 2
C NaCO NaOH NaO NaCl
2 3 2
D CO CO CaCO C
2 3
二、填空简答题(共4小题,满分20分)9.(2分)(2014•黔东南州)有机合成材料是以 ________ _ 、煤、水、空气等为原料,经一系
列化学反应制得的.常见的有机合成材料有 ________ _ 、合成纤维、合成橡胶等.
10.(5分)(2014•黔东南州)化学用语是最简明、信息丰富、国际通用的语言.
(1)用化学符号和有关数字表示:4个五氧化二磷分子 ________ _ 3个铵根离子
_________
(2)指出下列化学符号中数字“2”的意义:
2Cu ________ _ S2﹣ ________ _
(3)某些含氟牙膏中含有一种化学式为NaFPO 的物质,已知其中的F元素为﹣1价,则磷元
2 3
素的化合价为 ________ _ 价.
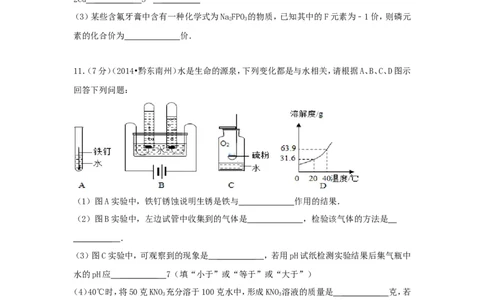
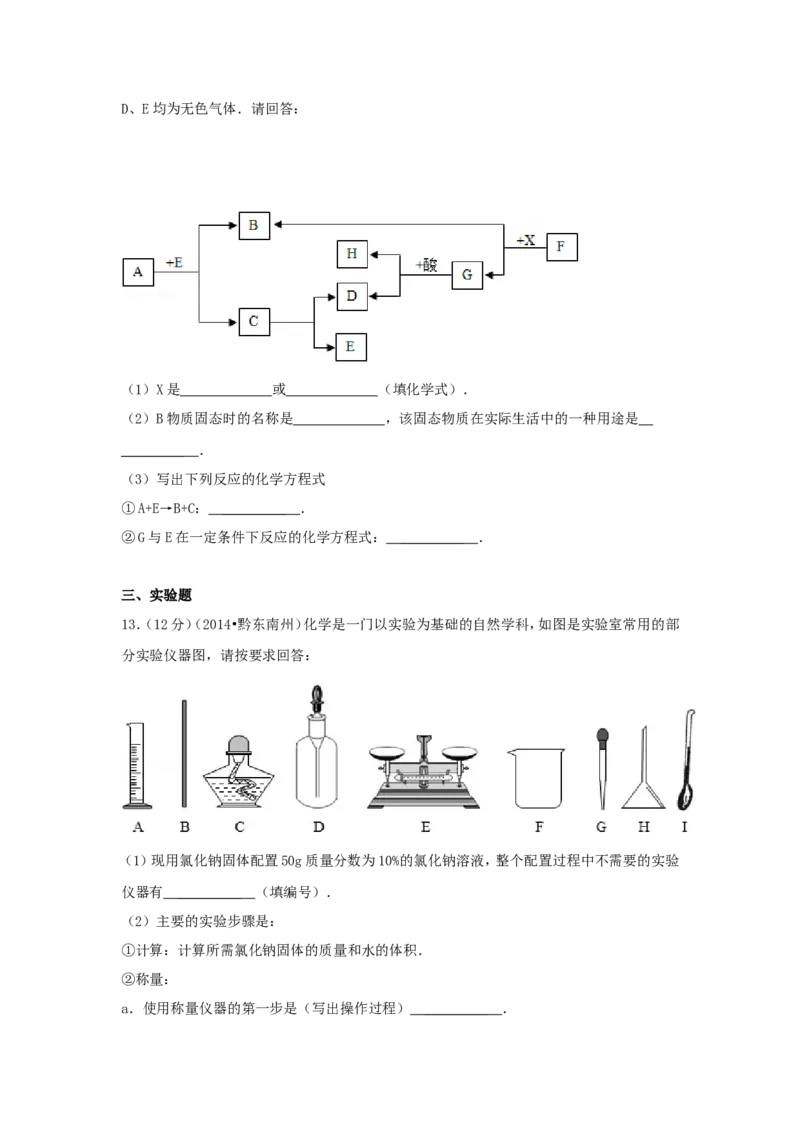
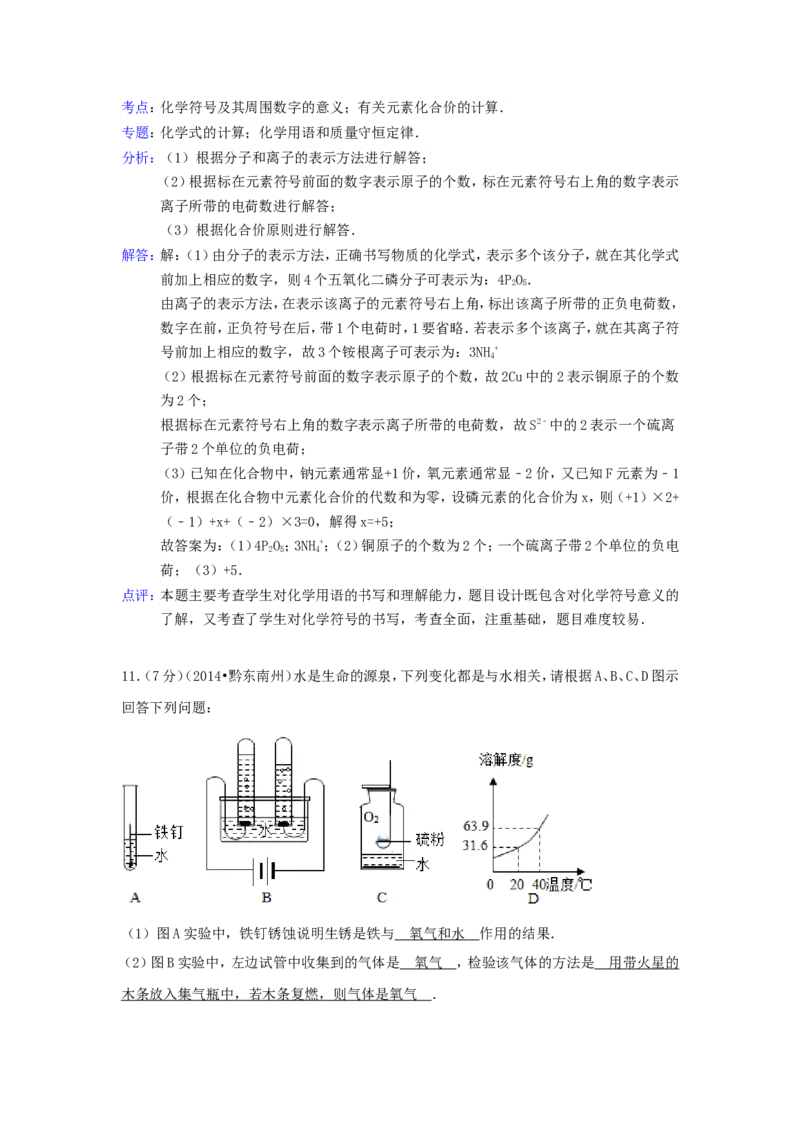
11.(7分)(2014•黔东南州)水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示
回答下列问题:
(1)图A实验中,铁钉锈蚀说明生锈是铁与 ________ _ 作用的结果.
(2)图B实验中,左边试管中收集到的气体是 ________ _ ,检验该气体的方法是
________ _ .
(3)图C实验中,可观察到的现象是 ________ _ ,若用pH试纸检测实验结果后集气瓶中
水的pH应 ________ _ 7(填“小于”或“等于”或“大于”)
(4)40℃时,将50克KNO 充分溶于100克水中,形成KNO 溶液的质量是 ________ _ 克,若
3 3
将溶液降温到20℃,溶液中溶质的质量分数是 ________ _ .
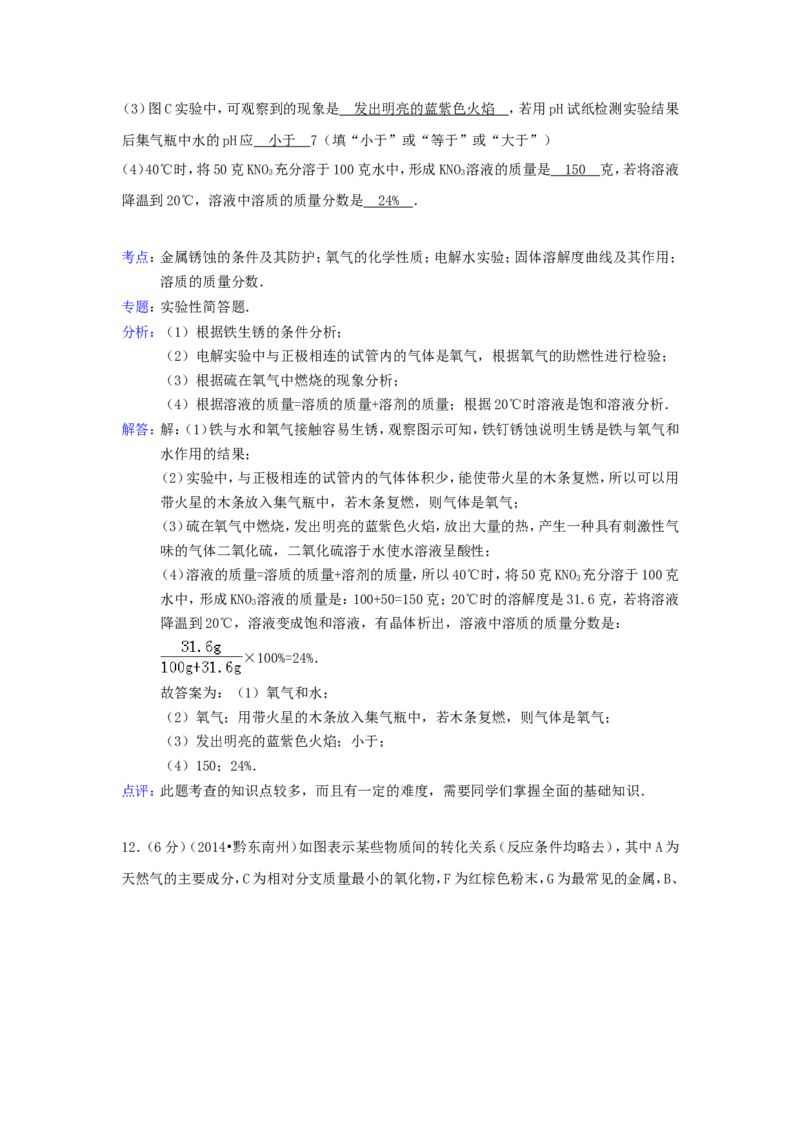
12.(6分)(2014•黔东南州)如图表示某些物质间的转化关系(反应条件均略去),其中A为
天然气的主要成分,C为相对分支质量最小的氧化物,F为红棕色粉末,G为最常见的金属,B、D、E均为无色气体.请回答:
(1)X是 ________ _ 或 ________ _ (填化学式).
(2)B物质固态时的名称是 ________ _ ,该固态物质在实际生活中的一种用途是
________ _ .
(3)写出下列反应的化学方程式
①A+E→B+C: ________ _ .
②G与E在一定条件下反应的化学方程式: ________ _ .
三、实验题
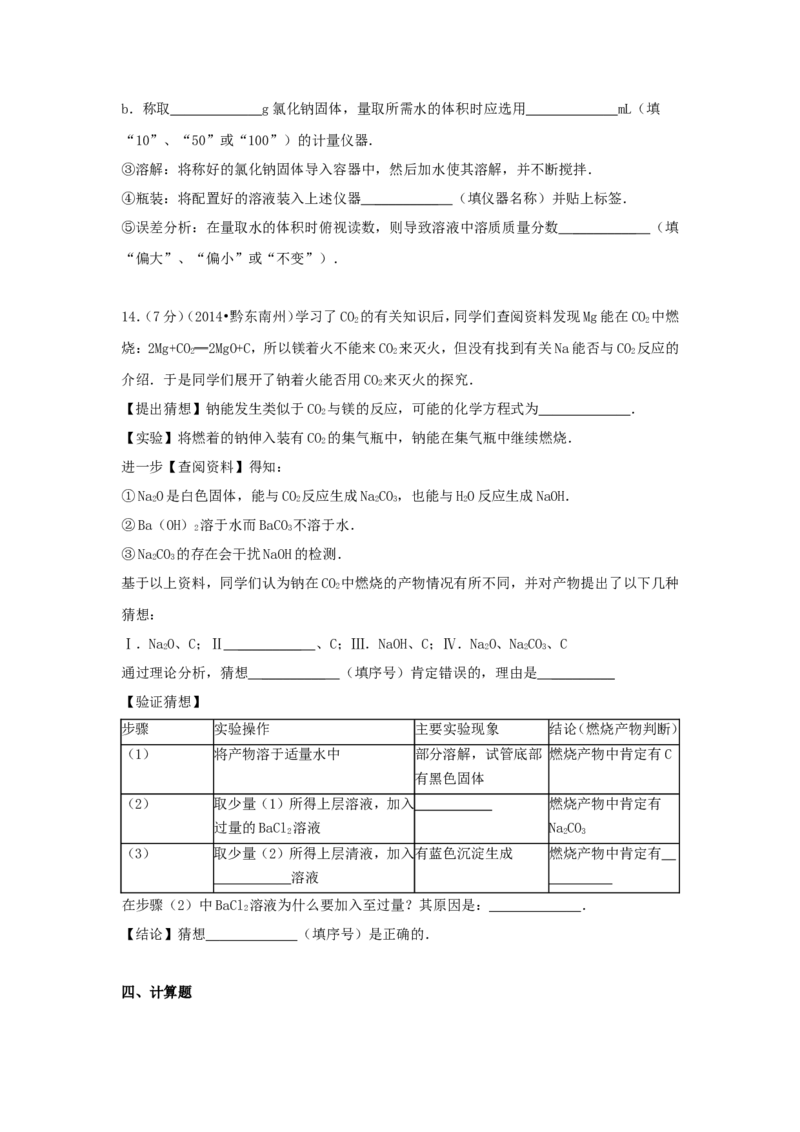
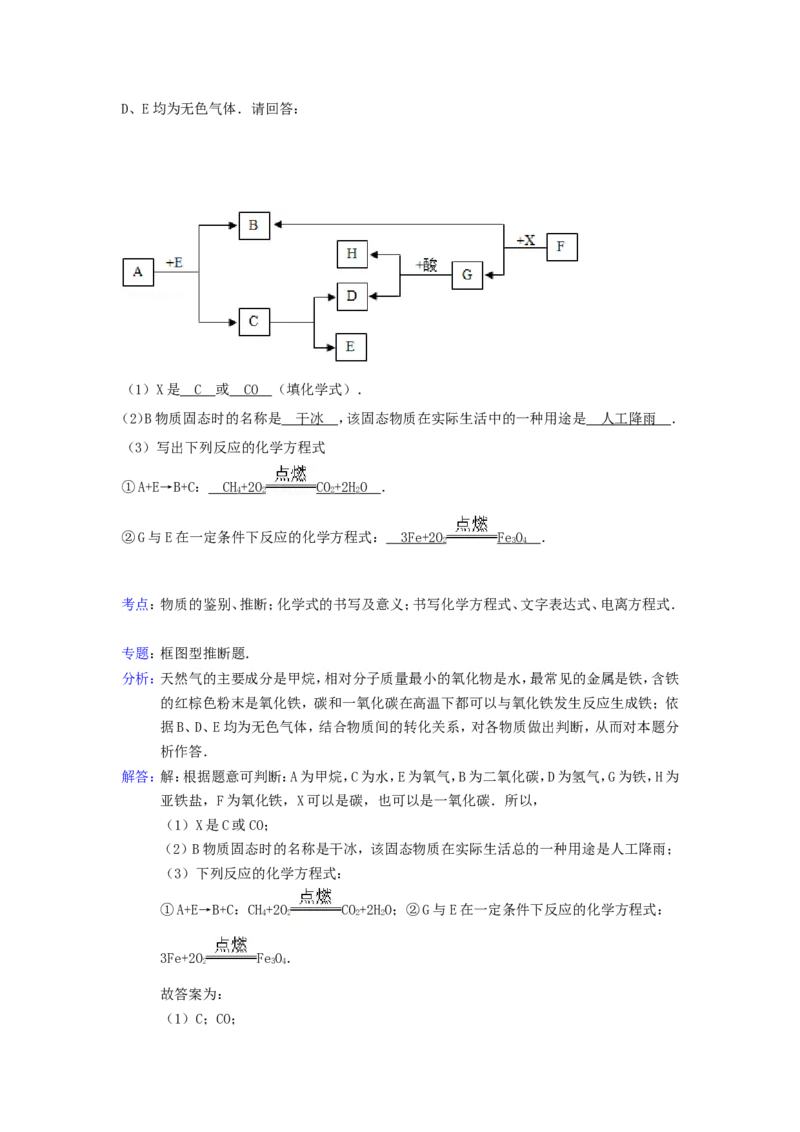
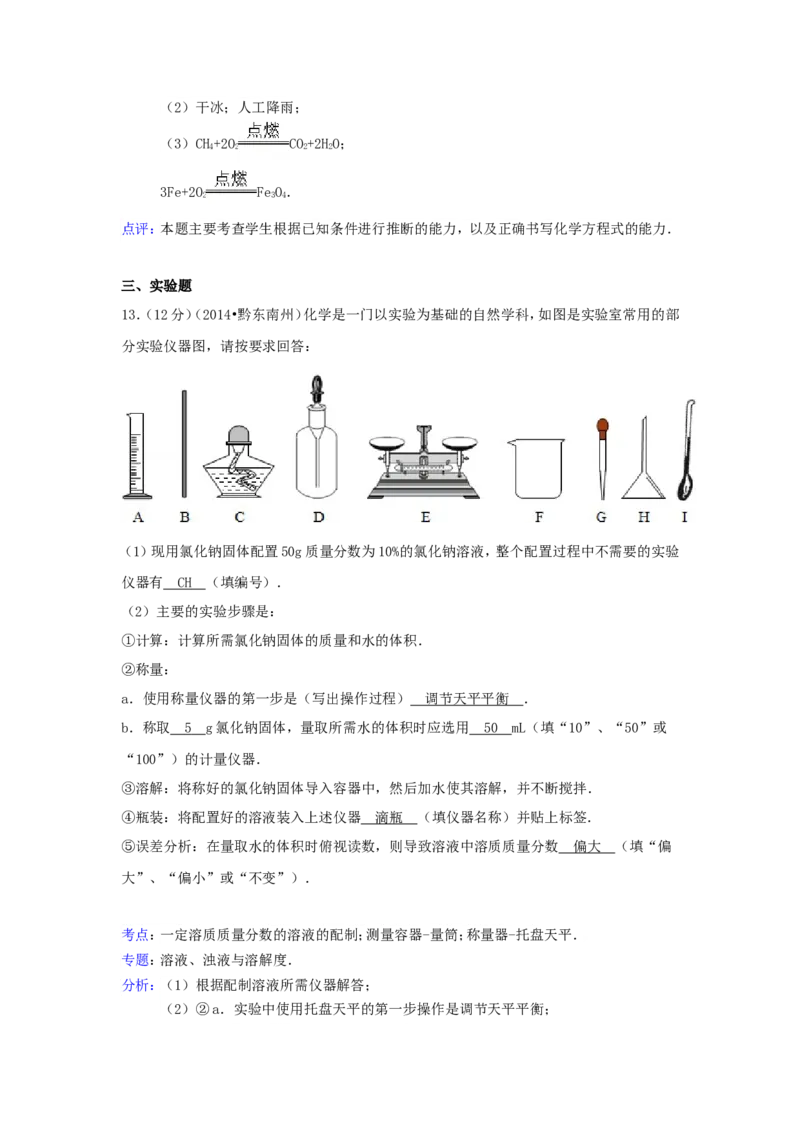
13.(12分)(2014•黔东南州)化学是一门以实验为基础的自然学科,如图是实验室常用的部
分实验仪器图,请按要求回答:
(1)现用氯化钠固体配置50g质量分数为10%的氯化钠溶液,整个配置过程中不需要的实验
仪器有 ________ _ (填编号).
(2)主要的实验步骤是:
①计算:计算所需氯化钠固体的质量和水的体积.
②称量:
a.使用称量仪器的第一步是(写出操作过程) ________ _ .b.称取 ________ _ g氯化钠固体,量取所需水的体积时应选用 ________ _ mL(填
“10”、“50”或“100”)的计量仪器.
③溶解:将称好的氯化钠固体导入容器中,然后加水使其溶解,并不断搅拌.
④瓶装:将配置好的溶液装入上述仪器 ________ _ (填仪器名称)并贴上标签.
⑤误差分析:在量取水的体积时俯视读数,则导致溶液中溶质质量分数 ________ _ (填
“偏大”、“偏小”或“不变”).
14.(7分)(2014•黔东南州)学习了CO 的有关知识后,同学们查阅资料发现Mg能在CO 中燃
2 2
烧:2Mg+CO═2MgO+C,所以镁着火不能来CO 来灭火,但没有找到有关Na能否与CO 反应的
2 2 2
介绍.于是同学们展开了钠着火能否用CO 来灭火的探究.
2
【提出猜想】钠能发生类似于CO 与镁的反应,可能的化学方程式为 ________ _ .
2
【实验】将燃着的钠伸入装有CO 的集气瓶中,钠能在集气瓶中继续燃烧.
2
进一步【查阅资料】得知:
①NaO是白色固体,能与CO 反应生成NaCO,也能与HO反应生成NaOH.
2 2 2 3 2
②Ba(OH) 溶于水而BaCO 不溶于水.
2 3
③NaCO 的存在会干扰NaOH的检测.
2 3
基于以上资料,同学们认为钠在CO 中燃烧的产物情况有所不同,并对产物提出了以下几种
2
猜想:
Ⅰ.NaO、C;Ⅱ ________ _ 、C;Ⅲ.NaOH、C;Ⅳ.NaO、NaCO、C
2 2 2 3
通过理论分析,猜想 ________ _ (填序号)肯定错误的,理由是 ________ _
【验证猜想】
步骤 实验操作 主要实验现象 结论(燃烧产物判断)
(1) 将产物溶于适量水中 部分溶解,试管底部 燃烧产物中肯定有C
有黑色固体
(2) 取少量(1)所得上层溶液,加入 ________ _ 燃烧产物中肯定有
过量的BaCl 溶液 NaCO
2 2 3
(3) 取少量(2)所得上层清液,加入 有蓝色沉淀生成 燃烧产物中肯定有
________ _ 溶液 _________
在步骤(2)中BaCl 溶液为什么要加入至过量?其原因是: ________ _ .
2
【结论】猜想 ________ _ (填序号)是正确的.
四、计算题15.(5分)(2014•黔东南州)欲测定某锌﹣铜合金中铜的质量分数,进行如下实验:取合金样
品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成气体质量/g 0.08 m 0.04
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= ________ _ 克;
(2)计算该合金样品中铜的质量分数.
2014年贵州省黔东南州中考化学试卷
参考答案与试题解析
一、选择题(共8小题,每小题2分,满分16分)
1.(2分)(2014•黔东南州)化学与我们的生活息息相关,下列有关说法中正确的是( )
A 人类需求的不断增加以及对自然资源的过度开发和不恰当使用,造成了温室效应、酸雨、
.赤潮、白色污染、潮汐等环境问题
B 绿色化学是指绿色植物为原料的化学新工艺
.
C 北京等城市雾霾天气是由液态水变成水蒸气导致的结果
.
D 氯氟烃(一种用于冰箱的制冷剂)是破坏臭氧层,导致臭氧层空洞的祸首
.
考点:目前环境污染问题;绿色化学;空气的污染及其危害.菁优网版权所有
专题:化学与环境保护.
分析:A、潮汐属于自然现象;
B、根据绿色化学的定义分析;
C、雾霾天气是环境污染造成的;
D、氯氟烃破坏臭氧层.
解答:解:A、温室效应、酸雨、赤潮、白色污染是不合理的利用资源造成的,但潮汐属于自然
现象,故错误;
B、绿色化学是指无污染、无公害、尽可能地把反应物转化为环保、健康、安全的产品,
并不是绿色植物为原料的化学新工艺,故错误;
C、雾霾天气是环境污染造成的,与水蒸气无关,故错误;D、氯氟烃破坏臭氧层,故正确.
故选D.
点评:环境的污染和保护是社会关注的焦点问题,与之相关的考题就成为考查的重点之一.
2.(2分)(2014•黔东南州)物质发生化学变化常伴随着一些现象,下列需要借助酸碱指示剂
才能观察到化学反应发生的是( )
A B C D
. . . .
考点:酸碱盐的应用;酸的化学性质;碱的化学性质.菁优网版权所有
专题:实验现象的观察和记录.
分析:物质间的反应若有明显的反应现象,如产生沉淀、气体、固体溶解的现象等,则不需要
借助酸碱指示剂就能判断出反应发生;若物质间反应时没有明显现象的可以借助指示
剂,如酸碱的中和反应等.
解答:解:A、氢氧化钠溶液和稀盐酸反应生成氯化钠和水,反应无明显现象,需要借助指示
剂才能判断出反应发生,故选项正确.
B、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色絮状沉淀,现象明显,不需借助
酸碱指示剂就能判断出反应发生,故选项错误.
C、碳酸钠与稀盐酸反应生成有大量气泡产生,现象明显,不需借助酸碱指示剂就能判
断出反应发生,故选项错误.
D、氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,反应后瓶内压强减小,会观察到软
塑料瓶变瘪了,现象明显,不需借助酸碱指示剂就能判断出反应发生,故选项错误.
故选:A.
点评:本题难度不大,掌握酸的化学性质、物质发生化学反应时的现象是正确解答此类题的
关键.
3.(2分)(2014•黔东南州)下列叙述中正确的是( )
A 量取一定体积的液体药品时要用到量筒,药品的状态属于物质的化学性质
.
B 可以用燃着的酒精灯去点燃另一盏酒精灯,酒精燃烧属于化学变化
.
C 稀释浓硫酸时,将浓硫酸慢慢倒入盛有水的烧杯中,并用玻璃棒不断搅拌,稀硫酸属于混
.合物D 实验室制取CO 需要用酒精灯、锥形瓶、分液漏斗、导管、集气瓶等仪器,该反应属于复分
2
.解反应
考点:测量容器-量筒;加热器皿-酒精灯;浓硫酸的性质及浓硫酸的稀释;二氧化碳的实验室
制法;纯净物和混合物的判别;化学变化和物理变化的判别;化学性质与物理性质的差
别及应用;反应类型的判定.菁优网版权所有
专题:物质的变化与性质;化学反应的基本类型和能量变化;物质的分类;常见仪器及化学实
验基本操作.
分析:A、根据液体的量取仪器分析;
B、根据酒精灯的使用分析;
C、根据浓硫酸的稀释分析;
D、根据二氧化碳的制取分析.
解答:解:A、量取一定体积的液体药品时要用到量筒,药品的状态属于物质的物理性质,错
误;
B、不可以用燃着的酒精灯去点燃另一盏酒精灯,应该用火柴引燃,酒精燃烧属于化学
变化,错误;
C、稀释浓硫酸时,将浓硫酸慢慢倒入盛有水的烧杯中,并用玻璃棒不断搅拌,稀硫酸
属于混合物,正确;
D、实验室制取CO 不需要用酒精灯,错误.
2
故选C.
点评:了解化学学习中的仪器使用问题和注意事项,会举出相关的例子,能反驳题目得出正
确结论.
4.(2分)(2014•黔东南州)青少年过多摄入蛋糕里的人造奶油会产生一种影响身体发育的
反式脂肪酸,其化学式为C H O,下列反式脂肪酸的说法中正确的是( )
18 34 2
A 该物质中C、H、O三种元素的质量比为9:17:1
.
B 该物质是由18个碳原子、34个氢原子、2个氧原子构成的
.
C 该物质的相对分子质量为282g
.
D 该物质在空气中完全燃烧的产物只有CO 和HO
2 2
.
考点:化学式的书写及意义;相对分子质量的概念及其计算;元素质量比的计算;质量守恒定
律及其应用.菁优网版权所有
专题:化学用语和质量守恒定律.分析:A.根据物质中元素的质量比来分析;
B.根据物质的构成情况来分析;
C.根据相对分子质量的规定来分析;
D.根据物质的组成和质量守恒定律来分析.
解答:解:A.由反式脂肪酸的化学式C H O 可知,该物质中C、H、O三种元素的质量比为:
18 34 2
(12×18):(1×34):(16×2)=108:17:16,故A错误;
B.反式脂肪酸是由分子构成的,而不是由原子直接构成的,故B错误;
C.相对分子质量的单位不是“g”,而是“1”,通常省略,故C错误;
D.由反式脂肪酸的化学式C H O 可知,该物质中含有碳、氢、氧元素,所以在空气完全
18 34 2
燃烧会生成水和二氧化碳,故D正确.
故选D.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析
问题、解决问题的能力.
5.(2分)(2014•黔东南州)下列有关溶液的说法中正确的是( )
A 常温下将100mL饱和Ca(OH) 溶液加热到50℃,会使溶液由饱和溶液变为不饱和溶液
2
.
B 从浓度为25%的HSO 溶液中取出10mL,则取出的10mL HSO 溶液浓度仍为25%
2 4 2 4
.
C 20℃时,50克水中溶解了18克NaCl,则20℃时NaCl的溶解度为36克
.
D 将95克KCl溶液蒸干得到5克KCl固体,则原溶液中KCl的浓度为5%
.
考点:饱和溶液和不饱和溶液相互转变的方法;溶液的概念、组成及其特点;固体溶解度的概
念;有关溶质质量分数的简单计算.菁优网版权所有
专题:溶液、浊液与溶解度.
分析:A、Ca(OH) 的溶解度随温度的升高而减小;
2
B、根据溶液的“均一、稳定”特点进行分析;
C、溶解度是指在一定温度下,100g溶剂中达到饱和状态所溶解的溶质质量;
D、该题中的溶液的质量是95克,不是100克.
解答:解:A、Ca(OH)的溶解度随温度的升高而减小,因此将饱和Ca(OH)溶液变为不饱和溶
2 2
液的方法为降温,而不是升温,故A说法错误;
B、因为HSO 溶液具有均一性和稳定性,所以从浓度为25%的HSO 溶液中取出10mL,
2 4 2 4
则取出的10mL HSO 溶液浓度仍为25%,故B说法正确;
2 4
C、20℃时,50克水中溶解了18克NaCl,此时的溶液不一定是饱和溶液,所以20℃时
NaCl的溶解度不一定为36克,故C说法错误;D、将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的浓度为: ×100%≈5.26%,
故D说法错误.
故选:B.
点评:熟练掌握饱和溶液和不饱和溶液相互转换方法,溶液的特点以及溶质质量分数的简单
计算是解题的关键.
6.(2分)(2014•黔东南州)将一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定
条件下发生化学反应,一段时间后,测得各物质的质量数据如下
物质 甲 乙 丙 丁
反应前各物质的质 3 2 9 4
量/g
反应后各物质的质 5 2 未知数 6
量/g
下列选项中正确的是( )
A 该反应中甲和丙两物质变化的质量比为1:1
.
B 乙一定是该反应的催化剂
.
C 丙一定是化合物
.
D 该反应一定是化合反应
.
考点:质量守恒定律及其应用;催化剂的特点与催化作用;单质和化合物的判别;反应类型的
判定.菁优网版权所有
专题:化学用语和质量守恒定律.
分析:根据质量守恒定律进行分析,反应后质量增加的是生成物,减少的是反应物.由表格信
息可知反应后甲质量增加了5g﹣3g=2g,是生成物;乙质量不变,可能做催化剂;丙的
未知数为(3g+2g+9g+4g)﹣(5g+2g+6g)=5g,质量减少9g﹣5g=4g,为反应物;丁质量增
加了6g﹣4g=2g,是生成物;参加反应的丙等于生成的甲和丁的质量,所以推断,反应
物是丙,生成物是甲和丁,符合“一变多”,所以是分解反应.
解答:解:根据质量守恒定律进行分析,反应后质量增加的是生成物,减少的是反应物.由表
格信息可知反应后甲质量增加了5g﹣3g=2g,是生成物;乙质量应该不变,可能做催化
剂;丙的未知数为(3g+2g+9g+4g)﹣(5g+2g+6g)=5g,质量减少9g﹣5g=4g,为反应物;
丁质量增加了6g﹣4g=2g,是生成物;参加反应的丙等于生成的甲和丁的质量,所以推
断,反应物是丙,生成物是甲和丁,符合“一变多”,所以是分解反应.A、由分析可知:该反应中甲和丙两物质变化的质量比为2g:4g=1:2,故错误;
B、乙质量不变,可能做催化剂,也可能没有参与反应,故错误;
C、反应物是丙,生成物是甲和丁,符合“一变多”,所以是分解反应,故丙一定是化合
物,故正确;
D、反应物是丙,生成物是甲和丁,符合“一变多”,所以是分解反应,故错误.
故选:C.
点评:解此题需根据质量守恒定律,认真分析各物质的质量变化情况,仔细推敲,即可求解.
7.(2分)(2014•黔东南州)下列叙述与对应的坐标图表示正确的是( )
A
.
表示将相同质量的铁粉和锌粉分别放入足量的稀盐酸中
B
.
表示加热一定质量的高锰酸钾制取氧气
C
.
表示用等质量、等浓度的过氧化氢溶液分别制取氧气
D
.
表示加水稀释氢氧化钠溶液过程中pH的变化情况
考点:金属的化学性质;实验室制取氧气的反应原理;催化剂的特点与催化作用;酸碱溶液的
稀释.菁优网版权所有专题:实验操作型.
分析:A、等质量的锌和铁与足量的盐酸反应,锌反应的速率大,生成的氢气少;
B、高锰酸钾能分解生成氧气,需要一定得温度;
C、催化剂只能改变反应的速率;
D、加水稀释碱的溶液,其pH将会不断减小,但是不会小于或等于7.
解答:解:A、等质量的锌和铁与足量的盐酸反应,锌反应的速率大,在坐标中斜线陡,铁的反
应速率小,在坐标中的斜线缓,等质量的锌反应生成氢气的质量小于铁生成的氢气的
质量,故正确;
B、加热高锰酸钾能分解生成氧气,需要一定到温度,不能从一加热就产生气体,故错
误;
C、过氧化氢溶液制氧气时加入二氧化锰不会增加氧气的产量,只会加快反应的速度,
故错误.
D、加水稀释碱的溶液,其pH将会不断减小,但是不会小于或等于7,故错误.
故选:A.
点评:本题考查了化学反应与图象的结合,完成此题,可以依据已有的知识结合具体的图象
进行解答,要熟记金属与酸反应的速率和质量关系,对于提高此类选择题的速度有很
大的帮助.
8.(2分)(2014•黔东南州)下表各组物质中,物质之间按箭头方向通过一步反应就能实现如
图所示转换的是( )
选项 甲 乙 丙 丁
A Cu CuO Cu(OH) CuSO
2 4
B CaCO CaO Ca(OH) CaCl
3 2 2
C NaCO NaOH NaO NaCl
2 3 2
D CO CO CaCO C
2 3
A A B B C C D D
. . . .
考点:物质的鉴别、推断;一氧化碳的化学性质;金属的化学性质;碳酸钙、生石灰、熟石灰之
间的转化;盐的化学性质.菁优网版权所有
专题:常见物质的推断题.分析:A.CuO 不能一步反应生成Cu(OH);
2
B.CaCO 高温加热分解生成CO 和CaO,CaO与水反应生成Ca(OH),Ca(OH)与HCl反应
3 2 2 2
生成CaCl,CaCl 与NaCO 反应生成CaCO;
2 2 2 3 3
C.NaOH不能一步反应生成NaO;
2
D.CaCO 不能一步反应生成C.
3
解答:解:A.CuO 不能一步反应生成Cu(OH),故A错误;
2
B.CaCO 高温加热分解生成CO 和CaO,CaO与水反应生成Ca(OH),Ca(OH)与HCl反应
3 2 2 2
生成CaCl,
2
CaCl 与NaCO 反应生成CaCO,故B正确;
2 2 3 3
C.NaOH不能一步反应生成NaO,故C错误;
2
D.CaCO 不能一步反应生成C,故D错误.
3
故答案应选:B.
点评:本题属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出
了正确的实验结论.
二、填空简答题(共4小题,满分20分)
9.(2分)(2014•黔东南州)有机合成材料是以 石油 、煤、水、空气等为原料,经一系列化
学反应制得的.常见的有机合成材料有 塑料 、合成纤维、合成橡胶等.
考点:合成材料的使用及其对人和环境的影响.菁优网版权所有
专题:化学与生活.
分析:根据已有的知识进行分析,三大合成材料指的是塑料、合成纤维、合成橡胶.
解答:解:有机合成材料是以石油、煤、水、空气等位原料,经一系列化学反应制得的.常见的
有机合成材料有塑料、合成纤维、合成橡胶等.
故答案为:石油;塑料.
点评:本题考查了材料的类别,完成此题,可以依据已有的知识进行.
10.(5分)(2014•黔东南州)化学用语是最简明、信息丰富、国际通用的语言.
(1)用化学符号和有关数字表示:4个五氧化二磷分子 4 PO 3个铵根离子 3N H+
2 5 4
(2)指出下列化学符号中数字“2”的意义:
2Cu 铜原子的个数为 2 个 S2﹣ 一个硫离子带 2 个单位的负电荷
(3)某些含氟牙膏中含有一种化学式为NaFPO 的物质,已知其中的F元素为﹣1价,则磷元
2 3
素的化合价为 + 5 价.考点:化学符号及其周围数字的意义;有关元素化合价的计算.菁优网版权所有
专题:化学式的计算;化学用语和质量守恒定律.
分析:(1)根据分子和离子的表示方法进行解答;
(2)根据标在元素符号前面的数字表示原子的个数,标在元素符号右上角的数字表示
离子所带的电荷数进行解答;
(3)根据化合价原则进行解答.
解答:解:(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式
前加上相应的数字,则4个五氧化二磷分子可表示为:4PO.
2 5
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,
数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符
号前加上相应的数字,故3个铵根离子可表示为:3NH+
4
(2)根据标在元素符号前面的数字表示原子的个数,故2Cu中的2表示铜原子的个数
为2个;
根据标在元素符号右上角的数字表示离子所带的电荷数,故S2﹣中的2表示一个硫离
子带2个单位的负电荷;
(3)已知在化合物中,钠元素通常显+1价,氧元素通常显﹣2价,又已知F元素为﹣1
价,根据在化合物中元素化合价的代数和为零,设磷元素的化合价为x,则(+1)×2+
(﹣1)+x+(﹣2)×3=0,解得x=+5;
故答案为:(1)4PO;3NH+;(2)铜原子的个数为2个;一个硫离子带2个单位的负电
2 5 4
荷;(3)+5.
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的
了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.
11.(7分)(2014•黔东南州)水是生命的源泉,下列变化都是与水相关,请根据A、B、C、D图示
回答下列问题:
(1)图A实验中,铁钉锈蚀说明生锈是铁与 氧气和水 作用的结果.
(2)图B实验中,左边试管中收集到的气体是 氧气 ,检验该气体的方法是 用带火星的
木条放入集气瓶中,若木条复燃,则气体是氧气 .(3)图C实验中,可观察到的现象是 发出明亮的蓝紫色火焰 ,若用pH试纸检测实验结果
后集气瓶中水的pH应 小于 7(填“小于”或“等于”或“大于”)
(4)40℃时,将50克KNO 充分溶于100克水中,形成KNO 溶液的质量是 15 0 克,若将溶液
3 3
降温到20℃,溶液中溶质的质量分数是 24 % .
考点:金属锈蚀的条件及其防护;氧气的化学性质;电解水实验;固体溶解度曲线及其作用;
溶质的质量分数.菁优网版权所有
专题:实验性简答题.
分析:(1)根据铁生锈的条件分析;
(2)电解实验中与正极相连的试管内的气体是氧气,根据氧气的助燃性进行检验;
(3)根据硫在氧气中燃烧的现象分析;
(4)根据溶液的质量=溶质的质量+溶剂的质量;根据20℃时溶液是饱和溶液分析.
解答:解:(1)铁与水和氧气接触容易生锈,观察图示可知,铁钉锈蚀说明生锈是铁与氧气和
水作用的结果;
(2)实验中,与正极相连的试管内的气体体积少,能使带火星的木条复燃,所以可以用
带火星的木条放入集气瓶中,若木条复燃,则气体是氧气;
(3)硫在氧气中燃烧,发出明亮的蓝紫色火焰,放出大量的热,产生一种具有刺激性气
味的气体二氧化硫,二氧化硫溶于水使水溶液呈酸性;
(4)溶液的质量=溶质的质量+溶剂的质量,所以40℃时,将50克KNO 充分溶于100克
3
水中,形成KNO 溶液的质量是:100+50=150克;20℃时的溶解度是31.6克,若将溶液
3
降温到20℃,溶液变成饱和溶液,有晶体析出,溶液中溶质的质量分数是:
×100%=24%.
故答案为:(1)氧气和水;
(2)氧气;用带火星的木条放入集气瓶中,若木条复燃,则气体是氧气;
(3)发出明亮的蓝紫色火焰;小于;
(4)150;24%.
点评:此题考查的知识点较多,而且有一定的难度,需要同学们掌握全面的基础知识.
12.(6分)(2014•黔东南州)如图表示某些物质间的转化关系(反应条件均略去),其中A为
天然气的主要成分,C为相对分支质量最小的氧化物,F为红棕色粉末,G为最常见的金属,B、D、E均为无色气体.请回答:
(1)X是 C 或 C O (填化学式).
(2)B物质固态时的名称是 干冰 ,该固态物质在实际生活中的一种用途是 人工降雨 .
(3)写出下列反应的化学方程式
①A+E→B+C: C H+2O CO+2H O .
4 2 2 2
②G与E在一定条件下反应的化学方程式: 3Fe+2 O FeO .
2 3 4
考点:物质的鉴别、推断;化学式的书写及意义;书写化学方程式、文字表达式、电离方程式.
菁优网版权所有
专题:框图型推断题.
分析:天然气的主要成分是甲烷,相对分子质量最小的氧化物是水,最常见的金属是铁,含铁
的红棕色粉末是氧化铁,碳和一氧化碳在高温下都可以与氧化铁发生反应生成铁;依
据B、D、E均为无色气体,结合物质间的转化关系,对各物质做出判断,从而对本题分
析作答.
解答:解:根据题意可判断:A为甲烷,C为水,E为氧气,B为二氧化碳,D为氢气,G为铁,H为
亚铁盐,F为氧化铁,X可以是碳,也可以是一氧化碳.所以,
(1)X是C或CO;
(2)B物质固态时的名称是干冰,该固态物质在实际生活总的一种用途是人工降雨;
(3)下列反应的化学方程式:
①A+E→B+C:CH+2O CO+2HO;②G与E在一定条件下反应的化学方程式:
4 2 2 2
3Fe+2O FeO.
2 3 4
故答案为:
(1)C;CO;(2)干冰;人工降雨;
(3)CH+2O CO+2HO;
4 2 2 2
3Fe+2O FeO.
2 3 4
点评:本题主要考查学生根据已知条件进行推断的能力,以及正确书写化学方程式的能力.
三、实验题
13.(12分)(2014•黔东南州)化学是一门以实验为基础的自然学科,如图是实验室常用的部
分实验仪器图,请按要求回答:
(1)现用氯化钠固体配置50g质量分数为10%的氯化钠溶液,整个配置过程中不需要的实验
仪器有 C H (填编号).
(2)主要的实验步骤是:
①计算:计算所需氯化钠固体的质量和水的体积.
②称量:
a.使用称量仪器的第一步是(写出操作过程) 调节天平平衡 .
b.称取 5 g氯化钠固体,量取所需水的体积时应选用 5 0 mL(填“10”、“50”或
“100”)的计量仪器.
③溶解:将称好的氯化钠固体导入容器中,然后加水使其溶解,并不断搅拌.
④瓶装:将配置好的溶液装入上述仪器 滴瓶 (填仪器名称)并贴上标签.
⑤误差分析:在量取水的体积时俯视读数,则导致溶液中溶质质量分数 偏大 (填“偏
大”、“偏小”或“不变”).
考点:一定溶质质量分数的溶液的配制;测量容器-量筒;称量器-托盘天平.菁优网版权所有
专题:溶液、浊液与溶解度.
分析:(1)根据配制溶液所需仪器解答;
(2)②a.实验中使用托盘天平的第一步操作是调节天平平衡;b.根据溶质质量=溶液质量×溶质质量分数解答;
④配置好的溶液装入细口试剂瓶;
⑤在量取水的体积时俯视读数,造成量取的水偏少,导致溶液中溶质质量分数偏大;
解答:解:(1)现用氯化钠固体配置50g质量分数为10%的氯化钠溶液,整个配置过程中需要
的实验仪器有量筒、天平、玻璃棒、烧杯、滴管、药匙、细口试剂瓶;图中不需要的仪器
是:酒精灯、漏斗;
(2)a.实验中使用托盘天平的第一步操作是调节天平平衡;
b.配置50g质量分数为10%的氯化钠溶液需要氯化钠的质量是:50g×10%=5g,需水的
体积是: =45mL;故需选择与量程最接近的量筒50mL来量取;
④配置好的溶液装入细口试剂瓶,需选择图中的滴瓶;
⑤在量取水的体积时俯视读数,造成量取的水偏少,导致溶液中溶质质量分数偏大;
答案:(1)CH;
(2)a.调节天平平衡;
b.5,50;
④滴瓶;
⑤偏大.
点评:要熟练掌握配置溶液的基本步骤:计算、称量、溶解的基本操作,初步掌握和溶液相关
的计算.
14.(7分)(2014•黔东南州)学习了CO 的有关知识后,同学们查阅资料发现Mg能在CO 中燃
2 2
烧:2Mg+CO═2MgO+C,所以镁着火不能来CO 来灭火,但没有找到有关Na能否与CO 反应的
2 2 2
介绍.于是同学们展开了钠着火能否用CO 来灭火的探究.
2
【提出猜想】钠能发生类似于CO 与镁的反应,可能的化学方程式为 4Na+C O 2NaO+C
2 2 2
.
【实验】将燃着的钠伸入装有CO 的集气瓶中,钠能在集气瓶中继续燃烧.
2
进一步【查阅资料】得知:
①NaO是白色固体,能与CO 反应生成NaCO,也能与HO反应生成NaOH.
2 2 2 3 2
②Ba(OH) 溶于水而BaCO 不溶于水.
2 3
③NaCO 的存在会干扰NaOH的检测.
2 3
基于以上资料,同学们认为钠在CO 中燃烧的产物情况有所不同,并对产物提出了以下几种
2
猜想:
Ⅰ.NaO、C;Ⅱ N aCO 、C;Ⅲ.NaOH、C;Ⅳ.NaO、NaCO、C
2 2 3 2 2 3通过理论分析,猜想 Ⅲ (填序号)肯定错误的,理由是 NaO H 中有氢元素而反应物中没有
氢元素,根据质量守恒定律可知Ⅲ错误
【验证猜想】
步骤 实验操作 主要实验现象 结论(燃烧产物
判断)
(1) 将产物溶于适量水中 部分溶解,试管底部燃烧产物中肯定
有黑色固体 有C
(2) 取少量(1)所得上层溶液,加入过量的 有白色沉淀生成 燃烧产物中肯定
BaCl 溶液 有NaCO
2 2 3
(3) 取少量(2)所得上层清液,加入 有蓝色沉淀生成 燃烧产物中肯定
CuSO (或 CuC l) 溶液 有 N aO
4 2 2
在步骤(2)中BaCl 溶液为什么要加入至过量?其原因是: 完全除去 N aCO ,以免 N aCO 干
2 2 3 2 3
扰 NaO H 的检验 .
【结论】猜想 Ⅳ (填序号)是正确的.
考点:实验探究物质的组成成分以及含量;碱的化学性质;盐的化学性质;书写化学方程式、
文字表达式、电离方程式.菁优网版权所有
专题:科学探究.
分析:【提出猜想】钠能发生类似于CO 与镁的反应,用类比的方法可书写其发生的化学方程
2
式;
【实验】根据资料,同学们认为钠在CO 中燃烧的产物应该与Mg在CO 中燃烧的产物情
2 2
况有所不同,并对产物提出几种猜想;通过质量守恒定律可知分析,猜想Ⅲ肯定是错误
的;
【验证猜想】
由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,推测操作.了
解在步骤(2)中BaCl 溶液为什么要加入至过量的原因.
2
【结论】由猜想得结论.
解答:解:【提出猜想】钠能发生类似于CO 与镁的反应,故可用类比的方法书写其发生的化
2
学方程式为:4Na+CO 2NaO+C.
2 2
【实验】将燃着的钠伸入装有CO 的集气瓶中,钠能在CO 中继续燃烧.
2 2
进一步查阅资料得知:①NaO是白色固体,能与CO 反应生成NaCO,与HO反应生成
2 2 2 3 2
NaOH.②Ba(OH)溶于水而BaCO 不溶于水.③NaCO 的存在会干扰NaOH的检测.基于
2 3 2 3
以上资料,同学们认为钠在CO 中燃烧的产物应该与Mg在CO 中燃烧的产物情况有所
2 2
不同,并对产物提出了以下几种猜想:ⅠNaO、C;ⅡNaCO、C;ⅢNaOH、C;ⅣNaO、
2 2 3 2
NaCO、C;
2 3
通过理论分析,猜想:Ⅲ肯定是错误的,理由是:NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知Ⅲ错误.
【验证猜想】由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,
推测操作:故
步骤 实验操作 主要实验现象结论(燃烧产物判断)
(1) 将产物溶于适量水中 部分溶解,试燃烧产物中肯定有C
管 (炭)
底部有黑色固
体
(2) 取(1)所得少量上层清液,加入过量的有白色沉淀生燃烧产物中肯定有
BaCl 溶液 成 NaCO
2 2 3
(3) 取(2)所得少量上层清液,加入 CuSO有蓝色沉淀生燃烧产物中肯定有
4
(或CuCl)溶液 成 NaO
2 2
在步骤(2)中BaCl 溶液要加入至过量,目的是完全除去NaCO,以免NaCO 干扰NaOH
2 2 3 2 3
的检验.
【结论】通过实验验证可知猜想Ⅳ正确.
故答案为:【提出猜想】4Na+CO 2NaO+C;
2 2
【实验】NaCO;Ⅲ;NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知Ⅲ
2 3
错误;
【验证猜想】
步骤 实验操作 主要实验现象 结论(燃烧产物判断)
(1)
(2) 有白色沉淀生成
(3) CuSO(或CuCl) NaO
4 2 2
完全除去NaCO,以免NaCO 干扰NaOH的检验;
2 3 2 3
【结论】Ⅳ.
点评:掌握质量守恒定律的也是守恒的思想处理问题;了解物质的鉴别与推断的方法.
四、计算题
15.(5分)(2014•黔东南州)欲测定某锌﹣铜合金中铜的质量分数,进行如下实验:取合金样
品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成气体质量/g 0.08 m 0.04
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= 0.0 8 克;(2)计算该合金样品中铜的质量分数.
考点:根据化学反应方程式的计算.菁优网版权所有
专题:综合计算(图像型、表格型、情景型计算题).
分析:(1)分析题中三次数据可以知道,第三次加入稀硫酸后仍然生成气体,所以可以判断
第二次生成气体的质量为0.08g,可以据此解答;
(2)根据生成气体的质量结合反应的化学方程式可以计算出锌的质量,然后求出铜的
质量分数即可.
解答:解:(1)分析题中三次数据可以知道,第三次加入稀硫酸后仍然生成气体,所以可以判
断第二次生成气体的质量为0.08g;
(2)由题意可以知道10g合金与酸反应生成气体的质量为:0.08g+0.08g+0.04g=0.2g
设锌的质量为x
Zn+HSO═ZnSO+H↑
2 4 4 2
65 2
x 0.2g
=
解得:x=6.5g
该合金样品中铜的质量分数为: ×100%=35%
答:该合金样品中铜的质量分为35%.
点评:本考点考查了表格型计算题,属于质量分数和化学方程式的综合应用,是中考计算题
中经常出现的题型.做题时要注意:化学方程式要写正确.本考点主要出现在计算题
中.