文档内容
2015 浙江省台州市中考化学真题
一、选择题(本题有15小题,每小题4分,共60分.请选出一个符合题意的正确选项,不选、
多选、错选均不给分)
1.(4分)(2015•台州)科学实验必须按规范进行操作,下列实验操作中规范的是( )
A. B. C. D.
取少量氯化钠
闻药品气味
稀释浓硫酸
滴加液体
2.(4分)(2015•台州)下列变化中属于物理变化的是( )
A. 氢气燃烧 B. 菜刀生锈 C. 冰雪熔化 D. 电解水
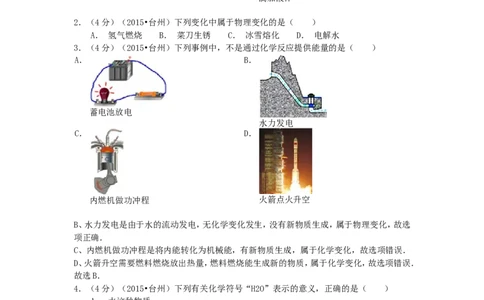
3.(4分)(2015•台州)下列事例中,不是通过化学反应提供能量的是( )
A. B.
蓄电池放电
水力发电
C. D.
内燃机做功冲程 火箭点火升空
B、水力发电是由于水的流动发电,无化学变化发生,没有新物质生成,属于物理变化,故选
项正确.
C、内燃机做功冲程是将内能转化为机械能,有新物质生成,属于化学变化,故选项错误.
D、火箭升空需要燃料燃烧放出热量,燃料燃烧能生成新的物质,属于化学变化,故选项错误.
故选B.
4.(4分)(2015•台州)下列有关化学符号“H2O”表示的意义,正确的是( )
A. 水这种物质
B. 水由氢原子和氧原子构成
C. 一个水分子中含有一个氢分子
D. 水由两个氢元素和一个氧元素组成
B、水是由水分子构成的,水分子是由氢原子和氧原子构成,故选项说法错误.
C、分子是由原子构成的,一个水分子中含有2个氢原子,不含氢分子,故选项说法错误.
D、元素只讲种类、不讲个数,故选项说法错误.故选:A.
C、湿衣服摊开比堆着的表面积大,据此进行分析判断.
D、根据氧气能支持燃烧,不具有可燃性,进行分析判断.解:A、氢气能还原氧化铜,氢气夺取了氧化铜的氧,说明其具有还原性,故选项说法正
确.
B、常温下氯酸钾能溶于水而难溶于酒精,说明氯酸钾的溶解性跟溶剂有关,故选项说法正确.
C、相同条件下,湿衣服摊开比堆着干得快,说明水蒸发快慢与水的表面积有关,故选项说法
正确.
D、铁丝能在氧气中剧烈燃烧,说明铁丝具有可燃性,但氧气能支持燃烧,不具有可燃性,故
选项说法错误.故选:D.
二、填空题(本题有3小题,7空格,每空格2分,共14分)
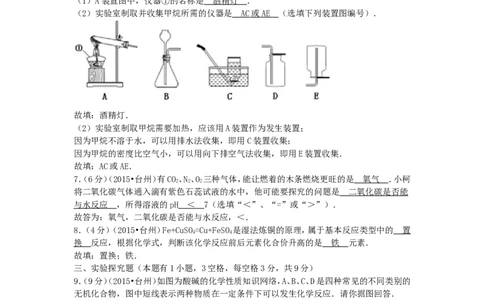
6.(4分)(2015•台州)实验室用加热无水醋酸钠和碱石灰固体混合物制取甲烷.标准状况下,
甲烷密度比空气密度小,难溶于水.
(1)A装置图中,仪器①的名称是 酒精灯 .
(2)实验室制取并收集甲烷所需的仪器是 A C 或 A E (选填下列装置图编号).
故填:酒精灯.
(2)实验室制取甲烷需要加热,应该用A装置作为发生装置;
因为甲烷不溶于水,可以用排水法收集,即用C装置收集;
因为甲烷的密度比空气小,可以用向下排空气法收集,即用E装置收集.
故填:AC或AE.
7.(6分)(2015•台州)有CO、N、O 三种气体,能让燃着的木条燃烧更旺的是 氧气 .小柯
2 2 2
将二氧化碳气体通入滴有紫色石蕊试液的水中,他可能要探究的问题是 二氧化碳是否能
与水反应 ,所得溶液的pH < 7(选填“<”、“=”或“>”).
故答为:氧气,二氧化碳是否能与水反应,<.
8.(4分)(2015•台州)Fe+CuSO=Cu+FeSO 是湿法炼铜的原理,属于基本反应类型中的 置
4 4
换 反应,根据化学式,判断该化学反应前后元素化合价升高的是 铁 元素.
故填:置换;铁.
三、实验探究题(本题有1小题,3空格,每空格3分,共9分)
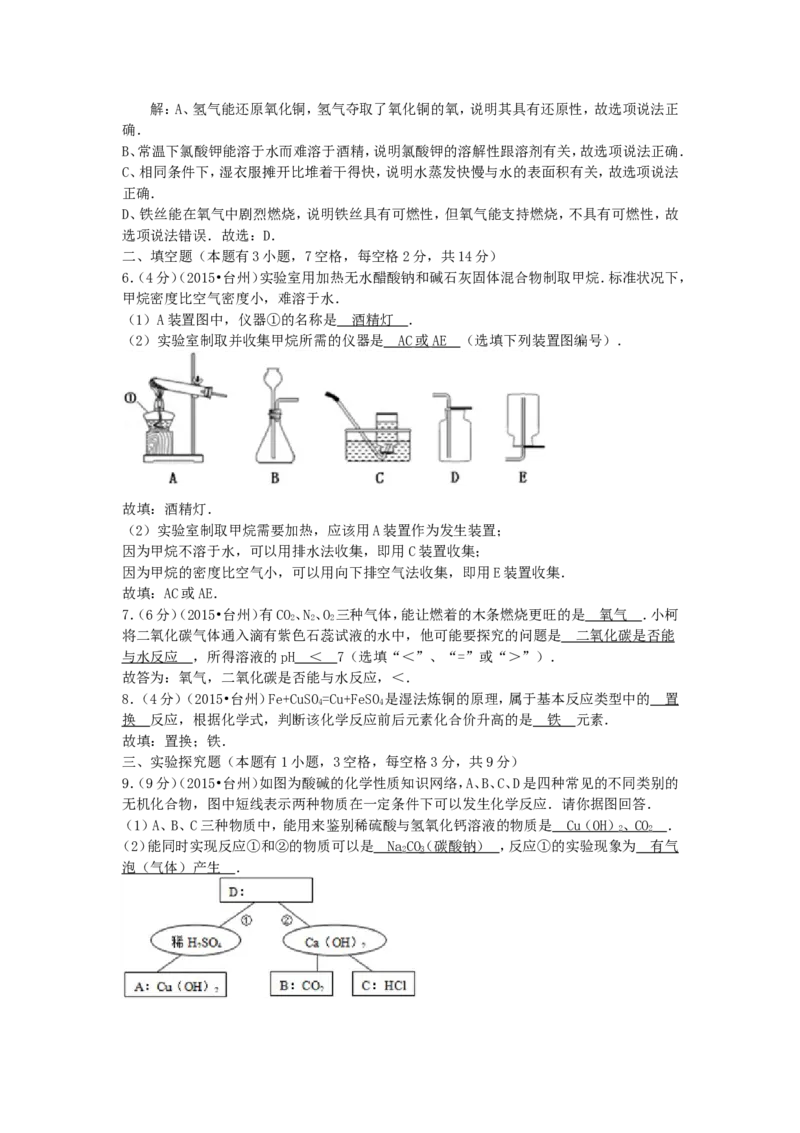
9.(9分)(2015•台州)如图为酸碱的化学性质知识网络,A、B、C、D是四种常见的不同类别的
无机化合物,图中短线表示两种物质在一定条件下可以发生化学反应.请你据图回答.
(1)A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是 C u( O H ) 、 C O .
2 2
(2)能同时实现反应①和②的物质可以是 N aCO(碳酸钠) ,反应①的实验现象为 有气
2 3
泡(气体)产生 .(2)碳酸钠既可与稀硫酸反应又可与氢氧化钙溶液反应,所以能同时实现反应①和②的物质
可以是:NaCO(碳酸钠);碳酸钠与稀硫酸反应会生成二氧化碳气体,所以反应①的实验现
2 3
象为:有气泡(气体)产生.
故本题答案为:
(1)Cu(OH)、CO.
2 2
(2)NaCO(碳酸钠); 有气泡(气体)产生.
2 3
四、解答题(本题有2小题,各8分,共16分)
10.(8分)(2015•台州)铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗
淡,故又称假银箔.
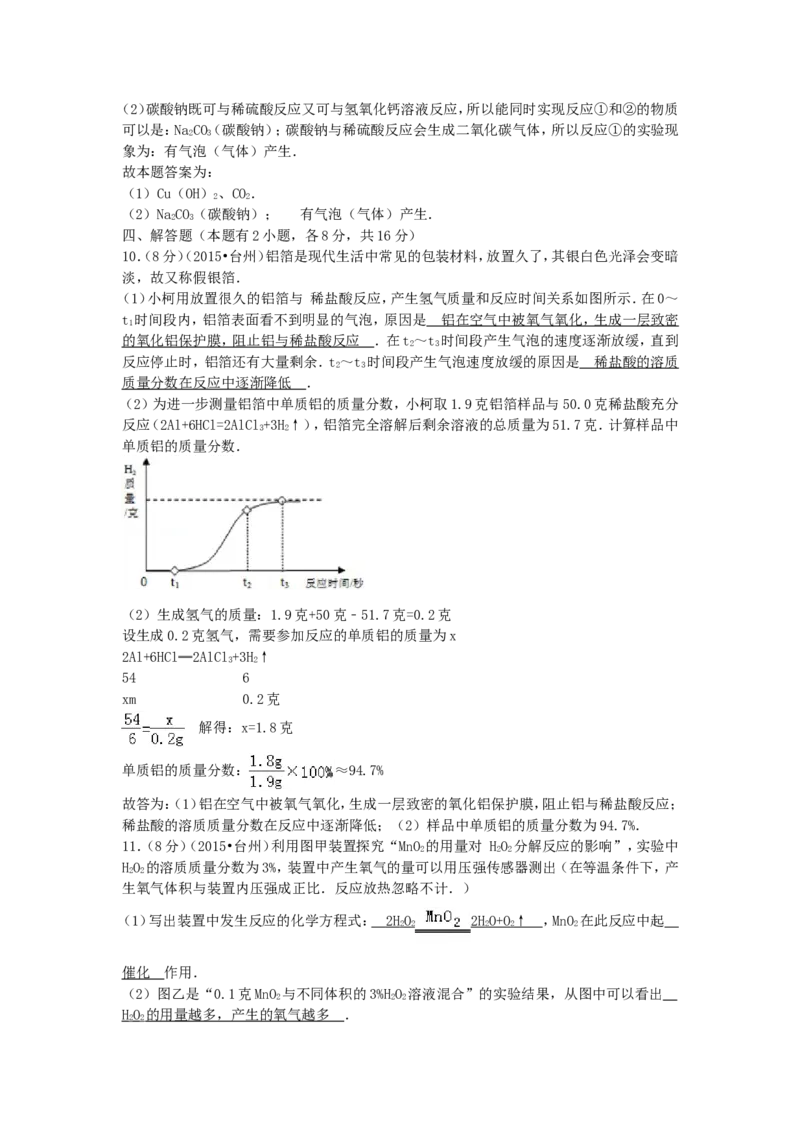
(1)小柯用放置很久的铝箔与 稀盐酸反应,产生氢气质量和反应时间关系如图所示.在0~
t 时间段内,铝箔表面看不到明显的气泡,原因是 铝在空气中被氧气氧化,生成一层致密
1
的氧化铝保护膜,阻止铝与稀盐酸反应 .在t~t 时间段产生气泡的速度逐渐放缓,直到
2 3
反应停止时,铝箔还有大量剩余.t~t 时间段产生气泡速度放缓的原因是 稀盐酸的溶质
2 3
质量分数在反应中逐渐降低 .
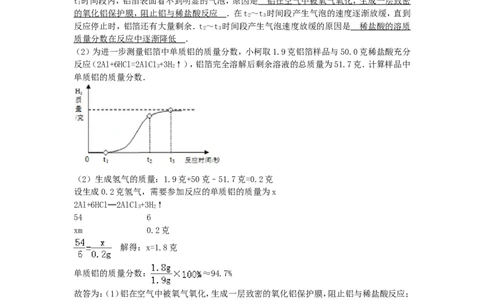
(2)为进一步测量铝箔中单质铝的质量分数,小柯取1.9克铝箔样品与50.0克稀盐酸充分
反应(2Al+6HCl=2AlCl+3H↑),铝箔完全溶解后剩余溶液的总质量为51.7克.计算样品中
3 2
单质铝的质量分数.
(2)生成氢气的质量:1.9克+50克﹣51.7克=0.2克
设生成0.2克氢气,需要参加反应的单质铝的质量为x
2Al+6HCl═2AlCl+3H↑
3 2
54 6
xm 0.2克
解得:x=1.8克
单质铝的质量分数: ≈94.7%
故答为:(1)铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,阻止铝与稀盐酸反应;
稀盐酸的溶质质量分数在反应中逐渐降低;(2)样品中单质铝的质量分数为94.7%.
11.(8分)(2015•台州)利用图甲装置探究“MnO 的用量对 HO 分解反应的影响”,实验中
2 2 2
HO 的溶质质量分数为3%,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产
2 2
生氧气体积与装置内压强成正比.反应放热忽略不计.)
(1)写出装置中发生反应的化学方程式: 2 HO 2HO+O↑ ,MnO 在此反应中起
2 2 2 2 2
催化 作用.
(2)图乙是“0.1克MnO 与不同体积的3%HO 溶液混合”的实验结果,从图中可以看出
2 2 2
HO 的用量越多,产生的氧气越多 .
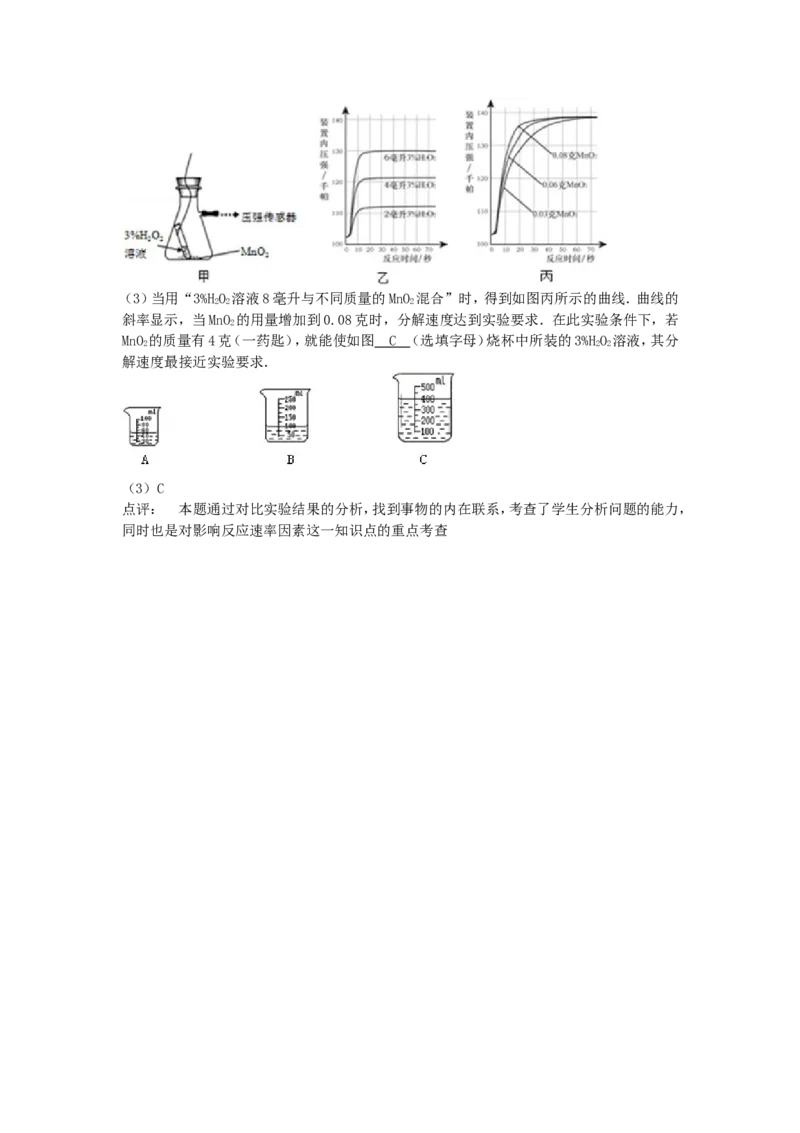
2 2(3)当用“3%HO 溶液8毫升与不同质量的MnO 混合”时,得到如图丙所示的曲线.曲线的
2 2 2
斜率显示,当MnO 的用量增加到0.08克时,分解速度达到实验要求.在此实验条件下,若
2
MnO 的质量有4克(一药匙),就能使如图 C (选填字母)烧杯中所装的3%HO 溶液,其分
2 2 2
解速度最接近实验要求.
(3)C
点评: 本题通过对比实验结果的分析,找到事物的内在联系,考查了学生分析问题的能力,
同时也是对影响反应速率因素这一知识点的重点考查