文档内容
2017 年湖南省衡阳市中考化学真题及答案
可能要用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 Al 27 S 32 Ca 40 Cu 64 Zn 65 Ag
108
一、选择题(每小题只有一个正确答案,每小题2分,共46分)
1、(2017衡阳)下列变化中,不属于化学变化的是( )。A.铁钉生锈 B.水的沸腾 C.纸张燃烧 D.食
物腐败
2、(2017衡阳)下列实验操作错误的是( )。
100ml
A、滴加液体 B、检查气密性 C、加热液体 D、量取9.5ml液体
3、(2017衡阳)栀子花开,淡淡的清香。香满校园的原因是( )。
A.分子是由原子构成的 B.分子的质量和体积都很小 C.分子在不停的运动 D.分子之间有间隔
4、(2017衡阳)天宫二号是我国首个真正意义上的空间实验室。在太空舱里,常用NiFe O 作催化剂将宇航员
2 4
呼出的CO 转化为O,已知NiFe O 中Ni为+2价,则Fe的化合价为( )。A.+1 B.+2 C.+3 D.+4
2 2 2 4
5、(2017衡阳)如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间
的结合.下列说法中错误的是( )。A、该反应属于置换反应 B、该反应前后分子个数不变
C、该反应中有三种元素参与 D、该反应的生成物均为化合物
6、(2017衡阳)下列有关实验现象的描述,错误的是( )。
A、细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B、分别点燃一小块棉纤维和羊毛纤维,都产生烧焦羽毛的气味
C、红磷在空气中燃烧,产生大量白烟 D.一氧化碳高温还原氧化铁时,红棕色粉末逐渐变成黑色
7、(2017衡阳)下列化学方程式符合题意且书写正确的是( )。A、正常的雨水略呈酸性的原因:CO +
2
HO==HCO
2 2 3
B、生活中用天然气作燃料:CHOH + 3O 点 燃 2CO + 3HO
2 5 2 2 2
C、胃舒平(含氢氧化铝)治疗胃酸过多症:Al(OH) + HCl == AlC + HO
3 l3 2
D、用大理石和盐酸制取二氧化碳:CaCO + 2HCl == CaCl + HO + CO
3 2 2 2
8、(2017衡阳)下列有关溶液的叙述正确的是( )。A.凡是均一稳定的液体一定是溶液 B.不饱和溶液一
定是稀溶液
C、增加溶质可使不饱和溶液变成饱和溶液 D、可溶性物质溶于水时一定会放出热量
9、(2017衡阳)“雾霾”、“灰霾”、PM2.5已成电视新闻熟词,下列做法不符合“环境友好”的是
( )。
A、使用清洁能源,减少煤的燃烧 B、减少交通压力,提倡私家车出行
C、种植沙漠防护林,减少沙尘暴 D、综合利用秸秆,严禁露天焚烧
10、(2017衡阳)下列常见生活物品中所含的主要材料属于有机合成材料的是( )。
A、橡胶轮胎 B、铝制门窗 C、蚕丝围巾 D、玻璃水杯
11、(2017衡阳)下列归纳和推理,你认为合理的是( )。
A、氧化物一定含有氧元素,含有氧元素的物质一定是氧化物
B、离子是带电荷的粒子,带电荷的粒子一定是离子C、碱性溶液能使无色酚酞变红,能使无色酚酞变红的是碱性溶液
D、盐中含有金属离子和酸根离子, 中不含金属离子,不属于盐类
12、(2017衡阳)为除去物质中的杂质(括号内为杂质),选用试剂及操作方法错误的是( )。
物 质 选 用 试 剂 及 操 作 方 法
A Cu(CuO) 加入足量的稀硫酸,在充分反应后过滤。
B O(CO) 通入足量的氢氧化钠溶液,充分反应后干燥
2 2
C CaCl 溶液(盐酸) 加入足量的碳酸钙粉末,充分反应后过滤
2
D CuSO(FeSO) 加入过量的铁粉,充分反应后过滤
4 4
13、(2017衡阳)有关碳和碳氧化物的说法中,错误的是( )。
A、古代用墨书写或绘制的字画长久不变色,是因为碳的化学性质不活泼
B、金刚石和石墨物理性质不同,是因为它们的碳原子排列方式不同
C、二氧化碳的排放是导致温室效应的原因之一
D、用煤火取暖是应注意通风,防止一氧化碳中毒
14、(2017衡阳)碘是甲状腺激素的重要成分。如图是碘元素在元素周期表中的有关信息,下列说法错误的是(
)。
A.碘的原子序数数是53 B.碘属于非金属元素 C.碘是人体必需的微量元素 D.碘的相对原子质量是
126.9g
15、(2017衡阳)下列离子在PH=1的溶液中,能大量存在,且为无色溶液的是( )。
A、 B、 C、 D、
16、(2017衡阳)下列四种氮肥样品中,分别加入熟石灰混合、研磨后,无氨味的是( )。
A、硫酸铵 B、氯化铵 C、硝酸铵 D、尿素
17、(2017衡阳)生活中一些常见的食物近似PH如下,其中酸性最强的食物是( )。
A、西瓜汁(5.3~6.2) B、苹果汁(2.6~3.3) C、牛奶 (6.3~6.6) D、鸡蛋清(7.6~8.0)
18、(2017衡阳)中央第六环保督察组4月24日——5月23日进驻衡阳市开展环保督查工作。防止垃圾污染
环境,分类回收是关键,下图表示可回收标志是( )。
A B C D
19、(2017衡阳)下列图像与对应选项关系合理的是( )。
生 有MnO 2 食
沉 气
成 盐
无MnO
2
淀 体
质
质 质
的 量
量 量
质 /g /g /g
量
/ 氢 氧 化 钠 溶
反应时间/s 水的质量/g
g A B C D
A、用等质量、等浓度的过氧化氢( )溶液分别制取氧气
B、向含有盐酸的氯化铜溶液中滴加氢氧化钠溶液,产生沉淀的质量变化
C、等质量的镁、铝与足量的稀硫酸反应
D、将溶质质量分数为20%的食盐水稀释成10%,稀释过程中溶质的质量变化20、(2017衡阳)下列关于物质的分类的叙述错误的是( )。
A、熟石灰、烧碱、氨水都属于碱 B、金刚石、石墨、C 均属于单质
60
C、甲烷、酒精、蔗糖均属于有机化合物 D、生石灰、氧气、水均属于氧化物
21、(2017衡阳)某石灰石样品中含有不含钙元素的杂质,测得该石灰石样品中含钙的质量分数为36%,该样
品中碳酸钙的质量分数为( )。 A、36% B、40% C、72% D、90%
22、(2017衡阳)在一个密闭的容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量,数
据见下表,下列说法正确的是( )。
物 质 甲 乙 丙 丁
反应前质量/g 1 20 17 2
反应后质量/g m 29 0 10
A.m的值是0 B.甲是该反应的催化剂 C.化学反应中乙、丁的质量比是9:8 D.该反应是化合反应
23、(2017衡阳)向一定质量的AgNO 和Cu(NO) 的混合溶液中加入一定质量的锌粉,充分反应后过滤,往滤
3 3 2
渣中加入少量的稀盐酸,无气泡产生。下列说法正确的是:( )。
A.滤液一定呈蓝色 B.滤液中一定有Zn(NO) C.反应前后溶液的质量不变 D.滤渣中的物质至少有两种
3 2
二、填空题(本题共24分)
24、(2017衡阳)现有下列四种物质:A.氖气 B.干冰 C.可燃冰 D.硫酸铜,请用合适的物质的字母代号
填空:
(1)可制农药波尔多液的是 ; (2)可用于人工降雨的是 ;
(3)可用作未来新能源的是 ; (4)可用在城市霓虹灯的是 ;
25、(2017衡阳)用化学用语填空:(1)2个氮气分子 ;(2)氢氧根离子 ;
(3)3个硫原子 ; (4)氧化铁中铁的化合价 。
溶解度/g
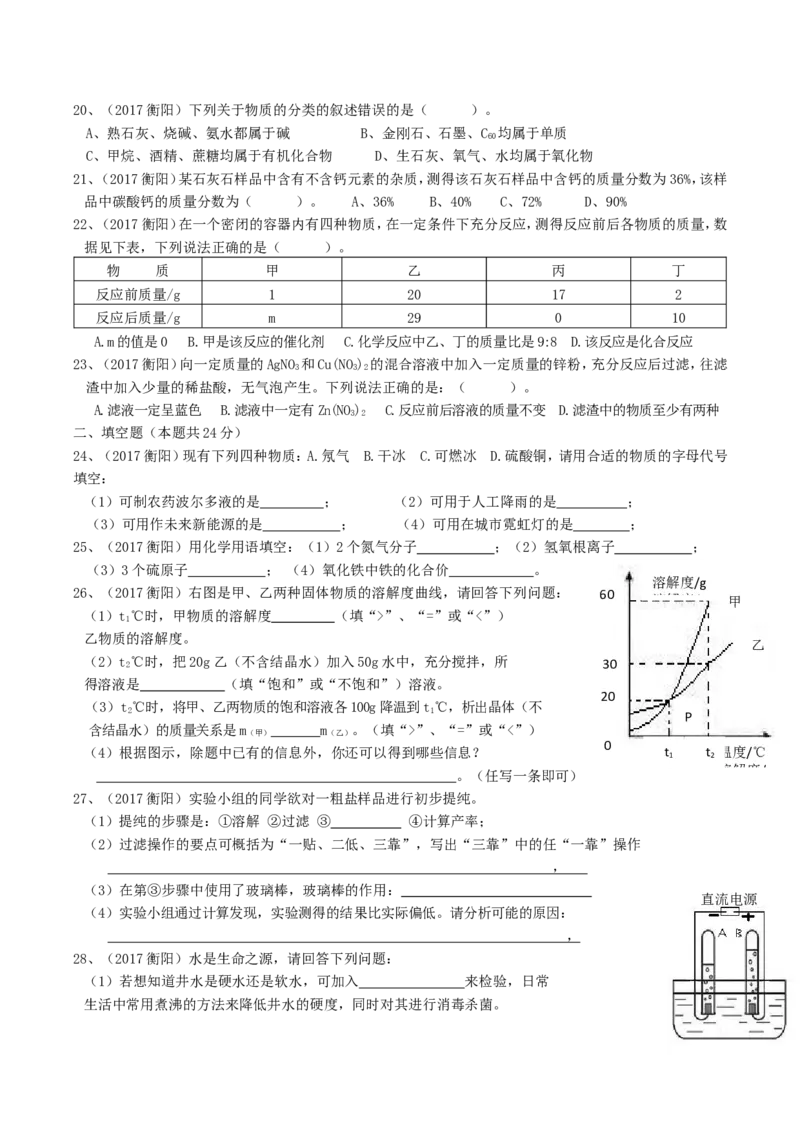
26、(2017衡阳)右图是甲、乙两种固体物质的溶解度曲线,请回答下列问题: 60
溶解度/g 甲
(1)t℃时,甲物质的溶解度 (填“>”、“=”或“<”)
1
乙物质的溶解度。
乙
(2)t 2 ℃时,把20g乙(不含结晶水)加入50g水中,充分搅拌,所 30
得溶液是 (填“饱和”或“不饱和”)溶液。
20
(3)t℃时,将甲、乙两物质的饱和溶液各100g降温到t℃,析出晶体(不
2 1
P
含结晶水)的质量关系是m m 。(填“>”、“=”或“<”)
(甲) (乙)
0
(4)根据图示,除题中已有的信息外,你还可以得到哪些信息? t t 温度/℃
1 2
。(任写一条即可)
溶解度/g
27、(2017衡阳)实验小组的同学欲对一粗盐样品进行初步提纯。
(1)提纯的步骤是:①溶解 ②过滤 ③ ④计算产率;
(2)过滤操作的要点可概括为“一贴、二低、三靠”,写出“三靠”中的任“一靠”操作
,
(3)在第③步骤中使用了玻璃棒,玻璃棒的作用:
直流电源
(4)实验小组通过计算发现,实验测得的结果比实际偏低。请分析可能的原因:
,
28、(2017衡阳)水是生命之源,请回答下列问题:
(1)若想知道井水是硬水还是软水,可加入 来检验,日常
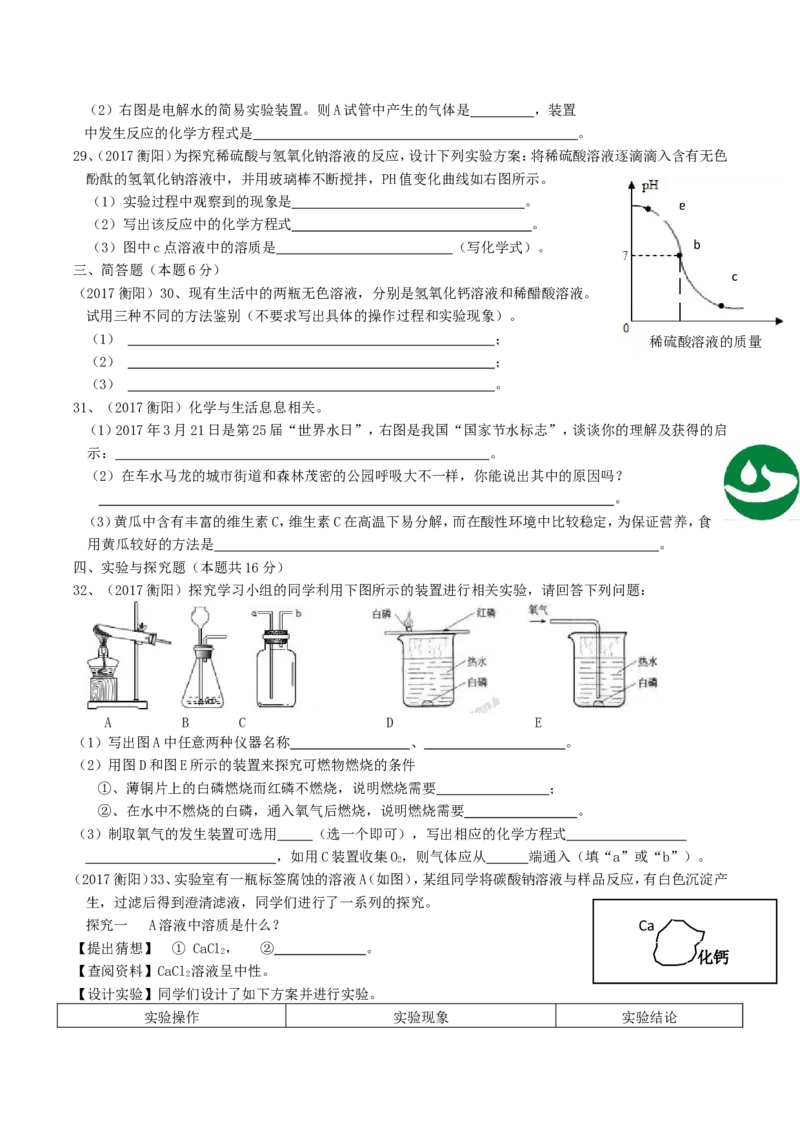
生活中常用煮沸的方法来降低井水的硬度,同时对其进行消毒杀菌。(2)右图是电解水的简易实验装置。则A试管中产生的气体是 ,装置
中发生反应的化学方程式是 。
29、(2017衡阳)为探究稀硫酸与氢氧化钠溶液的反应,设计下列实验方案:将稀硫酸溶液逐滴滴入含有无色
酚酞的氢氧化钠溶液中,并用玻璃棒不断搅拌,PH值变化曲线如右图所示。
(1)实验过程中观察到的现象是 。
a
(2)写出该反应中的化学方程式 。
(3)图中c点溶液中的溶质是 (写化学式)。 b
三、简答题(本题6分)
c
(2017衡阳)30、现有生活中的两瓶无色溶液,分别是氢氧化钙溶液和稀醋酸溶液。
试用三种不同的方法鉴别(不要求写出具体的操作过程和实验现象)。
(1) ; 稀硫酸溶液的质量
(2) ;
(3) 。
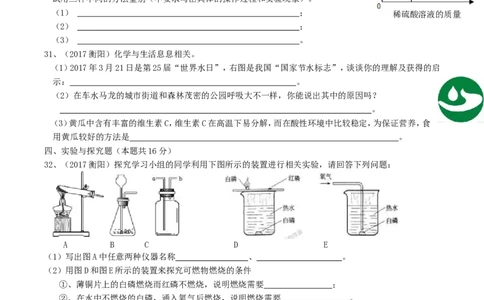
31、(2017衡阳)化学与生活息息相关。
(1)2017年3月21日是第25届“世界水日”,右图是我国“国家节水标志”,谈谈你的理解及获得的启
示: 。
(2)在车水马龙的城市街道和森林茂密的公园呼吸大不一样,你能说出其中的原因吗?
。
(3)黄瓜中含有丰富的维生素C,维生素C在高温下易分解,而在酸性环境中比较稳定,为保证营养,食
用黄瓜较好的方法是 。
四、实验与探究题(本题共16分)
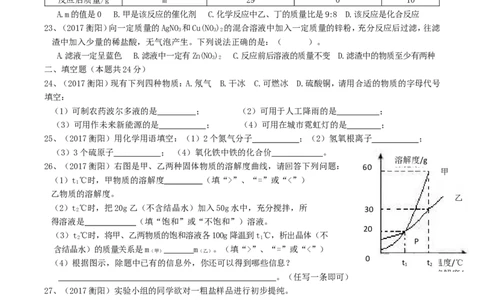
32、(2017衡阳)探究学习小组的同学利用下图所示的装置进行相关实验,请回答下列问题:
A B C D E
(1)写出图A中任意两种仪器名称 、 。
(2)用图D和图E所示的装置来探究可燃物燃烧的条件
①、薄铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要 ;
②、在水中不燃烧的白磷,通入氧气后燃烧,说明燃烧需要 。
(3)制取氧气的发生装置可选用 (选一个即可),写出相应的化学方程式 。
,如用C装置收集O,则气体应从 端通入(填“a”或“b”)。
2
(2017衡阳)33、实验室有一瓶标签腐蚀的溶液A(如图),某组同学将碳酸钠溶液与样品反应,有白色沉淀产
生,过滤后得到澄清滤液,同学们进行了一系列的探究。
探究一 A溶液中溶质是什么? Ca
【提出猜想】 ① CaCl, ② 。
2 化钙
【查阅资料】CaCl 溶液呈中性。
2
【设计实验】同学们设计了如下方案并进行实验。
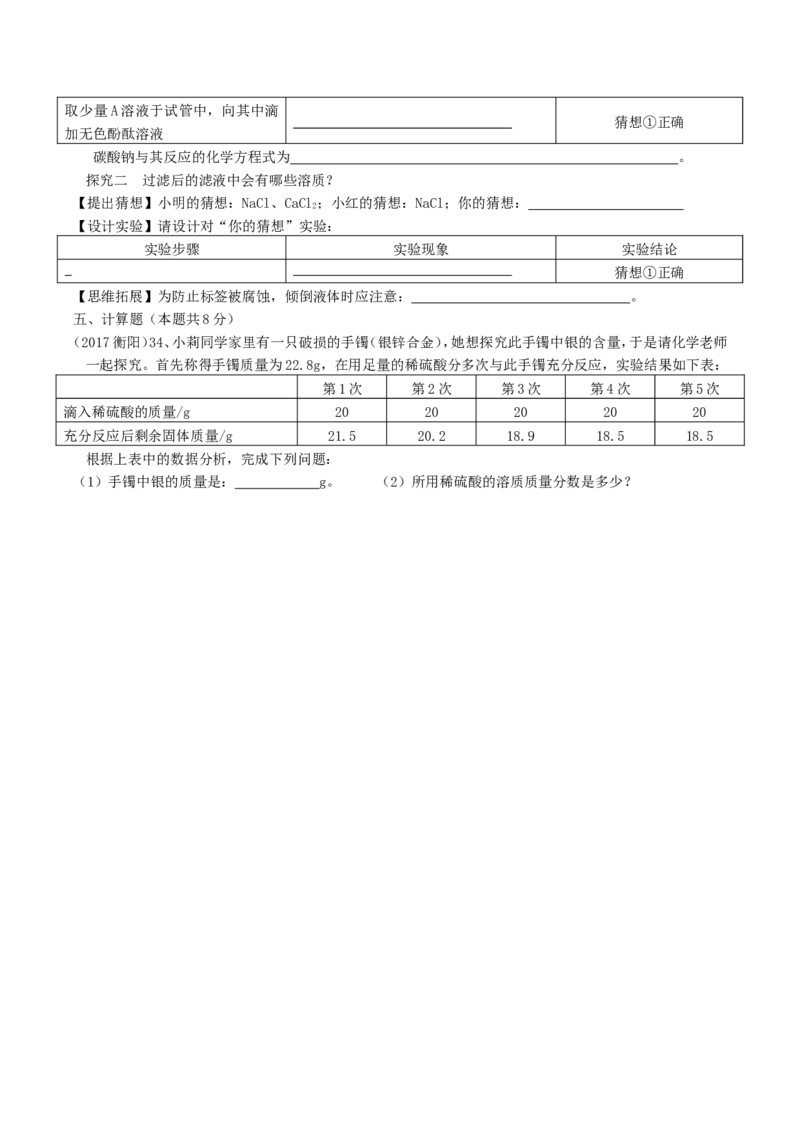
实验操作 实验现象 实验结论取少量A溶液于试管中,向其中滴
猜想①正确
加无色酚酞溶液
碳酸钠与其反应的化学方程式为 。
探究二 过滤后的滤液中会有哪些溶质?
【提出猜想】小明的猜想:NaCl、CaCl;小红的猜想:NaCl;你的猜想:
2
【设计实验】请设计对“你的猜想”实验:
实验步骤 实验现象 实验结论
猜想①正确
【思维拓展】为防止标签被腐蚀,倾倒液体时应注意: 。
五、计算题(本题共8分)
(2017衡阳)34、小莉同学家里有一只破损的手镯(银锌合金),她想探究此手镯中银的含量,于是请化学老师
一起探究。首先称得手镯质量为22.8g,在用足量的稀硫酸分多次与此手镯充分反应,实验结果如下表:
第1次 第2次 第3次 第4次 第5次
滴入稀硫酸的质量/g 20 20 20 20 20
充分反应后剩余固体质量/g 21.5 20.2 18.9 18.5 18.5
根据上表中的数据分析,完成下列问题:
(1)手镯中银的质量是: g。 (2)所用稀硫酸的溶质质量分数是多少?参考答案
一、选择题(每小题2分共46分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 B D C C A B A C B A C D
题号 13 14 15 16 17 18 19 20 21 22 23
答案 C D A D B B C D D C B
二、填空题(共24分)(反应化学方程式每个2分,其余每空1分)
24、(4分) (1)D (2)B (3)C (4)A +3
25、(4分) (1)2N (2)OH - (3)3S (4)FeO
2 2 3
26、(4分) (1) = (2) 饱和 (3) >
(4)t℃时,甲、乙两种物质的溶解度相等,均为20g。(合理答案均可)
1
27、(4分)(1)蒸发 (2)倾倒待过滤的液体时,烧杯嘴要靠在玻璃棒上;玻璃棒下端要靠在三层滤纸一边;漏斗
的颈部要紧靠接收滤液的烧杯的内壁。(任写一条)
(3)搅拌,使液体均匀受热,防止局部温度过高,引起液滴飞溅。
(4)溶解粗盐时,水量略少,或搅拌不充分,有少量NaCl未溶解;蒸发时,未用玻璃棒搅拌,有液滴飞溅;加
热过度,水分完全蒸干才停止加热,有NaCl粉末飞溅。(任写一条)
28、(4分) (1)肥皂水 (2)氢气 2HO 通电 2H ↑ + O ↑
2 2 2
29、(4分) (1) 溶液由红色变成无色 (2) 2NaOH + HSO == NaSO + 2HO
2 4 2 4 2
(3) NaSO、HSO
2 4 2 4
三、简答题(6分)
30、(1)通入二氧化碳 (2)滴入石蕊试液 (3)加入碳酸钠溶液(合理答案均可)
31、(1)爱护水资源人人有责 (2)森林可以净化空气,使周围空气清新
(3)用醋凉拌吃 (合理答案均可)
四、实验探究题(16分)(反应化学方程式每个2分,其余每空1分)
32、(8分)(1) 铁架台、酒精灯、试管、带导管橡皮塞(任写两样) (2) 温度达到着火点
(3) A 2KMnO4 △ KMnO4 + MnO + O ↑ (或 2KClO MnO2 △ 2KCl + 3 O ↑ ) a
2 2 2 3 2
( 答案二: B 2HO MnO2 H O + O ↑ a )
2 2 2 2
33、(8分)(1) Ca(OH) (2) 溶液不变色 (3) NaCO + CaCl == CaCO ↓+ 2NaCl
2 2 3 2 3
(4) NaCl、NaCO (5) 取少量过滤溶液于试管中,向其中滴入盐酸 有气泡产生
2 3
(6) 标签向着手心
五、计算题(8分)
34、(1)18.5g 98:65 = x:1.3g
(2)解:设20g硫酸中溶质质量为x x = 1.96g
HSO + Zn == ZnSO + H ↑ 稀硫酸溶质质量分数:1.96/20 × 100%
2 4 4 2
98 65 = 9.8%
x (22.8-21.5)g 答:稀硫酸溶质质量分数为9.8% 。