文档内容
德州市二○一八初中学业水平考试化学试题
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Cl—35.5
一、选择题(1-12题,每题2分,13-16题,每题3分)
1. 我国有着悠久的历史和灿烂的文化。下列工艺中一定发牛化学变化的是( )
A. 刺绣 B. 织布 C. 剪纸 D. 酿酒
【答案】D
【解析】刺绣、织布、剪纸过程中只是物质形态、状态发生改变,均没有新物质生成,属于物理
变化;酿酒过程中有新物质乙醇生成,属于化学变化。故选D。
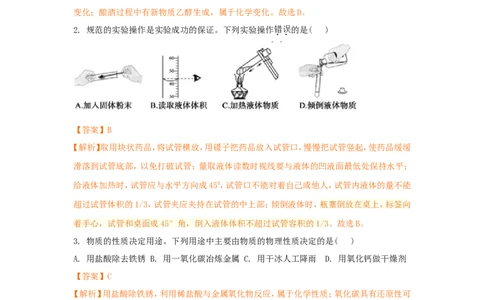
2. 规范的实验操作是实验成功的保证。下列实验操作错误的是( )
【答案】B
【解析】取用块状药品,将试管横放,用镊子把药品放入试管口,慢慢把试管竖起,使药品缓缓
滑落到试管底部,以免打破试管;量取液体读数时视线要与液体的凹液面最低处保持水平;
给液体加热时,试管应与水平方向成450,试管口不能对着自己或他人,试管内液体的量不能
超过试管体积的1/3,试管夹应夹持在试管的中上部;倾倒液体时,瓶塞倒放在桌上,标签向
着手心,试管和桌面成45°角,倒入液体体积不超过试管容积的1/3。故选B。
3. 物质的性质决定用途。下列用途中主要由物质的物理性质决定的是( )
A. 用盐酸除去铁锈 B. 用一氧化碳冶炼金属 C. 用干冰人工降雨 D. 用氧化钙做干燥剂
【答案】C
【解析】用盐酸除铁锈,利用稀盐酸与金属氧化物反应,属于化学性质;氧化碳具有还原性可
以冶炼金属,属于化学性质;干冰用于人工降雨,是利用了干冰升华时吸热的性质,属于物理
性质;氧化钙与水反应,可作干燥剂,属于化学性质。故选C。
4. 下列有关氧气的描述正确的是( )
A. 氧气参与燃烧是高能燃料 B. 氧气能使带火星木条复燃
C. 红磷与氧气反应产生浓厚白雾 D. 低温下氧气可以变成无色液体
【答案】B
【解析】氧气参与燃烧可作助燃剂,不属于高能燃料;氧气具有助燃性,能使带火星木条复燃;红磷与氧气反应产生浓厚白烟;低温下氧气可以变成淡蓝色液体。故选B。
5. 下图是水电解实验示意图,下列有关说法正确的是( )
A. 正极连接的玻璃管内产生氢气B. 产生两种气体质量比为2:1
C. 水是由氢分子和氧分子组成 D. 在化学变化中原子重新组合
【答案】D
【解析】与电源正极相连的玻璃管内产生的是氧气;与直流电源的正极和负极相连管内产生
气体的质量比为8:1,体积比为1:2;水通电分解是化学变化,水通电后生成氢气和氧气,说
明水是由氢元素和氧元素组成的;在化学变化中,构成物质的的分子分裂成原子,原子重新
组合成新的分。故选D。
6. 近日,中国在四川某地发现了一个超大规模的锂矿,储量高达52万吨,被称之为“中国
锂谷”。锂矿是重要的国家战略资源,有着21世纪改变世界格局的“白色石油”和“绿色
能源金属”之称。下图是锂原子结构示意图和锂元素在元素周期表中的相关信息。下列说法
正确的是( )
A. 锂元素属于非金属元素 B. 锂原子在化学反应中易得电子
C. 锂原子的相对原子质最是6.94lg D. 锂原子核内有3个质子
【答案】D
【解析】锂元素属于金属元素;锂元素的原子核外最外层有1个电子,易失去最外层的1个电
子形成离子(Li+);元素的相对原子质量为6.941;锂元素原子序数=质子数=核电荷数=核外
电子数=3。故选D。
7. 下列各图中“O”、“●”分别表示不同元素的原子,则其中表示化合物的是( )【答案】C
【解析】A图表示由一种原子构成的一种分子,属于单质;B图表示由不同种原子构成的两种
分子,属于混合物;C图表示由不同种原子构成的一种分子,属于化合物;D图表示由不同种
原子构成的三种分子,属于混合物。故选C。
8. 下列化学用语书写正确的是( )
A. 银元素—AG B. 3个氧原子—O C. 4个水分子——4HO D. 镁离子——Mg+2
3 2
【答案】C
【解析】银的元素符号是Ag;三个氧原子可表示为:3O,而O 表示臭氧、一个臭氧分子和一个
3
臭氧分子由3个氧原子构成;4个水分子可表示为:4HO;镁离子可表示为:Mg2+。故选C。
2
9. 铜锈主要成分是Cu(OH)CO。加热分解的化学方程式为:Cu(OH)CO 2X+HO+CO↑,
2 2 3 2 2 3 2 2
其中X的化学式是( )
A. Cu B. CuO C. Cu(OH) D. CuCO
2 3
【答案】B
【解析】根据质量守恒定律元素种类、原子个数和质量不变判断X的化学式是CuO。故选B。
10. “美丽中国,我是行动者”是我国生态环境部3月23日发布的2018年环境日主题。我
们要携手行动,建设天蓝、地绿、水清的美丽中国。下列做法与上述主题不相符的是( )
A. 重复使用某些塑料袋 B. 垃圾分类回收 C. 提倡使用一次性餐具 D. 用淘米水浇花
【答案】C
【解析】重复使用某些塑料袋,可以减少“白色污染”,保护资源和环境;垃圾分类,资源再利
用,能节约资源,提高资源利用效益;提倡使用一次性餐具,增加污染,不利于保护资源和环
境;用淘米水浇花,可以节约用水,保护水资源。故选C。
11. 向某稀盐酸中逐渐加入试剂X后溶液的pH变化如图。试剂X可能是下列物质中的( )A. HO B. HSO C. NaOH D. CaCO
2 2 4 3
【答案】C
【解析】水为中性物质,可以减低稀盐酸的酸性,但是溶液始终呈酸性,溶液的pH<7;硫酸为
酸性物质,可以增强稀盐酸的酸性,但是溶液始终呈酸性,溶液的pH值<7;氢氧化钠为碱,可
以和稀盐酸反应,而使溶液的酸性减弱,当恰好完全反应时溶液的pH值为7,继续加入氢氧
化钠则溶液呈碱性,而使pH值大于7;碳酸钙可以消耗盐酸,溶液的pH≤7。故选C。
12. 珍爱生命,关注安全。从安全角度考虑,以下做法正确的是( )
A. 油锅起火时用锅盖盖灭 B. 甲醛浸泡海鲜品用来保鲜
C. 冬季吃水炭火锅关严门窗 D. 稀释浓硫酸时将水倒入浓硫酸
【答案】A
【解析】盖上锅盖时,油与空气或氧气隔绝,从而达到灭火目的;甲醛有毒,食用甲醛浸泡的海
鲜会危害身体健康;木炭不完全燃烧生成一氧化碳,关严门窗容易造成煤气中毒;稀释浓硫
酸时将浓硫酸倒入水中。故选A。
13. 下列化学方程式书写正确的是( )
A. 3Fe+2O=FeO B. Cu+2AgNO=2Ag+Cu(NO)
2 3 4 3 3 2
C. 2Fe+6HCl=2FeCl+3H↑ D. KCl+NaNO=KNO+NaCl
3 2 3 3
【答案】B
【解析】铁在氧气中燃烧:3Fe+2O FeO;铜与硝酸银溶液反应生成银和硝酸铜:
2 3 4
Cu+2AgNO=2Ag+Cu(NO);铁和盐酸反应生成氯化亚铁和氢气:Fe+2HCl=FeCl+H↑;
3 3 2 2 2
KCl+NaNO 不符合复分解反应反生的条件。故选B。
3
14. 金属锰与氯化亚铁溶液可发生如下反应:Mn+FeCl===MnCl+ Fe,下列说法错误的是(
2 2
)
A. 该反应属于置换反应 B. 锰的金属活动性比铁强
C. 锰能置换出盐酸中的氢 D. 反应前后元素化合价都不变
【答案】D
【解析】该反应符合置换反应的条件,属于置换反应;锰能与氯化亚铁反应置换出铁,说明锰
的金属活动性比铁强;锰的金属活动性比铁强,能与稀盐酸反应;氯化亚铁中铁元素为+2价,
铁单质中铁为0价。故选D。
15. 下图是甲、乙、丙三种物质在水中的溶解度曲线。以下说法正确的是( )A. t℃时溶解度由大到小的顺序是乙>丙>甲
2
B. 由t℃降到t℃析出晶体最多的是甲溶液
2 1
C. 由t℃降到t℃丙溶液浓度一定不发生变化
2 1
D. 甲乙丙三种物质溶解度都随温度升高而增大
【答案】C
【解析】根据溶解度曲线判断,在t℃时,三种物质的溶解度大小关系是甲>乙>丙;甲和乙
2
的溶解度随温度的降低而减小,降温时两物质的饱和溶液中都会有晶体析出,但不知道溶液
的质量,析出晶体的多少无法比较;丙的溶解度随温度的降低而增大,降温时它的饱和溶液
中不会有晶体析出;丙的溶解度随温度的降低而增大,降温时丙的饱和溶液中不会有晶体析
出,丙溶液浓度没有发生变化;丙的溶解度随温度的升高而减小。故选C。
16. 下列实验操作中,不能达到实验目的是( )
【答案】C
【解析】生活中可用肥皂水来区分硬水和软水,产生泡沫较多的是软水,较少的硬水;食盐能
溶于水,泥沙不溶于水,将粗盐加适量水溶解、过滤、蒸发结晶,能提纯粗盐;二氧化碳能和氢
氧化钠反应,而一氧化碳不能,不符合除杂原则;将铁丝插入氯化镁溶液中,铁与氯化镁不反
应,说明铁不如镁活泼;将铁丝插入氯化铜溶液中,铁丝表面有红色固体出现,说明铁比铜活
泼。故选C。
二、理解与应用
17. 从①熟石灰、②硝酸钾、⑧金刚石、④小苏打中,选择适当的物质填空(填化学式):(1)常用于发酵粉的是__________; (2)可用来裁玻璃的是__________;
(3)可用作复合肥的是__________; (4)可用于改良酸性土壤的是__________。
【答案】(1) NaHCO (2) C (3)KNO (4)Ca(OH)
3 3 2
【解析】(1)小苏打是焙制糕点所用的发酵粉的主要成分之一,其化学式为:NaHCO;(2)金刚
3
石硬度大,可用来裁玻璃,其化学式为:C;(3)硝酸钾中含有氮元素和钾元素,属于复合肥料,
其化学式为:KNO;(4) 熟石灰可用于改良酸性土壤,其化学式为:Ca(OH)。
3 2
18. 化学就在我们身边,与我们的生活息息村{关。请根据所学知识回答下列问题:
(1)豆腐、鸡蛋、瘦肉等食物为人体提供的主要营养素是___________。
(2)厨房中用洗洁精除去餐具上的油污时,会出现________(填“溶解”或“乳化”)现象。
(3)使用碳素墨水书写的文字很长时间不变色,是因为________________________。
(4)在酒厂附近常可以闻到酒味。请从微观角度加以解释_______________________。
【答案】(1)蛋白质 (2)乳化 (3)碳在常温下化学性质稳定 (4)分子在不停地运动
【解析】(1)豆腐、鸡蛋、瘦肉中都富含蛋白质;(2)厨房中用洗洁精除去餐具上的油污,是利用
洗洁精的乳化作用;(3)碳在常温下化学性质稳定,使用碳素墨水书写的文字很长时间不变
色;(4)在酒厂附近常可以闻到酒味,是因为构成物质的分子在不停地运动。
19. 能源、材料问题越来越引起人们的重视。
(l)目前人类需要的能量主要来自化石燃料的燃烧,化石燃料包括煤、石油和________等。
(2)锰钢是一种重要的合金,比组成它的纯金属硬度________,韧性好,可用于制作钢轨。
(3)篝火晚会时为使木柴燃烧的更旺,常把木柴架空,其原理是____________________。
(4)登山运动员用氢化钙(CaH)与水反应制取的氢气作为燃料, 同时得到一种碱。氢化钙与
2
水反应的化学方程式为______________________,为防止爆炸,点燃氢气前一定要进行的操
作是__________。
【答案】(1)天然气 (2)大 (3)增大木柴与空气的接触面积,促进燃烧
(4)CaH+HO=Ca(OH)+H↑ (5)检验气体的纯度
2 2 2 2
【解析】(l)常见的化石燃料包括煤、石油和天然气;(2)合金比组成它的纯金属硬度大;(3)篝
火晚会时为使木柴燃烧的更旺,常把木柴架空,是为了增大木柴与空气的接触面积,促进燃
烧;(4)氢化钙(CaH)与水反应生成氢气和氢氧化钙,反应的化学方程式为:
2
CaH+HO=Ca(OH)+H↑;为防止爆炸,点燃氢气前一定要检验气体的纯度。
2 2 2 2
20. 社会发展让人们的出行更加方便,汽车逐渐走进寻常百姓家。请根据要求回答有关问题:(1)在上图汽车的部件中主要由有机合成材料制成的是__________;
(2)在汽车的电路中主要使用的是铜线,这是利用了铜的______性;
(3)汽车表面的烤漆不仅美观,还能起到__________的作用
(4)化石燃料的大量使用,带来了环境的污染和资源的枯竭等问题。我市自2018年开始推广
使用车用乙醇汽油,到2019年实现全市全覆盖。乙醇(CHOH)燃烧的化学方程式是
2 5
______________,推广使用乙醇汽油的好处是______________ ,______________ (写出两
条即可)。
【答案】(1)轮胎、塑料保险杠 (2)导电 (3)防止金属锈蚀 (4)CHOH+3O 3HO+2CO
2 5 2 2 2
(5)一定程度上减少汽车尾气的污染 (6)可适当节省石油资源
【解析】钢价车门、铝合金轮彀属于金属材料,轮胎(合成橡胶)、塑料保险杠属于合成材料;
(2)铜有导电性,可作导线;(3)汽车表面的烤漆不仅美观,还可以防止金属生锈;(4)乙醇燃
烧:CHOH+3O 3HO+2CO,使用乙醇汽油可以节约石油资源,减少环境污染。
2 5 2 2 2
21. 推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。请对下列错误观
点举出相应的否定例证(填化学式或化学方程式)。
【答案】(1) CHOH或NaCO (2) NaCO 或NaHCO (3) FeO+6HCl=2FeCl+3HO 或
2 5 2 3 2 3 3 2 3 3 2
2NaOH+CO=NaCO+HO
2 2 3 2
【解析】②碳酸钠(NaCO)、酒精(CHOH)等,都含氧,但不是氧化物;③与酸反应放出气体的
2 3 2 5物质,不一定是活泼金属,如NaCO 或NaHCO 等许多碳酸盐和酸反应生成二氧化碳气体;④
2 3 3
酸与碱作用生成盐和水的反应属于中和反应,反应物必须是酸和碱,生成物是盐和水的反应
不一定是中和反应,如二氧化碳与氢氧化钠反应生成碳酸钠和水,生成物是盐和水,化学方
程式为:2NaOH+CO=NaCO+HO (或FeO+6HCl=2FeCl+3HO),但是不属于中和反应。
2 2 3 2 2 3 3 2
三、实验与探究
22. 实验室中分别用高锰酸钾、过氧化氢、氯酸钾制取比较纯净的氧气。请你按照要求回答
问题:
(l)结合下图所提供装置完成下列表格
(2)请结合上图回答问题:
①写出甲、乙所指仪器名称:甲_______________;乙_______________;
②用过氧化氢制氧气的装置与其他两种方法的装置相比具有的优点____________,
_____________(写出两条);
③若用下图装置收集一瓶氧气,气体应从____(填a或b)端进入集气瓶。
【答案】(1)AD (2)2HO 2HO+O↑(3)BD (4)2KClO 2KCl+3O↑(5)酒精灯 (6)集气
2 2 2 2 3 2
瓶 (7)可随时添加液体药品 (8)操作简便或节能安全 (9)b
【解析】(1)实验室用高锰酸钾制取氧气的反应是固体,反应条件是加热,排水法收集的氧气纯净,所以应选用的装置组合是AD;过氧化氧在二氧化锰做催化剂的条件下生成水和氧气,
化学方程式为:2HO 2HO+O↑,实验室用过氧化氧和二氧化锰制取氧气的反应是固体
2 2 2 2
和液体,反应条件是常温,排水法收集的氧气纯净,所以应选用的装置组合是BD;加热二氧化
锰和氯酸钾的混合物生成氯化钾和氧气,化学方程式为:2KClO 2KCl+3O↑;(2)①据图
3 2
可知甲、乙所指仪器名称:甲是酒精灯;乙是集气瓶;②用过氧化氢制氧气的装置与其他两种
方法的装置相比具有的优点是:可随时添加液体药品、操作简便或节能安全等;③用排水法
收集氧气时,在瓶中装满水,氧气应从b端进入。
23. 在学习“酸和碱”后,瑞娟同学对“硫在氧气中燃烧”实验进行再探究。想到实验生成
的二氧化硫是非金属氧化物,提出疑问:二氧化硫能否与水反应生成酸?
为此,瑞娟同学做了如F实验:将点燃的硫伸人盛有氧气的集气瓶(有少量的水)中,反应中
产生刺激性气味的气体;反应后,盖紧集气瓶口的玻璃片,振荡集气瓶;再打开玻璃片,仍能
闻到刺激性气味;随后向其中滴入几滴紫色的石蕊试液,瓶中液体变为红色。
瑞娟同学产生许多困惑:这种能使石蕊试液变红色的物质是什么?怎样防止二氧化硫排放
到空气中去?
瑞娟询问老师,老师告知:在涉及的反应中,二氧化硫与二氧化碳的性质相似;二氧化硫与水
反应生成“亚硫酸”(化学式为HSO);亚硫酸还可进一步与氧气反应生成硫酸。
2 3
请你帮助瑞娟同学解答下列问题:
(1)请结合下列图示中所给实验用品,设计一个实验用来验证:二氧化硫不能使石蕊变红色。实验操作:__________________________________;
(2)分别写出生成亚硫酸、硫酸的两个化学方程式:①____________;②_____________。
(3)以上两个化学反应都属于________反应(填基本反应类型);亚硫酸中硫元素的化合价为
____价。
(4)亚硫酸、硫酸、盐酸和碳酸都能使石蕊试液变红色,从微观角度分析原因是________;
(5)为更多的吸收二氧化硫,防止二氧化硫散发至空气中。有以下试剂, 你认为用来代替集
气瓶中的水最为合适的是_________(填序号)。
①饱和氧氧化钙溶液; ②饱和氯化钠溶液; ③浓盐酸; ④饱和氢氧化钠溶液
【答案】(1)将石蕊试液染成紫色的干燥的纸花放入盛有二氧化硫的集气瓶内 (2)
SO+HO=HSO (3) 2HSO+O=2HSO (4)化合 (5)+4 (6)溶液中都有H+ (7)④
2 2 2 3 2 3 2 2 4
【解析】(1)验证二氧化硫不能使石蕊变红色的实验操作:取一朵用石蕊溶液染成的紫色的干
燥纸花,将干燥的纸花放入盛满二氧化硫的集气瓶中,观察纸花是否变红;(2)二氧化硫与水
反应生成亚硫酸,反应的化学方程式为:SO+HO=HSO;亚硫酸与氧气反应生成硫酸,反应的
2 2 2 3
化学方程式为:2HSO+O=2HSO;(3) 以上两个化学反应的生成物只有一种,属于化合反应;
2 3 2 2 4
HSO 中氢元素显+1价,氧元素显-2价,所以硫元素显+4价;(4)亚硫酸、硫酸、盐酸和碳酸都
2 3
显酸性是因为它们的溶液中都含有氢离子;(5)①饱和氧氧化钙溶液能和二氧化硫反应,但
溶液浓度较小,效果不好,故不行;②饱和氯化钠溶液不和二氧化硫反应,故不行;③浓盐酸
不和二氧化硫反应,故不行;④饱和氢氧化钠溶液能和二氧化硫反应,但溶液浓度较大,效果
好,故可行。
四、计算题
24. 葡萄糖经过肠壁吸收进入血液称为血糖,为人体组织提供能量。已知葡萄糖的化学式为
CH O。
6 12 6
(l)一个葡萄糖分子由______个原子构成;
(2)葡萄糖中碳元素的质量分数为___________。
【答案】(1) 24 (2) 40%
【解析】(l)根据葡萄糖的化学式为CH O 可知:一个葡萄糖分子由24个原子构成;(2) 葡萄
6 12 6
糖中碳元素的质量分数= ×100%=40%。
25. 向盛有10 g纯碱样品(含有少量氯化钠)的烧杯中加入稀盐酸。加入80 g稀盐酸时,恰
好完全反应。反应后烧杯内物质总质量为86.7 g。
(l)该反应生成二氧化碳的质量为_________g;(2)求该纯碱样品中碳酸钠质量分数为___________(写出计算过程)。
【答案】(1)3.3 (2)79.5%
【解析】(1)由质量守恒定律可知,生成的二氧化碳的质量:80g+10g-86.7g=3.3g;
(2)设原固体混合物中碳酸钠的质量为x,
NaCO+2HCl=2NaCl+HO+CO↑
2 3 2 2
106 44
x 3.3g
x=7.95g,
纯碱样品中碳酸钠质量分数: ×100%=79.5%;
答:(l)生成二氧化碳的质量是3.3g;(2)纯碱样品中碳酸钠质量分数为79.5%。