文档内容
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}2025 年春季学期百色市普通高中期末教学质量调研测试
高二化学 参考答案
一、选择题:本题共14题,每题3分,共42分,每小题只有1个选项符合题意。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 B B C C A B B A D C B B D C
1.B 【详解】A.靖西绣球所用材质之一的真丝绸缎主要成分是蛋白质,
故A错误;B.茶多酚易被氧化而发挥抗氧化的功效,故B正确;C.百色芒果
的香味来自于酯类和萜类物质,其中的酯类物质密度小于水,故C错误;D.山
茶油所含油脂的主要成分是不饱和脂肪酸甘油酯,故D错误。
2.B 【详解】A.NF 的电子式为 ,故A 错误;B.异戊二烯的结构
3
简式为: ,天然橡胶的主要成分是顺式聚异戊二烯(双键上的取代基甲基和
氢位于同侧),其结构简式为: ,B正确;C.基态C 原子价层电子
排布图为 ,故C错误;D.SO 中心原子S周围的价层电子对数为:
2
1
2+ (6-22)=3,故其价层电子对互斥(VSEPR)模型: ,D错误。
2
3.C 【详解】A.SO 与O 的反应为可逆反应,1molSO 与足量的O 反应,生
2 2 2 2
成的SO 分子数小于N ,A错误;B.CHCl 在标准状况下不是气体,标准状况下,
3 A 3
22.4LCHCl 的物质的量不是1mol,氯原子的数目不为3N ,B错误;C.C H 含有4个
3 A 5 12
C-C 单键,故1molC H 分子中含有碳碳单键数目为4N ,C 正确; D.甲醛
5 12 A
30g
和乙酸的最终简式均为CH O,所以30g混合物中含有氢原子 22mol,
2 30gmol1
在乙酸中存在O-H键,所以混合物中含C-H键的数目小于2N ,D错误。
A
4.C 【详解】A.氢的电负性(鲍林标度2.20)大于硼的电负性(鲍林标度2.04),
故电负性:BB,故B 正确;C.同主族从上到下,第一电离能逐渐减小,同一
周期从左往右元素的第一电离能呈增大趋势,但ⅡA 与ⅢA、ⅤA与ⅥA反常,故
第一电离能:N>O>S,故C错误;D.同主族元素从上到下金属性逐渐增强,故
金属性:Li NaK,故D正确。
5.A 【详解】A.碱金属单质的熔点从 Li 到Cs 也逐渐降低,A错误;B. 同
主族两种元素原子的核外电子数的差值可能为36,例如氢、铷, B 正确;C. 砹
(At)为第七周期、VIIA族元素,该族元素单质的颜色逐渐加深,对于AgX的溶解度
逐渐减小,C正确;D.氢氧化铝能与氢氧化钠溶液反应,则氢氧化铍也能与氢
氧化钠反应,故D正确。
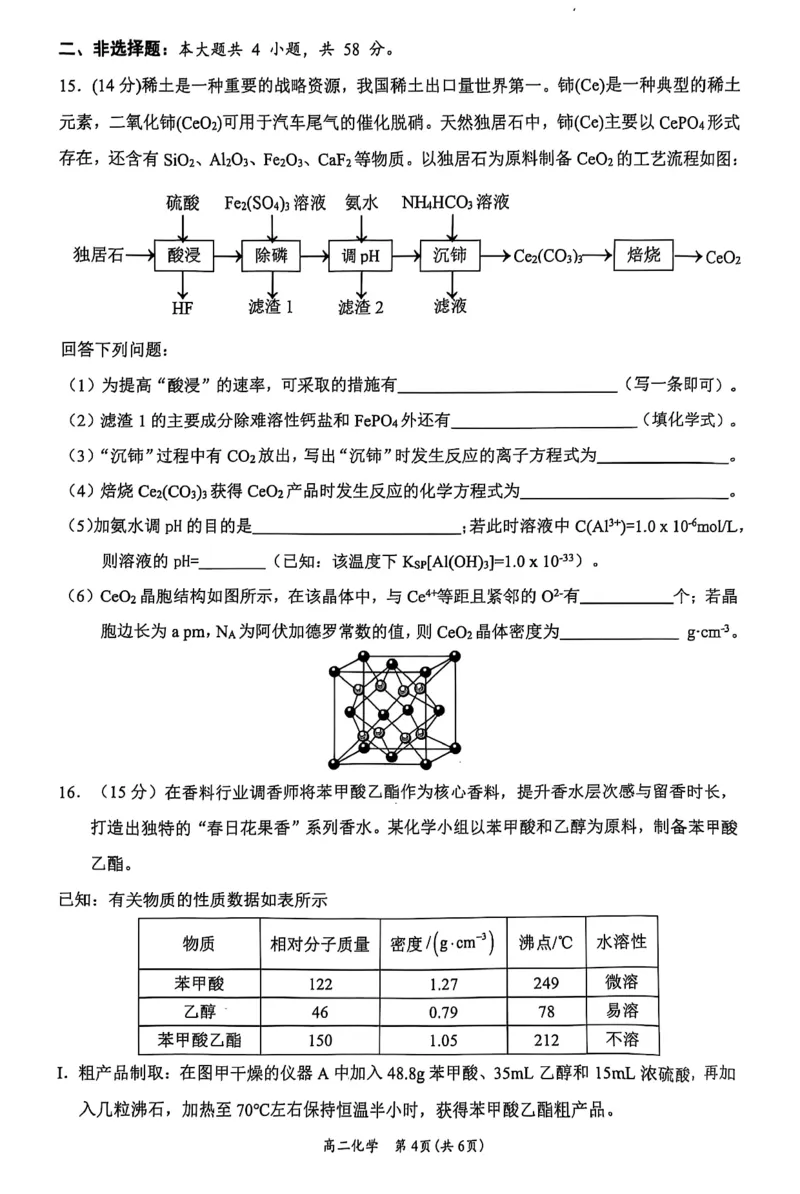
6.B 【详解】A.醋酸具有挥发性,且酸性比碳酸强,所以醋酸也能使苯
酚钠溶液反应生成苯酚,无法验证苯酚的酸性比碳酸的弱,A错误;B.羟基不
与Br 反应,碳碳双键与Br 反应,能达到实验目的,故B 正确;C.溴化铁做
2 2
第 1 页 共 7 页
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}催化剂条件下苯和液溴发生取代反应生成溴苯和溴化氢,用硝酸银溶液检验反应
生成的溴化氢能证明苯和溴发生取代反应,但溴具有挥发性,挥发出的溴也能与
硝酸银溶液反应生成淡黄色的溴化银沉淀,干扰溴化氢的检验,所以题给装置不
能达到验证苯和溴发生取代反应的实验目的,故C错误;D.乙醇和乙酸可以互
溶,不能用分液的方法分离,故D错误。
7.B 【详解】A.CO 分子呈直线形(O=C=O),结构对称,正、负电中心重
2
合,属于非极性分子,但COS分子虽然呈直线形(O=C=S),不是对称分子,分
4-22
子存在极性,故A错误;B.CO 中的C 的价层电子对数为2+ =2,C 采取
2 2
sp 杂化,键角为180°;NH 中的N采取sp3杂化,键角约为105°;所以键角:
3
CO >NH ,故B 正确;C.H S的S 原子价层电子对数为4,含有2对孤电子对,
2 3 2
4-22
空间构型为V形,故C错误;D.CO 与COS的中心原子C价层电子对数为2+ =2,
2 2
C采取sp杂化,VSEPR模型都是直线形,故D错误。
8.A【详解】A.甲基为供电子基团,使得氨基中氮的电子云密度更大,
更容易结合氢离子,使得CH NH 的碱性强于NH ,故A错误;B.邻硝基苯酚
3 2 3
能形成分子内氢键,使邻硝基苯酚沸点低于对硝基苯酚,故B 正确;C.乙醇与
水任意比互溶,主要是因为乙醇与水易形成分子间氢键,增加了分子之间的吸引作
用,故C正确;D.对于结构相似的物质,分子的相对分子质量越大,范德华力
就越大,则克服分子间作用力使物质熔化、汽化消耗的能量就越多,物质的熔沸
点就越高。I 、Cl 都是由分子构成,二者结构相似,相对分子质量:I >Cl ,范
2 2 2 2
德华力:I >Cl ,所以沸点:I >Cl ,故D正确。
2 2 2 2
9.D【详解】A.草酸与酸性高锰酸钾溶液反应,草酸为弱酸,被氧化为CO ,
2
KMnO 被还原为Mn2+,则反应的方程式为:
4
5H C O 2MnO6H 10CO 2Mn28H O,A正确;B.少量二氧化硫与氢氧
2 2 4 4 2 2
化钠溶液反应生成亚硫酸钠和水,反应的离子方程式为SO +2OH-=SO2+H O,
2 3 2
故B 正确;C.苯酚钠溶液中通入二氧化碳产生碳酸氢钠:
+CO +H O→ +NaHCO ,C正确;D.乙醛与银氨溶液反应:
2 2 3
CH CHO2AgNH OH水浴加热CH COONH 2Ag3NH H O,D错误;
3 3 2 3 4 3 2
10.C【详解】A.根据该化合物的结构简式可知,其分子式为C H O ,A
11 12 3
正确;B.该分子含有醛基,使溴水和酸性KMnO 溶液褪色的原理相同,都是
4
发生氧化还原反应,B 正确;C.结构中有共面的苯环和醛基结构, sp3杂化的碳
原子最多3个原子共面,分子中最多17个原子共面,C错误;D.该分子含有醛基
和苯环都可以跟H 发生加成反应,醛基、苯环分别消耗1和3mol的H , D 正
2 2
确。
11.B 【分析】X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,X
原子在s区元素原子中半径最小,故X是H;基态Z原子的价电子排布式为2s22p4,
故Z是O;Y 元素的简单氢化物可用作制冷剂,故Y是N;基态W原子的s 能
第 2 页 共 7 页
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}级电子数等于p能级电子数,故W 是Mg;Q的常见单质为气体,且原子序数最
大,故Q为Cl。【详解】A.非金属性越强,则最高价氧化物对应水化物的酸
性越强,因此酸性:HClO >HNO ,A 正确;B.工业上通过电解熔融的无水氯
4 3
化镁制备金属镁,B 错误;C.Y、Z、W 的简单离子具有相同的核外电子排布,
原子序数越大,离子半径越小,有Y>Z>W,C正确;D.Y元素的简单氢化物
为NH ,N的成键电子对数为3、孤电子对数=(5-1×3)/2=1,价层电子对数=
3
成键电子对数为+孤电子对数=4,杂化方式为sp3杂化,D正确。
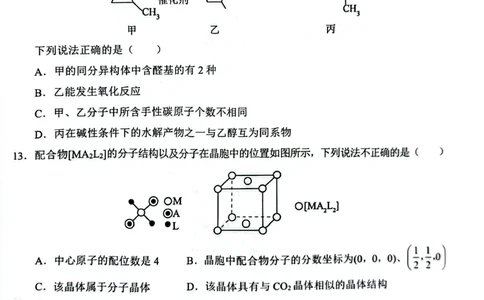
12.B 【详解】A.甲的分子式为C H O,不饱和度为1,甲的同分异构体
3 6
中含醛基的只有1种:CH CH CHO,A 错误;B.乙能发生燃烧的氧化反应,B
3 2
正确;C.手性碳原子是指与四个各不相同原子或基团相连的碳原子,甲中含有
1个手性碳原子,位置为 ,乙中含有1个手性碳原子,位置为 ,C 错
误;D.丙的水解产物有HOCH CH(CH )OH,为二醇,与为一醇的乙醇不是同
2 3
系物关系 D错误。
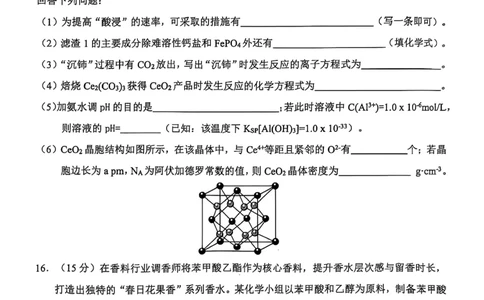
13.D 【详解】A.观察中配合物[MA L ]的分子结构,可看到中心原子M
2 2
周围与4个原子形成配位键,配位数是直接与中心原子(离子)配位的原子(离
子)数目,所以中心原子M 的配位数为4, A正确。
B.由题干晶胞可知,晶胞中配合物分子位于晶胞的8个顶点和上下底面的面心
1 1
上,故晶胞中配合物分子的分数坐标为(0,0,0)、
,,0 ,B 正确;C.由晶
2 2
胞结构可知,该晶体由[MA L ]分子通过分子间作用力结合而成,分子晶体是通
2 2
过分子间作用力(范德华力、氢键等)将分子结合成晶体的,所以该晶体属于分
子晶体,C 正确;D.CO 晶胞中二氧化碳分子处于晶胞顶点和面心,利用均摊法
2
计算,1个 CO 晶胞中含二氧化碳分子数为8×1/8+6×1/2=4个,而本题晶胞含2个配
2
合物分子,二者晶胞中所含分子数量不同,晶体结构不相似,D错误。
14.C 【详解】A.溴乙烷与NaOH 溶液混合共热,充分反应并冷却后,检
验是否发生了取代反应,先向溶液中加稀HNO 酸化中和碱,再滴加AgNO 溶
3 3
液,产生淡黄色沉淀,A错误;B.向某样品溶液中滴加氯化铁溶液,溶液显紫色,
只能证明样品物质含有酚羟基,但不能确定是苯酚,B错误;C.向淀粉溶液中加
入稀硫酸,充分加热,冷却后,再加入碘水,溶液变蓝,证明后面的溶液中含有
淀粉,可能是淀粉未完全水解,不一定是未水解,C 正确;D.将乙醇和浓硫酸
共热产生的气体除乙烯外还有挥发的乙醇蒸气、乙醇炭化后与浓硫酸生成的二氧
化硫都可以使酸性高锰酸钾褪色,不能证明生成了乙烯气体, D错误。
二、非选择题:本大题共 4 小题,共 58 分。
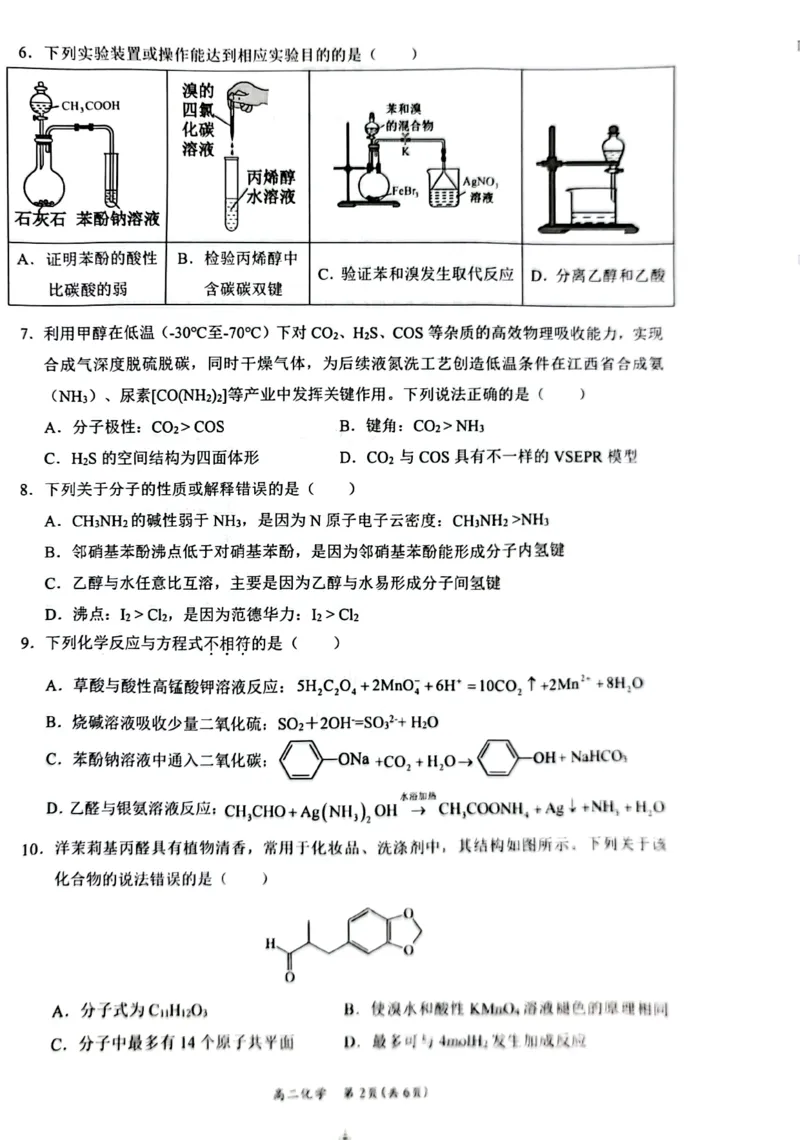
15.(14分)【答案】(1)将独居石粉碎增大接触面积、增大硫酸浓度或搅拌
等(任写一条)(1分)
(2) SiO (2分)(3)6HCO 2Ce3 Ce CO 3CO 3H O(2分)
2 3 2 3 3 2 2
高温
(4)2Ce 2 (CO 3 ) 3 +O 2 4CeO 2 +6CO 2 (2分)
(5)使溶液中的Fe3+、Al3+转化 Fe(OH) 、Al(OH) 而除去(2分) 5(2分)
3 3
第 3 页 共 7 页
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}6.881032
(6)8(1分) (2分)
a3N
A
【分析】向独居石中加入硫酸酸浸时,硫酸将CePO 转化为Ce (SO ) 和
4 2 4 3
H PO ,Fe O 转化为Fe (SO ) ,CaF 转化为CaSO 沉淀和HF 气体,SiO 不参
3 4 2 3 2 4 3 2 4 2
与反应;加入Fe (SO ) 溶液,将溶液中的H PO 转化为FePO 沉淀,过滤得到
2 4 3 3 4 4
滤渣1主要含有难溶性钙盐、FePO 和SiO ;向滤液中加入氨水调节溶液pH,
4 2
将Fe3+、Al3+转化 Fe(OH) 、Al(OH) 沉淀过滤除去,滤渣2主要含有Al(OH)
3 3 3
和Fe(OH) ;再向滤液中加入NH HCO 溶液,将溶液中的Ce3+转化为Ce (CO )
3 4 3 2 3 3
沉淀,过滤得到Ce (CO ) ,最后经焙烧后得到CeO ,据此解答。
2 3 3 2
【解析】(1)为提高“酸浸”的速率,可采取的措施有将独居石粉碎、增大硫酸浓度、
适当升高温度、充分搅拌等。(2)由分析可知,滤渣1的主要成分为难溶性钙盐、
FePO 和SiO ,则滤渣1的主要成分除难溶性钙盐、FePO 外还有SiO 。(3)已知
4 2 4 2
用碳酸氢铵“沉铈”过程中有CO 放出,则结合原子守恒、电荷守恒可知生成
2
Ce (CO ) 时发生的离子方程式为:6HCO 2Ce3 Ce CO 3CO 3H O。
2 3 3 3 2 3 3 2 2
(4)焙烧Ce (CO ) 获得CeO ,铈元素被氧化,需要氧气参与反应,则发生反应
2 3 3 2
高温
的化学方程式为:2Ce 2 (CO 3 ) 3 +O 2 4CeO 2 +6CO 2 。(5)由分析可知,加入氨水调
节pH目的是使溶液中的Fe3+、Al3+转化为 Fe(OH) 、Al(OH) 而除去。当溶液中
3 3
c(Al3+)=1.0x10-6mol/L时,根据K [Al(OH) ]=c(Al3+)×c3(OH-)=1.0 x10-33,则该溶
SP 3
液中 ,pOH= -lgC(OH-)= -lg 10-9=9,则pH=14-
pOH=14-9=5。(6)在CeO 晶胞中,黑球数目为:8× 1 +6× 1 =4,灰球数目为8,
2
8 2
即每个晶胞中有4个CeO ,可知灰球为O2-,黑球为Ce4+,则由晶胞结构图可知,
2
处于面心的铈离子周围最近且等距离的氧离子有4个,根据晶胞无隙并置原则,
在该晶体中,铈离子周围最近且等距离的氧离子的个数为2×4=8。若晶胞边长为
apm,N 为阿伏加德罗常数的值,则CeO 晶体的密度
A 2
4(14032)
N 6.881032 。
A g/cm3 g/cm3
(a1010)3 a3N
A
16.(15分)【答案】(1) 三颈烧瓶(1分) b(2分)
(2) 水浴加热(2分)
+CH CH OH +H O(2分)
3 2 2
(3) 使酯化反应向正反应方向进行,提高苯甲酸的转化率(2分)
(4) 饱和Na CO 溶液(2分) 蒸馏(2分) (5)80(2分)
2 3
【分析】本实验将苯甲酸、乙醇在浓硫酸作催化剂和脱水剂的作用下水浴加热即
可得苯甲酸乙酯粗产品,苯甲酸乙酯粗产中除苯甲酸乙酯外,还含有苯甲酸、乙
醇等溶液,试剂a选用饱和碳酸钠溶液,用于溶解乙醇、消耗苯甲酸、降低苯甲
酸乙酯溶解度,据分析答题。【详解】(1)仪器a 的名称为三颈烧瓶;为了增强
冷凝效果,冷凝管中冷凝水应下进上出,所以装置中冷却水的进口为b。(2)粗产
品制取时所需的温度为70℃左右,且需要均匀受热、便于控制温度,所以采用
第 4 页 共 7 页
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}的加热方式为水浴加热(或保持70℃水浴加热);利用苯甲酸、乙醇在浓硫酸作催
化剂和脱水剂的作用下水浴加热制备苯甲酸异丙酯,化学方程式为:
+CH CH OH +H O。(3)酯化反应为可逆
3 2 2
反应,由于乙醇沸点低易挥发,使乙醇稍过量有利于酯化反应向正反应方向进行,
提高苯甲酸的转化率。(4)粗产品中含有未反应的苯甲酸、乙醇以及生成的水等
杂质 。饱和Na CO 溶液可以与苯甲酸反应将其转化为易溶于水的苯甲酸钠,
2 3
同时能溶解乙醇,降低苯甲酸乙酯在水中的溶解度,便于通过分液分离出苯甲酸
乙酯,所以试剂 a 最好选用饱和Na CO 溶液。经过操作①分液得到的有机层中
2 3
可能还含有少量的其他杂质,由于苯甲酸乙酯与这些杂质沸点不同,可通过蒸馏
的方法进一步提纯,所以操作②的名称是蒸馏。(5)48.8g 苯甲酸的物质的量
n=m/M=48.8g/122g·mol-1=0.4mol,35mL乙醇质量m=ρv=0.79g·cm-3×35mL=27.65g,
乙醇物质的量n=m/M=27.65g/46g·mol-1≈0.6mol,由反应方程式可知乙醇过量,
根据苯甲酸的量计算理论上生成苯甲酸乙酯的物质的量,根据化学计量数之比,
苯甲酸与苯甲酸乙酯物质的量之比为1:1,所以理论上生成苯甲酸乙酯的物质的
量n=0.4mol,则理论上生成苯甲酸乙酯的质量0.4mol×150g/mol=60.0g,则产率
=实际产量/理论产量=48.0g÷60.0g×100%=80%。
17.(14分)【答案】
3
(2分 ( ) 1)CH3O 不 H( 能 g)+ (2 1 O 分 2( ) g) = CO2(g) ( + 1 2 分 H ) 2O(g)△H =−
676.4kJ/mol (2)① ②D
(3) (1分) (2分) (2分) (1分)
4
不
①
(
0
2
.0
分
25
) (4)
②27 50% ③
(
<
2分)
− − 2−
CH3OH−6e +8OH = CO3 +6H2O
【解析】 已知:
(1) ①2H2(g)+O2(g) = 2H2O(g)△H =−483.6kJ/mol
② 盖斯 CH 定3O 律 H 计 (g 算 )+H2O(g) = C 得 O 到2( 甲 g) 醇 + 燃 3H 烧2( 生 g) 成 △H =+4 的 9 热 .0k 化 J/ 学 m 方 ol 程式:
3
②+①×2 H2O(g)
。
3
CH3OH(g)+2O2(g) = CO2(g)+2H2O(g)△H =−676.4kJ/mol
,熵变 ,
( 则 2) 反 ① 应 2 焓 CO 变 (g)+4H2( , g) ⇌ CH3OCH3(l)+ ,不 H2能 O( 满 l) 足 △H =+71kJ/mol ,反应 △ 不 S 能 < 自 0
发进行,故答案为:不能。
△H > 0 △H−T△S > 0 △H−T△S < 0
向 密闭容器中加入 、 ,发生反应:
② 1L 2mol CO 4molH2 2CO(g)+4H2(g) ⇌
。 向 密闭容器中加入 、
CH3OCH3(l)+H2O(l)△H =+71kJ/mol a. 1L 2mol CO
,按照 反应,混合气体的平均相对分子质量始终不变,故不能说达
4
到
m
平
ol
衡
H
状2 态,故
1:2
错误; 起始量和变化量之比相同, 和 的转化率始终相
等,不能说明反应达到平衡状态,故 错误; 由于生成物都是液体,气体体积
a b. CO H2
b c.
第 5 页 共 7 页
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}分数始终不变, 和 的体积分数保持不变不能说明反应达到平衡状态,故
错误; 反应前后气体体积不变,气体质量变化,当混合气体的密度保持不变说
CO H2 c
明反应达到平衡状态,故 正确; 生成的同时有 键断裂,
d.
只能说明反应逆向进行,不能说明正逆反应速率相同,故 错误;故答案为: 。
d e.1mol CO 1mol O−H
, ~ 内氢气物质
e d
(3)①CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g)△H < 0 0 10min
的量变化 ,计算氢气表示的反应速率
1.5mol
2L
6mol−4.,5m速o率l =之1比.5m等o于l 化学方程式计量数之比, v(H2) = 10min =
1
0.075mol/(L⋅min)
,故答案为: 。 图表中计算
v(H
时
2O
二
)
氧
= 化3v
碳
(H
消
2)
耗
=
物质的量 ,同时生成 甲醇, 甲醇物质的量为 ,则
0.025mol/(L⋅min) 0.025 ② 20min
反应达到平衡状态,
1mol 1mol 30min 1mol 20min
起始量
CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g)△H < 0
变化量
(mol/L) 1 3 0 0
平衡量
(mol/L) 0.5 1.5 0.5 0.5
平衡常数 ,氢气转化率 , 在其它条件
(mol/L) 0.5 1.5 0.5 0.5
0.5×0.5 4 1.5mol/L
不变的情况下图表中3平衡状态下氢气物质的量为 ,若 时改变温度为
K = 0.5×1.5 = 27 = 3mol/L ×100% = 50% ③
,此时 的物质的量为 ,正反应为放热反应,说明升温平衡逆向进
3mol 30min
行, ,在其他条件不变的情况下,若 时向容器中再充入
T2℃ H2 3.2mol
和 T1 < T2 , 3 , 0m 说 in 明平衡不动。 1molCO2(g)
0.5×(0.5+0.5) 4
1
若
m
用
ol
甲 H2醚
O(
作
g)
为燃
Qc
料
=
电
(0
池
.5+
的
0.5
原
)×
料
1.5
3,
=
甲
27
醚
=
在
K
负极失电子发生氧化反应,在碱性介
质中电池负极的电极反应式: 。
(4)
− − 2−
CH3OH−6e +8OH = CO3 +6H2O
18.(15分)【答案】(1) 碳氯键 (2分) (2分) 聚苯乙
烯(1分)(2)②⑥(2分) (3)
+NaOH醇 +NaCl+H O(2分)
2
Δ
(4)2 + O Cu/Ag 2 + 2H O(2分)(5) 13 (2分)
2 Δ 2
(2分)
【分析】C H 为乙烯,与HCl发生加成反应得到B为CH CH Cl,B(CH CH Cl)
2 4 3 2 3 2
与苯发生取代反应得到C 为乙苯,乙苯被酸性高锰酸钾溶液氧化为苯甲酸;乙
苯与Cl 光照下反应得到D,D在 NaOH 溶液作用下加热发生取代反应得到
2
第 6 页 共 7 页
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#},可推知D为 ,D在NaOH 醇溶液中加热发生消去反应得
到E , 发生加聚反应得到F 为聚苯乙烯。
【解析】(1) 所含官能团为碳氯键;G 是由乙苯被酸性高锰酸钾溶液
氧化生成的苯甲酸,G的结构简式为 ; 发生加聚反
应得到F 为聚苯乙烯。
(2)步骤①为 B(CH CH Cl)与苯发生取代反应得到 C 为乙苯,反应类型为取代反
3 2
应,②⑥也是取代反应。
(3)反应③D 在NaOH 醇溶液中加热发生消去反应得到E ,化学方
程式为 +NaOH醇 +NaCl+H O。
2
Δ
(4)H 发生氧化反应生成C H O,该反应方程式为2 + O
8 8 2
Cu/Ag2 +2H O。
Δ 2
(5)D 为 ,属于芳香族化合物的侧链可以为:-Cl 和-CH CH ,共3种;
2 3
-CH Cl 和-CH ,共3种;-CH 、-CH 和-Cl,共6种;-CH CH Cl,1种;故共
2 3 3 3 2 2
13种。其中核磁共振氢谱峰面积之比为2:2:2:2:1的结构为 。
第 7 页 共 7 页
{#{QQABTQAAoggIQAJAAQgCAQU4CAGQkAECAYoGRAAQsAAACANABCA=}#}