文档内容
2024 年重庆市普通高中学业水平选择性考试
高三第一次联合诊断检测 化学参考答案
1~5 ADCBC 6~10 BACDD 11~14 BBBD
1.A
2.D
【解析】
A.该方程不是HSO-水解,是HSO-电离;
3 3
B.CO 通入BaCl 溶液中不会生成BaCO 沉淀;
2 2 3
C.Mg(OH) 比MgCO 更难溶,所以碳酸氢镁溶液与足量NaOH溶液反应生成Mg(OH) 。
2 3 2
3.C
【解析】
A.CO 的电子式为: ;
2
B.NH+的VSEPR模型为正四面体形;
4
D.(NH ) SO 既含共价键,又含离子键。
4 2 4
4.B
【解析】
A.浓硝酸见光分解的产物有NO 、O 、H O;
2 2 2
B.K (CaSO )>K (CaCO );所以可转化;
sp 4 sp 3
C.苏打是Na CO ,受热不分解;
2 3
D.铜与S粉在加热条件下反应生成Cu S.
2
5.C
【解析】
A.因为Fe3+要水解,所得溶液中Fe3+的数目小于0.5N ;
A
B.由于生成的NO 一部分转化为N O ,收集到的NO 分子数少于1.5N ;
2 2 4 2 A
D.反应消耗28g Fe粉,生成1.5mol H O,所含共价键数为3N 。
2 A
6.B
【解析】B.第一电离能:I (F)>I (N)>I (C)>I (B)。
1 1 1 1
7.A
【解析】
B.Fe(OH) 胶体可以透过滤纸,过滤不能除去Fe(OH) 胶体中的NaCl;
3 3
C.测溶液的pH时,不能把pH试纸放入溶液中;
D.配制银氨溶液是把氨水滴入AgNO 溶液中。
3
8.C
【解析】根据题意,可知M为Pb,Y为Cu,再由M Y (XW ) W和化合价守恒可知X是P,W是O。
(10-x) x 4 6
A.简单氢化物的稳定性:H O>PH ;
2 3
B.原子半径:Pb>Cu>P;
C.Cu与浓硫酸在加热条件下,可以生成SO 气体;
2
D.X是P,P元素最高价氧化物对应的水化物不属于强酸。
第一次联合诊断检测(化学)参考答案 第5页 共9页9.D
【解析】
A.a、b两点的温度相同,两点的K 相等;
w
B.由图可知,等浓度等体积的HCl溶液与NaOH溶液的导电能力不相同;
C.c、d两点的溶质分别为NaCl、CH COONa,c点有:c(Na+)+c(H+)=c(Cl-)+c(OH-),
3
d点有:c(Na+)+c(H+)=c(CH COO-)+c(OH-),由于CH COONa溶液呈碱性,c(OH-)>c(H+),
3 3
故NaCl溶液中的c(H+)大于CH COONa溶液中的c(H+),两种溶液中c(Na+)一样大,c点溶液中阴离子总浓
3
度大于d点溶液中阴离子总浓度;
D.e点是等物质的量的CH COONa和CH COOH的混合溶液,
3 3
由电荷守恒得c(Na+)+c(H+)=c(CH COO-)+c(OH-),
3
由物料守恒得,2c(Na+)=c(CH COO-)+c(CH COOH),
3 3
联合得:2c(H+)+c(CH COOH)=2c(OH-)+c(CH COO-)。
3 3
10.D
【解析】
A.G的分子式为C H O ;
8 14 2
B.F是醇,与NaOH不发生反应;
C.G和H反应生成M的反应类型为加聚反应;
D.M中左边酯基有m个,右边酯基有n个,1mol M完全水解,需要H O的物质的量为(m+n)mol。
2
11.B
【解析】由题意可知,该电池是金属钠失电子,放电时N为负极,M为正极。
A.放电时Na+应由N极迁移至M极;
C.充电时,M极为阳极,发生氧化反应;
D.充电时,每消耗1mol Na V (PO ) ,转移2mol电子,理论上生成46g Na。
3 2 4 3
12.B
【解析】
A.由图2可知,FeCu N能量高于Fe CuN,故稳定性FeCu N比Fe CuN差;
3 3 3 3
C.基态N原子核外电子排布为1s22s22p3,核外电子的空间运动状态有5种;
D.获取晶体结构信息的是X射线衍射仪。
13.B
【解析】
A.盐酸不是氯元素的最高价含氧酸,所以A结论不能由此判断;
C.NaHCO 溶液中同时存在HCO-的电离和水解,不能通过pH直接比较HCO-和CH COO -的水解平衡常数;
3 3 3 3
D.NaOH溶液与MgCl 反应后,NaOH过量,再滴加CuCl 溶液生成蓝色沉淀,不能说明是Mg(OH) 转化成
2 2 2
Cu(OH) 。
2
14.D
【解析】由于K =1,容器中CO和CO 的分压是相等的,都为800kPa。
p1 2
A.反应②的平衡常数为K =p(CO)=800 kPa;
p
B.由于容器体积不变,当气体密度不变时,说明CO和CO 的质量不改变,反应都达到平衡;
2
C.温度不变,K 不变,CO和CO 的平衡分压均为800 kPa不变,容器内总压强不变;
p 2
D.温度不变,K 不变,CO和CO 的平衡分压均为800 kPa不变。
p 2
第一次联合诊断检测(化学)参考答案 第6页 共9页15.(14分)
3d
(1) (1分) 平面三角形(1分)
(2)搅拌、粉碎、适当升温、适当增加酸的浓度等(2分)
盐酸与二氧化锰会发生反应,电解制锰时会产生污染气体(2分)
(3)MnO +2Fe2++4H+=Mn2++2Fe3++2H O(2分)
2 2
(4)Fe(OH) (2分)
3
(5)Ni2+(2分) 10<pS≤19(2分)
【解析】
(1)Mn为25号元素,价电子排布式为3d54s2,Mn2+在此基础上失去最外层电子,故为3d5;CO2-的中心原子
3
无孤电子对,3个σ键电子对,故为sp2杂化,空间结构为平面三角形。
(2)盐酸可能会与二氧化锰发生氧化还原反应,同时引入的氯离子在最后电解制锰时会在阳极放电,从而生成
污染气体氯气。
(4)根据金属氢氧化物的溶度积数据可知,调节pH 为4左右,目的是为了除去 Fe3+,故滤渣2的主要成分是
Fe(OH) 。
3
(5)结合金属硫化物的溶度积常数数据可知,加入适量的(NH ) S除去的主要离子是Ni2+,此时硫离子需要刚
4 2
好完全沉淀Ni2+但不能沉淀Mn2+;根据NiS和MnS的K 数据可计算出pS的范围是10<pS≤19。
sp
16.(14分)
(1)三颈烧瓶(1分) 无水氯化钙(或碱石灰、五氧化二磷固体)(1分)。
(2)f g a b d e h(2分)
(3)将装置内的NO全部赶入Ⅵ中除去(1分)
(4)铜片表面有气泡产生,铜片不断变小,溶液变蓝(2分)
(5)防止Ⅵ中的水蒸气进入Ⅲ装置中(1分)
(6)2NO+Cr O2-+6H+=2Cr3++2NO-+3H O(2分)
2 7 3 2
205a49.2bV 82(25a6bV)
(7)①NaNO +NH Cl N ↑+NaCl+2H O (2分) ② % [或 100%](2分)
2 4 2 2
3m 3000m
【解析】
(7)②还原NO-的反应为:NO-+3Fe2++4H+=3Fe3++NO↑+2H O,
3 3 2
滴定Fe2+的反应为:6Fe2++Cr O2-+14H+=6Fe3++2Cr3++7H O。
2 7 2
1 1 1
n(NO-)= (25103a6V 103b),m[Ca(NO ) ]= (25103a6V 103b)164
3 3 3 2 2 3
205a49.2bV 82(25a6bV)
Ca(NO ) 的质量分数= %或 100%
3 2
3m 3000m
17.(15分)
(1)③(1分) -7.69kJ/mol(2分)
25
(2)X(1分) a(1分) 4.2(或 )(2分)
6
280℃前以反应①为主,随温度升高二氧化碳转化率下降,280℃后以反应②为主,随温度升高二氧化碳转
化率升高(2分)
(3)氢键、分子间作用力(或范德华力)(2分) 23︰45(2分)
第一次联合诊断检测(化学)参考答案 第7页 共9页(4)H +CO2--2e-=H O+CO (2分)
2 3 2 2
【解析】
(1)③的活化能最大,反应速率最慢,因此为决速步。
由中间产物T2到产物的∆H=-[5.31-(-2.38)]=-7.69kJ/mol。
(2)反应①放热,随温度升高,反应逆向移动,而反应②吸热,随温度升高,反应正向移动,故甲醇的选择性
随温度升高而降低,与这个变化一致的是X曲线。
a、c两点CO 转化率相等,但a点甲醇选择性更高,故甲醇产率更高。
2
恒容密闭容器中,起始时物质的分压p(CO )=10MPa,p(H )=11.2MPa,
2 2
a点时CO 转化率为40%,甲醇选择性为80%,故反应①、②有如下转化:
2
CO (g) + 3H (g) CH OH(g) + H O(g)
2 2 3 2
起始 10MPa 11.2MPa 0 0
转化 3.2MPa 9.6MPa 3.2MPa 3.2MPa
CO (g) + H (g) CO(g) + H O(g)
2 2 2
起始 10MPa 11.2MPa 0 0
转化 0.8MPa 0.8MPa 0.8MPa 0.8MPa
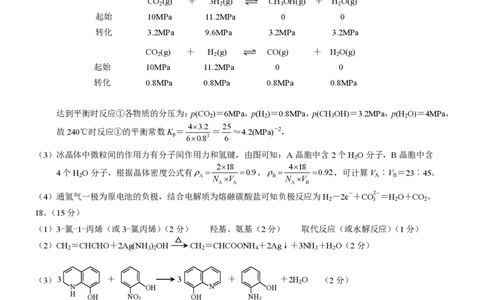
达到平衡时反应①各物质的分压为:p(CO )=6MPa,p(H )=0.8MPa,p(CH OH)=3.2MPa,p(H O)=4MPa,
2 2 3 2
43.2 25
故240℃时反应①的平衡常数K = = ≈4.2(MPa)-2,
p 60.83 6
(3)冰晶体中微粒间的作用力有分子间作用力和氢键,由图可知:A晶胞中含2个H O分子,B晶胞中含
2
218 418
4个H O分子,根据晶体密度公式有 0.9, 0.92,可计算V ︰V =23︰45。
2 A N V B N V A B
A A A B
(4)通氢气一极为原电池的负极,结合电解质为熔融碳酸盐可知负极反应为H -2e-+CO2-=H O+CO 。
2 3 2 2
18.(15分)
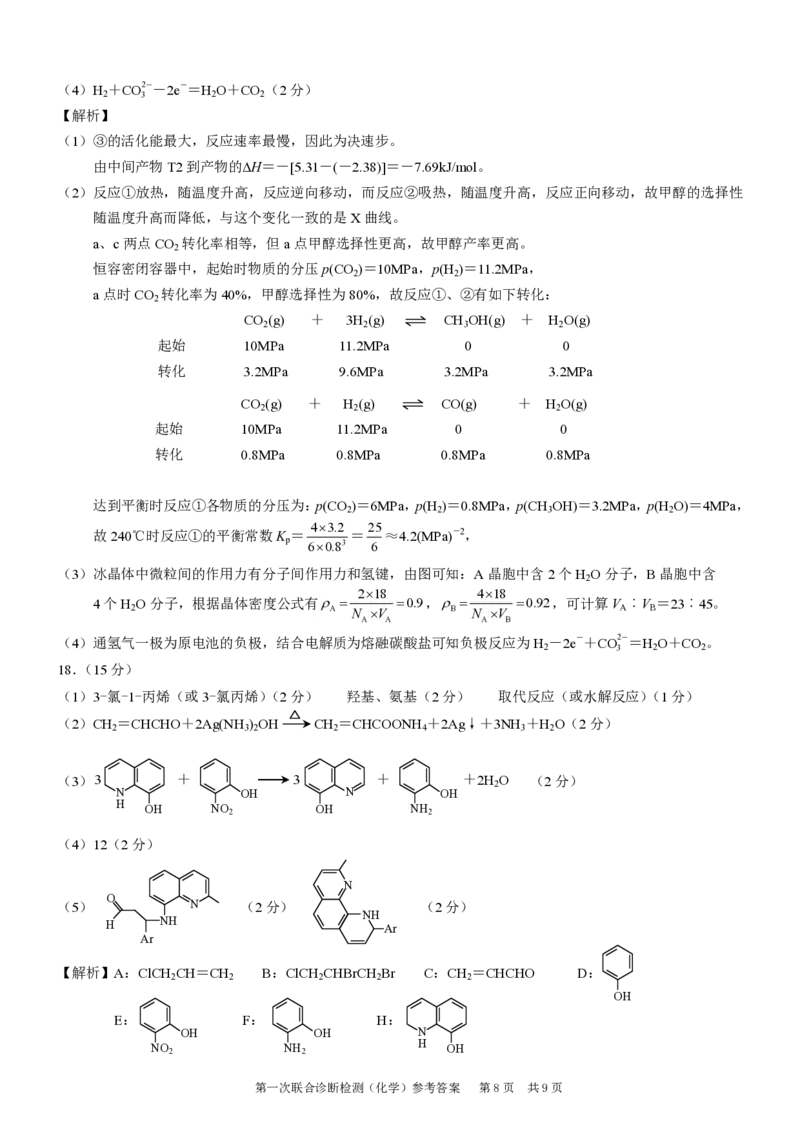
(1)3-氯-1-丙烯(或3-氯丙烯)(2分) 羟基、氨基(2分) 取代反应(或水解反应)(1分)
(2)CH =CHCHO+2Ag(NH ) OH CH =CHCOONH +2Ag↓+3NH +H O(2分)
2 3 2 2 4 3 2
(3) 3 + 3 + + 2 H O (2分)
2
N OH N OH
H
OH NO
2
OH NH
2
(4)12(2分)
NN
O
(5) N (2分) (2分)
NH
H
Ar
NH Ar
【解析】A:ClCH CH=CH B:ClCH CHBrCH Br C:CH =CHCHO D:
2 2 2 2 2
OH
E: F: + H:
OH OH N
H
NO NH OH
2 2
第一次联合诊断检测(化学)参考答案 第8页 共9页(4)苯环上只有两个取代基,有邻、间、对三种位置,符合条件的,只下列四种情况:
①-OH,-CH CH(NH )CHO有3种;
2 2
②-OH,-CH(NH )CH CHO有3种;
2 2
③-OH,-C(NH )(CH )CHO有3种;
2 3
④-OH,-CH(CHO)CH NH 有3种,共12种。
2 2
第一次联合诊断检测(化学)参考答案 第9页 共9页