文档内容
辽宁·高二化学 第1
页(共5页)
辽宁省2024—2025学年度(下)重点高中联合体高二年级期末检测
化学参考答案
1.【答案】A
【解析】油脂不属于高分子,A项错误;果糖和葡萄糖的化学式均为C6H12O6,二者互为同分异构体,B项正确;蛋
白质既能与酸反应,又能与碱反应,为两性分子,C项正确;“北燕鸭形玻璃注”的主要成分为硅酸盐,属于无机非
金属材料,D项正确。
2.【答案】C
【解析帨
師
師
】
O
NH2属于酰胺类化合物,A项错误;NaOH的电子式为Na
+[·
· O
··
··
·
·H]
-,B项错误;NH3的空间填
充模型为
,C项正确
師
師
帩
;
O
NH2
師
師
帩
能与热的盐酸反应生成
COOH和NH4Cl,D项错误。
3.【答案】B
【解析】实验室提纯含有少量氯化钠和泥沙的苯甲酸的方法为重结晶,涉及的操作为加热溶解、趁热过滤、冷却结
晶,B项符合题意。
4.【答案】D
【解析】甲烷是一种温室气体,A项正确;硫化剂将聚合物中的双键打开,以二硫键等把线型结构连接为网状结
构,得到既有弹性又有强度的顺丁橡胶,B项正确;醋酸酸性强于碳酸,能与水垢中的CaCO3反应,C项正确;淀
粉水解为葡萄糖,葡萄糖在酒曲的催化下转变为乙醇,D项错误。
5.【答案】A
【解析】M的名称为2-甲基丁酸乙酯,A项正确;M的物质的量未知,B项错误;M与油脂不互为同系物,C项错
误;M属于酯类,难溶于水,D项错误。
6.【答案】C
【解析】会引入新的杂质H2,A项错误;醛基也能使溴水褪色,B项错误;加入CaO,将H2O转化为Ca(OH)2,然后
蒸馏,可以获得乙醇,C项正确;甲苯和环己烯均能使酸性KMnO4溶液褪色,D项错误。
7.【答案】C
【解析】“水洗1”是为了除去易溶于水的FeBr
3、HBr,不能除去剩余的苯,A项错误;“水洗1”之后溶液分层,“操
作1”为分液,B项错误;“碱洗”的目的是将Br
2转化为易溶于水的NaBr和NaBrO,便于在“水洗2”时除去,C项
正确;加入CaCl
2的目的干燥溴苯,D项错误。
8.【答案】A
【解析】28gCH2
CH2
的物质的量为1
nmol,含有的碳原子数为1
n×2n×NA=2NA,A项正确;在标准状况下,
氯仿(CHCl
3)不是气态,无法通过气体摩尔体积计算其物质的量,B项错误;1mol—OH含有的电子总数为9NA,
C项错误;9.3g苯胺帨
師
師
(
NH2
)的物质的量为0.1mol,含有σ键总数为1.4NA,D项错误。
辽宁·高二化学 第2
页(共5页)
9.【答案】B
【解析】该反应为缩聚反应,A项错误;BHET含有酯基,能发生水解反应,与羟基相连的碳的相邻碳上有氢原子,
能发生消去反应,B项正确;根据质量守恒定律可知EG为HOCH2CH2OH,C项错误;PET含有酯基,在强酸、强
碱性环境中会水解,因此PET不能用于长时间保存强酸、强碱性物质,D项错误。
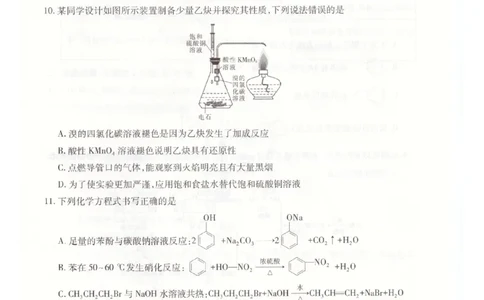
10.【答案】D
【解析】饱和硫酸铜溶液能除去乙炔中的H2S等杂质,溴的四氯化碳溶液褪色是因为乙炔与溴发生了加成反
应,酸性KMnO4溶液褪色说明乙炔将KMnO4还原,A、B项均正确;乙炔中碳元素的质量分数很大,燃烧时火焰
明亮且有大量黑烟,C项正确;若用饱和食盐水替代饱和硫酸铜溶液,会有H2S等杂质干扰实验,D项错误。
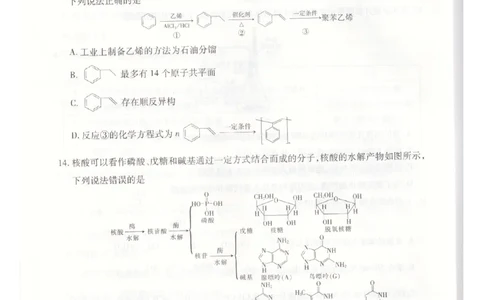
11.【答案】B
【解析】苯酚与碳酸钠溶液反应不能生成CO2,A项错误;在浓硫酸作用下,苯在50~60℃与浓硝酸发生硝化反
应生成硝基苯,B项正确;CH3CH2CH2Br与NaOH水溶液共热会发生水解反应:CH3CH2CH2Br+NaOH
H2O
→
△
CH3CH2CH2OH+NaBr,C项错误;油脂在碱性溶液中的水解反应称为皂化反应,题中化学方程式为油酸甘油酯
的氢化反应,D项错误。
12.【答案】C
【解析】在碱催化下,苯酚与过量的甲醛反应生成网状结构的酚醛树脂,A项正确;具有网状结构的酚醛树脂受
热后不能软化或熔融,B项正确;当苯酚不慎沾到皮肤上时,应立即用乙醇冲洗,再用水冲洗,若用70℃水洗
涤,会烫伤皮肤,C项错误;常温下苯酚为固体,取用苯酚时可把试剂瓶放入温水中待苯酚熔化后,趁热取出液
态的苯酚,D项正确。
13.【答案】B
【解析】工业上常利用石油裂解的方法制备乙烯,A项错误;单键可以旋转帨
師
師
,
最多有14个原子(用黑色
球标记)在同一平面上:
,B项正确帨
師
師
;
中碳碳双键的一端碳原子连接两个氢原
子,不存在顺反异构,C项错误;反应③的化学方程式为帨
師
師
n
→
一定条件
!
,D项错误。
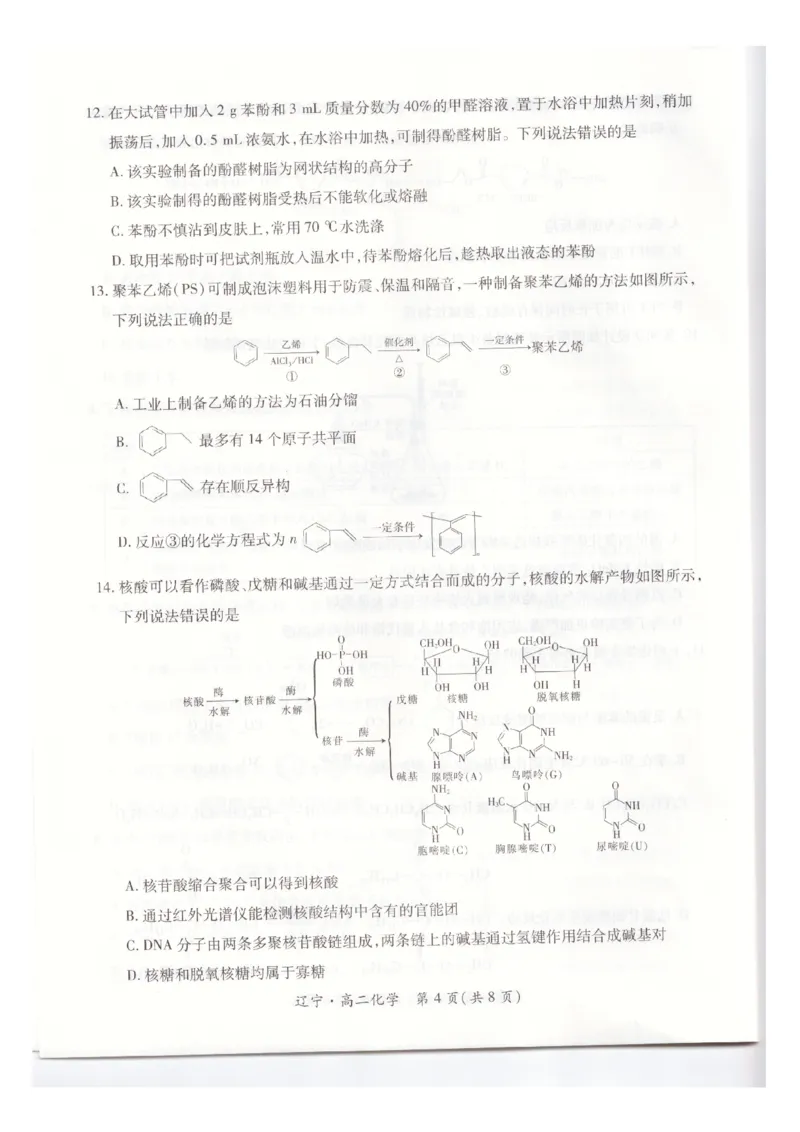
14.【答案】D
【解析】核苷与磷酸缩合形成了组成核酸的基本单元———核苷酸,核苷酸缩合聚合可以得到核酸,A项正确;通
过红外光谱仪能检测核酸结构中含有的官能团的种类,B项正确;DNA分子由两条多聚核苷酸链组成,两条链
上的碱基通过氢键作用,腺嘌呤(A)与胸腺嘧啶(T)配对,鸟嘌呤(G)与胞嘧啶(C)配对,结合成碱基对,C项正
确;1mol糖水解后能产生2~10mol单糖的称为寡糖或低聚糖,核糖和脱氧核糖均属于单糖,不属于寡糖,D项
错误。
15.【答案】C
【解析】没有中和多余的酸,故未观察到银镜不能证明没有葡萄糖生成,A项错误;含有苯环的蛋白质能与浓硝
辽宁·高二化学 第3
页(共5页)
酸发生显色反应,B项错误;KMnO4被草酸还原,是因为HOOC—COOH中两个—COOH直接相连导致C—C键
电子云密度降低,易被氧化断裂,C项正确;甘油含有羟基,能与Na反应产生H2,D项错误。
16.【答案】(1)①防止暴沸(1分,相似描述即可) ②催化剂(1分,唯一答案)
③a.Ⅱ(1分,有错不得分) b.Ⅰ和Ⅱ(2分,漏选、错选不得分)
④乙醇可能被浓硫酸炭化,C与浓硫酸反应生成的SO2也能使溴水褪色(2分,体现SO2能使溴水褪色即可
得分)
(2)①CH
2
CH2+Br
→
2
BrCH2CH2Br(2分,物质、配平错误不给分,键线式等合理形式均可
→
,
写成等号扣
1分)
②溶液中发生反应Br
2+H2幑幐
O
H
++Br
-+HBrO,Br
2与乙烯反应后,Br
2浓度减小,平衡逆向移动,溶液pH
变大(2分,写出方程式1分,平衡逆向移动1分)
③不是(1分,唯一答案)
④CH
2
CH2+H2O+Br
→
2
BrCH2CH2OH+HBr(2分,键线式等合理形式均可
→
,
写成等号扣1分)
【解析】(1)①加热溶液时加入碎瓷片可防止暴沸。②浓硫酸的作用是做脱水剂和催化剂。③根据乙醇和有机
产物的结构可分析键的断裂情况:a.乙醇制备溴乙烷断Ⅱ键;b.乙醇和浓硫酸混合后控制温度在140℃下发生
反应生成乙醚断Ⅰ和Ⅱ键。④乙醇可能被浓硫酸炭化,C与浓硫酸反应生成的SO2也能使溴水褪色,不能证明
生成了乙烯。
(2)①乙烯和Br
2发生加成反应生成1,2-二溴乙烷的化学方程式为CH
2
CH2+Br
→
2
BrCH2CH2Br。②溶液
中发生反应Br
2+H2幑幐
O
H
++Br
-+HBrO,Br
2与乙烯反应后,平衡逆向移动,溶液pH变大。③实验现象与预测
现象不符,乙烯与溴水反应的主要产物不是1,2-二溴乙烷。④溶液不分层,有机产物易溶于水,结合水参与了
反应,有机产物有两种官能团,除碳溴键外还有亲水的羟基,同时生成HBr导致溶液pH降低,故乙烯与溴水反
应的总反应方程式为CH
2
CH2+H2O+Br
→
2
BrCH2CH2OH+HBr。
17.【答案】(1)环己醇(1分)
HO
OH(1分,或HOCH2CH2OH等合理表示) C3H5(1分) sp
2、sp
3(2分,1
个1分)
(2)2(2分)
(3)浓硫酸,170℃(2分,试剂1分,条件1分)
(4帪
)
(2分)
(5)
n
COOH
COOH+n
HO
OH
催化剂
幑
幐
帯
△
HOC(CH2)4COOCH2CH2O
O
H+(2n-1)H2O(2分,物质、配平错误
不给分,条件和幑幐
“
”最多扣1分)
【解析】(1)G的名称为环己醇,CH3CH2OH发生消去反应生成CH
2CH2,CH
2CH2与Br
2发生加成反应生成
CH2BrCH2Br,CH2BrCH2Br发生水解反应生成HOCH2CH2OH帪
;
的分子式为C6H10,实验式为C3H5
;
COOH
COOH中,羧基上的碳原子为sp
2杂化,其余碳原子为sp
3杂化。
(2)
1mol
COOH
COOH中含有2mol羧基,与足量NaHCO3溶液反应生成2molCO2。
辽宁·高二化学 第4
页(共5页)
(3)CH3CH2OH在浓硫酸的作用下,加热至170℃时发生消去反应生成CH
2CH2。
(4帪
)
能与1,3-丁二烯发生第尔斯-阿尔德反应帪
:
+
→
帪
△
。
(5)己二酸与乙二醇发生缩聚反应生成聚己二酸乙二酯:
n
COOH
COOH+n
HO
OH
催化剂
幑
幐
帯
△
HOC(CH2)4COOCH2CH2O
O
H+(2n-1)H2O。
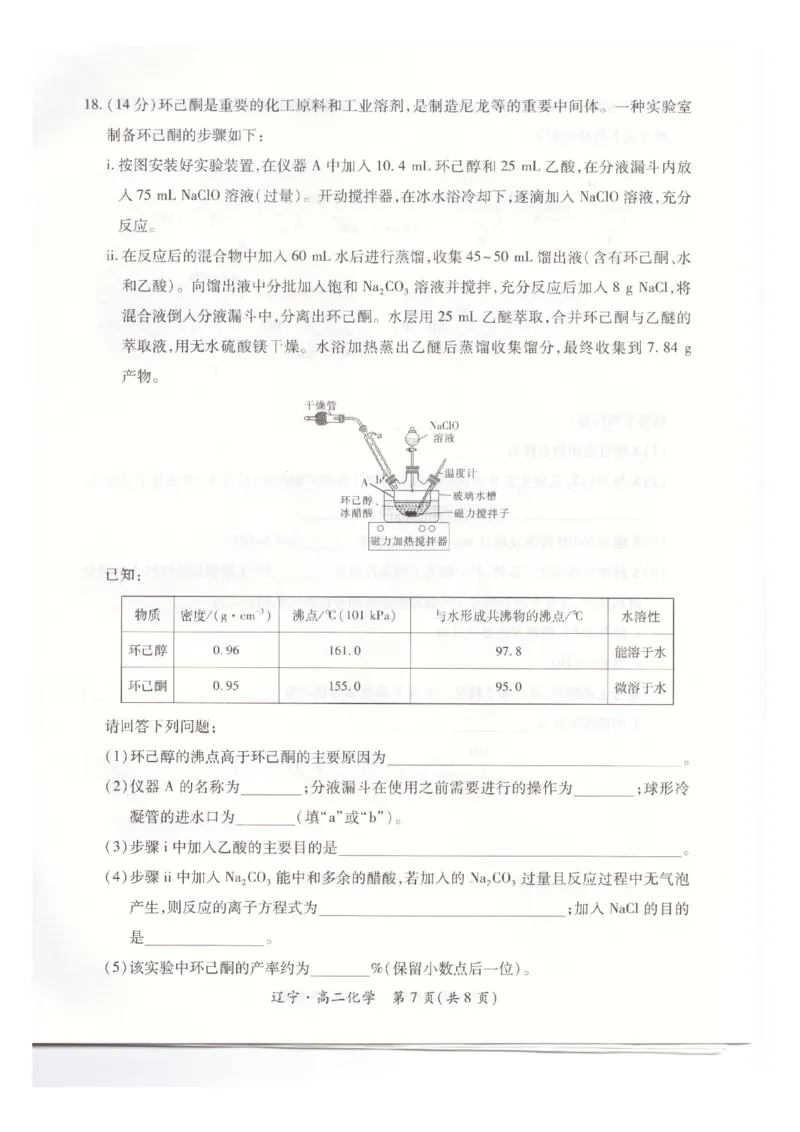
18.【答案】(1)环己醇能形成分子间氢键(2分)
(2)三颈烧瓶(2分,写三口烧瓶不扣分) 检验是否漏液(1分) b(1分)
(3)将ClO
-转化为氧化性更强的HClO(2分,类似表述即可)
(4)CO
2-
3+CH3
COOH
HCO
-
3+CH3COO
-(2分,物质、配平错误不给分) 增强水溶液的极性,降低环己酮在
水中的溶解度,减少环己酮的损耗(2分,答到降低环己酮在水中的溶解度,减少环己酮的损耗给1分)
(5)80.1(2分)
【解析】(1)环己醇能形成分子间氢键,而环己酮不能形成分子间氢键,故环己醇的沸点高于环己酮。
(2)分液漏斗使用之前需要检验是否漏液;冷凝水从下口进、上口出会使冷凝效果更好。
(3)HClO的氧化性强于ClO
-,加入醋酸可以使ClO
-转化为HClO,提高氧化能力。
(4)醋酸是弱酸,不能拆写成离子形式,反应过程中无气泡产生,说明生成了HCO
-
3,反应的离子方程式为CO
2-
3+
CH3
COOH
HCO
-
3+CH3COO
-;丙酮在极性强的溶剂中溶解度更小,往水中加入NaCl,能增强水溶液的极性,
降低环己酮在水中的溶解度,减少环己酮的损耗。
(5)环己酮的产率为
7.84g
10.4×0.96
100
mol×98g·mol
-1
×100%≈80.1%。
19.【答案】(1)(酚)羟基、(酮)羰基(2分,1个1分)
(2
帨
師
師
)
HO
O
+SO2Cl
→
帨
師
師
2
HO
O
Cl
+SO2↑+HCl↑(2分,物质、配平错误不给分,未写“↑”不
扣分) 取代反应(1分,少写“反应”不给分)
(3)2(2分)
(4)13(2分)
師
師
帩
HO
CHO
(2分)
(5)2
OH
+O2
Cu→
△2
O
+2H2O(2分,物质、配平错误不给分,条件和
→
“
”最多扣1分)帨
師
師
N
O
(1分)
【解析】(2)A
帨
師
師
(
HO
O
)与SO2Cl
2发生取代反应生成B
帨
師
師
(
HO
O
Cl
)、SO2和HCl
帨
師
師
:
HO
O
+
SO2Cl
→
帨
師
師
2
HO
O
Cl
+SO2↑+HCl↑。
辽宁·高二化学 第5
页(共5页)
(3)B
帨
師
師
(
HO
O
Cl
)含有酚羟基和碳氯键,1molB最多能消耗2molNaOH
帨
師
師
:
HO
O
Cl
+2NaOH
水→
帨
師
師
△
NaO
O
OH
+NaCl+H2O。
(4)A的同分异构体中,能与FeCl
3溶液发生显色反应,说明含有酚羟基,同时要满足含有醛基,则其同分异构
師
師
帩
体有
HO
CHO
師
師
帩
、
HO
CHO
師
師
帩
、
HO
CHO
師
師
帩
、
HO
CHO
師
師
帩
、
HO
CHO
師
師
帩
、
HO
CHO
師
師
帩
、
HO
OHC
師
師
帩
、
HO
OHC
師
師
帩
、
HO
CHO
師
師
帩
、
HO
CHO
師
師
帩
、
HO
OHC
師
師
帩
、
HO
OHC
師
師
帩
、
HO
CHO
,共13种;上述13种满足条件的A的同分异构体中,只有5种不同化学环境
師
師
帩
的氢原子的有机物的结构简式为
HO
CHO
。
(5)根据题干信息可推测C
帨
師
師
为
N
H
,则合成Y的路线为
OH
Cu/O2→
△
O
SO2Cl
→
2
O
帨
師
師
Cl
N
→
帨
師
師
H
N
O
,X、Y分别为
O
帨
師
師
、
N
O
。
OH
催化氧化生成
O
的化学方程式为
2
OH
+O2
Cu→
△2
O
+2H2O。