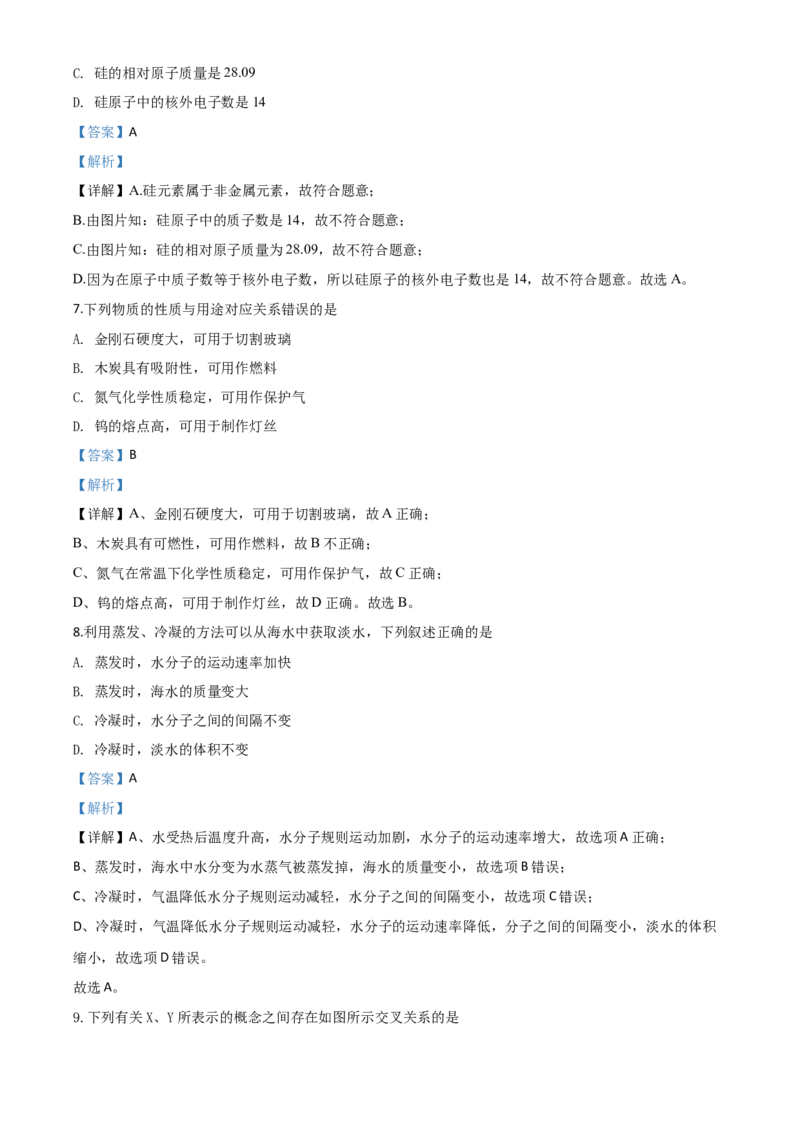文档内容
2020 年无锡市初中学业水平考试
化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 K-33 Co-59
第I卷(选择题共15分)
选择题(本题包括15小题,每小题只有1个选项符合题意,每小题1分,共15分)
1.新能源的开发利用是人类社会可持续发展的重要课题。下列属于新能源的是
A. 天然气 B. 石油 C. 氢气 D. 煤
【答案】C
【解析】
【分析】
根据人类正在开发利用的新能源分析。
【详解】新能源包括太阳能、核能、风能、氢能等;而煤、石油、天然气是化石燃料,属于常规能源。故
选C。
2.空气中最多的气体是
A. O B. N C. CO D. H O
2 2 2 2
【答案】B
【解析】
【详解】空气中各成分的体积分数:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体
和杂质0.03%。
故选B。
3.下列物质属于氧化物的是
A. O
2
B. PO
2 5
C. HCO
2 3
.
D KClO
3
【答案】B
【解析】
【详解】氧化物是由两种元素组成且其中一种是氧元素的化合物。
A.只有一种元素是单质,故错误;
B.有两种元素且一种是氧元素,故正确;
C.有三种元素,故错误;D.有三种元素,故错误。故选B。
4.下列化肥属于复合肥料的是
A. KCl
B. Ca (PO )
2 4 3
C. KNO
3
D. CO(NH)
2 2
【答案】C
【解析】
【详解】A.氯化钾中含钾元素是钾肥,故错误;
B.磷酸钙中含磷元素是磷肥,故错误;
C.硝酸钾中含钾元素和氮元素,是复合肥,故正确;
D.尿素中含氮元素是氮肥,故错误。故选C。
【点睛】利用含两种或两种以上营养元素的化学肥料称之为复合肥来解答。
5.下列化学用语所表达的意义正确的是
A. C ——60个碳原子
60
.
B 2O——2个氧分子
2
C. Fe2+——1个铁离子
D. 3N——3个氮元素
【答案】B
【解析】
【详解】A、由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,
则C 表示1个碳60分子或1个个碳60分子含有60个碳原子,故A不正确;
60
B、2O 表示2个氧分子,故B正确;
2
C、Fe2+表示1个亚铁离子,故C不正确;
D、3N表示3个氮原子,故D不正确。故选B。
6.5G时代已经来临,高纯度单质硅(Si)是制作芯片的材料,如图是硅元素在元素周期表中的信息,下列
叙述错误的是
A. 硅属于金属元素
B. 硅原子中的质子数是14C. 硅的相对原子质量是28.09
D. 硅原子中的核外电子数是14
【答案】A
【解析】
【详解】A.硅元素属于非金属元素,故符合题意;
B.由图片知:硅原子中的质子数是14,故不符合题意;
C.由图片知:硅的相对原子质量为28.09,故不符合题意;
D.因为在原子中质子数等于核外电子数,所以硅原子的核外电子数也是14,故不符合题意。故选A。
7.下列物质的性质与用途对应关系错误的是
A. 金刚石硬度大,可用于切割玻璃
B. 木炭具有吸附性,可用作燃料
C. 氮气化学性质稳定,可用作保护气
D. 钨的熔点高,可用于制作灯丝
【答案】B
【解析】
【详解】A、金刚石硬度大,可用于切割玻璃,故A正确;
B、木炭具有可燃性,可用作燃料,故B不正确;
C、氮气在常温下化学性质稳定,可用作保护气,故C正确;
D、钨的熔点高,可用于制作灯丝,故D正确。故选B。
8.利用蒸发、冷凝的方法可以从海水中获取淡水,下列叙述正确的是
A. 蒸发时,水分子的运动速率加快
B. 蒸发时,海水的质量变大
C. 冷凝时,水分子之间的间隔不变
D. 冷凝时,淡水的体积不变
【答案】A
【解析】
【详解】A、水受热后温度升高,水分子规则运动加剧,水分子的运动速率增大,故选项A正确;
B、蒸发时,海水中水分变为水蒸气被蒸发掉,海水的质量变小,故选项B错误;
C、冷凝时,气温降低水分子规则运动减轻,水分子之间的间隔变小,故选项C错误;
D、冷凝时,气温降低水分子规则运动减轻,水分子的运动速率降低,分子之间的间隔变小,淡水的体积
缩小,故选项D错误。
故选A。
9.下列有关X、Y所表示的概念之间存在如图所示交叉关系的是选项 A B C D
X 金属 纯净物 盐 化合反应
概念
Y 单质 混合物 碳酸盐 氧化反应
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、单质可分为金属单质和非金属单质,单质与金属属于包含关系,不属于交叉关系,不符合题
意;
B、物质可分为纯净物和混合物,纯净物和混合物属于并列关系,不属于交叉关系,不符合题意;
C、盐可分类硫酸盐、碳酸盐、硝酸盐等,盐和碳酸盐属于包含关系,不属于交叉关系,不符合题意;
D、有氧气参加的化合反应是氧化反应,氧化反应不一定是化合反应,化合反应也不一定是氧化反应,故
两者属于交叉关系,符合题意。故选D。
10.在给定条件下,下列物质间的转化不能一步实现的是
A.
B.
C.
D.
【答案】B
【解析】
【详解】A、硫在氧气中点燃生成二氧化硫,可以一步实现,故A正确;
B、二氧化碳没有还原性,不能还原三氧化三铁,故B不正确;
C、水通电生成氢气和氧气,可以一步实现,故C正确;
D、铝和氧气生成氧化铝,可以一步实现,故D正确。故选B。
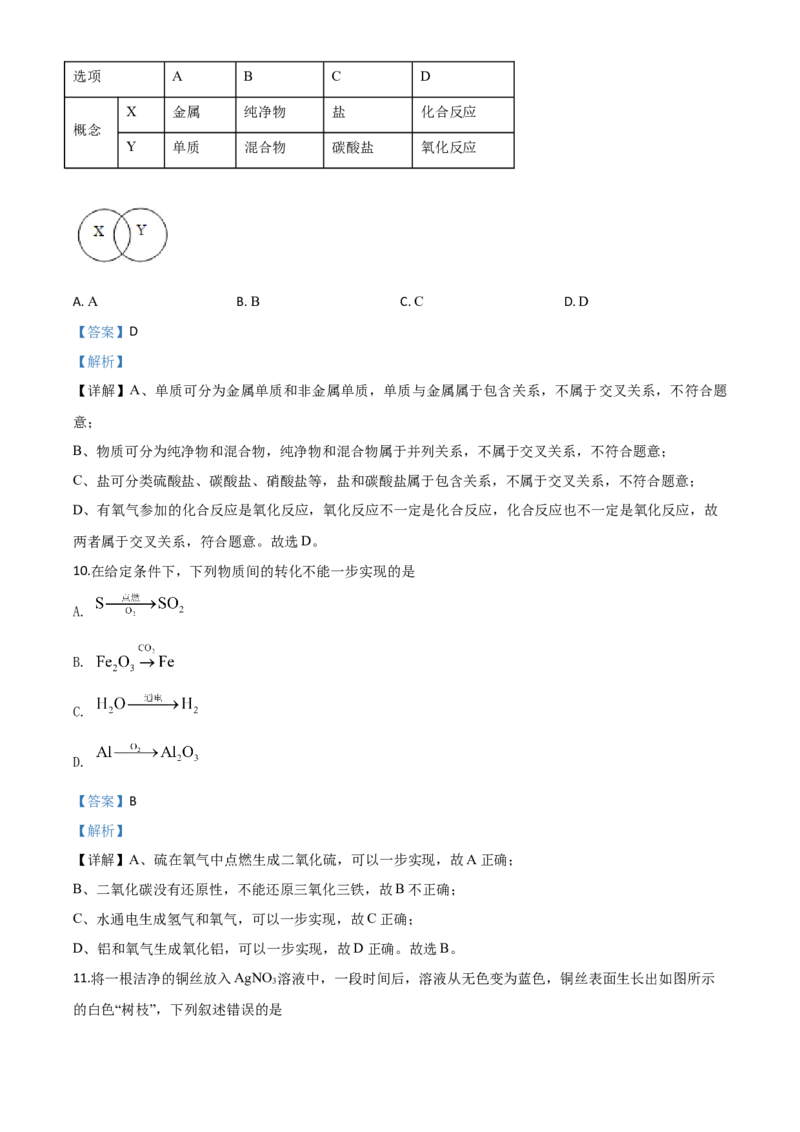
11.将一根洁净的铜丝放入AgNO 溶液中,一段时间后,溶液从无色变为蓝色,铜丝表面生长出如图所示
3
的白色“树枝”,下列叙述错误的是A. 白色“树枝”的成分是银
B. 溶液变为蓝色,表明Cu转变为Cu2+
C. 所得溶液中肯定不含有Ag+
D. 铜的金属活动性比银的强
【答案】C
【解析】
【详解】A、硝酸银和铜反应生成银和硝酸铜,白色“树枝”的成分是银,故正确;
B、硝酸银和铜反应生成银和硝酸铜,溶液由无色变为蓝色,是由于生成的硝酸铜能解离出铜离子,故正
确;
C、如果铜被银包裹起来不能和硝酸银接触,不能将硝酸银中的银离子全部置换出来,溶液中会含有Ag+,
故错误;
的
D、铜能够置换硝酸银中 银,说明铜的金属活动性比银的强,故正确。
故选:C。
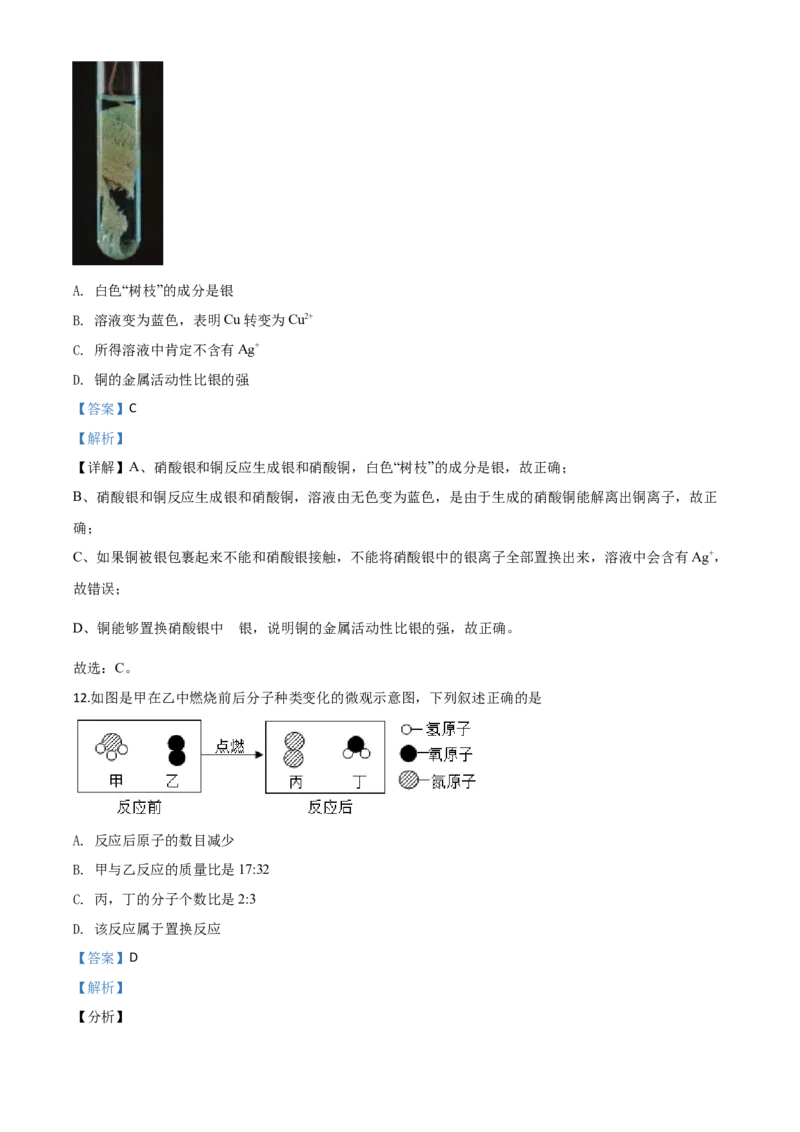
12.如图是甲在乙中燃烧前后分子种类变化的微观示意图,下列叙述正确的是
A. 反应后原子的数目减少
B. 甲与乙反应的质量比是17:32
C. 丙,丁的分子个数比是2:3
D. 该反应属于置换反应
【答案】D
【解析】
【分析】由粒子模型图可知该反应的化学方程式为:4NH +3O 2N +6H O
3 2 2 2
【详解】A.化学反应前后相同元素的原子数目不变,故错误;
B.参加反应的甲与乙的质量比为:(4×17):(3×32)=17:24,故错误;
C.丙与丁的分子个数比就是反应的化学计量数之比:2:6=1:3,故错误;
D.该反应是单质与化合物生成单质与化合物,所以属于置换反应,故正确。故选D。
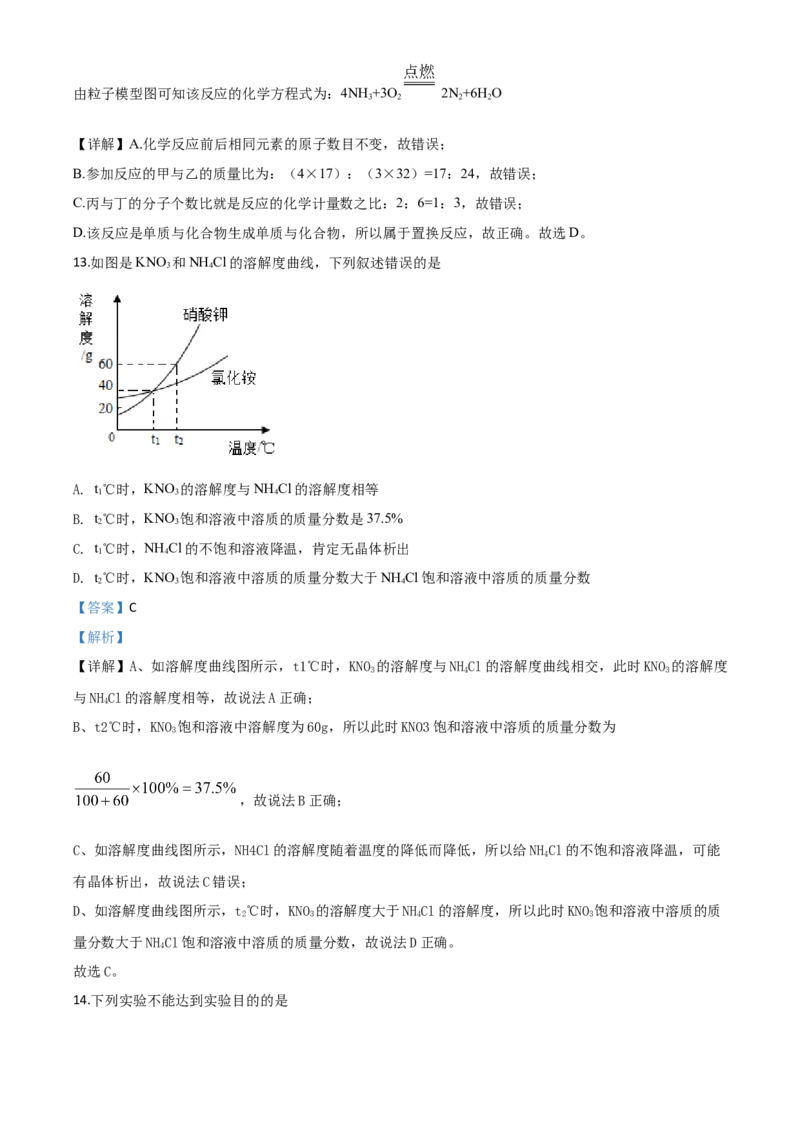
13.如图是KNO 和NH Cl的溶解度曲线,下列叙述错误的是
3 4
A. t℃时,KNO 的溶解度与NH Cl的溶解度相等
1 3 4
B. t℃时,KNO 饱和溶液中溶质的质量分数是37.5%
2 3
C. t℃时,NH Cl的不饱和溶液降温,肯定无晶体析出
1 4
D. t℃时,KNO 饱和溶液中溶质的质量分数大于NH Cl饱和溶液中溶质的质量分数
2 3 4
【答案】C
【解析】
【详解】A、如溶解度曲线图所示,t1℃时,KNO 的溶解度与NHCl的溶解度曲线相交,此时KNO 的溶解度
3 4 3
与NHCl的溶解度相等,故说法A正确;
4
B、t2℃时,KNO 饱和溶液中溶解度为60g,所以此时KNO3饱和溶液中溶质的质量分数为
3
,故说法B正确;
C、如溶解度曲线图所示,NH4Cl的溶解度随着温度的降低而降低,所以给NHCl的不饱和溶液降温,可能
4
有晶体析出,故说法C错误;
D、如溶解度曲线图所示,t℃时,KNO 的溶解度大于NHCl的溶解度,所以此时KNO 饱和溶液中溶质的质
2 3 4 3
量分数大于NHCl饱和溶液中溶质的质量分数,故说法D正确。
4
故选C。
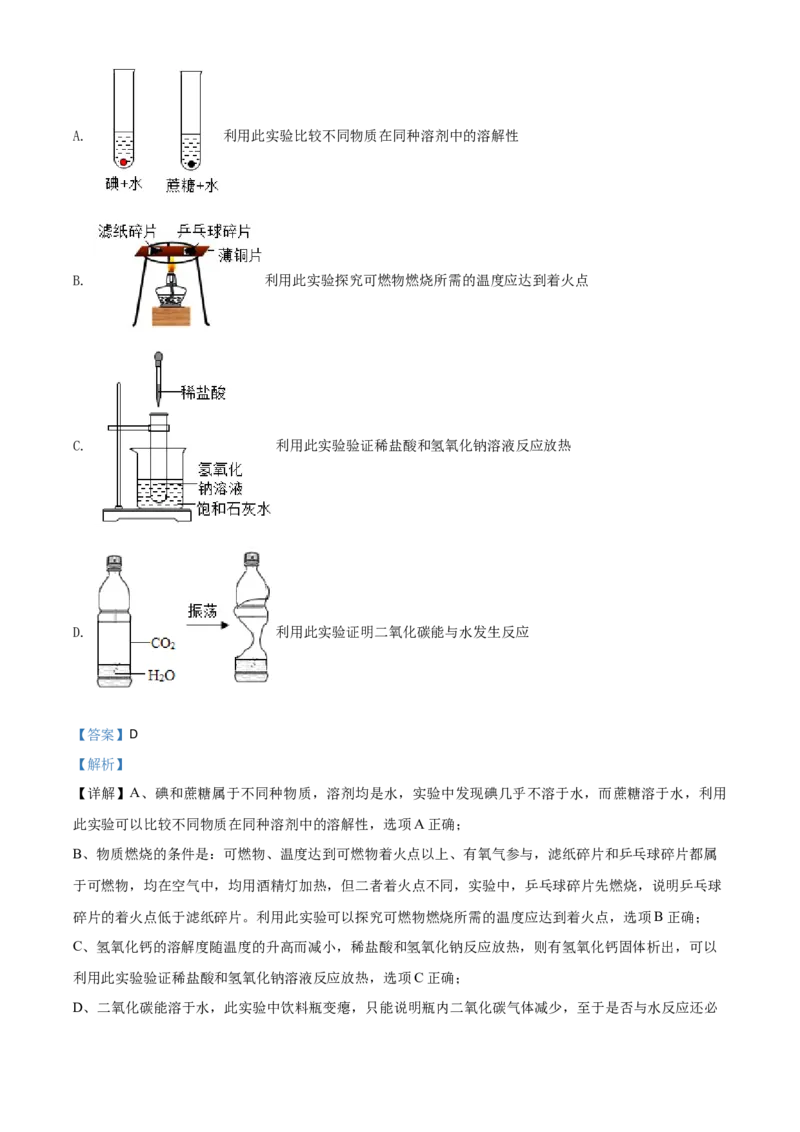
14.下列实验不能达到实验目的的是A. 利用此实验比较不同物质在同种溶剂中的溶解性
B. 利用此实验探究可燃物燃烧所需的温度应达到着火点
C. 利用此实验验证稀盐酸和氢氧化钠溶液反应放热
D. 利用此实验证明二氧化碳能与水发生反应
【答案】D
【解析】
【详解】A、碘和蔗糖属于不同种物质,溶剂均是水,实验中发现碘几乎不溶于水,而蔗糖溶于水,利用
此实验可以比较不同物质在同种溶剂中的溶解性,选项A正确;
B、物质燃烧的条件是:可燃物、温度达到可燃物着火点以上、有氧气参与,滤纸碎片和乒乓球碎片都属
于可燃物,均在空气中,均用酒精灯加热,但二者着火点不同,实验中,乒乓球碎片先燃烧,说明乒乓球
碎片的着火点低于滤纸碎片。利用此实验可以探究可燃物燃烧所需的温度应达到着火点,选项B正确;
C、氢氧化钙的溶解度随温度的升高而减小,稀盐酸和氢氧化钠反应放热,则有氢氧化钙固体析出,可以
利用此实验验证稀盐酸和氢氧化钠溶液反应放热,选项C正确;
D、二氧化碳能溶于水,此实验中饮料瓶变瘪,只能说明瓶内二氧化碳气体减少,至于是否与水反应还必须证明生成物,利用此实验不能证明二氧化碳能与水发生反应,选项D不正确。故选D。
15.元素钴(Co)有多种化合价,将9.3gCo(OH) 在空气中加热至290℃时完全脱水,得到8.3g钴的氧化
2
物,该氧化物的化学式是
A. CoO
B. CoO
3
C. Co O
2 3
D. Co O
3 4
【答案】C
【解析】
【详解】由化学式可知 9.3gCo(OH) 中和氧化钴中钴元素质量相等,Co 元素的质量为:9.3g×
2
,
则钴的氧化物中氧元素的质量为:8.3g-5.9g=2.4g 即Co与O的原子个数比为: ≈2:3,故选
C。
第Ⅱ卷(非选择题共35分)
16.中餐食材丰富、烹饪手法多样,深受大众喜爱。
(1)煎牛排,牛排中不能给人体活动提供能量的物质是_______________(填序号)
a 蛋白质 b油脂 c 水
(2)炸油条,油条制作中所用的小苏打的化学式是_______________(填序号)。
a NaCl b NaHCO c NH HCO
3 4 3
(3)蒸紫薯,紫薯中含有的元素属于人体必需的常量元素的是___________(填序号)
a 钙 b铁 c 硒
(4)煮海带,海带中含有碘元素,适量摄入可预防_______________(填序号)。
a 佝偻病 b 环血病 c 甲状腺肿大
【答案】 (1). c (2). b (3). a (4). c
【解析】
【详解】(1)a 蛋白质能给人体活动提供能量,不符合题意;
b油脂能给人体活动提供能量,不符合题意;
c 水不能给人体活动提供能量,不符合题意。故选c;的
(2)炸油条,油条制作中所用 小苏打,是碳酸氢钠的俗称,其化学式是NaHCO 故选b;
3
(3)钙属于人体必需的常量元素,铁、硒属于人体必需的微量元素,故选a;
(4)煮海带,海带中含有碘元素,碘元素甲状腺激素的重要成分,适量摄入可预防甲状腺肿大。故选c。
17.化学在抗击新冠肺炎中发挥重要作用。
(1)医用口罩熔喷布所用的聚丙烯塑料属于_______________(填“复合”或“合成”)材料。
(2)某中药中含有的金丝桃苷(C H O )在与病毒的主要蛋白酶的对接方面有一定效果,金丝桃苷中碳、
21 20 12
氢、氧的原子个数比为_______________。
(3)呼吸机提供的氧气来自于空气,分离液态空气获得氧气的变化属于______________ 变化,在人体组
织里,葡萄糖(C H O)在酶的催化作用下经缓慢氧化转变成_____________________。
6 12 6
(4)次氯酸钠(NaC1O)是一种杀菌消毒剂。电解饱和食盐水可制得次氯酸钠和一种可燃性气体,反应
的化学方程式为____________________;用漂白粉(有效成分为Ca(ClO) )制取次氯酸钠的反应为:
2
,X的化学式是_________________。
【答案】 (1). 合成 (2). 21:20:12 (3). 物理 (4). 二氧化碳和水 (5). NaCl+3H O
2
NaClO+3H ↑ (6). NaCO
3 2 2 3
【解析】
【详解】(1)医用口罩熔喷布所用的聚丙烯塑料,塑料属于合成材料,故填:合成。
(2)某中药中含有的金丝桃苷(C H O )在与病毒的主要蛋白酶的对接方面有一定效果,金丝桃苷中碳、
21 20 12
氢、氧的原子个数比为:21:20:12,故填:21:20:12。
(3)呼吸机提供的氧气来自于空气,分离液态空气获得氧气的变化中没有新物质生成,属于物理变化,
在人体组织里,葡萄糖(C H O)在酶的催化作用下经缓慢氧化即与氧气反应生成二氧化碳和水,故填:
6 12 6
物理 二氧化碳和水。
(4)次氯酸钠(NaC1O)是一种杀菌消毒剂。电解饱和食盐水可制得次氯酸钠和一种可燃性气体,根据
质量守恒定律可知,可燃性气体是氢气,所以反应的化学方程式为NaCl+3H O NaClO+3H ↑;用漂白
2 3 2
粉(有效成分为Ca(ClO) )制取次氯酸钠的反应为: ,根据质量守恒
2
定律可知反应前有钙原子1个,氯原子2个,氧原子2个,和X,反应后有钙原子1个,氯原子2个,氧
原子5个,碳原子1个,钠原子2个,所以X中有钠原子2个,碳原子1个,氧原子3个,所以X的化学式是NaCO。故填:NaCl+3H O NaClO+3H ↑ Na CO。
2 3 2 3 2 2 3
【点睛】根据质量守恒定律的相关特征:化学反应前后,元素种类不变,相同元素的原子个数不变来解答
最后第(4)小题。
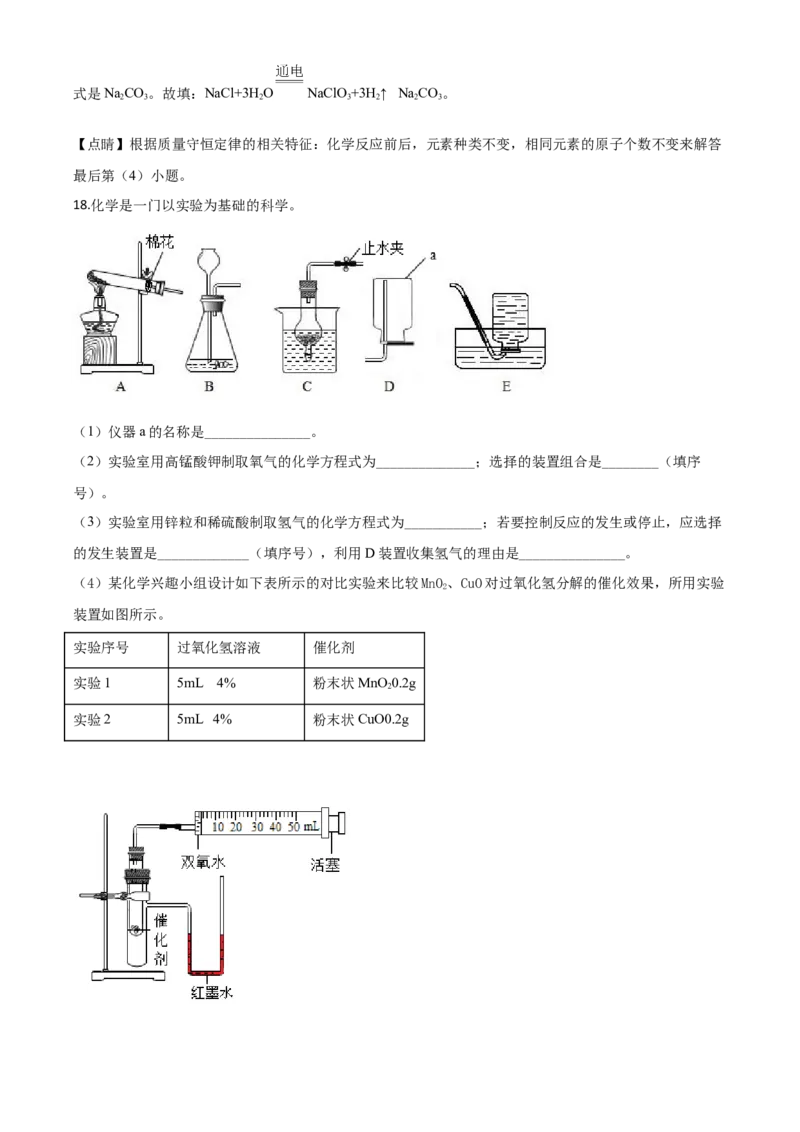
18.化学是一门以实验为基础的科学。
(1)仪器a的名称是_______________。
(2)实验室用高锰酸钾制取氧气的化学方程式为______________;选择的装置组合是________(填序
号)。
(3)实验室用锌粒和稀硫酸制取氢气的化学方程式为___________;若要控制反应的发生或停止,应选择
的发生装置是_____________(填序号),利用D装置收集氢气的理由是_______________。
(4)某化学兴趣小组设计如下表所示的对比实验来比较MnO、CuO对过氧化氢分解的催化效果,所用实验
2
装置如图所示。
实验序号 过氧化氢溶液 催化剂
实验1 5mL 4% 粉末状MnO 0.2g
2
实验2 5mL 4% 粉末状CuO0.2g①实验1中制取氧气的化学方程式为_______________。
②实验需要测量并记录的数据有:氧气体积和______________。
③实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据,实验过程中发现U
型管内右侧液面上升,原因是__________________。
④结论:MnO 对过氧化氢分解的催化效果比CuO好,得出该结论的依据是____________。
2
【答案】 (1). 集气瓶 (2). 2KMnO KMnO +MnO+O ↑ (3). AE (4). Zn+H SO =ZnSO +H ↑ (5). C
4 2 4 2 2 2 4 4 2
(6). 氢气的密度比空气小且不与空气中的成分反应 (7). 2HO 2HO+O↑ (8). 所需要的时间
2 2 2 2
(9). 反应放热 (10). 产生相同体积的氧气时MnO 所用的时间短
2
【解析】
【详解】(1)由图知:仪器a的名称是集气瓶,故填:集气瓶。
(2)实验室用高锰酸钾制取氧气时会锰酸钾、二氧化锰和氧气,所以反应的化学方程式为2KMnO
4
KMnO +MnO+O ↑;由此高锰酸钾制氧气是固体在加热条件下进行反应的,生成的氧气不易溶于水,所
2 4 2 2
以选择的装置组合是AE,故填:2KMnO KMnO +MnO+O ↑ AE。
4 2 4 2 2
(3)实验室用锌粒和稀硫酸制取氢气时还生成硫酸锌,所以反应的化学方程式为Zn+H SO =ZnSO +H ↑;
2 4 4 2
若要控制反应的发生或停止,应选择的发生装置是C,因为C可以通过将关闭止水夹来使固液分离反应停
止,利用D装置收集氢气的理由是氢气的密度比空气小且不与空气中的成分反应,因为D装置是向下排空
气法收集气体,适用于密度比空气小的气体,故填:Zn+H SO =ZnSO +H ↑ C 氢气的密度比空气小且不
2 4 4 2
与空气中的成分反应。
(4)①实验1使用了二氧化锰作催化剂,催化过氧化氢制氧气的,所以制取氧气的化学方程式为2HO
2 2
2HO+O↑。
2 2
②实验需要测量并记录的数据有:氧气体积和所需要的时间,因为可通过测定收集相同体积的氧气所以需
要的时间来比较两者的催化效果。
③实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据,实验过程中发现U型管内右侧液面上升,原因是反应放热,因为过氧化氢加入催化剂后生成氧气时会放出热量。
④结论:MnO 对过氧化氢分解的催化效果比CuO好,得出该结论的依据是产生相同体积的氧气时MnO
2 2
所用的时间短。故填:2HO 2HO+O↑ 所需要的时间 反应放热 产生相同体积的氧气时MnO 所
2 2 2 2 2
用的时间短。
【点睛】充分利用反应物的状态与反应条件来选择发生装置,根据气体的性质来选择收集装置。
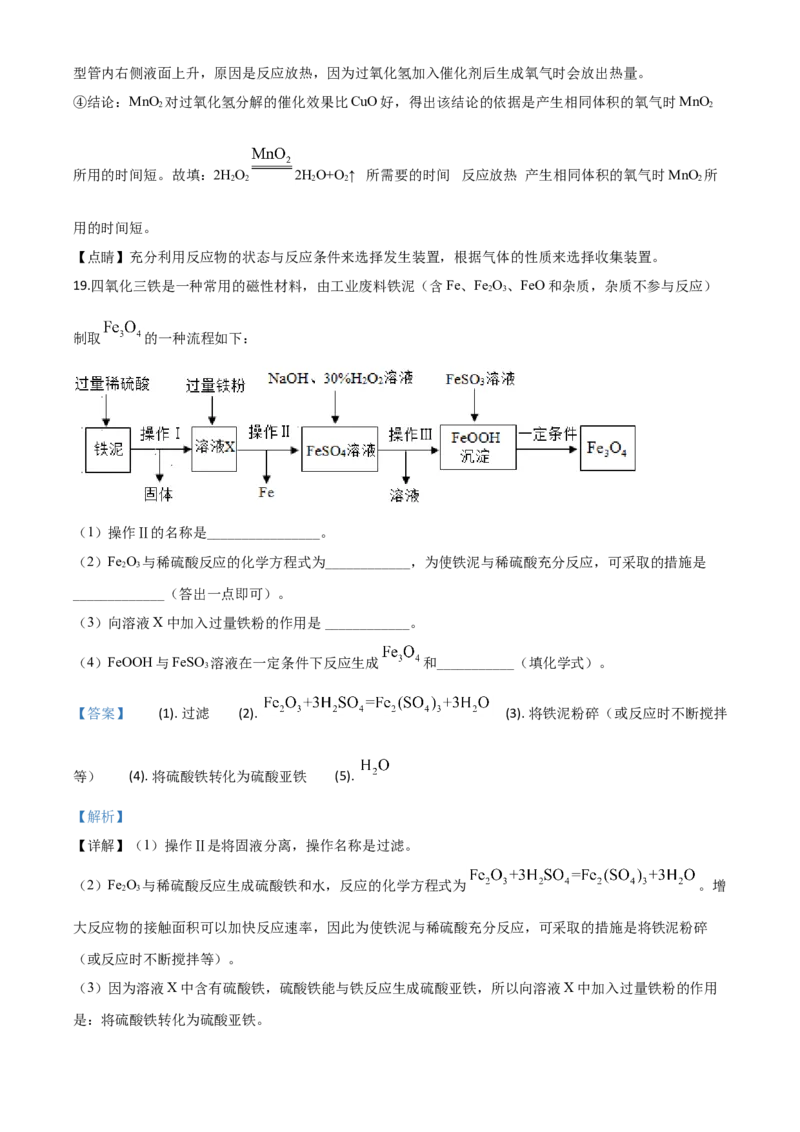
19.四氧化三铁是一种常用的磁性材料,由工业废料铁泥(含Fe、Fe O、FeO和杂质,杂质不参与反应)
2 3
制取 的一种流程如下:
(1)操作Ⅱ的名称是________________。
(2)Fe O 与稀硫酸反应的化学方程式为____________,为使铁泥与稀硫酸充分反应,可采取的措施是
2 3
_____________(答出一点即可)。
(3)向溶液X中加入过量铁粉的作用是 ____________。
(4)FeOOH与FeSO 溶液在一定条件下反应生成 和___________(填化学式)。
3
【答案】 (1). 过滤 (2). (3). 将铁泥粉碎(或反应时不断搅拌
等) (4). 将硫酸铁转化为硫酸亚铁 (5).
【解析】
【详解】(1)操作Ⅱ是将固液分离,操作名称是过滤。
(2)Fe O 与稀硫酸反应生成硫酸铁和水,反应的化学方程式为 。增
2 3
大反应物的接触面积可以加快反应速率,因此为使铁泥与稀硫酸充分反应,可采取的措施是将铁泥粉碎
(或反应时不断搅拌等)。
(3)因为溶液X中含有硫酸铁,硫酸铁能与铁反应生成硫酸亚铁,所以向溶液X中加入过量铁粉的作用
是:将硫酸铁转化为硫酸亚铁。(4)因为FeOOH与FeSO 溶液在一定条件下(碱性,假设使用的碱性物质是氢氧化钠溶液,合理即可)
3
转化为 的反应化学方程式为: ,所以FeOOH
与FeSO 溶液在一定条件下反应生成 和 (SO 2-和Na+都没有参加反应)。
3 3
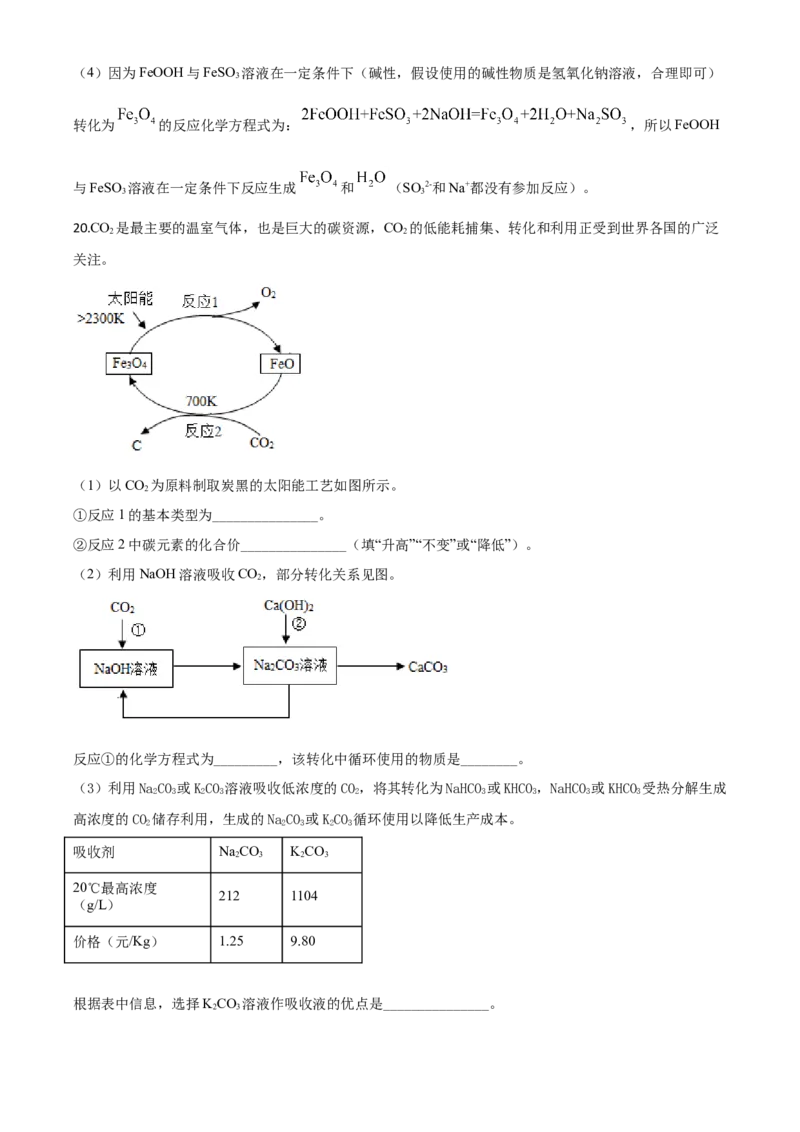
20.CO 是最主要的温室气体,也是巨大的碳资源,CO 的低能耗捕集、转化和利用正受到世界各国的广泛
2 2
关注。
(1)以CO 为原料制取炭黑的太阳能工艺如图所示。
2
①反应1的基本类型为_______________。
②反应2中碳元素的化合价_______________(填“升高”“不变”或“降低”)。
(2)利用NaOH溶液吸收CO,部分转化关系见图。
2
反应①的化学方程式为_________,该转化中循环使用的物质是________。
(3)利用NaCO 或KCO 溶液吸收低浓度的CO,将其转化为NaHCO 或KHCO,NaHCO 或KHCO 受热分解生成
2 3 2 3 2 3 3 3 3
高浓度的CO 储存利用,生成的NaCO 或KCO 循环使用以降低生产成本。
2 2 3 2 3
吸收剂 NaCO KCO
2 3 2 3
20℃最高浓度
212 1104
(g/L)
价格(元/Kg) 1.25 9.80
根据表中信息,选择KCO 溶液作吸收液的优点是_______________。
2 3的
(4)利用一种新型“人造树叶”将CO 转化为乙醇(C HOH) 反应如下:
2 2 5
,研究显示,1L“人造树叶”每天能从空气中吸收968gCO,计算
2
1L“人造树叶”工作1天可得到乙醇的质量(写出计算过程)。_____
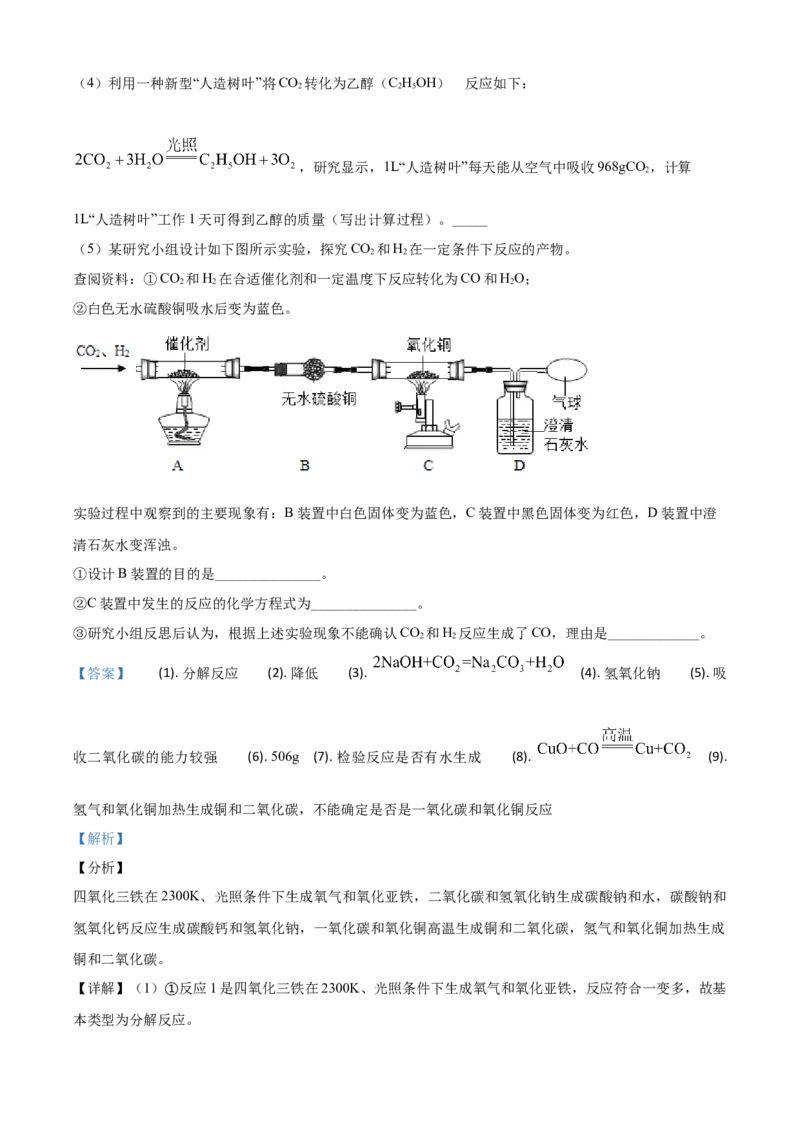
(5)某研究小组设计如下图所示实验,探究CO 和H 在一定条件下反应的产物。
2 2
查阅资料:①CO 和H 在合适催化剂和一定温度下反应转化为CO和HO;
2 2 2
②白色无水硫酸铜吸水后变为蓝色。
实验过程中观察到的主要现象有:B装置中白色固体变为蓝色,C装置中黑色固体变为红色,D装置中澄
清石灰水变浑浊。
①设计B装置的目的是_______________。
②C装置中发生的反应的化学方程式为_______________。
③研究小组反思后认为,根据上述实验现象不能确认CO 和H 反应生成了CO,理由是_____________。
2 2
【答案】 (1). 分解反应 (2). 降低 (3). (4). 氢氧化钠 (5). 吸
收二氧化碳的能力较强 (6). 506g (7). 检验反应是否有水生成 (8). (9).
氢气和氧化铜加热生成铜和二氧化碳,不能确定是否是一氧化碳和氧化铜反应
【解析】
【分析】
四氧化三铁在2300K、光照条件下生成氧气和氧化亚铁,二氧化碳和氢氧化钠生成碳酸钠和水,碳酸钠和
氢氧化钙反应生成碳酸钙和氢氧化钠,一氧化碳和氧化铜高温生成铜和二氧化碳,氢气和氧化铜加热生成
铜和二氧化碳。
【详解】(1)①反应1是四氧化三铁在2300K、光照条件下生成氧气和氧化亚铁,反应符合一变多,故基
本类型为分解反应。②反应2中反应物中碳元素在二氧化碳中,生成物中碳元素在碳单质中,二氧化碳中氧元素的化合价为-2
价,设碳元素的化合价为x,化合物中各元素的正负化合价代数和为零,则 , ,二氧
化碳中碳元素的化合价为+4价,碳单质中碳元素的化合价为0,故碳元素的化合价降低。
(2)反应①是二氧化碳和氢氧化钠生成碳酸钠和水,故反应的化学方程式为
,由转化关系图可知,氢氧化钠参加反应,碳酸钠和氢氧化钙反应生成碳
酸钙和氢氧化钠,故该转化中循环使用的物质是氢氧化钠。
(3)根据表中信息可知,碳酸钾吸收二氧化碳能力较强,碳酸氢钾加热生成碳酸钾、二氧化碳和水,故
选择KCO 溶液作吸收液的优点是吸收二氧化碳的能力较强。
2 3
(4)设1L“人造树叶”工作1天可得到乙醇的质量为y
故1L“人造树叶”工作1天可得到乙醇的质量为506g。
(5)①白色无水硫酸铜吸水后变为蓝色,故设计B装置的目的是检验反应是否有水生成。
②C装置中发生的反应是一氧化碳和氧化铜高温生成铜和二氧化碳,故反应的化学方程式为
。
③氢气和氧化铜加热生成铜和水,故根据上述实验现象不能确认CO 和H 反应生成了CO,理由是氢气和
2 2
氧化铜加热生成铜和水,不能确定是否是一氧化碳和氧化铜反应。
【点睛】分解反应是一种物质生成两种或两种以上物质的反应,化合物中各元素的正负化合价代数和为零,
KCO 溶液吸收二氧化碳的能力较强,氢气和一氧化碳均与氧化铜反应生成铜,不能确定是否存在一氧化
2 3
碳。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635