文档内容
化学评分细则
一、选择题:本题共14小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
题号 1 2 3 4 5 6 7
答案 C D A A B C B
题号 8 9 10 11 12 13 14
答案 C D B B D C B
【解析】
1.甲烷燃烧的火焰颜色是蓝色或淡蓝色,丙烷燃烧的火焰颜色为黄色,A错误。天然气灶具
和液化气灶具不可以通用,B错误。丙烷比甲烷易液化,C正确。水煤气的主要成分是CO
和H ,D错误。
2
2.Cl原子的半径大于C原子,中心原子半径小,A错误。聚丙烯的链节为 ,B
1
错误。NCl 中心原子N的价层电子对数为3 (531)314,VSEPR模型为四面体
3
2
形,C错误。p 轨道的电子云轮廓图为哑铃型, ,D正确。
x
3.碳酸钠为强碱弱酸盐,水解显碱性,加热能促进盐类的水解,所以用热的纯碱溶液洗去油
污,A正确。芯片主要成分是硅单质,B错误。Fe O 具有磁性,故磁铁的主要成分是Fe O ,
3 4 3 4
C错误。酚醛树脂是酚与醛在酸或碱催化下发生缩聚反应而成的,D错误。
4.布洛芬的成酯修饰分子有 9 个不饱和度,分子式为 C H NO ,A 正确。布洛芬分子中所
19 23 2
有碳原子不可以在同一平面,B 错误。1mol 布洛芬的成酯修饰分子可与 6mol H 反应,C
2
错误。布洛芬可以发生取代、氧化、加成反应,不能发生消去反应,D错误。
5.用图甲蒸发结晶制取NaCl,A正确。装置中的NH 能与水直接接触,无法防倒吸,B错误。
3
△
用图丙装置制备Cl ,反应方程式为4HCl(浓)+MnO =====MnCl +Cl ↑+2H O,C正确。难
2 2 2 2 2
溶于水的杂质可用过滤方法除去,D正确。
m 2.8
6.2.8g N 的物质的量n mol0.1mol,生成1mol N 转移的电子数为12N ,则生成
2 2 A
M 28
0.1mol N 转移的电子数为1.2N ,A错误。题中没有说明是否处于标准状况条件下,无法
2 A
化学评分细则·第1页(共7页)计算,B错误。KNO 晶体含有离子为K+、NO,0.5mol KNO 晶体中含离子数目为N ,
3 3 3 A
C正确。因为S2−水解,使1L 0.1mol·L−1K S溶液中S2−的数目小于0.1N ,D错误。
2 A
7 . 醋 酸 是 弱 酸 , 不 能 拆 , 反 应 的 离 子 方 程 式 为 IO 5I+6CH COOH =
3 3
3I 3H O+6CH COO,A 错误。氯化银、碘化银为同种类型沉淀,由于氯化银的 K 大
2 2 3 sp
于碘化银的 K ,因此向AgCl悬浊液中滴加KI 溶液可以得到碘化银沉淀,反应为
sp
AgCl(s)I(aq)AgI(s)Cl(aq),B正确。HI是一元强酸,电离产生氢离子和碘离子,
其中氢离子和硝酸铁电离出的硝酸根离子构成强氧化性的体系,又因为还原性的强酸过
量,所以两种氧化剂都完全反应,正确的离子方程式为 Fe3++ 3NO +12H++10I-
3
=Fe2++5I +3NO↑+6H O,C 错误。电荷及电子转移均不守恒,反应为
2 2
4H 4I+O =2I +2H O,D错误。
2 2 2
8. S 和 CS 都属于非极性分子,H O 是极性分子,由“相似相溶”原理可知,A 正确。NaCl
2 2
属于离子晶体,S 属于分子晶体,NaCl熔点大于S 熔点,B正确。NCl 和NH 中心原子
8 8 3 3
都采取 sp3杂化,且均含有 1 个孤电子对,因电负性:HO2−>Al3+,B 错误。氨气的沸点大于
甲烷的沸点,碳的氢化物有很多,随着碳原子数目的增加,沸点升高,C 错误。过氧化氢
的结构式为H—O—O—H,既有极性键又有非极性键,D正确。
10.向蔗糖中加入几滴蒸馏水,然后再加入浓硫酸,若产生疏松多孔的海绵状炭,说明浓硫
△
酸具有脱水性,放出刺激性气味的气体,发生的方程式为 C+2H SO (浓)=====
2 4
CO ↑+2SO ↑+2H O,则说明浓硫酸有强氧化性,A正确。高锰酸钾溶液一般用硫酸酸化,
2 2 2
化学评分细则·第2页(共7页)即酸性高锰酸钾溶液中本身就含有SO2,不通入二氧化硫气体,加入氯化钡溶液也会出
4
现白色沉淀,则不能通过测定白色沉淀的质量,推算二氧化硫的物质的量,B错误。实验
中控制了单一变量,结论有效,C正确。SO 将Br 还原,所以还原性SO > Br-,D正确。
2 2 2
11.该反应的化学方程式H +CO =HCOOH,据图可知物质Ⅰ虽然参与整个过程,但整个
2 2
反应前后没有变化,且反应从物质Ⅰ和氢气的反应开始,所以为该反应的催化剂,B正确。
据图可知催化剂也参与了整个循环,C错误。每生成2mol HCOOH放出62.4 kJ的能量,
据此可知反应物和生成物的能量之差,但不能确定反应的活化能,D错误。
12.电子流向:负极到通入 NO 一极;通入 SO 一极到正极,A 错误。通入 NO 一极发生还
x 2 x
原反应,是阴极,B 错误。溶液中阳离子向通入 NO 的电极移动,C 错误。由图,NO
x 2
在阴极得电子发生还原反应转变成铵根离子,根据元素守恒和电荷守恒即可得 NO +7e-
2
+8H+=NH+2H O,D正确。
4 2
13.图甲晶体是石墨晶体,每一层内原子之间为共价键,层与层之间存在的作用力为范德华
力,属于混合型晶体,A正确。图乙为某气态团簇分子的结构,该分子结构中有13个C,
14个Ti,因此其化学式为Ti C ,B正确。晶胞结构中,Zn2+周围等距且最近的S2−有4
14 13
个,即Zn2+的配位数为4,因为Zn2+∶S2−=1∶1,则S2的配位数为4,C错误。由图可知,
1 1
原子M 为坐标原点,原子N为上层的 晶胞正四面体的中心,在x 轴上位移为 ,在y
8 4
3 3 1 3 3
轴上位移为 ,在z轴上位移为 ,则原子N的坐标为( , , ),已知原子M的
4 4 4 4 4
1 3 3
坐标为(0,0,0),则原子N的坐标为( , , ),D正确。
4 4 4
14.y点时,溶液呈中性,水的电离不受影响,b点为KA溶液,发生A-的水解反应,从而促
进水的电离,所以水的电离程度:b 点>y 点,A 正确。HA 是弱酸,与氢氧化钾中和滴
定的指示剂应选酚酞,B错误。b点滴定分数为1.00,二者恰好完全反应,但是体积变成
原来的二倍,则浓度降为原来的一倍,所以c(K+) = c(HA) +c(A-) =0.05mol/L,C正确。a
点时,KA、HA 的物质的量浓度相同,但溶液的 pH<7,则表明以 HA 的电离为主,所
以溶液中存在:c(A)c(K)c(HA)c(H)c(OH),D正确。
二、非选择题:本题共4小题,共58分。
15.(每空2分,共14分)
(1)+(a+b)
1 1 3
11 11 11
(2)0.0125mol/(L·min) K
x 1 5
11 11
化学评分细则·第3页(共7页)(3)①CH CH=NH ②不断移出体系中的氢气
3
(4)①正 ②0.6N
A
【解析】(1)根据盖斯定律:Ⅰ+Ⅱ得总反应:H=+(a+b)kJ/mol。
(2)初始CH CH OH(g)充入1mol,NH (g)充入3mol;根据图示可知,平衡时乙醛和乙腈
3 2 3
物质的量分数都是 50%,说明二者物质的量相等,无乙醇存在,根据碳原子守恒,体系
中有0.5mol的乙醛和0.5mol乙腈;反应Ⅰ生成1mol氢气,反应Ⅱ消耗0.5mol氨气,生
成 0.5mol 水蒸气和 0.5mol 氢气,即平衡体系中有 0.5mol 乙醛,0.5mol 乙腈,1.5mol 氢
气,2.5mol氨气和0.5mol水蒸气。气体总物质的量5.5mol,乙醛、乙腈和水蒸气物质的
1 3 5
量分数: ,氢气物质的量是乙醛 3 倍为 ,氨气物质的量是乙醛 5 倍为 ,则 NH
3
11 11 11
0.5 1 1 3
2 11 11 11
的消耗速率为 0.0125mol/(L·min),代入表达式:K 。
20 x 1 5
11 11
(3)①根据Y和Z的结构简式及反应条件,可推出X的结构简式:CH CH=NH。
3
②结合反应过程可知,不断移出体系中的氢气,可有效减少副产物Y平衡产率。
(4)氢离子向右移动,则左侧为负极,b处进入的是乙醇;右侧是正极,c口通入氧气或
空 气 ; 2.3 g 乙 醇 完 全 反 应 生 成 CO 时 , 外 电 路 中 通 过 的 电 子 数 目 为
2
2.3g
12N 0.6N 。
46g/mol A A
16.(除特殊标注外,每空2分,共15分)
(1)恒压分液漏斗或恒压滴液漏斗(1分) 平衡气压,便于溶液顺利流下
(2)排尽空气 饱和NaHS溶液
(3)FeS+2H+=Fe2++H S↑
2
(4)b ③
(5)4NiS+O +2H O=4Ni(OH)S
2 2
【解析】(1)装置图中,仪器a的名称是恒压分液漏斗(或恒压滴液漏斗)。
(2)先通氮气排尽装置内空气,防止干扰后续试验;装置Ⅱ中的试剂为饱和NaHS溶液,
饱和NaHS溶液可以除去生成硫化氢气体中挥发的氯化氢气体杂质。
(3)装置Ⅰ中制硫化氢,反应为FeS+2H+=Fe2++H S↑。
2
(4)反应结束后关闭 K 、K ,在 b、c 处分别连接如图两个装置,打开 K 、K 进行抽滤
1 4 2 3
洗涤,抽滤洗涤时,洗涤水进入装置Ⅲ然后通过抽气装置抽出达到洗涤目的,故连有抽
化学评分细则·第4页(共7页)气泵的装置Ⅳ接在 b 处以便能够抽出洗涤水;由于 NiS 难溶于水可溶于稀酸,洗涤制备
出来的NiS可以用蒸馏水,故选择③。
(5)已知,NiS 在潮湿的空气中可转化为碱式硫化高镍[Ni(OH)S],从而降低除铜离子能
力,故随时间延长残留铜离子增加的原因是4NiS+O +2H O=4Ni(OH)S。
2 2
17.(每空2分,共14分)
(1)Fe O 、铝硅酸盐(2分,两个物质各1分)
2 3
(2)Al O +2OH-+3H O=2[Al(OH) ]- [Al(OH) ]-+CO =Al(OH) ↓+HCO或
2 3 2 4 4 2 3 3
2[Al(OH) ]-+CO =2Al(OH) ↓+CO2+H O也给分
4 2 3 3 2
(3)BC
(4)①0.7 ②能更快形成Al(OH) 胶体,使絮凝效果更好 ③pH过低,指示剂会与氢
3
离子反应生成重铬酸根离子,会氧化氯离子,导致消耗的硝酸银偏少,而pH过高,氢氧
根离子会与银离子反应,导致消耗的硝酸银偏多
【解析】(1)Fe O 和氢氧化钠溶液不反应、SiO 转变为难溶性的铝硅酸盐,步骤Ⅰ所得
2 3 2
滤渣为Fe O 、铝硅酸盐。
2 3
(2)步骤Ⅰ中主要反应为NaOH与Al O 反应,生成Na[Al(OH) ],步骤Ⅱ中主要反应为
2 3 4
Na[Al(OH) ]和过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,所发生反应的离子方程
4
式为 Al O +2OH-+3H O=2[Al(OH) ]-和[Al(OH) ]-+CO =Al(OH) ↓+HCO或
2 3 2 4 4 2 3 3
2[Al(OH) ]- +CO =2Al(OH) ↓+CO2+H O。
4 2 3 3 2
(3)为提高原料利用率可以将矿石粉碎,反应过程中适当搅拌,均可以使得反应更充分,
提高原料利用率,A正确。若步骤Ⅰ中采用盐酸处理铝土矿,则所得溶液中铝元素主要以
Al3+的形式存在,若加入过量NaOH溶液,则不能得到沉淀Al(OH) ,B错误。步骤Ⅲ,
3
洗涤时不能对漏斗中的沉淀进行搅拌,C错误。[Al (OH) Cl ] 中a、b可通过控制Al(OH)
2 a b m 3
和AlCl 的投料比控制,所以控制Al(OH) 和AlCl 的投料比可控制产品盐基度,D正确。
3 3 3
选BC。
(4)①平均消耗 0.1mol/L 的 AgNO 标准溶液 22.50mL,n(Cl-)=n(Ag+)=0.0225L×
3
0.00225mol
0.1mol/L=0.00225mol,c(Cl-)= 0.09mol/L,c(Al3+)=0.1000mol·L−1,根据电
0.025L
荷守恒,c(OH-)=0.21mol/L,所以产品的化学式为[Al (OH) Cl ] ,产品的盐基度为
2 4.2 1.8 m
4.2
0.7。
4.21.8
化学评分细则·第5页(共7页)②盐基度在0.60~0.85时,铝离子水解更快,所以絮凝效果较好。
③pH过低,指示剂会与氢离子反应生成重铬酸根离子,会氧化氯离子,导致消耗的硝酸
银偏少,而 pH 过高,氢氧根离子会与银离子反应,导致消耗的硝酸银偏多,所以测定
Cl-过程中溶液pH过低或过高均会影响测定结果。
18.(除特殊标注外,每空2分,共15分)
(1)2−氟甲苯(或邻氟甲苯) 氧化反应(1分)
(2)酰胺基、氨基(2分,两个名称各1分)
(3)F 的电负性大,具有吸电子效应,导致 B( )的羧基中的羟基的极性更大,
酸性更强
(4)
(5)Y中有—NH ,具有碱性,可以与HBr反应生成盐,促进反应正向进行
2
(6)4
(7)
【解析】(1)物质 A 的名称为 2−氟甲苯或邻氟甲苯;物质 B( )的生成是—CH
3
转变为—COOH,是氧化反应。
(2)物质F中含氮官能团的名称为酰胺基、氨基。
(3)从物质B( )的结构和苯甲酸( )的结构对比看,它们都含有苯环和
羧基结构,但由于物质B的羧基邻位还有1个F原子,由于F原子电负性强,具有吸电
子效应,对羧基中羟基的影响比较大,导致羧基中的羟基极性更大,更易电离出H,导
致酸性比苯甲酸强。
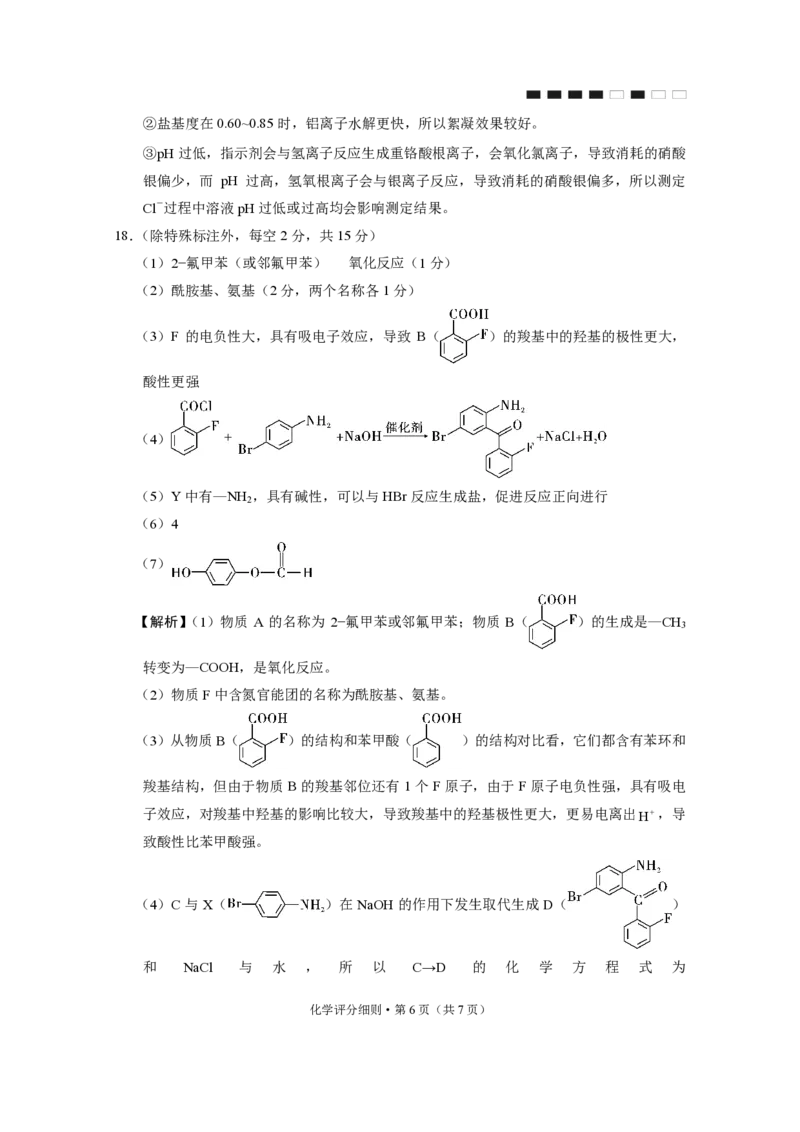
(4)C 与 X( )在 NaOH 的作用下发生取代生成 D( )
和 NaCl 与 水 , 所 以 C→D 的 化 学 方 程 式 为
化学评分细则·第6页(共7页)。
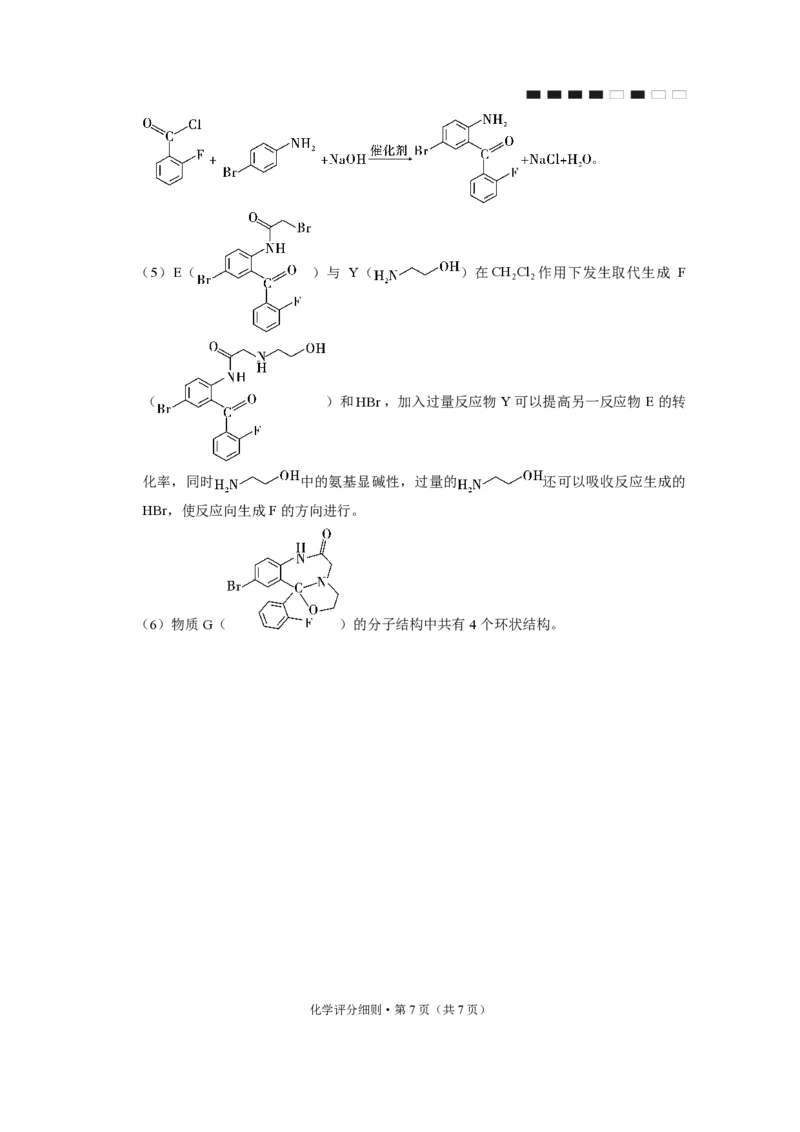
(5)E( )与 Y( )在CH Cl 作用下发生取代生成 F
2 2
( )和HBr,加入过量反应物Y可以提高另一反应物E的转
化率,同时 中的氨基显碱性,过量的 还可以吸收反应生成的
HBr,使反应向生成F的方向进行。
(6)物质G( )的分子结构中共有4个环状结构。
化学评分细则·第7页(共7页)