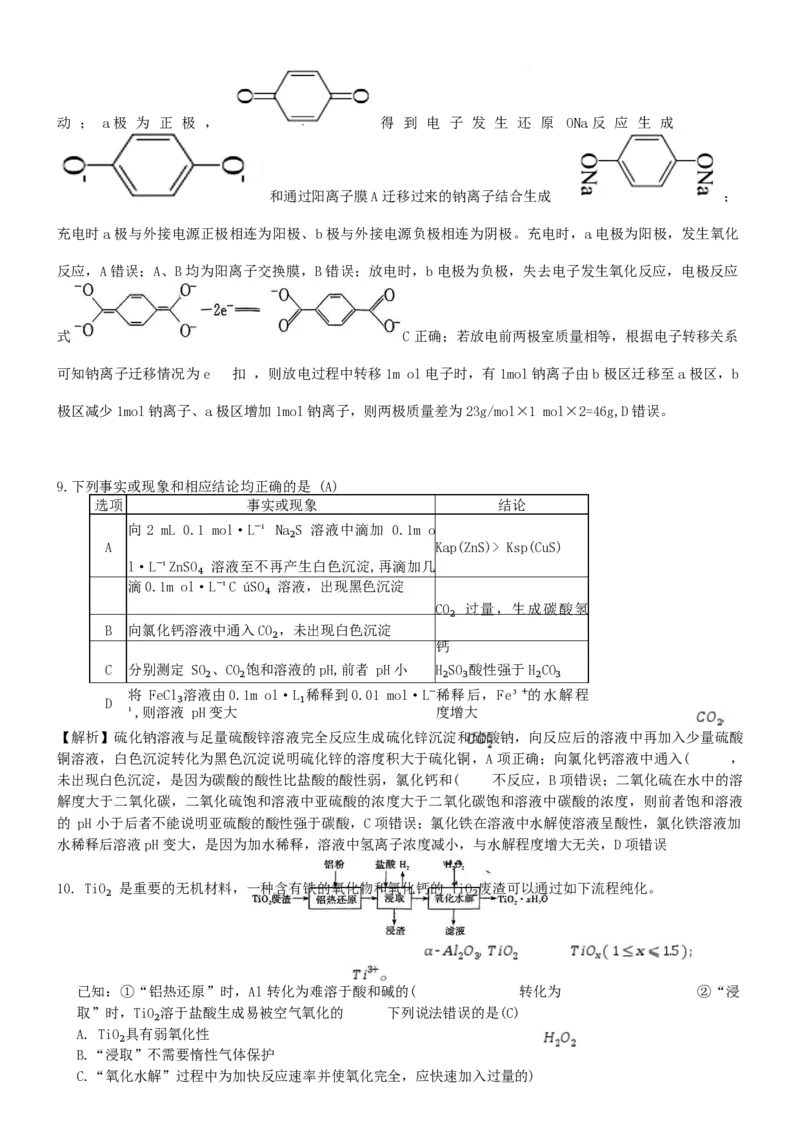
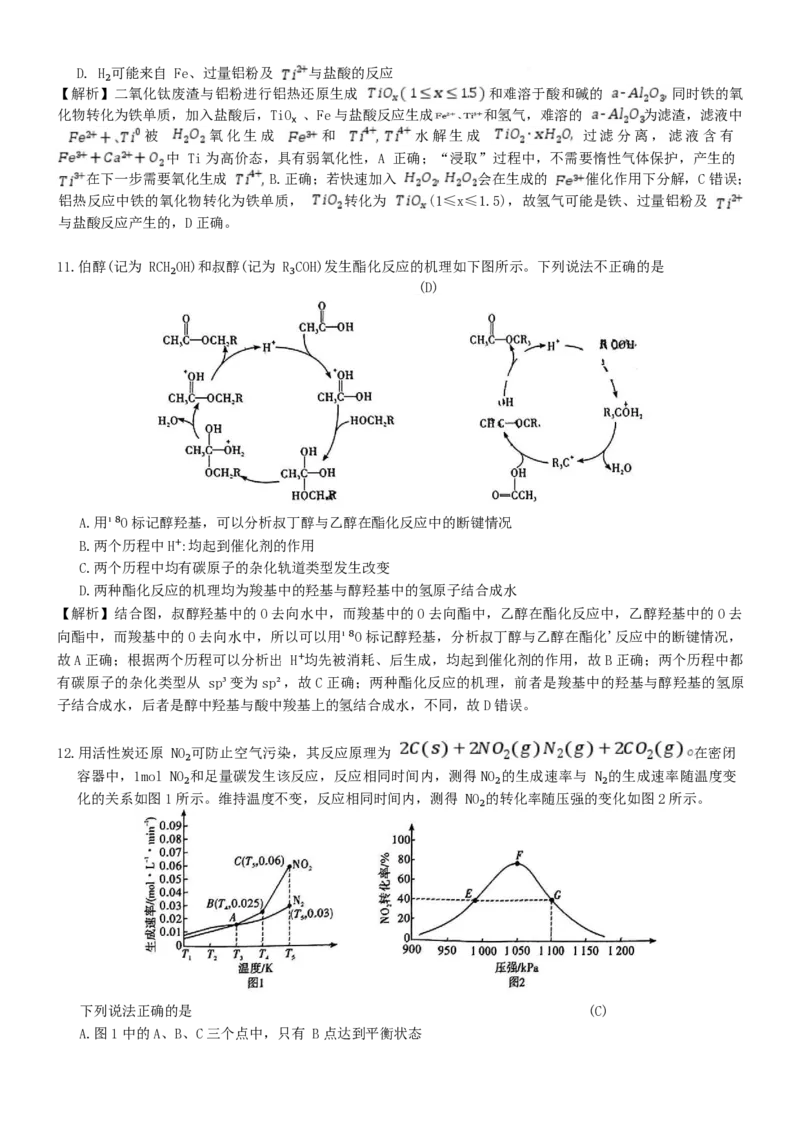
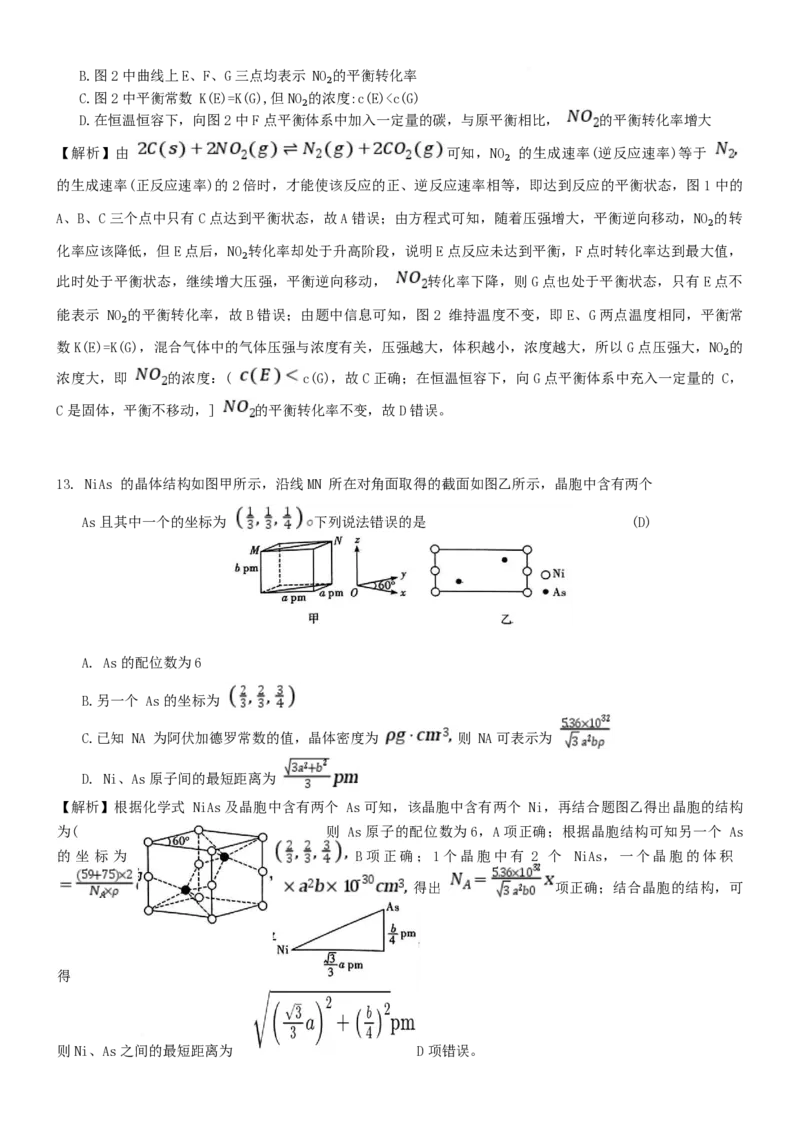
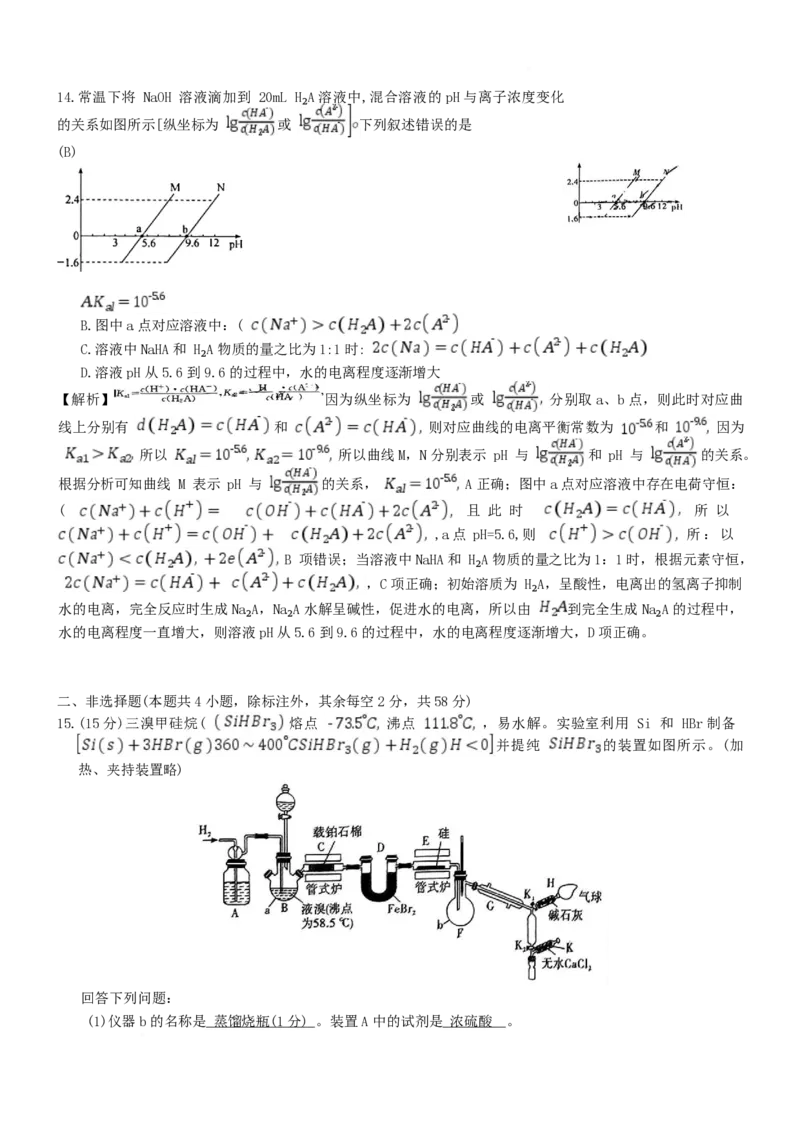
文档内容
长沙市一中 届高三月考试卷 七
2025 ( )
化 学(解析版)
可能用到的相对原子质量:H~1 O~16 Na~23 Si~28 Ni~59 As~75 Br~80
一、选择题(本题共 14 小题,每小题 3 分,共 42 分。每小题只有一项符合题目要求)
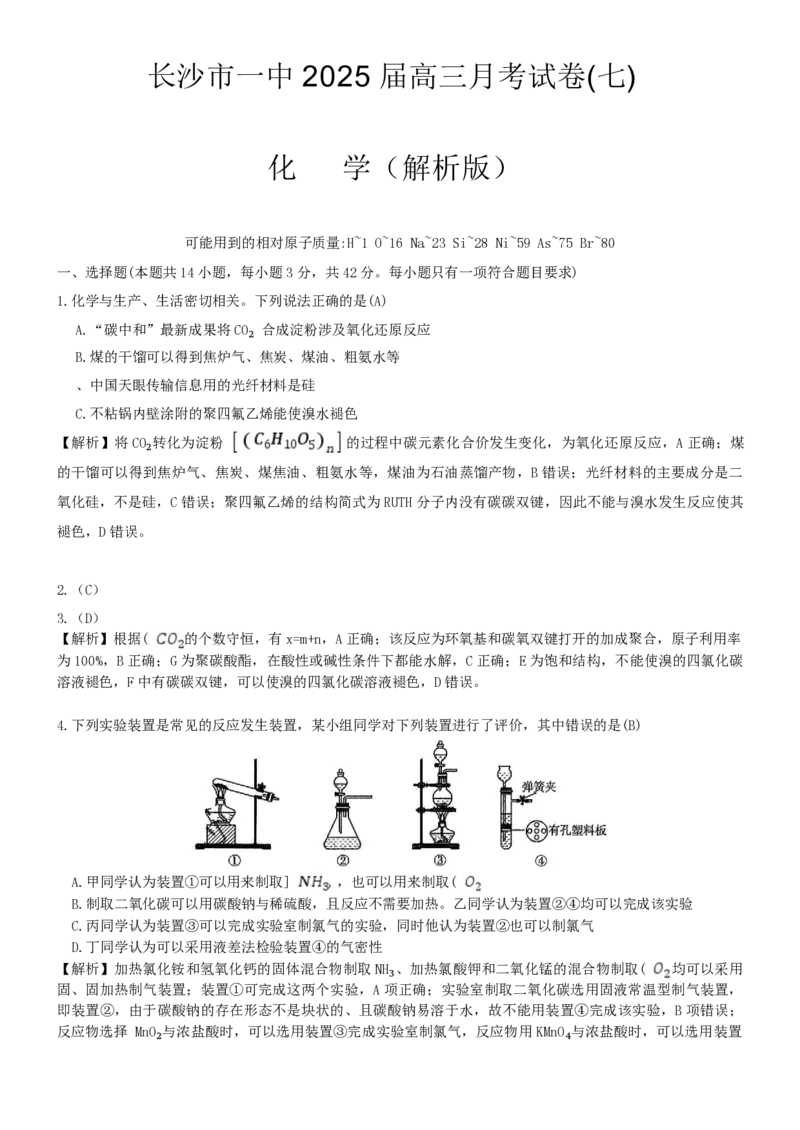
1.化学与生产、生活密切相关。下列说法正确的是(A)
A.“碳中和”最新成果将 CO₂ 合成淀粉涉及氧化还原反应
B.煤的干馏可以得到焦炉气、焦炭、煤油、粗氨水等
、中国天眼传输信息用的光纤材料是硅
C.不粘锅内壁涂附的聚四氟乙烯能使溴水褪色
【解析】将 CO₂转化为淀粉 的过程中碳元素化合价发生变化,为氧化还原反应,A 正确;煤
的干馏可以得到焦炉气、焦炭、煤焦油、粗氨水等,煤油为石油蒸馏产物,B 错误;光纤材料的主要成分是二
氧化硅,不是硅,C 错误;聚四氟乙烯的结构简式为 RUTH 分子内没有碳碳双键,因此不能与溴水发生反应使其
褪色,D 错误。
2.(C)
3.(D)
【解析】根据( 的个数守恒,有 x=m+n,A 正确;该反应为环氧基和碳氧双键打开的加成聚合,原子利用率
为 100%,B 正确;G 为聚碳酸酯,在酸性或碱性条件下都能水解,C 正确;E 为饱和结构,不能使溴的四氯化碳
溶液褪色,F 中有碳碳双键,可以使溴的四氯化碳溶液褪色,D 错误。
4.下列实验装置是常见的反应发生装置,某小组同学对下列装置进行了评价,其中错误的是(B)
A.甲同学认为装置①可以用来制取] ,也可以用来制取(
B.制取二氧化碳可以用碳酸钠与稀硫酸,且反应不需要加热。乙同学认为装置②④均可以完成该实验
C.丙同学认为装置③可以完成实验室制氯气的实验,同时他认为装置②也可以制氯气
D.丁同学认为可以采用液差法检验装置④的气密性
【解析】加热氯化铵和氢氧化钙的固体混合物制取 NH₃、加热氯酸钾和二氧化锰的混合物制取( 均可以采用
固、固加热制气装置;装置①可完成这两个实验,A 项正确;实验室制取二氧化碳选用固液常温型制气装置,
即装置②,由于碳酸钠的存在形态不是块状的、且碳酸钠易溶于水,故不能用装置④完成该实验,B 项错误;
反应物选择 MnO₂与浓盐酸时,可以选用装置③完成实验室制氯气,反应物用 KMnO₄与浓盐酸时,可以选用装置②完成实验室制氯气,C 项正确;可以采用液差法检验装置④的气密性,具体方法是:关闭弹簧夹,向长颈漏
斗中注水至长颈漏斗中液面高于试管中液面,静置一段时间后液面高度差保持不变,则装置气密性良好,D 项
正确。
5.下列离子方程式正确的是(D)
A.磁性氧化铁溶于 HI 溶液:
B.向 Na₂S 溶液通入过量 SO₂ 产生淡黄色沉淀:
C.用酸化的 KI 淀粉溶液检验加碘盐中的
D.向 溶液中加入 NaOH 至溶液呈碱性:(
【解析】磁性氧化铁溶于 HI 溶液,反应产生的 会与溶液中的 I⁻进一步发生氧化还原反应生成
故反应的离子方程式应该为 ,A 错误;向 溶液中
通 入 过 量 产 生 淡 黄 色 沉 淀 , 发 生 反 应 生 成 : 反 应 的 离 子 方 程 式 为
B 错 误 ; 未 配 平 方 程 式 , 用 酸 化 的 KI 淀 粉 溶 液 检 验 加 碘 盐 中 的
,C 错误;向 溶液中加入 NaOH 至溶液呈碱性,重铬酸根离
子转化为铬酸根离子,离子方程式为 D 正确。
6.实验小组用如下流程探究含氮化合物的转化。 为阿伏加德罗常数的值,下列说法正确的是(B)
A. “反应 1”中,每消耗( ,在 25 ℃、101 kPa 下得到
B. “反应 2”中,每生成 0.1m ol NO,转移电子数为 0.5NA
C.在密闭容器中进行“反应 3”,0.1m ol NO 充分反应后体系中有( 个
D. “反应 4”中,为使( 完全转化成 至少需要( 个 O₂
【 解 析 】 “反 应 1”为 实 验 室 制 取 氨 气 的 反 应 , 化 学 方 程 式 为
“反应 2”是氨气的催化氧化,化学方程式为 “反
应 3”为一氧化氮和氧气反应生成二氧化氮,化学方程式为 “反应 4”为二氧化氮、氧
气和水度应生成硝酸,化学方程式为 以此解题。根据分析可知,每消耗 0.1
m ol NH₄Cl,生成 0.1m ol 氨气,但是由于不是标准状况,则气体不是 2.24 L,A 错误;根据分析可知,“反应 2”
的化学方程式为 该反应转移 20e⁻,则每生成 0.1mol NO,转移电子数
为 0.5NA,B.正 确 ;根 据 “反 应 3”,0.1m ol NO 充 分 反 应 后 生 成 0.1NA 个 NO₂,但 是 体 系 中 存 在
,则最终二氧化氮分子的数目小于 0.1NA,C 错误;根据“反应·4”可知,使 0.1mol NO₂ 完全
转化成 HNO₃,至少需要 0.025NA 个 O₂,D 错误。
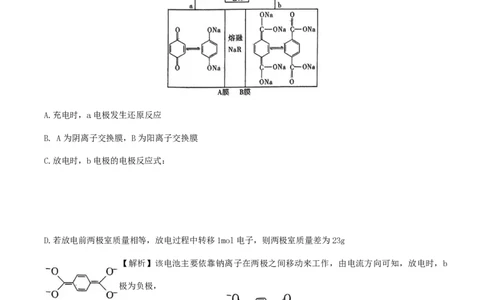
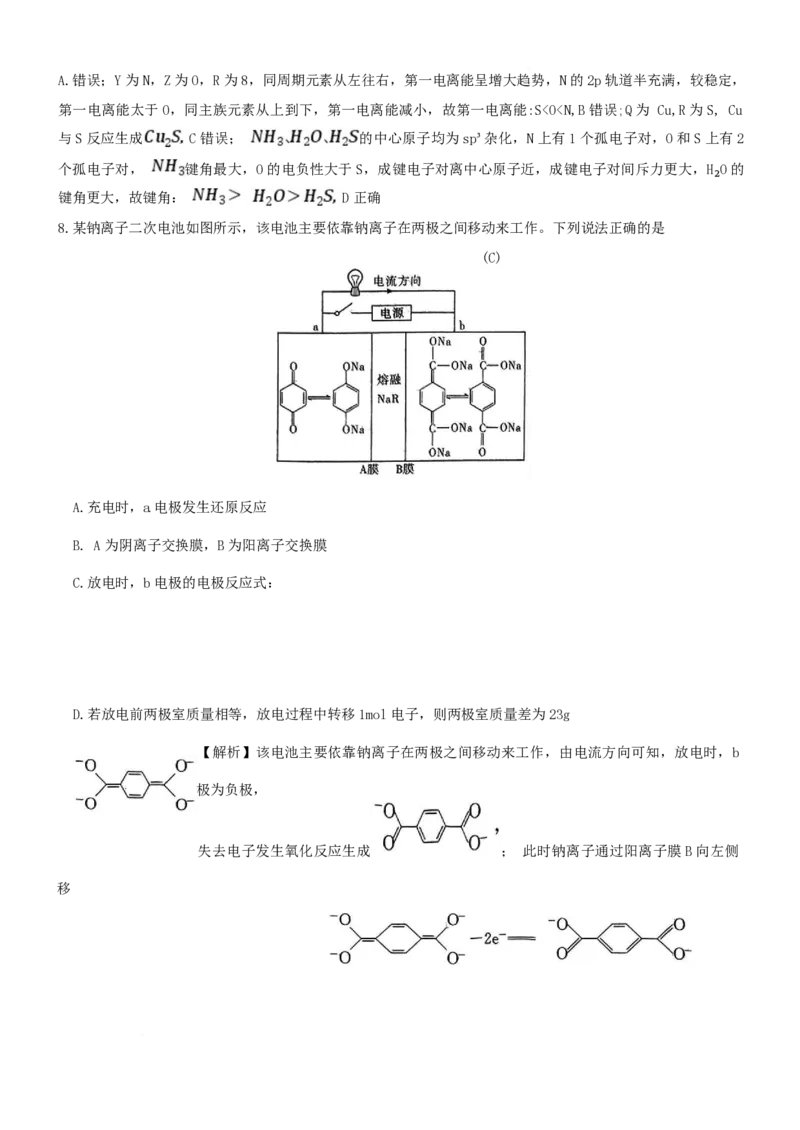
7.化合物 可作电镀液的制备原料,已知所含的 5 种元素 X、Y、Z、R、Q 原子序数依次增
大,且在前四周期均有分布,仅有 Y 与 Z 同周期。Z 与 R 同族,Z 在地壳中含量最高,基态离子 Q⁺的 M 层全
充满。下列说法正确的是(D)
A.简单氢化物的沸点:R>Z>Y
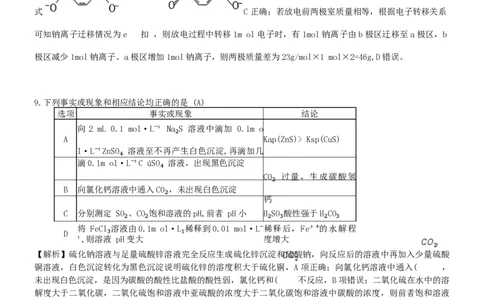
B.第一电离能:Y Ksp(CuS)
l·L⁻¹ZnSO₄ 溶液至不再产生白色沉淀,再滴加几
滴 0.1m ol·L⁻¹C úSO₄ 溶液,出现黑色沉淀
CO₂ 过量,生成碳酸氢
B 向氯化钙溶液中通入 CO₂,未出现白色沉淀
钙
C 分别测定 SO₂、CO₂饱和溶液的 pH,前者 pH 小 H₂SO₃酸性强于 H₂CO₃
将 FeCl₃溶液由 0.1m ol·L₁稀释到 0.01 mol·L⁻稀释后,Fe³⁺的水解程
D
¹,则溶液 pH 变大 度增大
【解析】硫化钠溶液与足量硫酸锌溶液完全反应生成硫化锌沉淀和硫酸钠,向反应后的溶液中再加入少量硫酸
铜溶液,白色沉淀转化为黑色沉淀说明硫化锌的溶度积大于硫化铜,A 项正确;向氯化钙溶液中通入( ,
未出现白色沉淀,是因为碳酸的酸性比盐酸的酸性弱,氯化钙和( 不反应,B 项错误;二氧化硫在水中的溶
解度大于二氧化碳,二氧化硫饱和溶液中亚硫酸的浓度大于二氧化碳饱和溶液中碳酸的浓度,则前者饱和溶液
的 pH 小于后者不能说明亚硫酸的酸性强于碳酸,C 项错误;氯化铁在溶液中水解使溶液呈酸性,氯化铁溶液加
水稀释后溶液 pH 变大,是因为加水稀释,溶液中氢离子浓度减小,与水解程度增大无关,D 项错误
10. TiO₂ 是重要的无机材料,一种含有铁的氧化物和氧化钙的 TiO₂废渣可以通过如下流程纯化。
已知:①“铝热还原”时,Al 转化为难溶于酸和碱的( 转化为 ②“浸
取”时,TiO₂溶于盐酸生成易被空气氧化的 下列说法错误的是(C)
A. TiO₂具有弱氧化性
B.“浸取”不需要惰性气体保护
C.“氧化水解”过程中为加快反应速率并使氧化完全,应快速加入过量的)D. H₂可能来自 Fe、过量铝粉及 与盐酸的反应
【解析】二氧化钛废渣与铝粉进行铝热还原生成 和难溶于酸和碱的 同时铁的氧
化物转化为铁单质,加入盐酸后,TiOₓ 、Fe 与盐酸反应生成 和氢气,难溶的 为滤渣,滤液中
被 氧 化 生 成 和 水 解 生 成 过 滤 分 离 , 滤 液 含 有
中 Ti 为高价态,具有弱氧化性,A 正确;“浸取”过程中,不需要惰性气体保护,产生的
在下一步需要氧化生成 B.正确;若快速加入 会在生成的 催化作用下分解,C 错误;
铝热反应中铁的氧化物转化为铁单质, 转化为 (1≤x≤1.5),故氢气可能是铁、过量铝粉及
与盐酸反应产生的,D 正确。
11.伯醇(记为 RCH₂OH)和叔醇(记为 R₃COH)发生酯化反应的机理如下图所示。下列说法不正确的是
(D)
A.用¹⁸O 标记醇羟基,可以分析叔丁醇与乙醇在酯化反应中的断键情况
B.两个历程中 H⁺:均起到催化剂的作用
C.两个历程中均有碳原子的杂化轨道类型发生改变
D.两种酯化反应的机理均为羧基中的羟基与醇羟基中的氢原子结合成水
【解析】结合图,叔醇羟基中的 O 去向水中,而羧基中的 O 去向酯中,乙醇在酯化反应中,乙醇羟基中的 O 去
向酯中,而羧基中的 O 去向水中,所以可以用¹⁸O 标记醇羟基,分析叔丁醇与乙醇在酯化'反应中的断键情况,
故 A 正确;根据两个历程可以分析出 H⁺均先被消耗、后生成,均起到催化剂的作用,故 B 正确;两个历程中都
有碳原子的杂化类型从 sp³变为 sp²,故 C 正确;两种酯化反应的机理,前者是羧基中的羟基与醇羟基的氢原
子结合成水,后者是醇中羟基与酸中羧基上的氢结合成水,不同,故 D 错误。
12.用活性炭还原 NO₂可防止空气污染,其反应原理为 在密闭
容器中,1mol NO₂和足量碳发生该反应,反应相同时间内,测得 NO₂的生成速率与 N₂的生成速率随温度变
化的关系如图 1 所示。维持温度不变,反应相同时间内,测得 NO₂的转化率随压强的变化如图 2 所示。
下列说法正确的是 (C)
A.图 1 中的 A、B、C 三个点中,只有 B 点达到平衡状态B.图 2 中曲线上 E、F、G 三点均表示 NO₂的平衡转化率
C.图 2 中平衡常数 K(E)=K(G),但 NO₂的浓度:c(E)0,△S>0,△G=△H-T△S<0 时该反应才能自发进行,故该反应高温条件下可自发进行。
中 Ca²⁺来自 CaCl₂,NH, 来自 NH₄Cl,[Fe(CN)₆]⁴⁻来自 所,
以反应物有 CaCl₂、NH₄Cl 和 根据元素守恒,除生成 外,还
有 KCl 生成,反应的化学方程式为 +4K
Cl。
(4)根据题给流程和题意可知,滤渣 3 应为 SrCrO₄和 BaCrO₄,加 3%醋酸后“漂洗”可将 溶解,得到
含 Sr²⁺的漂洗液,应该将漂洗液重新投入“一次沉钡”步骤中,C 将合题意。
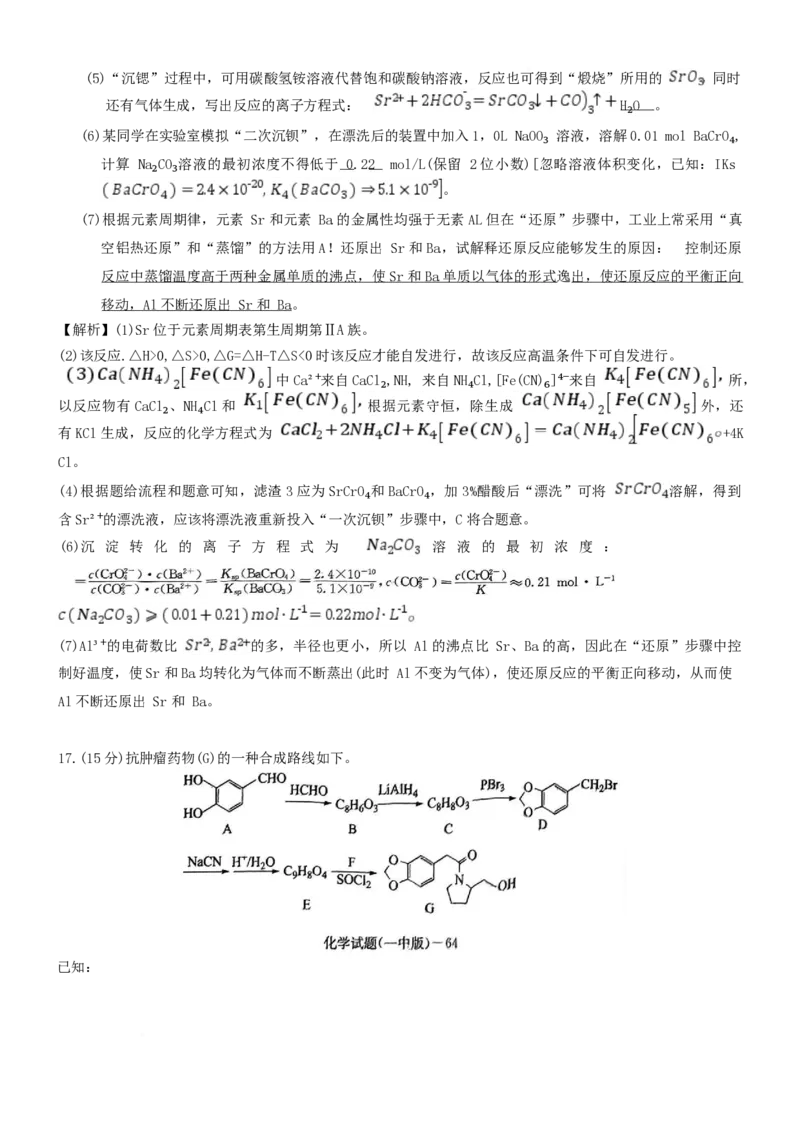
(6)沉 淀 转 化 的 离 子 方 程 式 为 溶 液 的 最 初 浓 度 :
(7)Al³⁺的电荷数比 的多,半径也更小,所以 Al 的沸点比 Sr、Ba 的高,因此在“还原”步骤中控
制好温度,使 Sr 和 Ba 均转化为气体而不断蒸出(此时 Al 不变为气体),使还原反应的平衡正向移动,从而使
Al 不断还原出 Sr 和 Ba。
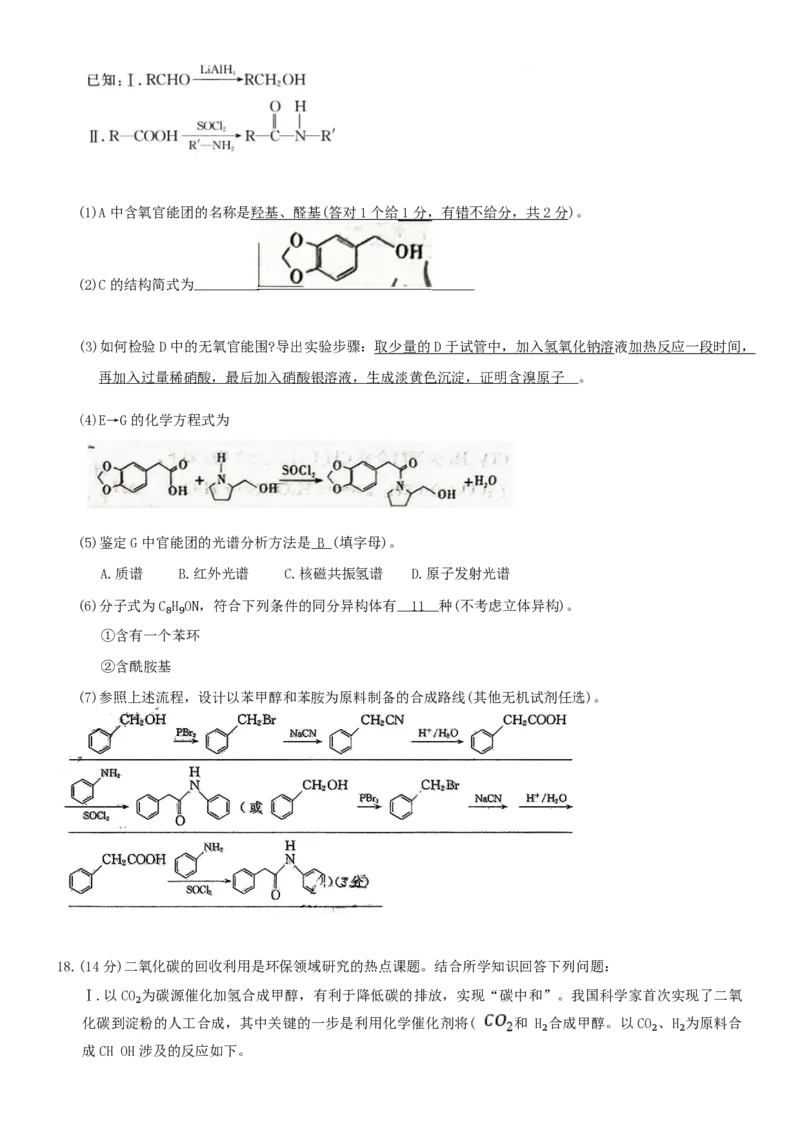
17.(15 分)抗肿瘤药物(G)的一种合成路线如下。
已知:(1)A 中含氧官能团的名称是羟基、醛基(答对 1 个给 1 分,有错不给分,共 2 分)。
(2)C 的结构简式为
(3)如何检验 D 中的无氧官能围?导出实验步骤:取少量的 D 于试管中,加入氢氧化钠溶液加热反应一段时间,
再加入过量稀硝酸,最后加入硝酸银溶液,生成淡黄色沉淀,证明含溴原子 。
(4)E→G 的化学方程式为
(5)鉴定 G 中官能团的光谱分析方法是 B (填字母)。
A.质谱 B.红外光谱 C.核磁共振氢谱 D.原子发射光谱
(6)分子式为 C₈H₉ON,符合下列条件的同分异构体有 11 种(不考虑立体异构)。
①含有一个苯环
②含酰胺基
(7)参照上述流程,设计以苯甲醇和苯胺为原料制备的合成路线(其他无机试剂任选)。
18.(14 分)二氧化碳的回收利用是环保领域研究的热点课题。结合所学知识回答下列问题:
Ⅰ.以 CO₂为碳源催化加氢合成甲醇,有利于降低碳的排放,实现“碳中和”。我国科学家首次实现了二氧
化碳到淀粉的人工合成,其中关键的一步是利用化学催化剂将( 和 H₂合成甲醇。以 CO₂、H₂为原料合
成 CH OH 涉及的反应如下。主反应Ⅰ:(
副反应Ⅱ:(
副反应Ⅲ:(
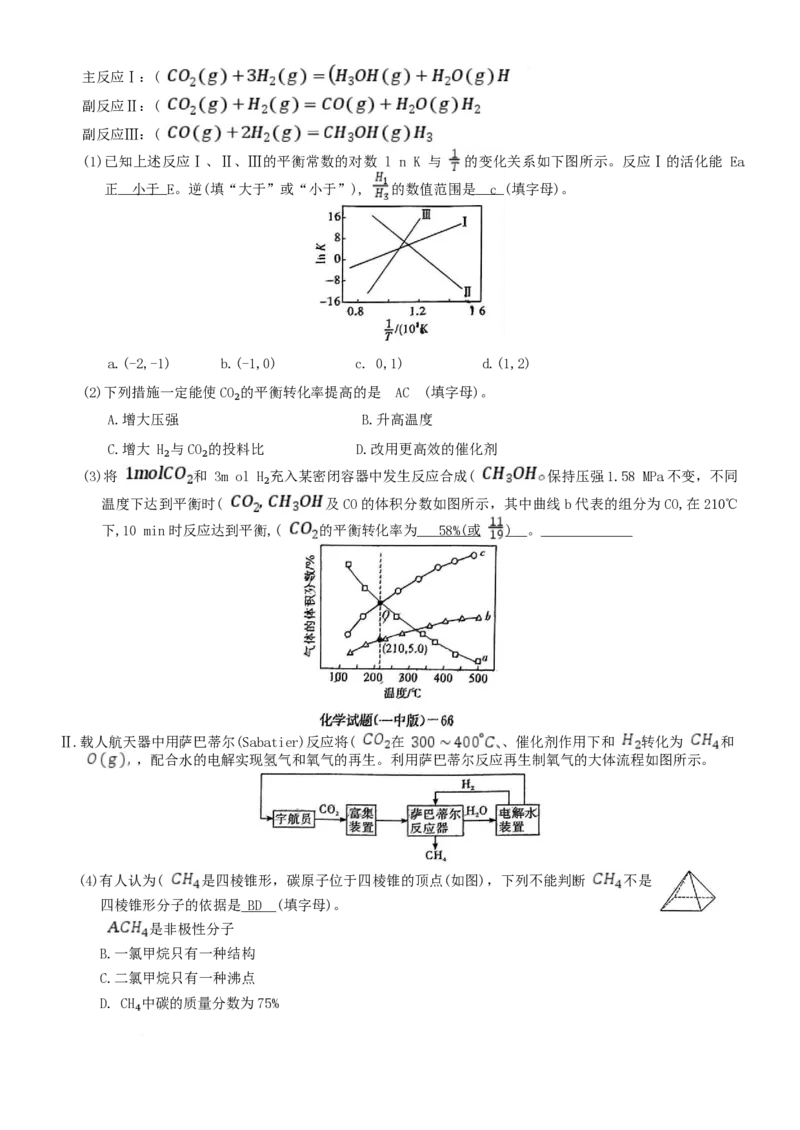
(1)已知上述反应Ⅰ、Ⅱ、Ⅲ的平衡常数的对数 l n K 与 的变化关系如下图所示。反应Ⅰ的活化能 Ea
正 小于 E。逆(填“大于”或“小于”), 的数值范围是 c (填字母)。
a.(-2,-1) b.(-1,0) c. 0,1) d.(1,2)
(2)下列措施一定能使 CO₂的平衡转化率提高的是 AC (填字母)。
A.增大压强 B.升高温度
C.增大 H₂与 CO₂的投料比 D.改用更高效的催化剂
(3)将 和 3m ol H₂充入某密闭容器中发生反应合成( 保持压强 1.58 MPa 不变,不同
温度下达到平衡时( 及 CO 的体积分数如图所示,其中曲线 b 代表的组分为 CO,在 210℃
下,10 min 时反应达到平衡,( 的平衡转化率为 58%(或 ) 。
Ⅱ.载人航天器中用萨巴蒂尔(Sabatier)反应将( 在 、催化剂作用下和 转化为 和
,配合水的电解实现氢气和氧气的再生。利用萨巴蒂尔反应再生制氧气的大体流程如图所示。
(4)有人认为( 是四棱锥形,碳原子位于四棱锥的顶点(如图),下列不能判断 不是
四棱锥形分子的依据是 BD (填字母)。
是非极性分子
B.一氯甲烷只有一种结构
C.二氯甲烷只有一种沸点
D. CH₄中碳的质量分数为 75%(5)已 知 H₂和 ( 的 燃 烧 热 分 别 是
请 写 出 萨 巴 蒂 尔 反 应 的 热 化 学 方 程 式 : 4
。
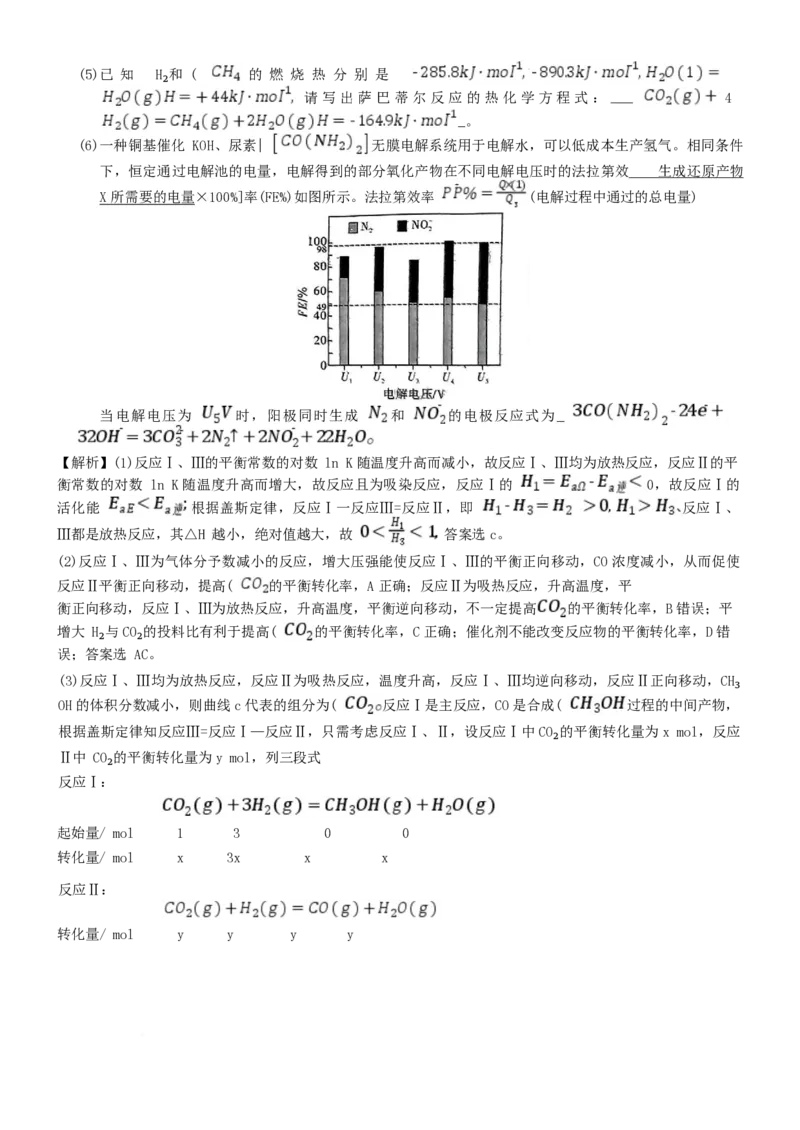
(6)一种铜基催化 KOH、尿素| 无膜电解系统用于电解水,可以低成本生产氢气。相同条件
下,恒定通过电解池的电量,电解得到的部分氧化产物在不同电解电压时的法拉第效 生成还原产物
X 所需要的电量×100%]率(FE%)如图所示。法拉第效率 (电解过程中通过的总电量)
当电解电压为 时,阳极同时生成 和 的电极反应式为
【解析】(1)反应Ⅰ、Ⅲ的平衡常数的对数 ln K 随温度升高而减小,故反应Ⅰ、Ⅲ均为放热反应,反应Ⅱ的平
衡常数的对数 ln K 随温度升高而增大,故反应且为吸染反应,反应Ⅰ的 0,故反应Ⅰ的
活化能 根据盖斯定律,反应Ⅰ一反应Ⅲ=反应Ⅱ,即 反应Ⅰ、
Ⅲ都是放热反应,其△H 越小,绝对值越大,故 答案选 c。
(2)反应Ⅰ、Ⅲ为气体分予数减小的反应,增大压强能使反应Ⅰ、Ⅲ的平衡正向移动,CO 浓度减小,从而促使
反应Ⅱ平衡正向移动,提高( 的平衡转化率,A 正确;反应Ⅱ为吸热反应,升高温度,平
衡正向移动,反应Ⅰ、Ⅲ为放热反应,升高温度,平衡逆向移动,不一定提高 的平衡转化率,B 错误;平
增大 H₂与 CO₂的投料比有利于提高( 的平衡转化率,C 正确;催化剂不能改变反应物的平衡转化率,D 错
误;答案选 AC。
(3)反应Ⅰ、Ⅲ均为放热反应,反应Ⅱ为吸热反应,温度升高,反应Ⅰ、Ⅲ均逆向移动,反应Ⅱ正向移动,CH₃
OH 的体积分数减小,则曲线 c 代表的组分为( 反应Ⅰ是主反应,CO 是合成( 过程的中间产物,
根据盖斯定律知反应Ⅲ=反应Ⅰ—反应Ⅱ,只需考虑反应Ⅰ、Ⅱ,设反应Ⅰ中 CO₂的平衡转化量为 x mol,反应
Ⅱ中 CO₂的平衡转化量为 y mol,列三段式
反应Ⅰ:
起始量/ mol 1 3 0 0
转化量/ mol x 3x x x
反应Ⅱ:
转化量/ mol y y y y由图知,在 210℃达到平衡时,甲醇和二氧化碳的体积分数相等,即甲醇和二氧化碳的物质的量相等,一氧化
碳的体积分数为 5%,n 总=(4-2x) mol,则 解得 x≈0.42,y≈0.16,平衡时,C
O₂为 0.42 mol,故 210℃时,二氧化碳的平衡转化率为 58%。
(4)CH₄是非极性分子,说明分子中正负电荷中心重合,如果 的结构是四棱锥形,则正负电荷中心不能重
合,为极性分子,A 不符合题意;四棱锥形、正四面体形结构中氢原子都只有一种情况,一氯甲烷只有一种结
构,不能判断是否为四棱锥形,B 符合题意;二氯甲烷只有一种沸点,说明只有一种结构,而四棱锥形的甲烷
结构的二氯取代物有两种结构,故 C 不符合题意;( 中碳的质量分数为 75%,不能判断是否为四棱锥形,D
符合题意。
(5)已 知 H₂和 CH₄ 的 燃 烧 热 分 别 是 - 则 反 应 Ⅰ 为
反应Ⅱ为 2H₂O(1) △
H=-890.3kJ·mol⁻¹,令反应Ⅲ为 根据盖斯定律,由反应Ⅰ×4-反
应Ⅱ+反应Ⅲ×2 得
△H ol⁻¹。
(6)由图知,当电解电压为 U₅V 时,N₂和 NO₂的法拉第效率各为 49%,两者的物质的量之比为 1:1,则阳极由 KO
H 和 尿 素 同 时 生 成 N₂ 和 的 电 极 反 应 式 为
(222 改为 22)