文档内容
2023-2024学年上学期佛山市S7高质量发展联盟高三联考试卷
化学学科
命题人:三水中学
本试卷共 8 页,共 20 题,全卷满分100分,考试用时75分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无
效。
3.考试结束后,将答题卡交回。
可能用到的相对原子质量:H:1 C:12 O:16 Mg:24 Al:27 Ca:40 Fe:56
第I卷(共44分)
一 、 选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1 . “化学,让生活更美好”。下列说法不正确的是
A. 医用口罩核心材料聚丙烯是一种合成有机高分子材料
B. 纤维素和淀粉水解的最终产物均是葡萄糖,二者互为同分异构体
C. 国产大飞机 C919 用到的氮化硅陶瓷是一种无机非金属材料
D.“ 中国芯”的主要材料是高纯度的单质硅 ,其结构类似于金刚石
2 . 下列化学用语的表达正确的是
A. 用电子式表示 H O 的形成过程:
2
B. 基态 Cu 原子的价层电子排布式为:3d104s1
C. 邻羟基苯甲醛分子内氢键示意图:
D. SO 的 VSEPR模型:
3
化学试卷 第1页(共8页)
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}3 . 某有机物结构简式如图 。关于该有机物说法错误的是
A. 可以发生取代反应和氧化反应
B. 碳原子杂化方式有两种
C. 分子中所有原子可能共平面
D. 1mol该物质最多可以与 2mol NaOH 反应
4 . 设 NA 为阿伏加德罗常数的值 。下列说法正确的是
A. 常温常压下,46g NO 中所含分子数目为 NA
2
B. 标准状况下,11.2L HF 含有 5NA 个质子
C. 1 mol 苯中含有 3NA 个碳碳双键
D. 1L 1mol·L-1 FeCl 溶液中所含阳离子数目大于 NA
3
5 . 下列反应的离子方程式正确的是
A. 向 KAl(SO ) 溶液中加入氨水:Al3+ + OH - = Al(OH) ↓
4 2 3
B. 过量铁粉与稀硝酸反应:Fe + 4H + + NO - = Fe3+ + NO↑ + 2H O
3 2
C. 用碳酸钠溶液处理水垢中的硫酸钙:CO 2- + CaSO = CaCO + SO 2-
3 4 3 4
D. 向酸性 KMnO 溶液中滴加双氧水:2MnO-+ HO+ 6H+= 2Mn2++ 3O↑+ 4HO
4 4 2 2 2 2
6. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 使淀粉-KI溶液变蓝的溶液:H、NH、S2、Br
4
B. 滴入酚酞呈红色的溶液:Na、K、CH COO、Cl
3
C. 滴入苯酚显紫色的溶液:Mg2、NH、Cl、SCN
4
D. 滴入甲基橙呈红色的溶液:K、Na、HCO、NO
3 3
7. 劳动创造美好生活。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 实践活动:豆浆加石膏“点卤”制豆腐 石膏使豆浆所含蛋白质沉淀
B 实验活动:用硝酸清洗银镜反应后的试管 硝酸具有较强的氧化性
C 农业活动:用熟石灰改良酸性土壤 CaO 是一种碱性氧化物
D 社区服务:回收铝制易拉罐 再利用废旧金属,节约资源
化学试卷 第2页(共8页)
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}8. 物质的变化体现了化学的美,下列物质的转化在给定条件下能实现的是
①Al O NaOH aq NaAlO aq CO 2Al OH
2 3 △ 2 3
②SO2 /点燃SO H2 OH SO
3 2 4
③饱和NaCl aq NH 3 ,CO2NaHCO △Na CO
△ 3 2 3
④
⑤NH O 2NO O2NO H2 OHNO
3 催化剂、加热 2 空气 3
⑥SiO CSi 粗 HClSiHCl 过量H 2Si 纯
2 高温 300℃ 3 1100℃
A. ②③④⑥ B. ①③④⑤ C. ①②④⑤ D. ①③⑤⑥
9. 类比是学习化学的重要方法,下列类比结果合理的是
选项 已知 推理
A 电解熔融的 MgCl 冶炼镁 电解熔融的 AlCl 也能冶炼铝
2 3
B CO 能使澄清石灰水变浑浊 SO 也能使澄清石灰水变浑浊
2 2
C C H 分子的空间结构为直线形 H O 分子的空间结构也为直线形
2 2 2 2
D 溶解度:Ca(HCO ) > CaCO 溶解度:NaHCO > NaCO
3 2 3 3 2 3
10.硫及其化合物的“价-类二维图”体现了化学变化之美。下列有关说法正确的是
A .硫在过量的氧气中燃烧直接生成Y
B .将X 通入BaCl 溶液中有白色沉淀生成
2
C .Z 常温下与Cu 生成M,有蓝色的固体粉末生成
D .HS 与Z 反应可生成X ,X 分子中的 S 是 sp2 杂化
2
11. MnO 催化除去HCHO的机理如图所示,下列说法不正确的是
2
A.反应①~④均是氧化还原反应
B.反应②中碳氧双键未断裂
C. HCHO中碳原子采取sp2杂化
D.上述机理总反应为HCHOO MnO2CO H O
2 2 2
化学试卷 第3页(共8页)
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}12.一种工业有机洗涤剂中间体结构式如图所示,其中短周期元素 X、Y、Z、Q、W 的原子序 数依次增大,X
和 W 同主族但不相邻,Y 和 Q 原子最外层电子数之和是 Z原子 L层电子数的二倍,X、Y、Z、W 均可与 Q
形成至少两种二元化合物 。下列说法正确的是
A. 第一 电离能:Z < Q
B. 键能:X2 < Z2
C. 简单离子半径:Q < W
D. 最简单氢化物的键角:Y < Q
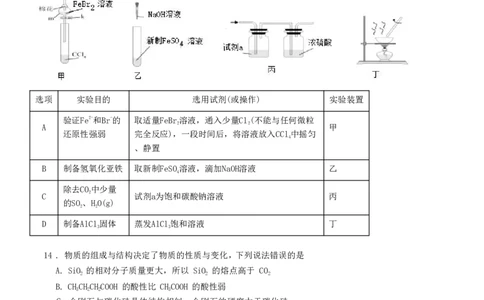
13. 化学是一门以实验为基础的学科。下列所选试剂(或操作)和实验装置合理的是
选项 实验目的 选用试剂(或操作) 实验装置
验证Fe2+和Br-的 取适量FeBr溶液,通入少量Cl(不能与任何微粒
A 2 2 甲
还原性强弱 完全反应),一段时间后,将溶液放入CCl中摇匀
4
、静置
B 制备氢氧化亚铁 取新制FeSO溶液,滴加NaOH溶液 乙
4
除去CO中少量
C 2 试剂a为饱和碳酸钠溶液 丙
的SO、HO(g)
2 2
D 制备AlCl固体 蒸发AlCl饱和溶液 丁
3 3
14 . 物质的组成与结构决定了物质的性质与变化,下列说法错误的是
A. SiO 的相对分子质量更大,所以 SiO 的熔点高于 CO
2 2 2
B. CHCHCHCOOH 的酸性比 CHCOOH 的酸性弱
3 2 2 3
C. 金刚石与碳化硅晶体结构相似,金刚石的硬度大于碳化硅
D. 配位能力 NH 大于 H O,向[Cu(H O) ]2+ 中加过量氨水生成[Cu(NH ) ]2+
3 2 2 4 3 4
15. FeF 是制备硫化物全固态钮电池高能正极材料的原料 。一种制备 FeF 材料的生产流 程如下:
3 3
下列叙述正确的是
A.“混合溶液”时要用到烧杯、玻璃棒
化学试卷 第4页(共8页)
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}B.“反应器”中温度越高,越有利于制备 FeF
3
C.“ 系列操作”得到的滤液,可采用分液的方法循环利用
D.“灼烧”时通入 Ar 的主要作用是带走水蒸气防止 FeF 水解
3
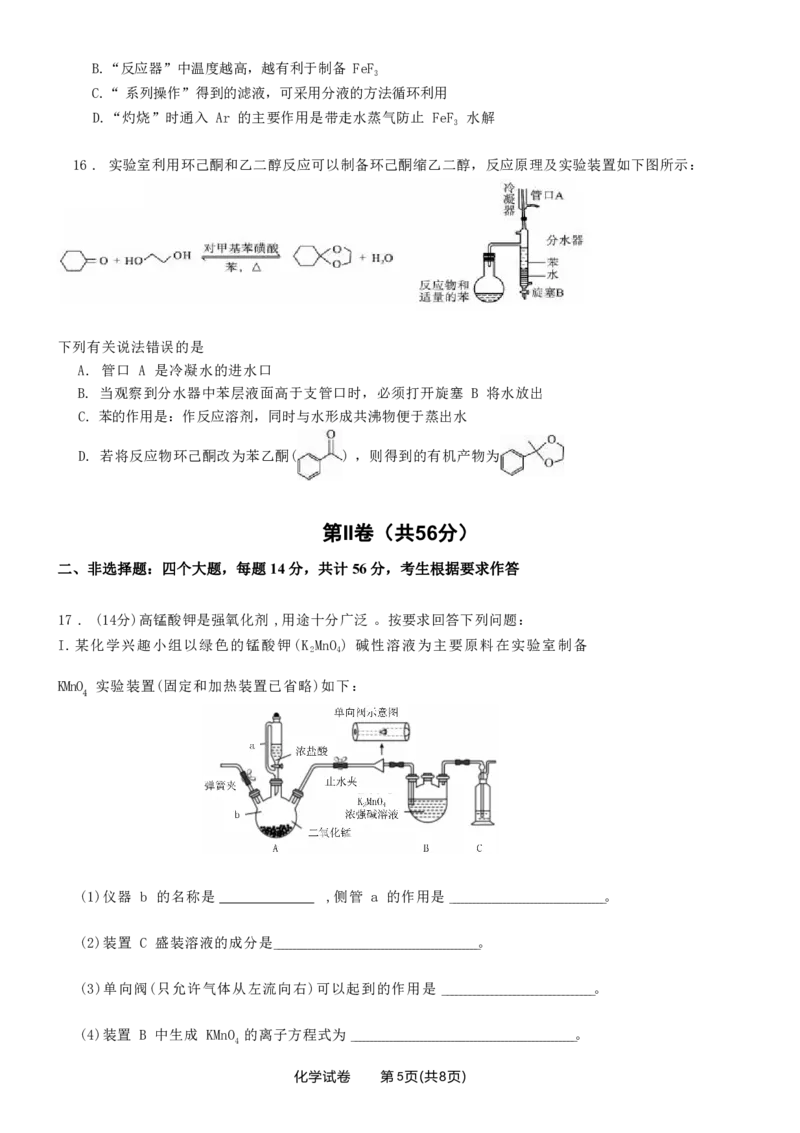
16 . 实验室利用环己酮和乙二醇反应可以制备环己酮缩乙二醇,反应原理及实验装置如下图所示:
下列有关说法错误的是
A. 管口 A 是冷凝水的进水口
B. 当观察到分水器中苯层液面高于支管口时,必须打开旋塞 B 将水放出
C. 苯的作用是:作反应溶剂,同时与水形成共沸物便于蒸出水
D. 若将反应物环己酮改为苯乙酮( ) ,则得到的有机产物为
第 卷(共 分)
II 56
二、非选择题:四个大题,每题14分,共计56分,考生根据要求作答
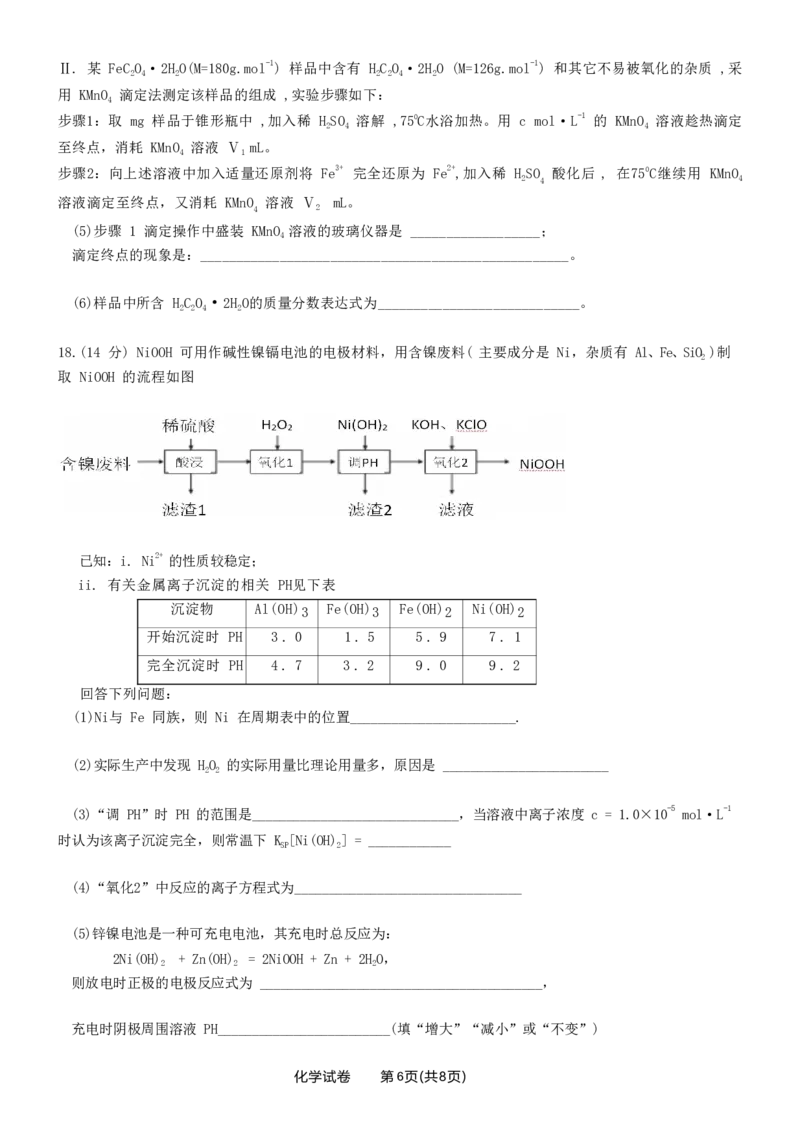
17 . (14分)高锰酸钾是强氧化剂 ,用途十分广泛 。按要求回答下列问题:
I.某化学兴趣小组以绿色的锰酸钾(K MnO ) 碱性溶液为主要原料在实验室制备
2 4
KMnO 实验装置(固定和加热装置已省略)如下:
4
(1)仪器 b 的名称是 ,侧管 a 的作用是 ________________________________________。
(2)装置 C 盛装溶液的成分是_____________________________________________________。
(3)单向阀(只允许气体从左流向右)可以起到的作用是 __________________________________。
(4)装置 B 中生成 KMnO 的离子方程式为 __________________________________________________________。
4
化学试卷 第5页(共8页)
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}Ⅱ. 某 FeC O ·2H O(M=180g.mol-1) 样品中含有 H C O ·2H O (M=126g.mol-1) 和其它不易被氧化的杂质 ,采
2 4 2 2 2 4 2
用 KMnO 滴定法测定该样品的组成 ,实验步骤如下:
4
步骤1:取 mg 样品于锥形瓶中 ,加入稀 H SO 溶解 ,750C水浴加热。用 c mol·L-1 的 KMnO 溶液趁热滴定
2 4 4
至终点,消耗 KMnO 溶液 Ⅴ mL。
4 1
步骤2:向上述溶液中加入适量还原剂将 Fe3+ 完全还原为 Fe2+,加入稀 H SO 酸化后 , 在750C继续用 KMnO
2 4 4
溶液滴定至终点,又消耗 KMnO 溶液 Ⅴ mL。
4 2
(5)步骤 1 滴定操作中盛装 KMnO 溶液的玻璃仪器是 __________________;
4
滴定终点的现象是:___________________________________________________。
(6)样品中所含 H C O ·2H O的质量分数表达式为____________________________。
2 2 4 2
18.(14 分) NiOOH 可用作碱性镍镉电池的电极材料,用含镍废料( 主要成分是 Ni,杂质有 Al、Fe、SiO )制
2
取 NiOOH 的流程如图
已知:i. Ni2+ 的性质较稳定;
ii. 有关金属离子沉淀的相关 PH见下表
沉淀物 Al(OH)3 Fe(OH)3 Fe(OH)2 Ni(OH)2
开始沉淀时 PH 3. 0 1. 5 5. 9 7. 1
完全沉淀时 PH 4. 7 3. 2 9. 0 9. 2
回答下列问题:
(1)Ni与 Fe 同族,则 Ni 在周期表中的位置________________________.
(2)实际生产中发现 HO 的实际用量比理论用量多,原因是 ________________________
2 2
(3)“调 PH”时 PH 的范围是______________________________,当溶液中离子浓度 c = 1.0×10-5 mol·L-1
时认为该离子沉淀完全,则常温下 K [Ni(OH)] = ____________
SP 2
(4)“氧化2”中反应的离子方程式为_________________________________
(5)锌镍电池是一种可充电电池,其充电时总反应为:
2Ni(OH) + Zn(OH) = 2NiOOH + Zn + 2HO,
2 2 2
则放电时正极的电极反应式为 _________________________________________,
充电时阴极周围溶液 PH_________________________(填“增大”“减小”或“不变”)
化学试卷 第6页(共8页)
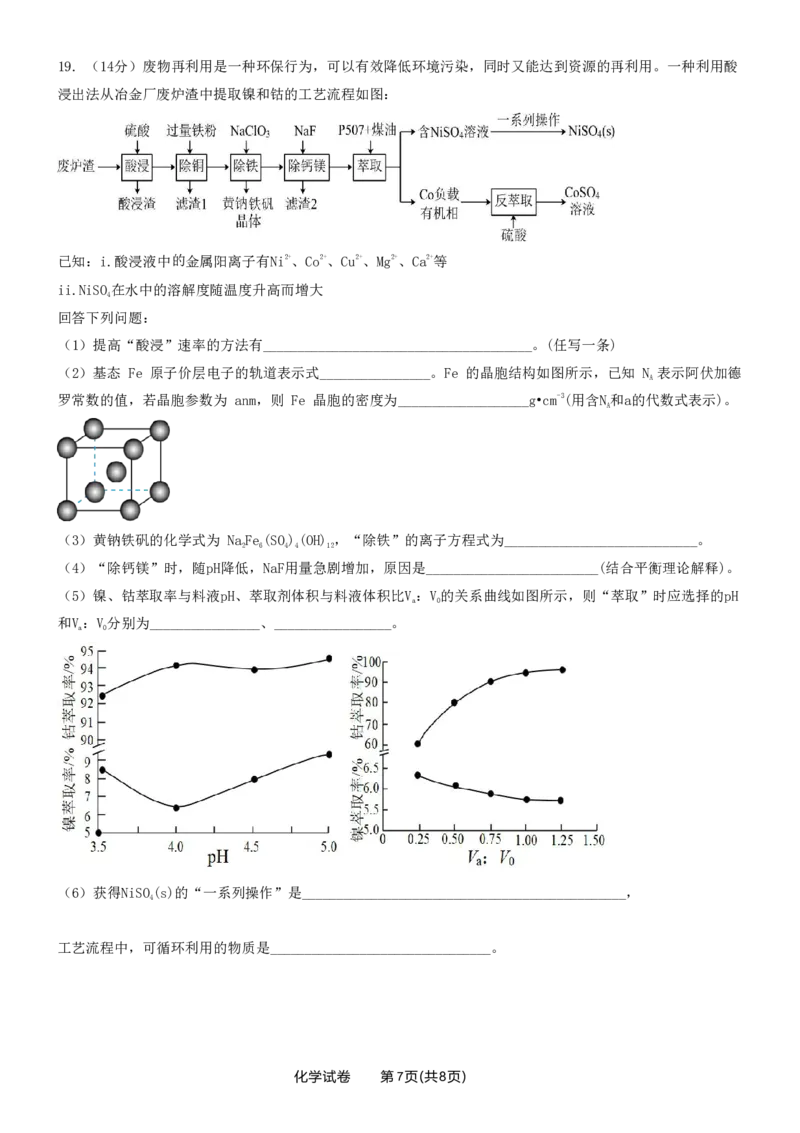
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}19. (14分)废物再利用是一种环保行为,可以有效降低环境污染,同时又能达到资源的再利用。一种利用酸
浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如图:
已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO在水中的溶解度随温度升高而增大
4
回答下列问题:
(1)提高“酸浸”速率的方法有_______________________________________。(任写一条)
(2)基态 Fe 原子价层电子的轨道表示式________________。Fe 的晶胞结构如图所示,已知 N 表示阿伏加德
A
罗常数的值,若晶胞参数为 anm,则 Fe 晶胞的密度为___________________g•cm-3(用含N和a的代数式表示)。
A
(3)黄钠铁矾的化学式为 NaFe(SO)(OH) ,“除铁”的离子方程式为____________________________。
2 6 4 4 12
(4)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是_________________________(结合平衡理论解释)。
(5)镍、钴萃取率与料液pH、萃取剂体积与料液体积比V:V的关系曲线如图所示,则“萃取”时应选择的pH
a 0
和V:V分别为________________、_________________。
a 0
(6)获得NiSO(s)的“一系列操作”是_______________________________________________,
4
工艺流程中,可循环利用的物质是________________________________。
化学试卷 第7页(共8页)
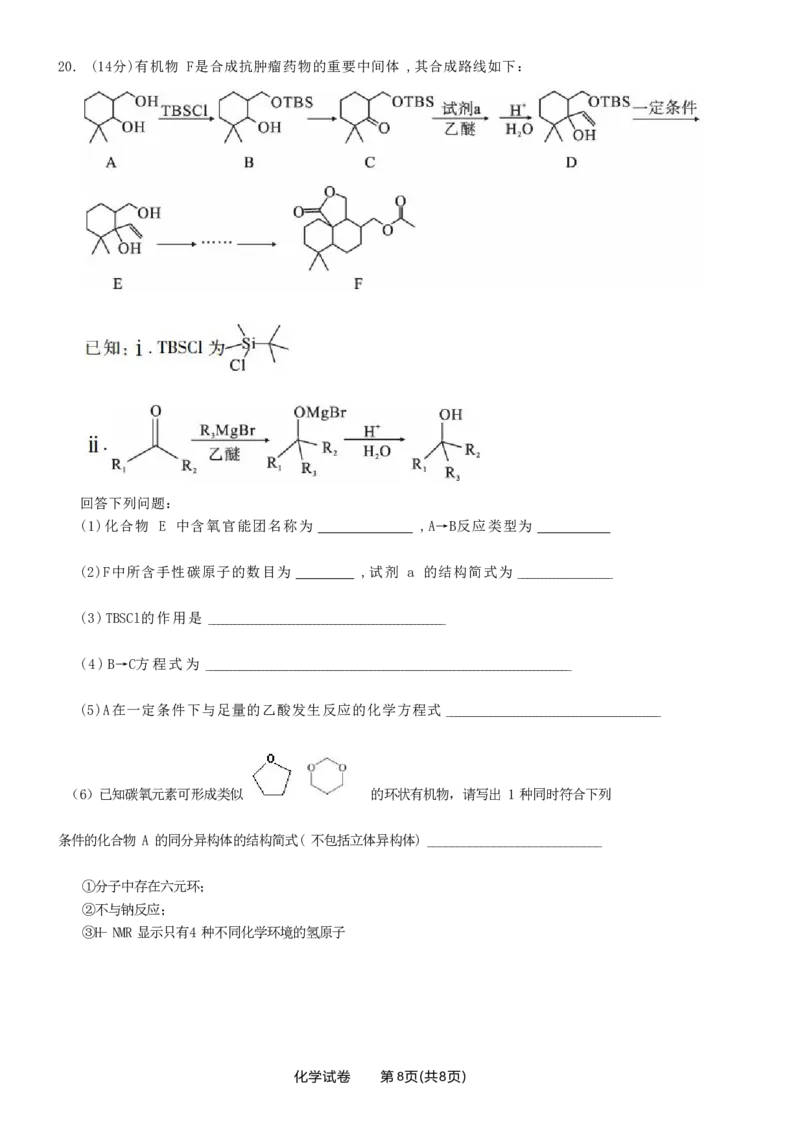
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}20. (14分)有机物 F是合成抗肿瘤药物的重要中间体 ,其合成路线如下:
回答下列问题:
(1)化合物 E 中含氧官能团名称为 ,A→B反应类型为
(2)F中所含手性碳原子的数目为 ,试剂 a 的结构简式为 ________________________
(3)TBSCl的作用是 ________________________________________________________
(4)B→C方程式为 ___________________________________________________________________________________________
(5)A在一定条件下与足量的乙酸发生反应的化学方程式 ______________________________________________________
(6)已知碳氧元素可形成类似 的环状有机物,请写出 1 种同时符合下列
条件的化合物 A 的同分异构体的结构简式( 不包括立体异构体) _____________________________
①分子中存在六元环;
②不与钠反应;
③H- NMR 显示只有4 种不同化学环境的氢原子
化学试卷 第8页(共8页)
{#{QQABBQCEggCAQABAAQhCEwViCAAQkBECACoOxAAIsAAAQANABAA=}#}