文档内容
本溪高中 2023-2024 学年度高考适应性测试(一)
化学参考答案
1.A
【详解】A.增大压强加快反应速率,且合成氨的反应为体积缩小的反应,则加压平衡正向移动,有利于提高产率,
选项A正确;
B.催化剂对平衡移动无影响,不影响产率,选项B错误;
C.二氧化硫的催化氧化反应为放热反应,则升高温度平衡逆向移动,产率降低,选项C错误;
D.侯氏制碱法循环利用母液可提高产率,但对反应速率无影响,选项D错误;
答案选A。
2.C
【详解】A、在bL时,溶液为NaCl、NaAlO 溶液,由图象可知:n[Al(OH)]=0.1mol,n(Mg(OH)]=0.2mol-
2 3 2
0.1mol=0.1mol,根据Mg原子守恒有n(MgCl )=n(Mg(OH)]=0.1mol,根据Al原子守恒有n(NaAlO )=n
2 2 2
(AlCl )=n[Al(OH)]=0.1mol,由Cl原子守恒有n(Cl)=n(NaCl)=2n(MgCl )+3n(AlCl )=
3 3 2 3
2×0.1mol+3×0.1mol=0.5mol,由Na原子守恒有n(NaOH)=n(NaCl)+n(NaAlO )=0.5mol+0.1mol=0.6mol,所
2
以c(NaOH)=0.6mol÷1L=0.6mol/L,A正确;
B、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,B正确;
C、根据以上分析可知混合溶液中n(Al3+)︰n(Mg2+)=1∶1,C错误;
D、加入aLNaOH溶液时,沉淀达最大值共0.2mol,由反应方程式可知,此时溶液为NaCl溶液,在bL时,即再继续
滴加NaOH溶液(b﹣a)L时,氢氧化铝与NaOH恰好反应,氢氧化铝完全溶解,沉淀为氢氧化镁0.1mol,溶液为
NaCl、NaAlO 溶液,所以两部分NaOH溶液的体积之比等于消耗的NaOH的物质的量之比,即为n(NaCl)与n
2
(NaAlO )之比,故oa:ab=a:(b﹣a)=0.5mol:0.1mol=5:1,D正确,
2
答案选C。
3.D
【详解】A.过氧化钠与水反应生成氢氧化钠和氧气,过氧化钠是氧化物,不能拆开,离子方程式为:
,A项错误;
B.将少量SO 通入NaClO溶液中,发生氧化还原反应,离子方程式为: ,B
2
项错误;
C.向硝酸银溶液中滴入少量稀氨水,氨水少量且生成的氢氧化银不稳定,所以离子方程式为:
,C项错误;
D.用饱和 溶液浸泡锅炉中的 ,利用溶解度较大的沉淀向溶解度较小的沉淀转化,离子方程式为:
答案第1页,共2页
学科网(北京)股份有限公司公众号:高中试卷君
,D项正确;
答案选D。
4.C
【详解】A.乙烯和溴的四氯化碳溶液发生加成反应生成1,2-二溴乙烷,故A错误;
B.乙烯和酸性高锰酸钾溶液发生氧化反应,乙烯被氧化为CO 气体,故B错误;
2
C.在光照条件下甲烷和氯气反应发生取代反应,生成甲烷的氯代物,故C正确;
D.在镍做催化剂、加热的条件下苯和氢气发生加成反应生成环己烷,故D错误;
故选:C。
5.C
【详解】A.由图示可知,核内质子数等于核外电子数,A表示原子,故A不符合题意;
B.由图示可知,核内质子数比核外电子数多1,带1个正电荷;依据简单离子所带的电荷和该元素的化合价的数值相
同,化合价为+1,故B不符合题意;
C.由图示可知:核内质子数比核外电子数多2,带2个正电荷;依据离子所带的电荷和该元素的化合价的数值相同,
化合价为+2,故C符合题意;
D.由图示可知:核内质子数比核外电子数多3,带3个正电荷;依据离子所带的电荷和该元素的化合价的数值相同,
化合价为+3,故D不符合题意;
故答案为C。
【点睛】明确原子结构与离子结构的特点是解题关键,根据当核电荷数=质子数=核外电子数,为原子;当核电荷数=
质子数>核外电子数,为阳离子;当核电荷数=质子数<核外电子数,为阴离子;特别注意离子所带的电荷和该元素
的化合价的数值相同。
6.A
【分析】根据球棍模型可知A是CH,B是C H,C是C H,D是C H,然后根据物质的性质分析解答。
4 2 4 2 2 6 6
【详解】A.根据图示可知物质C是乙炔,分子式是C H,物质D是苯,分子式是C H,二者最简式都是CH,其含
2 2 6 6
碳量较大,因此若将C进行燃烧,预测会和D一样火焰明亮,产生浓黑烟,A正确;
B.物质A是CH,B是C H,乙烯分子中含有不饱和的碳碳双键,能够被酸性KMnO 溶液氧化为CO 气体,因此若
4 2 4 4 2
A中混有B,不可用高锰酸钾溶液除杂,否则会引入新的杂质,B错误;
C.A分子是正四面体结构,分子中的键角为109°28′,C错误;
D.苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的一种特殊的化学键,它们的键长、键能都相同,不存在典型
的碳碳双键和碳碳单键,D错误;
故合理选项是A。
7.D
【详解】A.从图上可知,反应物能量比生成物能量高,反应放热,故A错误;
B.由图知, H=生成物总能量-反应物总能量=E-E ,故B错误;
1 2
△
答案第2页,共2页C.反应②为放热反应,因此 转变成 的过程不一定需要吸收热量,故C错误;
D.根据盖斯定律,将②×3-①×2可得:CHOH(g)+ O(g)=CO (g)+2HO(l)
3 2 2 2
△H=-192.9kJ/mol×3-49kJ/mol×2=-676.7kJ/mol,即 完全燃烧生成 和 放出的热量应
676.7kJ,故D正确;
故选D。
8.B
【详解】A.混合气进行循环利用可以节约能源、提高原料的利用率,这遵循绿色化学思想,选项A正确;
B.降低温度,反应速率减慢,为保证速率较快,催化剂的活性高,产物的产率又不低,则选择适宜的温度即可,不能
在低温下进行,选项B错误;
C.对原料气进行压缩,即增大压强,化学平衡正向移动,可以增大原料气的转化率,选项C正确;
D.催化剂的特点:提高反应的速率,但是不能使平衡移动,使用催化剂可以提高反应的速率,但是不能使平衡向正反
应方向移动,选项D正确;
故答案选B。
9.C
【详解】A.羟基中氧原子最外层为7个电子,羟基中含有1个氧氢键,羟基正确的电子式为 ,故A错误;
B.苯的分子式为C H,故B错误;
6 6
C.醛基为醛类的官能团,醛基的结构简式为−CHO,故C正确;
D.聚丙烯为丙烯通过加聚反应生成的,聚丙烯的链节中主链含有2个碳原子,聚丙烯正确的结构简式为
,故D错误。
答案选C。
10.D
【详解】A.铁为固体,不能用来表示反应速率,A不正确;
B.5.6g铁是0.1mol,消耗硫酸也是0.1mol,所以用硫酸表示的反应速率是v(H SO )= ,
2 4
B不正确;
C.氢气逸出,不知道氢气的体积,无法计算,C不正确;
D.由于反应速率之比是相应的化学计量数之比,所以v(FeSO )=v(H SO )=0.5 mol·L-1·min-1,D正确。
4 2 4
答案选D。
11.C
答案第3页,共2页
学科网(北京)股份有限公司公众号:高中试卷君
【详解】A.Ca(OH) 溶液与少量NaHCO 溶液反应生成碳酸钙、氢氧化钠和水,离子方程式为:
2 3
,与过量的NaHCO 反应也会有碳酸钙生成,A错误;
3
B.Fe (SO ) 与Ba(OH) 溶液混合反应的离子方程式为: ,B错误;
2 4 3 2
C.等体积等物质的量浓度的AlCl 、Ba(OH) 、HCl溶液混合离子方程式为:3H++Al3++6OH-=Al(OH) ↓+3H O,C正确;
3 2 3 2
D.“侯德榜制碱”离子方程式为:Na++CO +NH+H O= + ,D错误;
2 3 2
故选C。
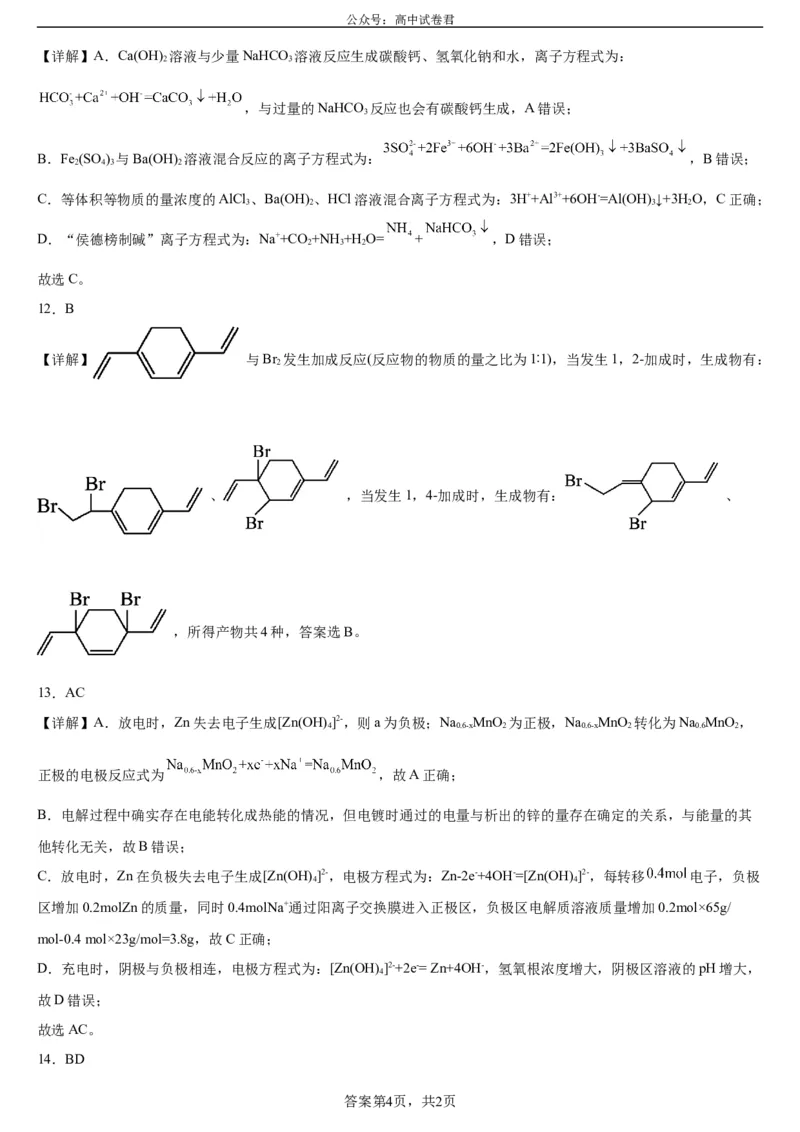
12.B
【详解】 与Br 发生加成反应(反应物的物质的量之比为1∶1),当发生1,2-加成时,生成物有:
2
、 ,当发生1,4-加成时,生成物有: 、
,所得产物共4种,答案选B。
13.AC
【详解】A.放电时,Zn失去电子生成[Zn(OH) ]2-,则a为负极;Na MnO 为正极,Na MnO 转化为Na MnO ,
4 0.6-x 2 0.6-x 2 0.6 2
正极的电极反应式为 ,故A正确;
B.电解过程中确实存在电能转化成热能的情况,但电镀时通过的电量与析出的锌的量存在确定的关系,与能量的其
他转化无关,故B错误;
C.放电时,Zn在负极失去电子生成[Zn(OH) ]2-,电极方程式为:Zn-2e-+4OH-=[Zn(OH) ]2-,每转移 电子,负极
4 4
区增加0.2molZn的质量,同时0.4molNa+通过阳离子交换膜进入正极区,负极区电解质溶液质量增加0.2mol×65g/
mol-0.4 mol×23g/mol=3.8g,故C正确;
D.充电时,阴极与负极相连,电极方程式为:[Zn(OH) ]2-+2e-= Zn+4OH-,氢氧根浓度增大,阴极区溶液的pH增大,
4
故D错误;
故选AC。
14.BD
答案第4页,共2页【详解】A. 6mol/L硫酸中加入 0.5 mol/L硫酸,硫酸浓度减小,反应速率减慢,硫酸物质的量增大,生成H 的总量增
2
多,故不选A;
B. 6mol/L硫酸中加水,硫酸浓度减小,反应速率减慢,硫酸物质的量不变,所以生成H 的总量不变,故选B;
2
C. 6mol/L硫酸中加入氢氧化钠固体,氢氧化钠消耗硫酸,硫酸浓度减小,反应速率减慢,硫酸物质的量减小,生成
H 的总量减少,故不选C;
2
D. 6mol/L硫酸中加入硫酸钠溶液,硫酸浓度减小,反应速率减慢,硫酸物质的量不变,所以生成H 的总量不变,故
2
选D;选BD。
15.BD
【分析】由题意判断图1为GaF 的晶胞,图2为AlCl 的结构,图3为 的晶胞。
2 3
【详解】A.图1中顶点和面心是Ga2+,四面体内较大的小球表示F-,距离钙离Ga2+子最近且等距离的F-有8个,则
Ga2+的配位数为8,距离F-最近且等距离的Ga2+有4个,则F-的配位数为4,故A正确;
B.图1为GaF 的晶胞,GaF 是离子晶体,图2为AlCl 的结构,AlCl 是共价化合物,离子化合物的熔点一般高于共
2 2 3 3
价化合物,则GaF 熔点高于AlCl ,故B错误;
2 3
C.由图3可看出,与体心原子等距离且最近的顶点原子有8个,故C正确;
D. 为离子化合物,故D错误;
故答案选BD。
16.(1)降温并冷凝
(2)f→g→h(i)→i(h)→b→c→d-e
(3)
(4)作脱水剂
(5)取最后一次洗涤液,滴加硝酸酸化的 溶液,若无白色沉淀生成,则说明固体已洗涤干净
(6)除去炭粉,并将 氧化为
(7)93.2%
【分析】I.回收锌元素时,SOCl 作为一种常用的脱水剂,可以去除ZnCl•xH O晶体中的HO,得到无水ZnCl;回收
2 2 2 2 2
SOCl 时需要加热,装置中的冰水可以降温并冷凝SOCl ,因为SOCl 与HO发生水解生成两种气体,根据提示,该反
2 2 2 2
应为 ;想要验证生成物中含有SO ,需要防止水蒸气倒吸入锥形瓶中,因此先连接盛放
2
浓硫酸的试剂瓶,再将气体通入品红溶液中进行SO 的检验,最后通入NaOH溶液中进行尾气处理,空瓶是为了防倒
2
吸。
答案第5页,共2页
学科网(北京)股份有限公司公众号:高中试卷君
【详解】(1)装置中冰水的作用是降温并冷凝SOCl ;
2
(2)根据分析,装置的正确连接顺序为a→f→g→h→i→b→c→d→e;
(3)三颈烧瓶中SOCl 与ZnCl•xH O晶体混合制取无水ZnCl,具体反应为:
2 2 2 2
xSOCl +ZnCl •xH O=ZnCl +xSO↑+2xHCl↑;
2 2 2 2 2
(4)SOCl 作脱水剂,与水反应生成HCl可以抑制氯化锌的水解;
2
(5)步骤①得到的固体表面有Cl-,判断固体洗涤干净的方法是检验洗涤液中是否含有Cl-,因此答案为:取最后一次
洗涤液,滴加硝酸酸化的AgNO 溶液,若无白色沉淀生成,则说明固体已洗涤干净;
3
(6)洗涤后的固体主要含有MnO 、MnOOH和C,高温灼烧可以将C转化为CO,同时将MnOOH转化为MnO ,因
2 2 2
此答案为:除去碳粉,并将MnOOH氧化为MnO ;
2
(7) 。
根据反应可得关系式: 、 ,
消耗的 的物质的量 ,
因此 消耗的 的物质的量 ,
产品的纯度: % %。
17.(1) 乙酸乙酯 乙酸钠 1,2-二溴乙烷
(2) CH COOCH CH+NaOH CHCOONa+CH CHOH 水解反应
3 2 3 3 3 2
(3)
(4) CH -CH-OH CH=CH ↑+H O 消去反应
3 2 2 2 2
(5)CH CHCHCOOH、CHCH(COOH)CH ;HCOOCH CHCH
3 2 2 3 3 2 2 3
【分析】某有机物A,分子式为C HO,它是具有水果香味的液体,难溶于水,说明A为酯,碱性水解生成B和C,
4 8 2
C能经过两步氧化,结合B的结构简式可知,A为乙酸乙酯, C为CHCHOH,根据题中各物质的转化关系,可以推
3 2
得D为CHCHO,E为CHCOOH,F为CH=CH ,H为 BrCHCHBr,据此分析解题。
3 3 2 2 2 2
【详解】(1)由上面的分析可知,A是乙酸乙酯,B是乙酸钠,C是乙醇,D是乙醛,E是乙酸,F是乙烯,H是1,
2-二溴乙烷;
(2)A生成B和C,是乙酸乙酯在碱性条件下水解为乙酸钠和乙醇,方程式为:CHCOOCH CH+NaOH
3 2 3
答案第6页,共2页CHCOONa+CH CHOH,反应类型为水解反应;
3 3 2
(3)根据分析可知C为乙醇,乙醇氧化为乙醛,C生成D的化学方程式 ;
(4)根据分析可知C为乙醇,F为乙烯,C生成F的化学方程式为:CH-CH-OH CH=CH ↑+H O,反应类型为消
3 2 2 2 2
去反应;
(5)分子式相同结构不同为同分异构体,A的三个同分异构体分别是:丁酸CHCHCHCOOH、2-甲基丙酸
3 2 2
CHCH(COOH)CH ;甲酸丙酯HCOOCH CHCH
3 3 2 2 3
丙酸甲酯CHCHCOOCH ,甲酸异丙酯HCOOCH(CH )CH,任选三种。
3 2 3 3 3
18. Na > 离子键,极性共价键 分液漏斗
稀硫酸 浑浊 HO>HS H O分子间存在氢键
2 2 2
【分析】由元素在周期表中的位置可知,A为 H,D为 C,F为 O,G为 Na,Q为 Al,M为 S,R 为 Cl。
【详解】(1)同周期从左到右半径减小,同主族从上到下半径增大,故半径最大元素为:Na
(2)金属性同周期从左到右减弱,G>Q
(3)Q为Al,铝原子原子结构示意图为: ;A、F为H、O,组成原子个数比为1:1的化合物为HO,电子式
2 2
为: ;D和F为C和O,能组成原子个数比为1:2的化合物为CO,结构式为: 。
2
(4) A、G、F三种元素为H、Na、O,组成的化合物为NaOH,离子化合物,含有离子键,OH-中含有极性共价键,故
A、G、F三种元素组成的化合物中有哪些化学键为:离子键,极性共价键
(5) ①如图所示A为分液漏斗;
②非金属性越强其最高价氧化物对应水化物的酸性越强,故证明D碳和M硫两种元素非金属性:S>C,可以通过硫酸
的酸性比碳酸强来证明,故通过硫酸和碳酸盐反应生成CO,强酸制弱酸来证明,故A中盛装稀硫酸,B中盛装碳酸
2
钠溶液,发生反应HSO +NaCO =Na SO +CO ↑+H O,C中盛装澄清石灰水,通过澄清石灰水变浑浊检验CO 的生成,
2 4 3 2 4 2 2 2
故答案为:A中盛装稀硫酸;C中澄清石灰水变浑浊;
(6) F、M的简单氢化物为HO、HS,HO分子间存在氢键,故HO的沸点更高,故沸点:HO>HS;因为HO分子
2 2 2 2 2 2 2
间存在氢键。
19.(1)增大其与酸的接触面积,加快反应速率,提高原料的浸出率;
(2)Cu
(3) 2Fe2++2H O+2H+=2Fe3++2H O 3.3