文档内容
江苏省南通市如皋市 2024 届上学期期初考试押题卷
化学学科
一、单项选择题:共 13题,每题 3分,共 39分。每题只有一个选项最符合题意。
1. 新型冠状病毒可通过气溶胶传播,气溶胶属于胶体的一种。下列关于胶体的叙述,不正确的是
A. 明矾净水利用了胶体的吸附性
B. 依据丁达尔效应可将分散系分为溶液、胶体与浊液
C. 雾是气溶胶,在阳光下可观察到丁达尔效应
D. 用渗析法分离胶体与溶液
2. 化学与生活密切相关。下列化学用语或描述表达正确的是
A. 基态硫原子的轨道表示式:
B. H S的电子式:
2
C. SO 的VSEPR模型:
2
D. 中子数为9的氮原子9N
7
3. X、Y、Z、N是原子序数依次增大的4种短周期元素,其元素性质或原子结构如下表。下列说法正确的
是
元素 元素性质或原子结构
X 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能低于同周期相邻元素
Y 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能高于同周期相邻元素
Z 其价电子中,在不同形状的原子轨道中运动的电子数相等
N 只有一个不成对电子
A. 原子半径:Z Y X
B. 元素的电负性:X>N>Z
C. 元素的第一电离能:Z>N>Y
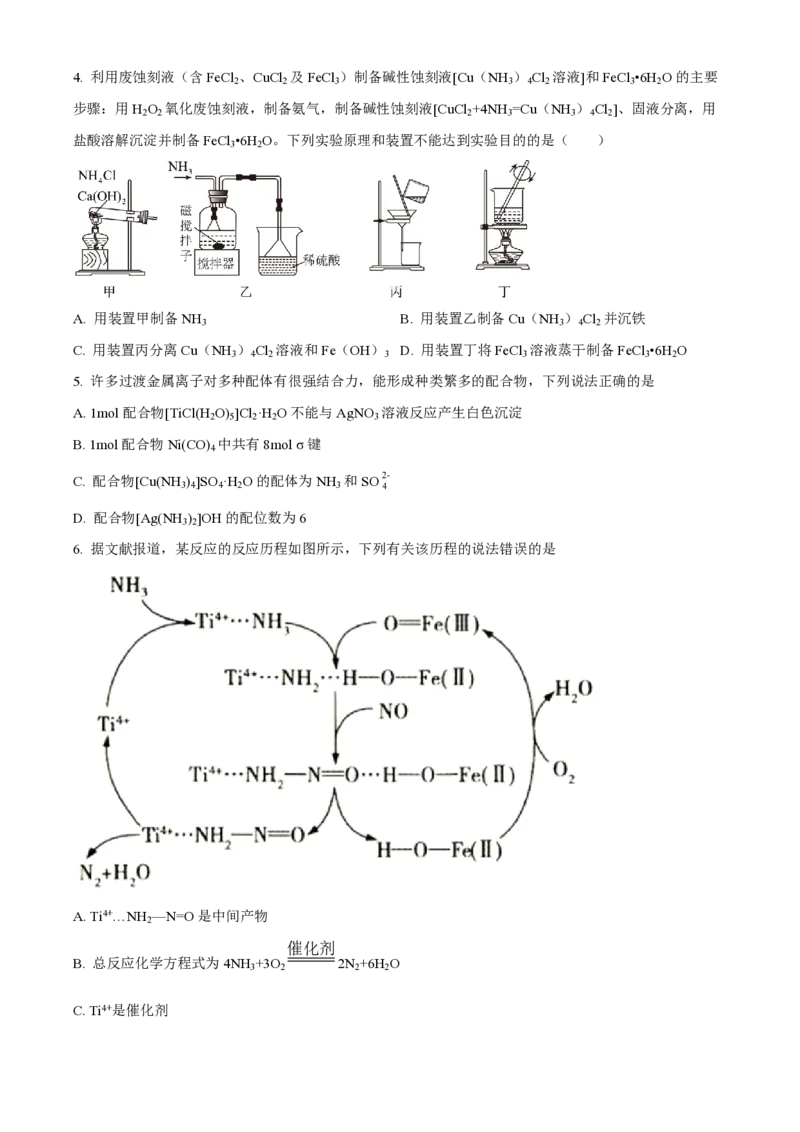
D. X的基态原子的电子轨道表示式:4. 利用废蚀刻液(含FeCl 、CuCl 及FeCl )制备碱性蚀刻液[Cu(NH ) Cl 溶液]和FeCl •6H O的主要
2 2 3 3 4 2 3 2
步骤:用H O 氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl +4NH =Cu(NH ) Cl ]、固液分离,用
2 2 2 3 3 4 2
盐酸溶解沉淀并制备FeCl •6H O。下列实验原理和装置不能达到实验目的的是( )
3 2
A. 用装置甲制备NH B. 用装置乙制备Cu(NH ) Cl 并沉铁
3 3 4 2
C. 用装置丙分离Cu(NH ) Cl 溶液和Fe(OH) D. 用装置丁将FeCl 溶液蒸干制备FeCl •6H O
3 4 2 3 3 3 2
5. 许多过渡金属离子对多种配体有很强结合力,能形成种类繁多的配合物,下列说法正确的是
A. 1mol配合物[TiCl(H O) ]Cl ·H O不能与AgNO 溶液反应产生白色沉淀
2 5 2 2 3
B. 1mol配合物Ni(CO) 中共有8mol σ键
4
C. 配合物[Cu(NH ) ]SO ·H O的配体为NH 和SO2-
3 4 4 2 3 4
D. 配合物[Ag(NH ) ]OH的配位数为6
3 2
6. 据文献报道,某反应的反应历程如图所示,下列有关该历程的说法错误的是
A. Ti4+…NH —N=O是中间产物
2
催化剂
B. 总反应化学方程式为4NH +3O 2N +6H O
3 2 2 2
C. Ti4+是催化剂D. Ti4+…NH —N=O→Ti4++N +H O属于分解反应
2 2 2
7. 硫酸钾是一种重要的无氯优质钾肥,利用某高钾明矾石制备硫酸钾的工艺流程如下:
已知:高钾明矾石的主要成分为K SO Al SO 2Al O H O和少量Fe O 。下列说法正确的是
2 4 2 4 3 2 3 2 2 3
A. 焙烧时Al SO 反应的化学方程式为2Al SO 3S2Al O 9SO
2 4 3 2 4 3 2 3 3
B. 调节pH的目的是使Fe3和Al3完全沉淀
C. 化合物Y可制成铝热剂用于焊接铁轨
D. SO 可回收利用后应用于本流程
3
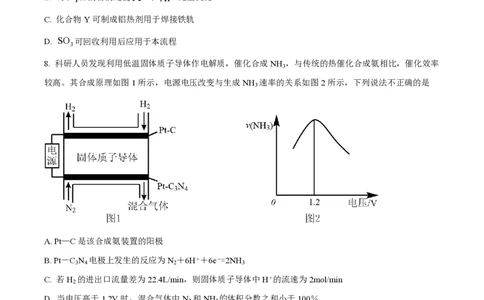
8. 科研人员发现利用低温固体质子导体作电解质,催化合成NH ,与传统的热催化合成氨相比,催化效率
3
较高。其合成原理如图1所示,电源电压改变与生成NH 速率的关系如图2所示,下列说法不正确的是
3
A. Pt—C是该合成氨装置的阳极
B. Pt-C N 电极上发生的反应为N +6H++6e-=2NH
3 4 2 3
C. 若H 的进出口流量差为22.4L/min,则固体质子导体中H+的流速为2mol/min
2
D. 当电压高于1.2V时,混合气体中N 和NH 的体积分数之和小于100%
2 3
9. 布洛芬是一种用于小儿发热的经典解热镇痛药,异丁基苯是合成它的一种原料,二者的结构简式如图。
下列说法正确的是
A. 异丁基苯属于芳香烃,与对二乙苯互为同分异构体B.
异丁基苯和布洛芬中碳原子均有sp和sp3杂化
C. 1mol布洛芬与足量的Na CO 溶液反应生成22gCO
2 3 2
D. 两者均能发生加成、取代和消去反应
10. 含氮物质可发生如下反应:①2NOO 2 2NO 2
②NO(g)NO (g)2NaOH(aq)2NaNO (aq)H O(l)
2 2 2
③NaNO NH Cl N NaCl2H O
2 4 2 2
下列说法正确的是
A. 常温下,NO与O 混合能立即看到红棕色气体,说明该反应已达平衡
2
B. 反应②的S0
C. 反应③消耗1molNaNO ,理论上会生成标准状况下约22.4LN
2 2
D. 利用反应①、②、③可以同时处理NO 含量较高的废气和含NH的废水
2 4
11. 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选
实验操作和现象 结论
项
向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶
A X溶液中一定含有Fe2+
液,溶液变为红色
向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶
B Br 的氧化性比I 的强
2 2
液,溶液显蓝色
用pH试纸测得: CH,COONa溶液的pH约为9,NaNO 溶 HNO 电离出H+的能力一定比
2 2
C
液的pH约为8 CH COOH的强
3
将Na SO 样品溶于水,滴加稀盐酸酸化的Ba( NO ) 溶液,
2 3 3 2
D Na SO 样品已变质
2 3
产生白色沉淀
A. A B. B C. C D. D
12. 室温下,通过下列实验探究Na CO 的性质。已知:25℃时,H SO 的K =1.410-2、
2 3 2 3 al
K =1.0107,H CO 的K 4.3107、K 5.61011。
a2 2 3 al a2实验1:配制50mL0.1molL1Na CO 溶液,测得溶液pH约为12;
2 3
实验2:取10mL0.1molL1Na CO 溶液,向其中加入少量CaSO 固体充分搅拌,一段时间后过滤。向
2 3 4
滤渣中加入足量稀盐酸,固体完全溶解;
实验3:取10mL0.1molL1Na CO 溶液,向其中缓慢滴入等体积0.1molL1稀盐酸。
2 3
下列说法正确的是
A. 实验1所得溶液中,c
Na
c
HCO
c
CO2
3 3
B. 根据实验2,可推测K CaCO K CaSO
sp 3 sp 4
C. 实验3反应后溶液中存在:c Na cH CO c HCO c CO2
2 3 3 3
D. 25℃时,反应CO 3 2 H 2 SO 3 HCO 3 HSO 3 的平衡常数K 2.5108
13. 碳热还原氧化锌反应可用于循环制氢。碳热还原氧化锌的主要反应如下:
反应I ZnOCO
ZnCO
2
;
反应Ⅱ CO
2
C
2CO
在不同容器中分别发生反应I、反应Ⅱ,不同压强(P 或P
)下分别达平衡时,两个反应中c(CO)/cCO
随
1 2 2
温度变化的关系如图所示。下列说法正确的是
A. 压强大小:P P
1 2
B. 在如图所示条件下,反应I可表示为ZnO(s)CO(g)Zn(s)CO (g) H 0
2
C.
选择反应Ⅱ的c(CO)/cCO
小于反应I的条件,将C与ZnO置于同一密闭容器中,碳热还原氧化锌
2
反应能顺利进行D. 一定条件下将C与ZnO置于同一密闭容器中反应,当n(C)/n(ZnO)1时,增大n(C)/n(ZnO)的
值,可减少平衡时气体中CO 的含量
2
二、非选择题:共 4题,共 61分。
14. 五氧化二钒 V O 是广泛用于冶金、化工等行业的催化剂。工业上以石煤(主要成分为VO ,含有少
2 5 2 3
量SiO 、PO 等杂质)为原料制备V O ,主要经过“焙烧、水浸、除杂、沉钒、灼烧”等过程。
2 2 5 2 5
已知:①NaVO 溶于水,NH VO 难溶于水。
3 4 3
②K MgSiO 2.5105,K Mg PO 2.51024。
sp 3 sp 3 4 2
回答下列问题:
(1)向石煤中加纯碱,在通入空气的条件下焙烧,VO 转化为NaVO ,该反应的化学方程式为
2 3 3
_______。
(2)向水浸后的溶液中加入MgSO 生成Mg PO 、MgSiO 沉淀以除去硅、磷,除杂后的溶液中
4 3 4 2 3
c
PO3-
MgSO 的浓度为0.1molL1,此时溶液中 4 =_______;磷、硅去除率随温度变化的曲线如图所
4
c
SiO2-
3
示,随着温度升高除磷率下降而除硅率升高,可能的原因是_______。
(3)“沉矾”时加入NH Cl析出NH VO ,沉钒温度需控制在50℃左右,温度不能过高的原因为
4 4 3
_______。
(4)NH VO 在空气中灼烧得VO 。称取0.80g灼烧后的产物,加入稀硫酸溶解后,向其中加入
4 3 2 5
0.2000molL1H C O 溶液25mL,再用0.1000molL1KMnO 溶液滴定过量的H C O 溶液至终点,
2 2 4 4 2 2 4
消耗KMnO 溶液的体积为4.00mL,则产物中V O 的质量分数为_______(写出计算过程)。已知:
4 2 5
V O 2H 2VO H O 2VO H C O 2VO 2CO 2H
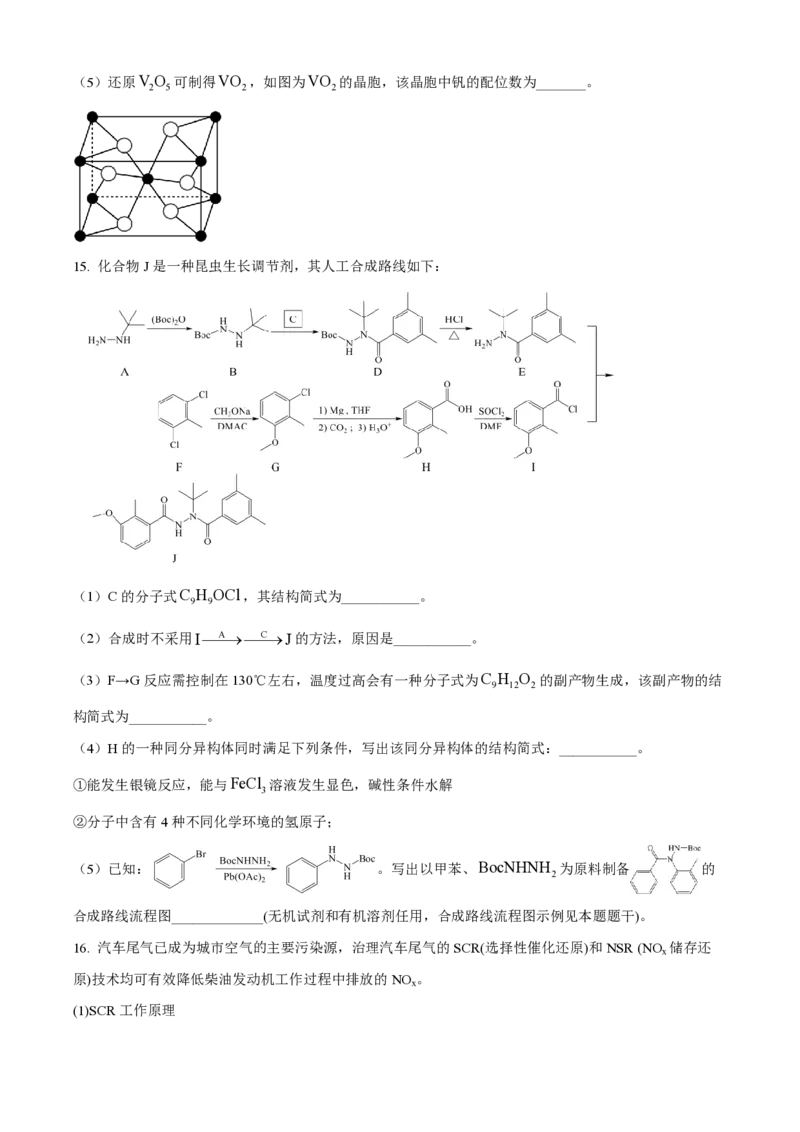
2 5 2 2 2 2 2 4 2 2(5)还原V O 可制得VO ,如图为VO 的晶胞,该晶胞中钒的配位数为_______。
2 5 2 2
15. 化合物J是一种昆虫生长调节剂,其人工合成路线如下:
(1)C的分子式C H OCl,其结构简式为___________。
9 9
(2)合成时不采用IACJ的方法,原因是___________。
(3)F→G反应需控制在130℃左右,温度过高会有一种分子式为C H O 的副产物生成,该副产物的结
9 12 2
构简式为___________。
(4)H的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___________。
①能发生银镜反应,能与FeCl 溶液发生显色,碱性条件水解
3
②分子中含有4种不同化学环境的氢原子;
(5)已知: 。写出以甲苯、BocNHNH 为原料制备 的
2
合成路线流程图_____________(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
16. 汽车尾气已成为城市空气的主要污染源,治理汽车尾气的SCR(选择性催化还原)和NSR (NO 储存还
x
原)技术均可有效降低柴油发动机工作过程中排放的NO 。
x
(1)SCR工作原理①尿素[CO(NH ) ]水溶液热分解为NH 和CO ,该反应的化学方程式是___________。
2 2 3 2
②反应器中NH 还原NO 的化学方程式是___________。
3 2
(2)NSR(NOx储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(O 充足、柴油较少)和富燃(O
2 2
不足、柴油较多)条件下交替进行,通过BaO和Ba(NO ) 的相互转化实现NOx 的储存和还原。
3 2
①BaO吸收NO 的反应中氧化剂与还原剂的物质的量之比是___________。
2
②富燃条件下Pt表面反应的化学方程式是___________。
③若柴油中硫含量较高,在稀燃过程中,BaO吸收氮氧化物的能力下降至很低水平,结合化学方程式解释
原因:___________。
④研究发现:尾气中的CO 对BaO吸收氮氧化物有影响。一定温度下,测得气体中CO 的体积分数与氮
2 2
氧化物吸收率的关系如下图所示。则:一定范围内,氮氧化物吸收率随CO 体积分数的增大而下降,原因
2
是___________;当CO 体积分数达到10%~20%时,氮氧化物吸收率依然较高,原因可能是
2
___________。17. CuCl用作有机合成催化剂等工业。CuCl露置于潮湿的空气中易被氧化和水解,酸性条件下易歧化,难
溶于水,易溶于浓盐酸并生成[CuCl ]-。
2
(1)基态Cu+核外电子排布式是_______。
(2)实验测得:CuCl属于共价化合物,气态CuCl分子的相对分子质量为199,该分子中含有配位键,则
气态CuCl分子的结构式可能为_______。
(3)已知:①Ksp(CuCl)≈1×10-7,②反应2Cu+=Cu+Cu2+平衡常数K≈1×106。有人预设用反应
Cu(s)+Cu2++2Cl-=2CuCl(s)制备CuCl (s),试预测该反应进行的程度大小:_______ (填写“几乎完全反应”或
“几乎不反应”)。
工业上有多种制备CuCl的方法:
方法一:将废铜粉与食盐水、浓盐酸料液混合,在60~70℃缓慢通入空气进行氧化。静置,取上层清液加水
稀释,生成CuCl沉淀,过滤,沉淀经洗涤、干燥得CuCl产品并真空保存。
方法二:将Na SO 的水溶液逐滴加入CuCl 的水溶液中,再加入少量浓盐酸混匀,充分反应后过滤,沉淀
2 3 2
经洗涤、干燥得CuCl产品并真空保存。
(4)“方法一”中:
①反应温度控制在60~70℃,目的是_______。
②加入浓盐酸的目的是_______。
(5)“方法二”中:
①总反应的离子方程式是_______。
②加入Na SO 溶液体积(V)与溶液pH关系如图1。当Na SO 溶液体积大于500 mL时,溶液pH增大的原
2 3 2 3
因是_______。③用酸或碱液调控反应混合液的pH,则CuCl产率见图2。pH<2.5时,CuCl产率相对较低;pH>3.5时,CuCl
产率又迅速下降。试分析原因: _______。