文档内容
龙岩市 2023 年高中毕业班三月教学质量检测
化学试题
(考试时间:75分钟 满分:100分)
注意:1.请将答案填写在答题卡上
2.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 P-31 Cl-35.5
一、选择题(本题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有一项符合题目要
求)
1.衣食住行与化学密切相关。下列说法或做法错误的是( )
A.棉衬衫和丝质衣服的主要原料均为高分子化合物
B.碳酸氢钠可作为面制食品的膨松剂
C.84消毒液与洁厕灵混合后用于消毒卫生间
D.汽车轮毂用密度小强度大的镁合金制造
2.布洛芬为解热镇痛类化学药物,直接服用会对胃肠等造成强烈刺激,故化学家进行如图所示的分子修饰,
以缓刺激。下列说法正确的是( )
A.布洛芬修饰分子中不含手性碳原子
B.1mol布洛芬分子最多可与 反应
C.布洛芬修饰分子中所有的碳原子可能共平面
D.在胃肠内布洛芬修饰分子会转化为布洛芬分子
3.X、Y、Z、W 是原子序数依次增大的短周期元素,X、Y 可以构成 ,W 的价电子排布式为
,Z、W同主族且能构成下图所示的阴离子 。以下说法正确的是( )
A. 中不存在配位键 B. 有很好的热稳定性
C.电负性 D.
4.测定食醋中总酸度有以下步骤:①将食醋精确稀释到原来的 10倍;②用烧碱固体配制100mL浓度约为
学科网(北京)股份有限公司的溶液;③用邻苯二甲酸氢钾固体标定步骤②所得溶液;④用移液管取20.00mL待测液;⑤用已
知浓度NaOH溶液滴定。以下对应步骤中的操作及选用仪器正确的是( )
A.步骤① B.步骤②
C.步骤③ D.步骤⑤
5. 为阿伏加德罗常数的值,将标况下 通入足量 中,下列说法正确的是( )
A.该反应中转移电子数为 B. 中含中子数为
C.所得溶液中 和 总数为 D. 中含H-Cl键数为
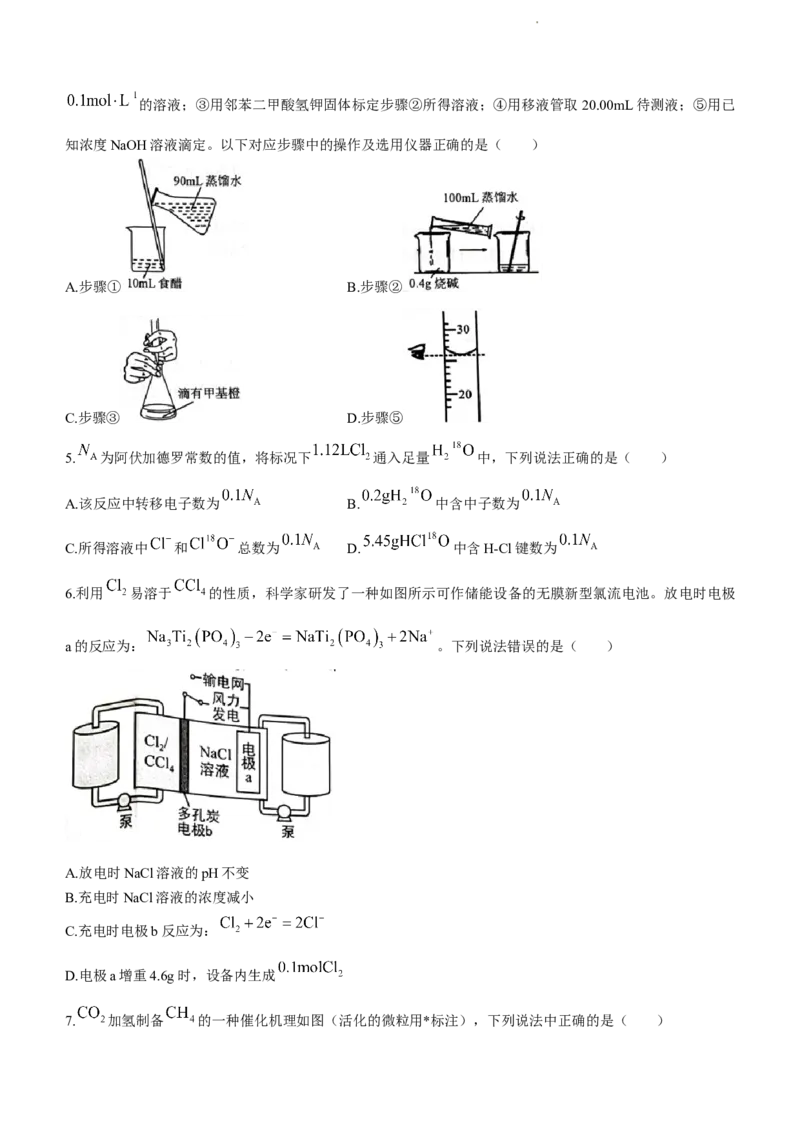
6.利用 易溶于 的性质,科学家研发了一种如图所示可作储能设备的无膜新型氯流电池。放电时电极
a的反应为: 。下列说法错误的是( )
A.放电时NaCl溶液的pH不变
B.充电时NaCl溶液的浓度减小
C.充电时电极b反应为:
D.电极a增重4.6g时,设备内生成
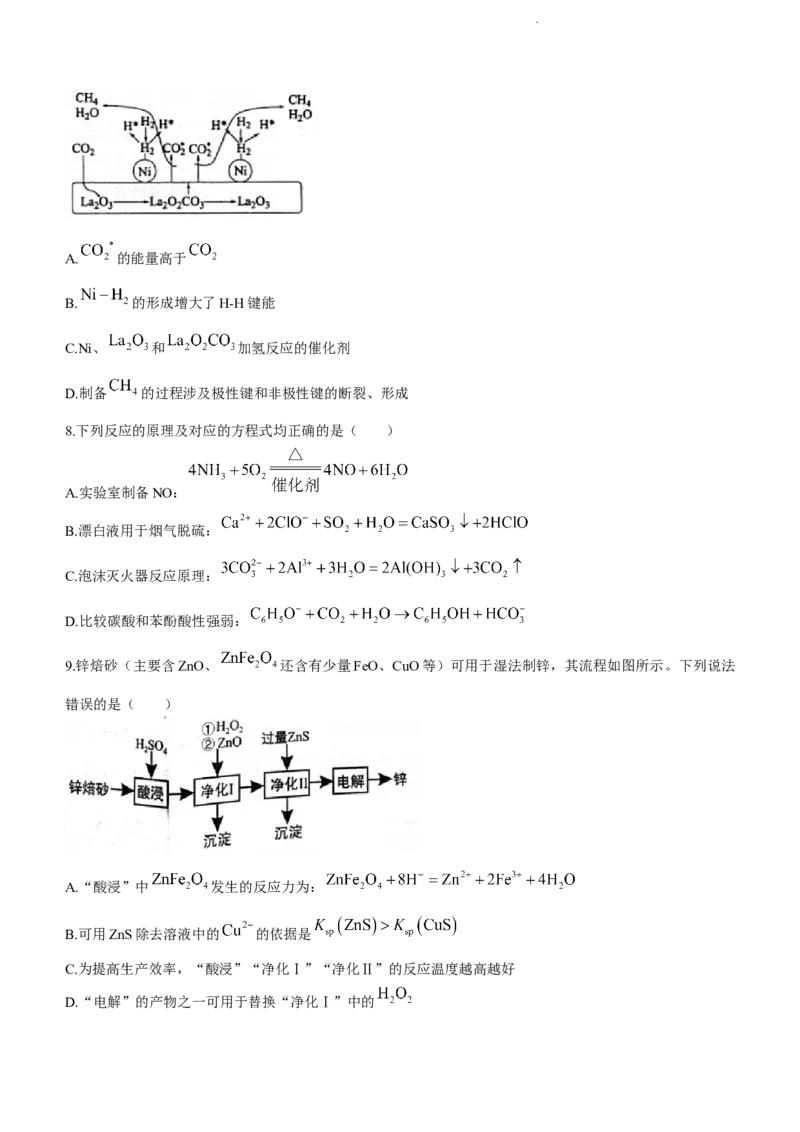
7. 加氢制备 的一种催化机理如图(活化的微粒用*标注),下列说法中正确的是( )
学科网(北京)股份有限公司A. 的能量高于
B. 的形成增大了H-H键能
C.Ni、 和 加氢反应的催化剂
D.制备 的过程涉及极性键和非极性键的断裂、形成
8.下列反应的原理及对应的方程式均正确的是( )
A.实验室制备NO:
B.漂白液用于烟气脱硫:
C.泡沫灭火器反应原理:
D.比较碳酸和苯酚酸性强弱:
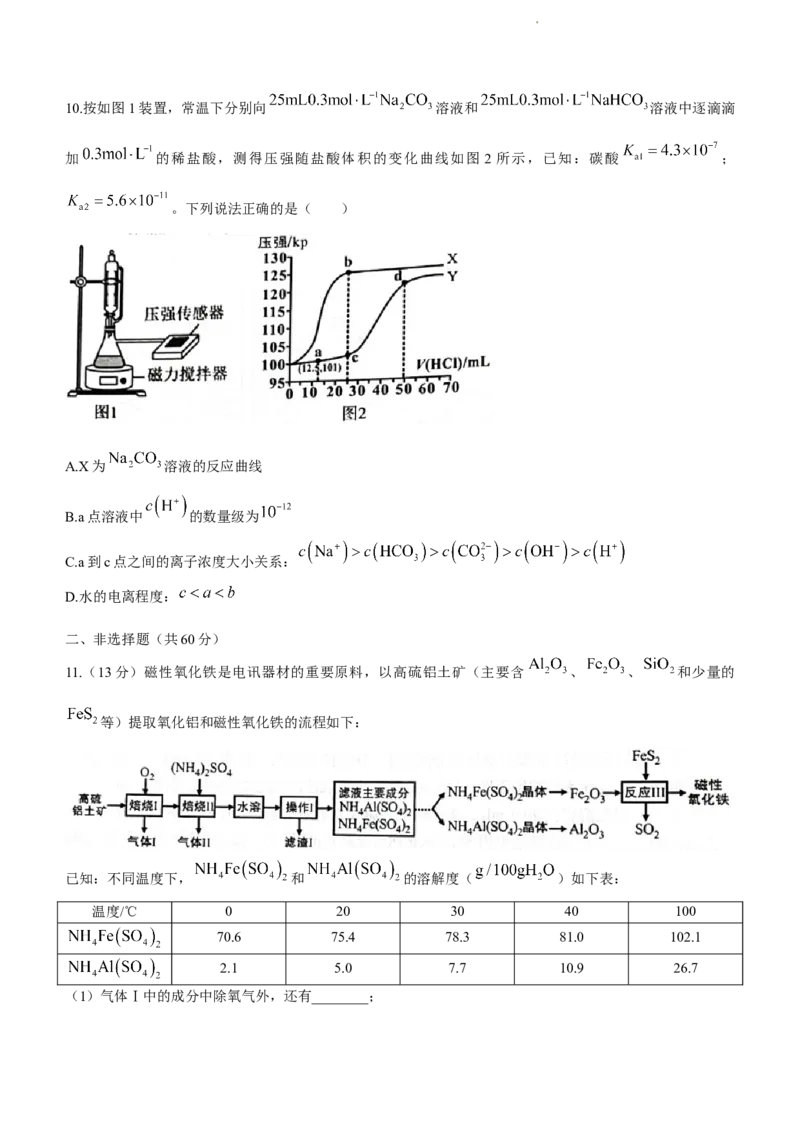
9.锌焙砂(主要含ZnO、 还含有少量FeO、CuO等)可用于湿法制锌,其流程如图所示。下列说法
错误的是( )
A.“酸浸”中 发生的反应力为:
B.可用ZnS除去溶液中的 的依据是
C.为提高生产效率,“酸浸”“净化Ⅰ”“净化Ⅱ”的反应温度越高越好
D.“电解”的产物之一可用于替换“净化Ⅰ”中的
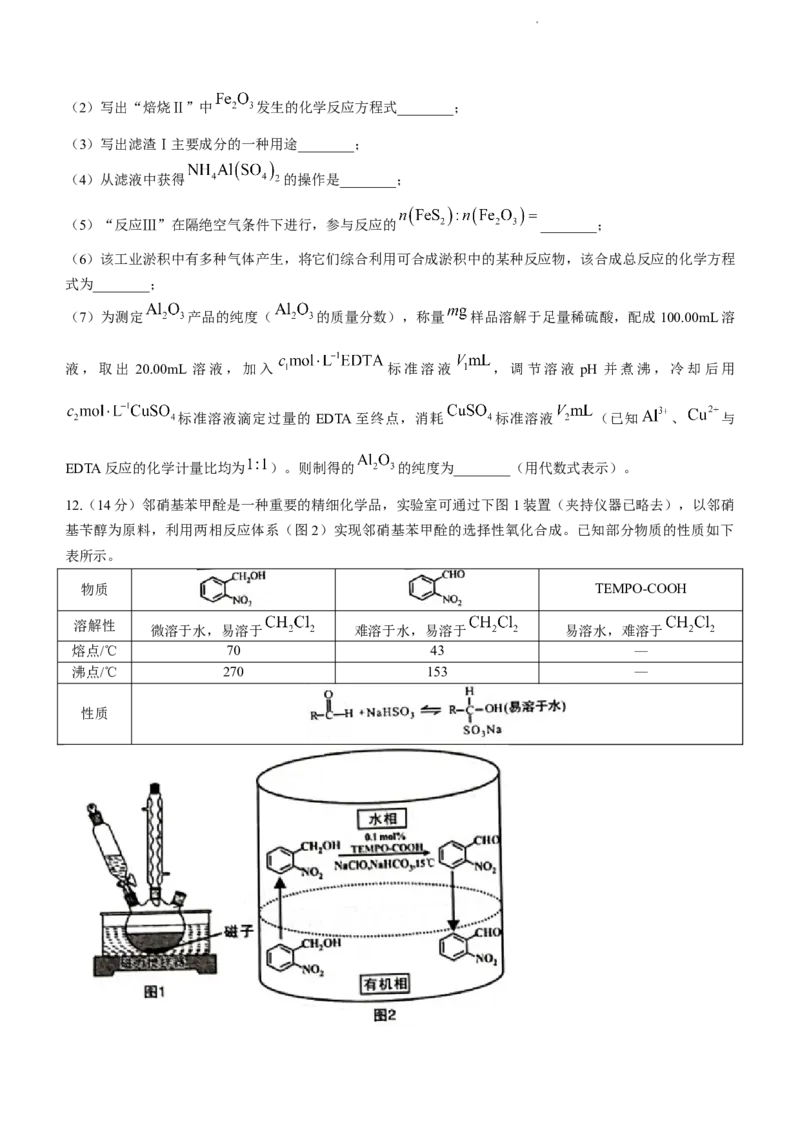
学科网(北京)股份有限公司10.按如图1装置,常温下分别向 溶液和 溶液中逐滴滴
加 的稀盐酸,测得压强随盐酸体积的变化曲线如图 2 所示,已知:碳酸 ;
。下列说法正确的是( )
A.X为 溶液的反应曲线
B.a点溶液中 的数量级为
C.a到c点之间的离子浓度大小关系:
D.水的电离程度:
二、非选择题(共60分)
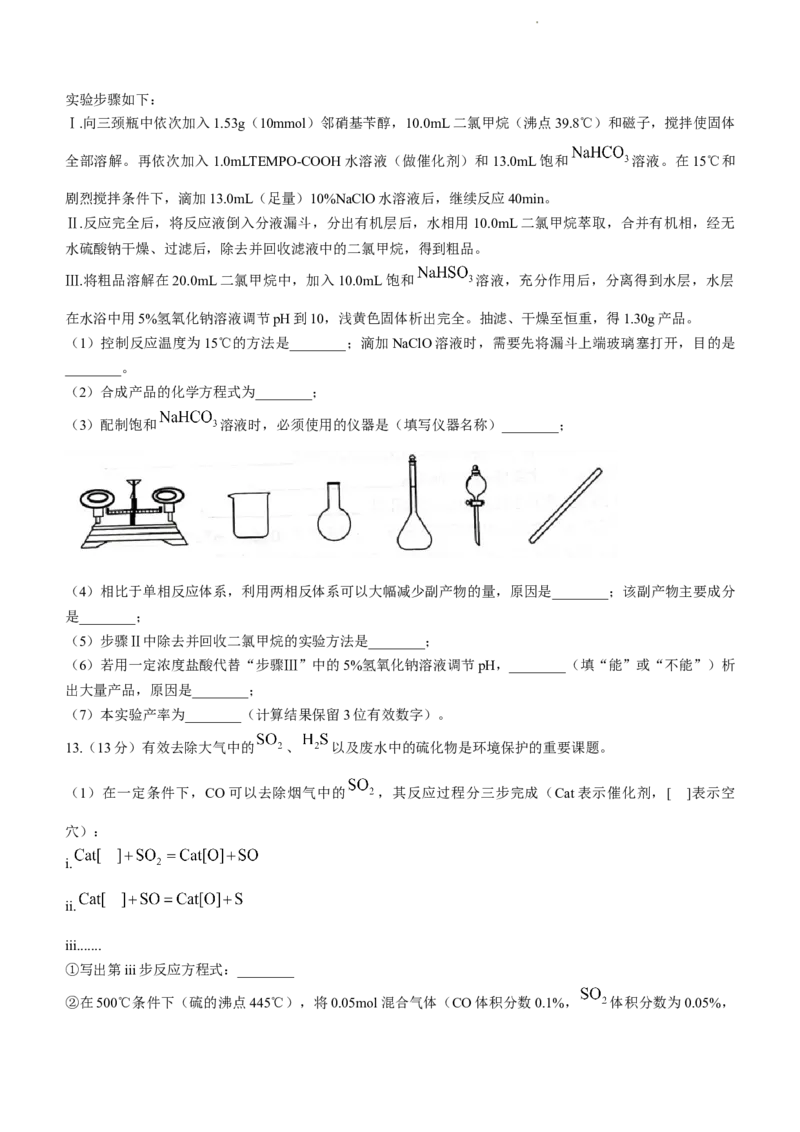
11.(13分)磁性氧化铁是电讯器材的重要原料,以高硫铝土矿(主要含 、 、 和少量的
等)提取氧化铝和磁性氧化铁的流程如下:
已知:不同温度下, 和 的溶解度( )如下表:
温度/℃ 0 20 30 40 100
70.6 75.4 78.3 81.0 102.1
2.1 5.0 7.7 10.9 26.7
(1)气体Ⅰ中的成分中除氧气外,还有________;
学科网(北京)股份有限公司(2)写出“焙烧Ⅱ”中 发生的化学反应方程式________;
(3)写出滤渣Ⅰ主要成分的一种用途________;
(4)从滤液中获得 的操作是________;
(5)“反应Ⅲ”在隔绝空气条件下进行,参与反应的 ________;
(6)该工业淤积中有多种气体产生,将它们综合利用可合成淤积中的某种反应物,该合成总反应的化学方程
式为________;
(7)为测定 产品的纯度( 的质量分数),称量 样品溶解于足量稀硫酸,配成100.00mL溶
液,取出 20.00mL 溶液,加入 标准溶液 ,调节溶液 pH 并煮沸,冷却后用
标准溶液滴定过量的 EDTA至终点,消耗 标准溶液 (已知 、 与
EDTA反应的化学计量比均为 )。则制得的 的纯度为________(用代数式表示)。
12.(14分)邻硝基苯甲酫是一种重要的精细化学品,实验室可通过下图 1装置(夹持仪器已略去),以邻硝
基苄醇为原料,利用两相反应体系(图2)实现邻硝基苯甲酫的选择性氧化合成。已知部分物质的性质如下
表所示。
物质 TEMPO-COOH
溶解性
微溶于水,易溶于 难溶于水,易溶于 易溶水,难溶于
熔点/℃ 70 43 —
沸点/℃ 270 153 —
性质
学科网(北京)股份有限公司实验步骤如下:
Ⅰ.向三颈瓶中依次加入1.53g(10mmol)邻硝基苄醇,10.0mL二氯甲烷(沸点39.8℃)和磁子,搅拌使固体
全部溶解。再依次加入1.0mLTEMPO-COOH水溶液(做催化剂)和13.0mL饱和 溶液。在15℃和
剧烈搅拌条件下,滴加13.0mL(足量)10%NaClO水溶液后,继续反应40min。
Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用10.0mL二氯甲烷萃取,合并有机相,经无
水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
Ⅲ.将粗品溶解在20.0mL二氯甲烷中,加入10.0mL饱和 溶液,充分作用后,分离得到水层,水层
在水浴中用5%氢氧化钠溶液调节pH到10,浅黄色固体析出完全。抽滤、干燥至恒重,得1.30g产品。
(1)控制反应温度为15℃的方法是________;滴加NaClO溶液时,需要先将漏斗上端玻璃塞打开,目的是
________。
(2)合成产品的化学方程式为________;
(3)配制饱和 溶液时,必须使用的仪器是(填写仪器名称)________;
(4)相比于单相反应体系,利用两相反体系可以大幅减少副产物的量,原因是________;该副产物主要成分
是________;
(5)步骤Ⅱ中除去并回收二氯甲烷的实验方法是________;
(6)若用一定浓度盐酸代替“步骤Ⅲ”中的5%氢氧化钠溶液调节pH,________(填“能”或“不能”)析
出大量产品,原因是________;
(7)本实验产率为________(计算结果保留3位有效数字)。
13.(13分)有效去除大气中的 、 以及废水中的硫化物是环境保护的重要课题。
(1)在一定条件下,CO可以去除烟气中的 ,其反应过程分三步完成(Cat表示催化剂,[ ]表示空
穴):
i.
ii.
iii.......
①写出第iii步反应方程式:________
②在500℃条件下(硫的沸点445℃),将0.05mol混合气体(CO体积分数0.1%, 体积分数为0.05%,
学科网(北京)股份有限公司其余为 )通入1L刚性容器中,在催化剂作用下发生反应,100min时测得CO体积分数0.01%。
i.100min时 去除率为________;
ii.0~100min内CO平均反应速率 ________;
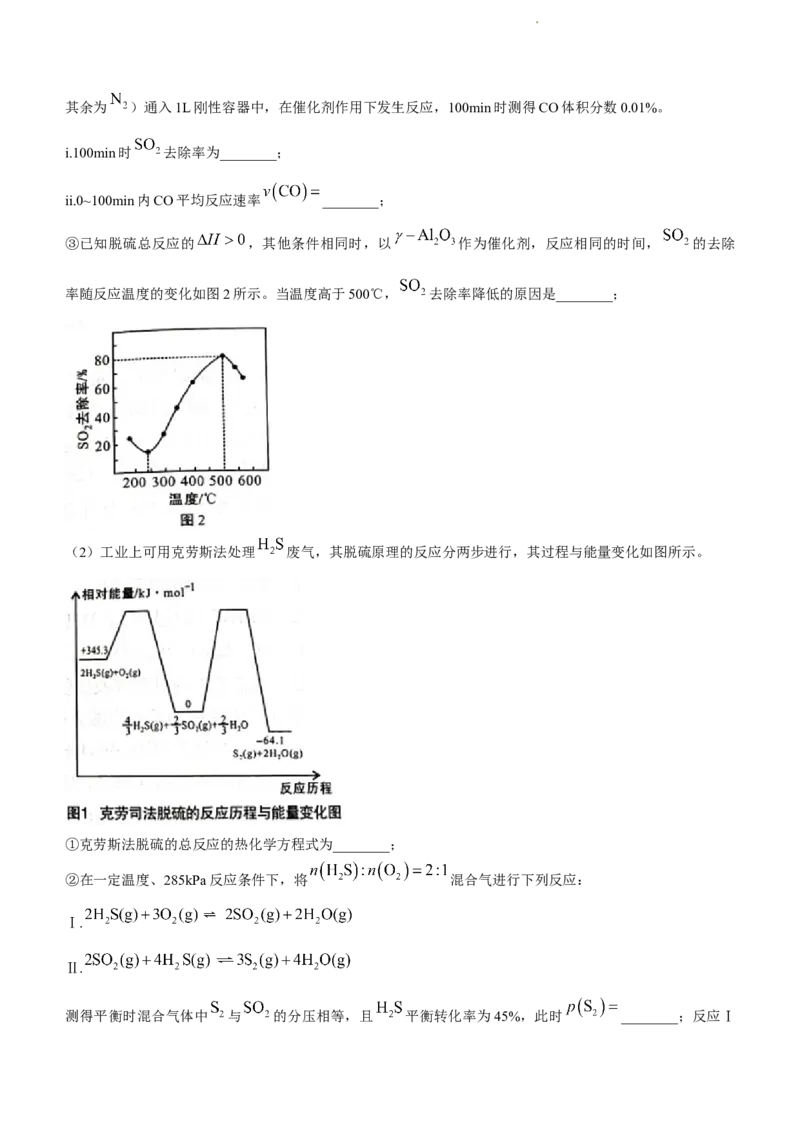
③已知脱硫总反应的 ,其他条件相同时,以 作为催化剂,反应相同的时间, 的去除
率随反应温度的变化如图2所示。当温度高于500℃, 去除率降低的原因是________;
(2)工业上可用克劳斯法处理 废气,其脱硫原理的反应分两步进行,其过程与能量变化如图所示。
①克劳斯法脱硫的总反应的热化学方程式为________;
②在一定温度、285kPa反应条件下,将 混合气进行下列反应:
Ⅰ.
Ⅱ.
测得平衡时混合气体中 与 的分压相等,且 平衡转化率为45%,此时 ________;反应Ⅰ
学科网(北京)股份有限公司的平衡常数 ________(列出数字运算表达式即可)。
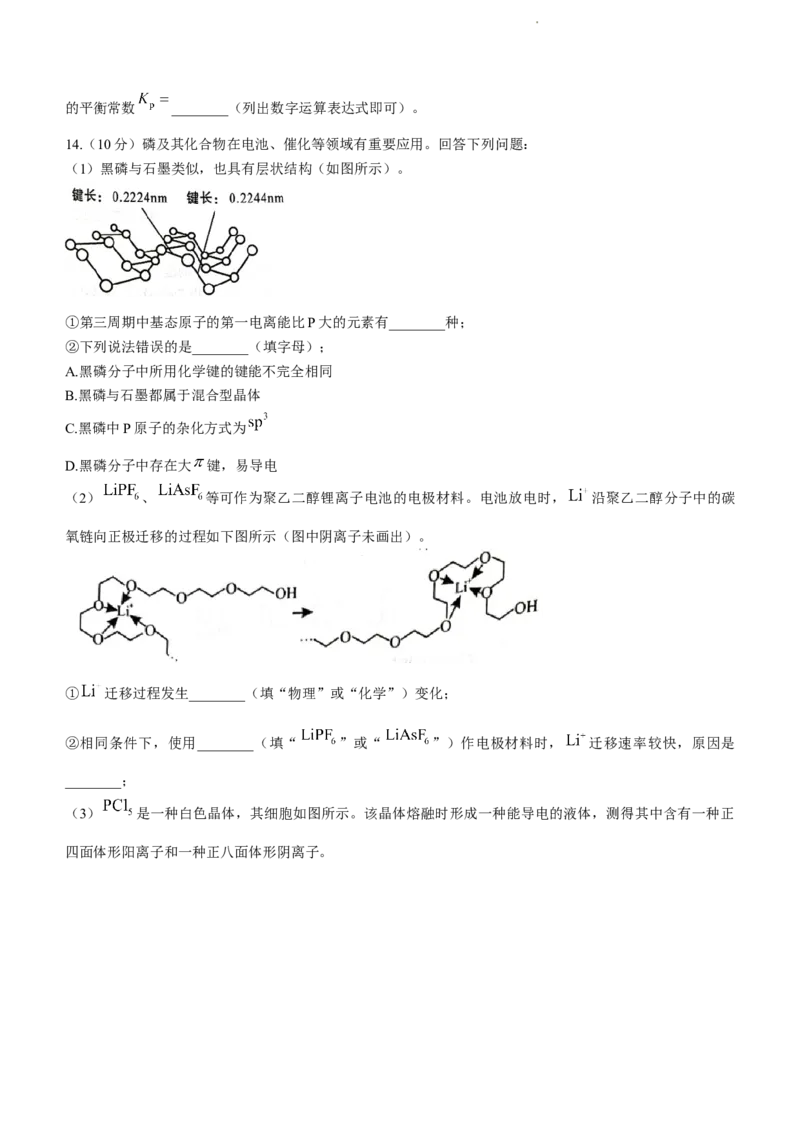
14.(10分)磷及其化合物在电池、催化等领域有重要应用。回答下列问题:
(1)黑磷与石墨类似,也具有层状结构(如图所示)。
①第三周期中基态原子的第一电离能比P大的元素有________种;
②下列说法错误的是________(填字母);
A.黑磷分子中所用化学键的键能不完全相同
B.黑磷与石墨都属于混合型晶体
C.黑磷中P原子的杂化方式为
D.黑磷分子中存在大 键,易导电
(2) 、 等可作为聚乙二醇锂离子电池的电极材料。电池放电时, 沿聚乙二醇分子中的碳
氧链向正极迁移的过程如下图所示(图中阴离子未画出)。
① 迁移过程发生________(填“物理”或“化学”)变化;
②相同条件下,使用________(填“ ”或“ ”)作电极材料时, 迁移速率较快,原因是
________;
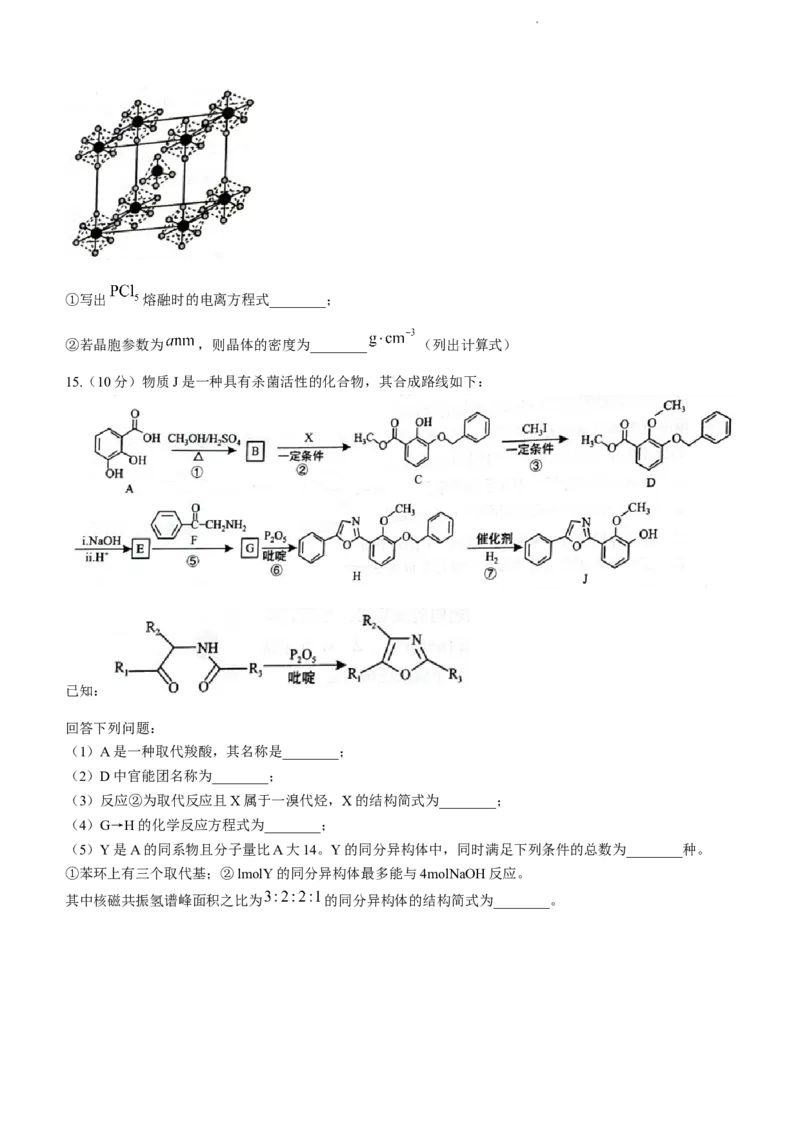
(3) 是一种白色晶体,其细胞如图所示。该晶体熔融时形成一种能导电的液体,测得其中含有一种正
四面体形阳离子和一种正八面体形阴离子。
学科网(北京)股份有限公司①写出 熔融时的电离方程式________;
②若晶胞参数为 ,则晶体的密度为________ (列出计算式)
15.(10分)物质J是一种具有杀菌活性的化合物,其合成路线如下:
已知:
回答下列问题:
(1)A是一种取代羧酸,其名称是________;
(2)D中官能团名称为________;
(3)反应②为取代反应且X属于一溴代烃,X的结构简式为________;
(4)G→H的化学反应方程式为________;
(5)Y是A的同系物且分子量比A大14。Y的同分异构体中,同时满足下列条件的总数为________种。
①苯环上有三个取代基;②lmolY的同分异构体最多能与4molNaOH反应。
其中核磁共振氢谱峰面积之比为 的同分异构体的结构简式为________。
学科网(北京)股份有限公司学科网(北京)股份有限公司