文档内容
2.2.2 影响化学平衡的因素 练习(原卷版)
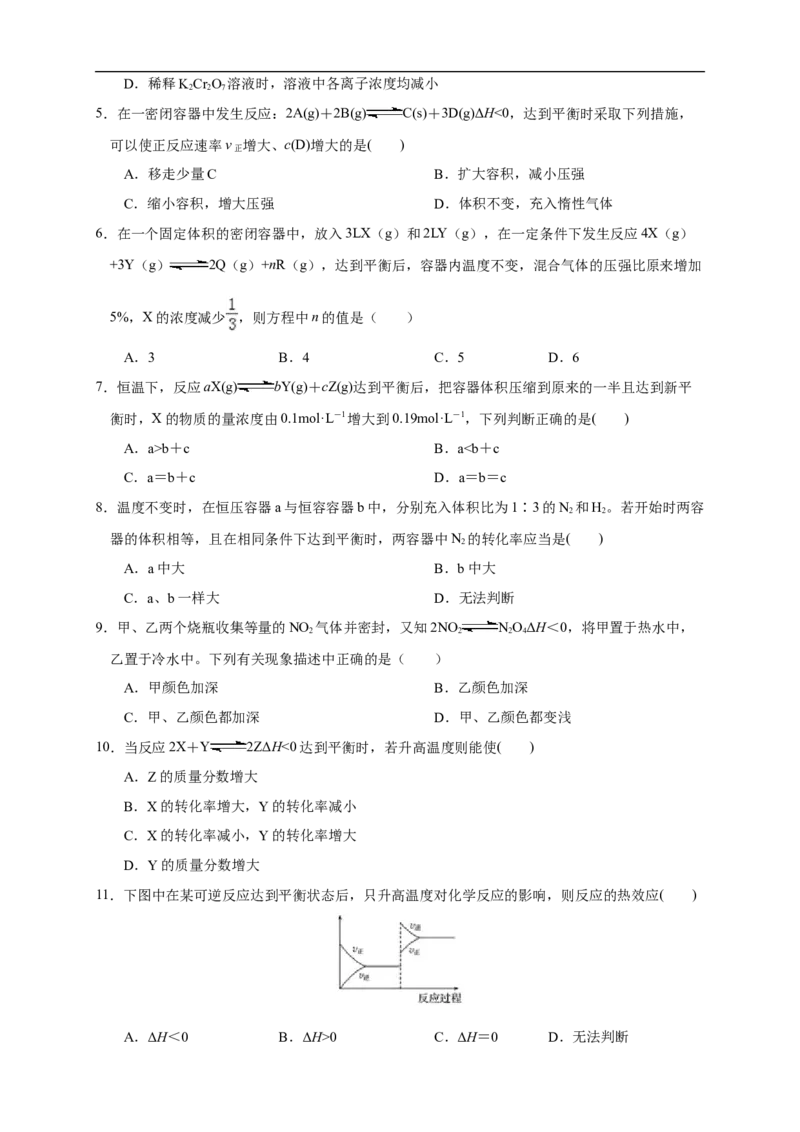
1.下图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的
是( )
A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ
C.该反应达到平衡态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ
D.同一种反应物在平衡态Ⅰ和平衡态Ⅱ时浓度不相等
2.在一个密闭容器中充入1molCO 和3molH ,在850℃时,气体混合物达到下式所示平衡:
2 2
CO(g)+H(g) CO(g)+HO(g)。已知达到平衡时生成0.75molCO。那么当H 改为9mol,在
2 2 2 2
上述条件下平衡时生成CO和HO的物质的量之和可能为( )
2
A.1.2mol B.1.5mol C.1.8mol D.2.5mol
3.向FeCl 溶液中加入KSCN溶液,混和溶液呈红色。在这个反应体系中存在下述平衡:Fe3++
3
3SCN- Fe(SCN) (红色);向上述溶液中加入NaOH浓溶液,以下说法正确的是( )
3
A.溶液颜色不变,产生红褐色沉淀,平衡不移动
B.溶液颜色变浅,产生红褐色沉淀,平衡向右移动
C.溶液颜色变深,平衡向右移动
D.溶液颜色变浅,产生红褐色沉淀,平衡向左移动
4.重铬酸钾溶液中存在如下平衡:CrO2-
(橙色)+H O
2H++2CrO2-
(黄色)①向
2 7 2 4
2mL0.1mol•L﹣1KCr O 溶液中滴入3滴6mol•L﹣1NaOH溶液,溶液由橙色变为黄色;向所得溶液
2 2 7
中再滴入5滴浓HSO ,溶液由黄色变为橙色。②向2mL0.1mol•L﹣1酸化的KCr O 溶液中滴入适
2 4 2 2 7
量(NH )Fe(SO ) 溶液,溶液由橙色变为绿色,发生反应:Cr O2-+14H++6Fe2+==2Cr3+(绿
4 2 4 2 2 7
色)+6Fe3++7H O。
2
下列分析正确的是( )
A.实验①和②均能证明KCr O 溶液中存在上述平衡
2 2 7
B.实验②能说明氧化性:Cr >Fe3+
2O2-
7
C.Cr 和Fe2+在酸性溶液中可以大量共存
O2-
4D.稀释KCr O 溶液时,溶液中各离子浓度均减小
2 2 7
5.在一密闭容器中发生反应:2A(g)+2B(g) C(s)+3D(g)ΔH<0,达到平衡时采取下列措施,
可以使正反应速率v 增大、c(D)增大的是( )
正
A.移走少量C B.扩大容积,减小压强
C.缩小容积,增大压强 D.体积不变,充入惰性气体
6.在一个固定体积的密闭容器中,放入3LX(g)和2LY(g),在一定条件下发生反应4X(g)
+3Y(g) 2Q(g)+nR(g),达到平衡后,容器内温度不变,混合气体的压强比原来增加
5%,X的浓度减少 ,则方程中n的值是( )
A.3 B.4 C.5 D.6
7.恒温下,反应aX(g) bY(g)+cZ(g)达到平衡后,把容器体积压缩到原来的一半且达到新平
衡时,X的物质的量浓度由0.1mol·L-1增大到0.19mol·L-1,下列判断正确的是( )
A.a>b+c B.a0 C.ΔH=0 D.无法判断12.图中a曲线表示一定条件下可逆反应X(g)+Y(g) 2Z(g)+W(s)(正反应为放热反应)的反应
过程。若使a曲线变为b曲线,可采取的措施是( )
A.加入催化剂 B.降低温度
C.减少体系压强 D.增大y的浓度
13.下列措施或事实能用勒夏特列原理解释的是( )
A.在合成氨(正反应是放热)的反应中,升温有利于氨的合成
B.H、I、HI三者的平衡混合气加压后颜色变深
2 2
C.钢铁在潮湿的空气中更容易生锈
D.含有酚酞的氨水中加入少量的氯化铵溶液的颜色变浅
14.下列事实不能用勒夏特列原理解释的是( )
A.光照新制的氯水时,溶液的pH逐渐减小
B.加催化剂,使N 和H 在一定条件下转化为NH
2 2 3
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.增大压强,有利于SO 与O 反应生成SO
2 2 3